文档内容
题型五 流程图
类型1 海水化学
1.(2016眉山)通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl 、CaCl 、NaSO
2 2 2 4
以及泥沙等杂质。以下是制备精盐水的实验方案,各步骤操作流程如下:
第1题图
[来源:学科网]
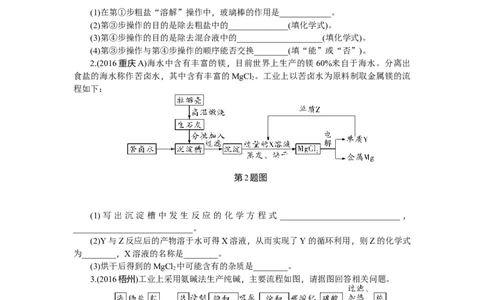
(1)在第①步粗盐“溶解”操作中,玻璃棒的作用是____________。
(2)第③步操作的目的是除去粗盐中的______________(填化学式)。
(3)第④步操作的目的是除去混合液中的____________________(填化学式)。
(4)第③步操作与第④步操作的顺序能否交换________(填“能”或“否”)。
2.(2016重庆A)海水中含有丰富的镁,目前世界上生产的镁60%来自于海水。分离出
食盐的海水称作苦卤水,其中含有丰富的MgCl 。工业上以苦卤水为原料制取金属镁的流
2
程如下:
第2题图
(1) 写 出 沉 淀 槽 中 发 生 反 应 的 化 学 方 程 式 ____________________________ ,
____________________________。
(2)Y与Z反应后的产物溶于水可得X溶液,从而实现了Y的循环利用,则Z的化学式
为________,X溶液的名称是________。
(3)烘干后得到的MgCl 中可能含有的杂质是________。
2
3.(2016梧州)工业上采用氨碱法生产纯碱,主要流程如图,请据图回答相关问题。
第3题图
(1)氨碱法生产所得产品为纯碱,向纯碱水溶液中滴入无色酚酞试液显__________色。
(2)从步骤①提取粗盐常用____________(填“蒸发结晶”或“降温结晶”)方法。
(3) 从 酸 碱 反 应 的 角 度 分 析 , 步 骤 ④ 中 通 入 氨 气 的 作 用 是
________________________________________。
(4)步骤⑤所得的碳酸氢钠在生产和生活中有许多重要用途,请写出它的一种用途____________________。
(5)步骤⑥中发生反应的化学方程式为______________________,该反应类型属于
________反应。
类型2 工业生产
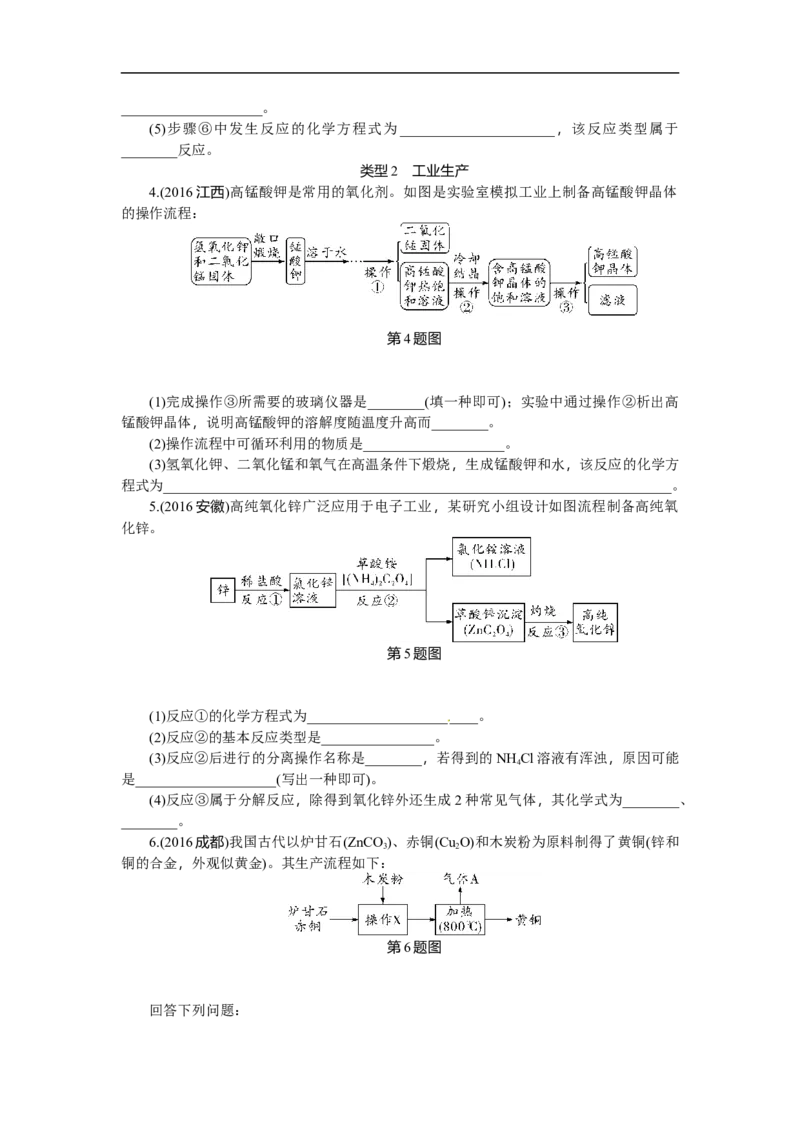
4.(2016江西)高锰酸钾是常用的氧化剂。如图是实验室模拟工业上制备高锰酸钾晶体
的操作流程:
第4题图
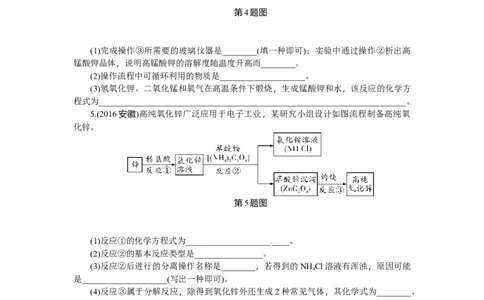
(1)完成操作③所需要的玻璃仪器是________(填一种即可);实验中通过操作②析出高
锰酸钾晶体,说明高锰酸钾的溶解度随温度升高而________。
(2)操作流程中可循环利用的物质是____________________。
(3)氢氧化钾、二氧化锰和氧气在高温条件下煅烧,生成锰酸钾和水,该反应的化学方
程式为________________________________________________________________________。
5.(2016安徽)高纯氧化锌广泛应用于电子工业,某研究小组设计如图流程制备高纯氧
化锌。
第5题图
(1)反应①的化学方程式为________________________。
(2)反应②的基本反应类型是________________。
(3)反应②后进行的分离操作名称是________,若得到的NH Cl溶液有浑浊,原因可能
4
是____________________(写出一种即可)。
(4)反应③属于分解反应,除得到氧化锌外还生成2种常见气体,其化学式为________、
________。
6.(2016成都)我国古代以炉甘石(ZnCO)、赤铜(Cu O)和木炭粉为原料制得了黄铜(锌和
3 2
铜的合金,外观似黄金)。其生产流程如下:
第6题图
回答下列问题:(1)赤铜中铜元素的化合价是________。
(2)黄铜的硬度比铜和锌都________(填“大”或“小”)。
(3)操作X的名称是________。
(4)加热时,发生的主要反应方程式为① ZnCO =====ZnO+CO↑、② 2ZnO+
3 2
C=====2Zn+CO↑、③____________________________(赤铜和木炭粉反应)。其中不属于
2
置换反应的是________(填反应序号)。
(5)气体A中,除二氧化碳外还有另一种生成气体,它的化学式是____________,该气
体的用途有________(写一条)。
(6) 鉴 别 黄 铜 和 黄 金 有 多 种 方 法 , 用 灼 烧 法 鉴 别 产 生 的 现 象 及 结 论 是
______________________________________。
7.(2016黄石)钛和钛合金被认为是21世纪的重要金属材料,被广泛用于火箭、导弹、
航天飞机、船舶等,如图为某化工企业生成钛流程示意图:
第7题图
请回答下列问题:
(1)FeTiO 中钛元素的化合价为________。
3
(2)① 中化学方程式为 2FeTiO +6C+7Cl=====2X+2TiCl +6CO,则 X 为
3 2 4
________(填化学式)。
(3)②中CO和H 以化学计量数 1∶2恰好完全反应,则该反应的基本反应类型是
2
____________________。
(4)③ 中氩气的作用是______________________,该步反应的化学方程式为
__________________________________。
8.(2016 株洲)铝和铝合金是一类重要的金属材料。工业上用铝土矿(含有 Al O 和
2 3
SiO,不考虑其他杂质)制取金属铝的基本流程如下:
2
第8题图
已知:①SiO 是一种难溶于水,也不与盐酸、硫酸反应的物质。
2
②铝盐与氨水反应,生成氢氧化铝沉淀和铵盐。
请回答下列问题:
(1)AlO 与稀硫酸反应的化学方程式为____________________。
2 3
(2)操作Ⅱ的名称是________。
(3)滤液Ⅱ中溶质的用途之一是________。
(4)电解熔融的Al O 除得到金属铝之外,还可得到的气体产物是________(填化学式)。
2 3
工业上在电解熔融的Al O 时,还加入了冰晶石(Na AlF)作熔剂,其作用是降低Al O 的熔
2 3 3 6 2 3
点。冰晶石在物质的分类中属于________(填字母)。A.酸 B.碱 C.盐 D.氧化物
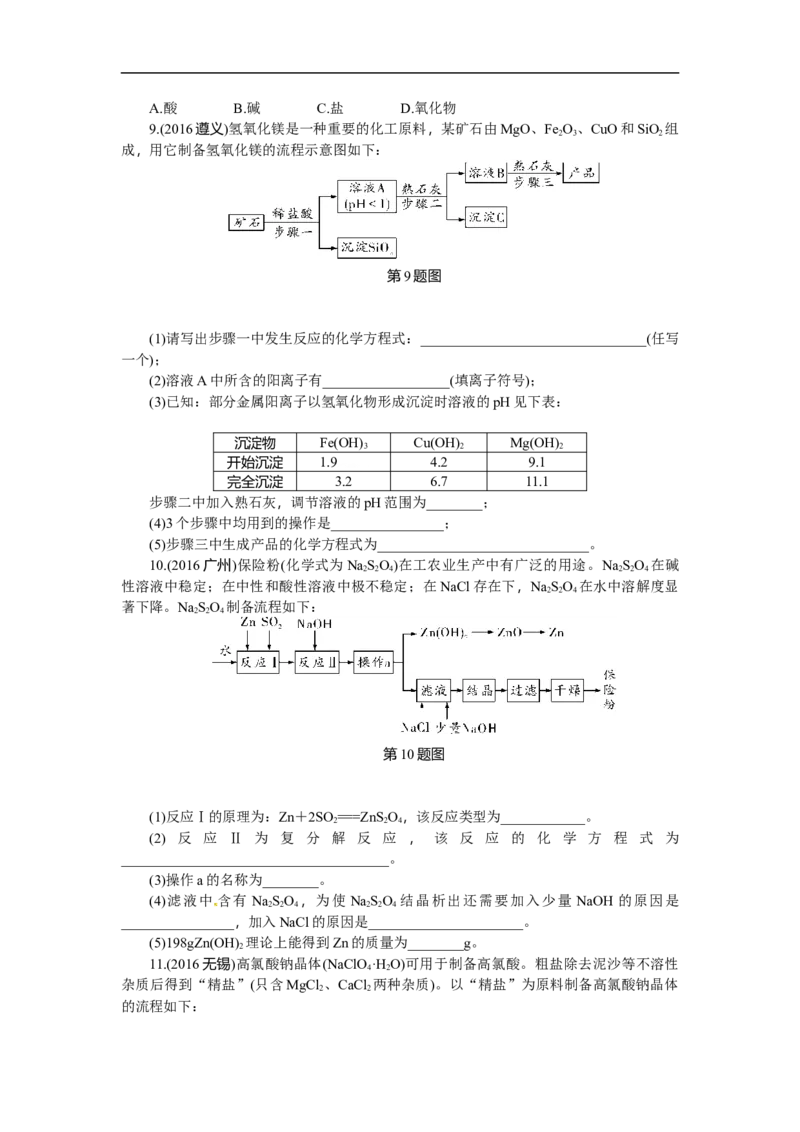
9.(2016遵义)氢氧化镁是一种重要的化工原料,某矿石由MgO、Fe O、CuO和SiO 组
2 3 2
成,用它制备氢氧化镁的流程示意图如下:
第9题图
(1)请写出步骤一中发生反应的化学方程式:________________________________(任写
一个);
(2)溶液A中所含的阳离子有__________________(填离子符号);
(3)已知:部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
沉淀物 Fe(OH) Cu(OH) Mg(OH)
3 2 2
开始沉淀 1.9 4.2 9.1
[来源:学_科_网Z_X_X_K]
完全沉淀 3.2 6.7 11.1
步骤二中加入熟石灰,调节溶液的pH范围为________;
(4)3个步骤中均用到的操作是________________;
(5)步骤三中生成产品的化学方程式为______________________________。
10.(2016广州)保险粉(化学式为NaSO)在工农业生产中有广泛的用途。NaSO 在碱
2 2 4 2 2 4
性溶液中稳定;在中性和酸性溶液中极不稳定;在NaCl存在下,NaSO 在水中溶解度显
2 2 4
著下降。NaSO 制备流程如下:
2 2 4
第10题图
(1)反应Ⅰ的原理为:Zn+2SO ===ZnS O,该反应类型为____________。
2 2 4
(2) 反 应 Ⅱ 为 复 分 解 反 应 , 该 反 应 的 化 学 方 程 式 为
______________________________________。
(3)操作a的名称为________。
(4)滤液中 含有 NaSO ,为使 NaSO 结晶析出还需要加入少量 NaOH 的原因是
2 2 4 2 2 4
________________,加入NaCl的原因是______________________。
(5)198gZn(OH) 理论上能得到Zn的质量为________g。
2
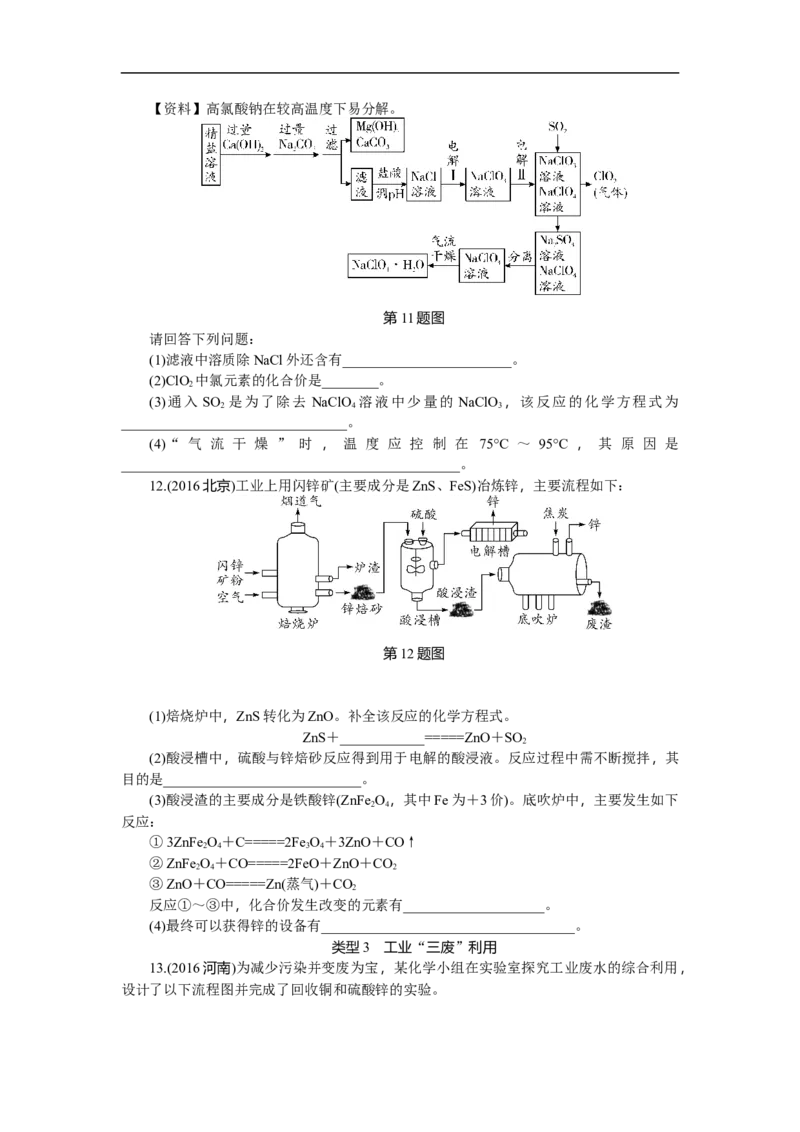
11.(2016无锡)高氯酸钠晶体(NaClO·H O)可用于制备高氯酸。粗盐除去泥沙等不溶性
4 2
杂质后得到“精盐”(只含MgCl 、CaCl 两种杂质)。以“精盐”为原料制备高氯酸钠晶体
2 2
的流程如下:【资料】高氯酸钠在较高温度下易分解。
第11题图
请回答下列问题:
(1)滤液中溶质除NaCl外还含有________________________。
(2)ClO 中氯元素的化合价是________。
2
(3)通入 SO 是为了除去 NaClO 溶液中少量的 NaClO ,该反应的化学方程式为
2 4 3
________________________________。
(4)“ 气 流 干 燥 ” 时 , 温 度 应 控 制 在 75°C ~ 95°C , 其 原 因 是
________________________________________________。
12.(2016北京)工业上用闪锌矿(主要成分是ZnS、FeS)冶炼锌,主要流程如下:
第12题图
(1)焙烧炉中,ZnS转化为ZnO。补全该反应的化学方程式。
ZnS+____________=====ZnO+SO
2
(2)酸浸槽中,硫酸与锌焙砂反应得到用于电解的酸浸液。反应过程中需不断搅拌,其
目的是____________________________。
(3)酸浸渣的主要成分是铁酸锌(ZnFe O ,其中Fe为+3价)。底吹炉中,主要发生如下
2 4
反应:
①3ZnFe O+C=====2Fe O+3ZnO+CO↑
2 4 3 4
②ZnFe O+CO=====2FeO+ZnO+CO
2 4 2
③ZnO+CO=====Zn(蒸气)+CO
2
反应①~③中,化合价发生改变的元素有____________________。
(4)最终可以获得锌的设备有____________________________________。
类型3 工业“三废”利用
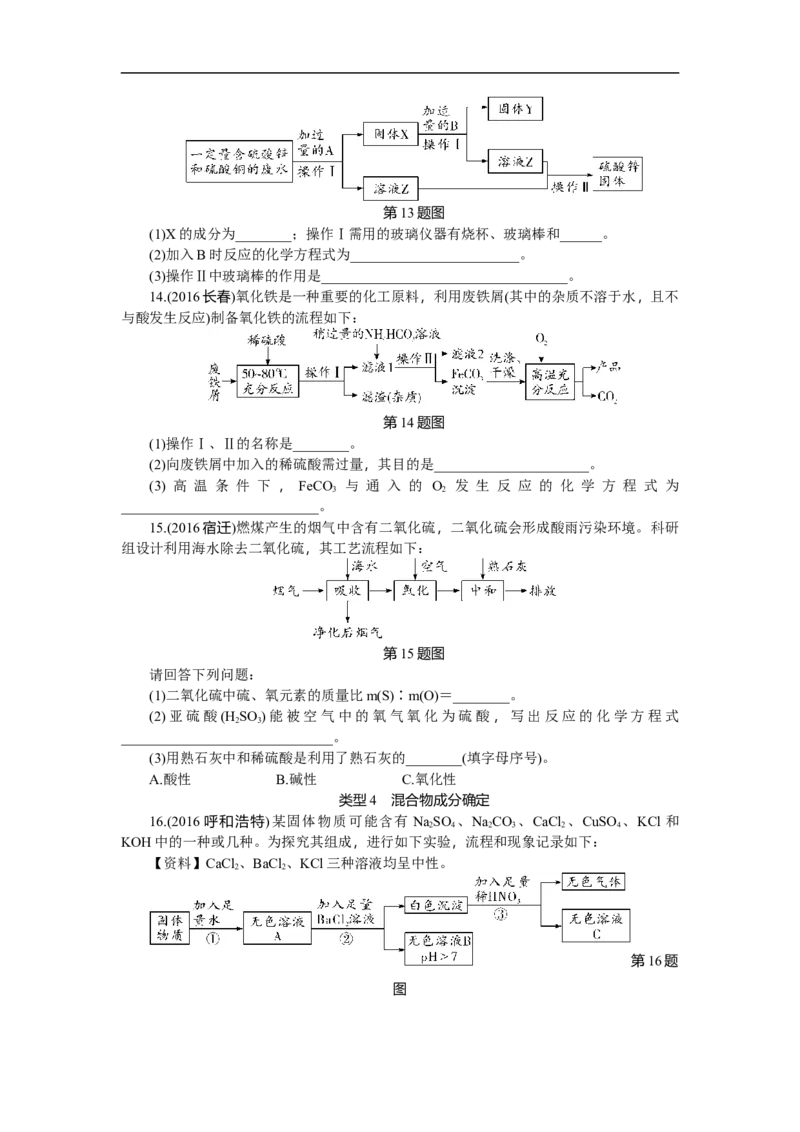
13.(2016河南)为减少污染并变废为宝,某化学小组在实验室探究工业废水的综合利用,
设计了以下流程图并完成了回收铜和硫酸锌的实验。第13题图
(1)X的成分为________;操作Ⅰ需用的玻璃仪器有烧杯、玻璃棒和______。
(2)加入B时反应的化学方程式为________________________。
(3)操作Ⅱ中玻璃棒的作用是___________________________________。
14.(2016长春)氧化铁是一种重要的化工原料,利用废铁屑(其中的杂质不溶于水,且不
与酸发生反应)制备氧化铁的流程如下:
第14题图
(1)操作Ⅰ、Ⅱ的名称是________。
(2)向废铁屑中加入的稀硫酸需过量,其目的是______________________。
(3) 高 温 条 件 下 , FeCO 与 通 入 的 O 发 生 反 应 的 化 学 方 程 式 为
3 2
____________________________。
15.(2016宿迁)燃煤产生的烟气中含有二氧化硫,二氧化硫会形成酸雨污染环境。科研
组设计利用海水除去二氧化硫,其工艺流程如下:
第15题图
请回答下列问题:
(1)二氧化硫中硫、氧元素的质量比m(S)∶m(O)=________。
(2)亚硫酸(H SO )能被空气中的氧气氧化为硫酸,写出反应的化学方程式
2 3
______________________________。
(3)用熟石灰中和稀硫酸是利用了熟石灰的________(填字母序号)。
A.酸性 B.碱性 C.氧化性
类型4 混合物成分确定
16.(2016 呼和浩特)某固体物质可能含有 NaSO 、NaCO 、CaCl 、CuSO 、KCl 和
2 4 2 3 2 4
KOH中的一种或几种。为探究其组成,进行如下实验,流程和现象记录如下:
【资料】CaCl 、BaCl 、KCl三种溶液均呈中性。
2 2
第16题
图(1)依据步骤①的实验现象得出固体物质中一定不含________(填化学式)。
(2)步骤②中发生反应的化学方程式为_____________________________。
(3)根据上述实验得出固体物质中一定含有____________(填化学式,下同),可能含有
________。为进一步确定可能含有的物质,采用的方法是______________________(写出实
验的操作、现象和结论)。
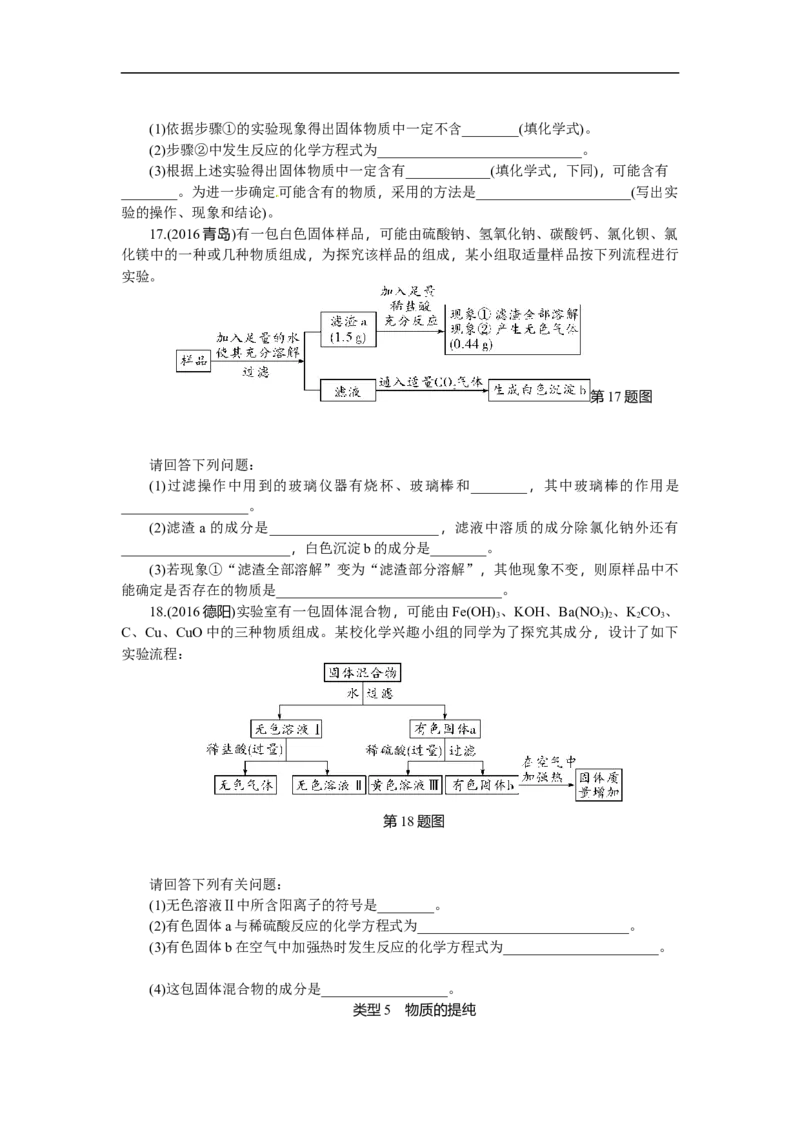
17.(2016青岛)有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯
化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行
实验。
第17题图
请回答下列问题:
(1)过滤操作中用到的玻璃仪器有烧杯、玻璃棒和________,其中玻璃棒的作用是
__________________。
(2)滤渣a的成分是________________________,滤液中溶质的成分除氯化钠外还有
________________________,白色沉淀b的成分是________。
(3)若现象①“滤渣全部溶解”变为“滤渣部分溶解”,其他现象不变,则原样品中不
能确定是否存在的物质是________________________________。
18.(2016德阳)实验室有一包固体混合物,可能由Fe(OH) 、KOH、Ba(NO ) 、KCO 、
3 3 2 2 3
C、Cu、CuO中的三种物质组成。某校化学兴趣小组的同学为了探究其成分,设计了如下
实验流程:
第18题图
请回答下列有关问题:
(1)无色溶液Ⅱ中所含阳离子的符号是________。
(2)有色固体a与稀硫酸反应的化学方程式为______________________________。
(3)有色固体b在空气中加强热时发生反应的化学方程式为______________________。
[来源:
Z,xx,k.Com]
(4)这包固体混合物的成分是__________________。
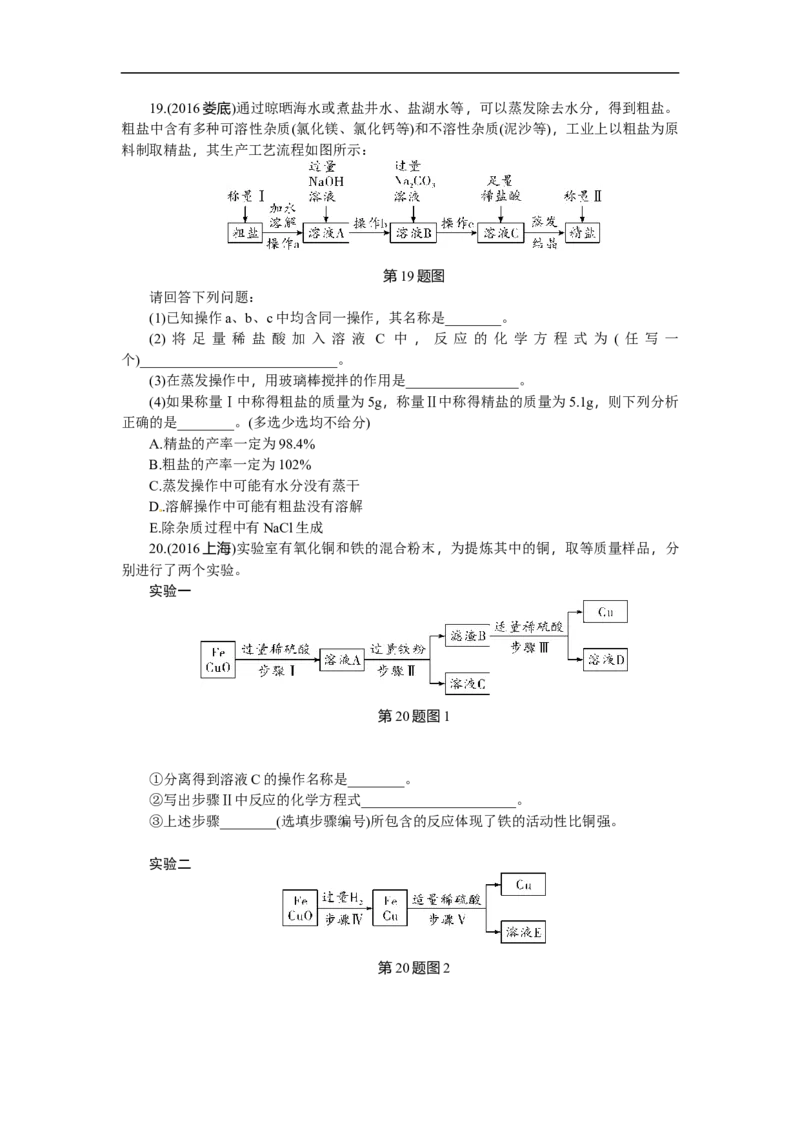
类型5 物质的提纯19.(2016娄底)通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分,得到粗盐。
粗盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等),工业上以粗盐为原
料制取精盐,其生产工艺流程如图所示:
第19题图
请回答下列问题:
(1)已知操作a、b、c中均含同一操作,其名称是________。
(2) 将 足 量 稀 盐 酸 加 入 溶 液 C 中 , 反 应 的 化 学 方 程 式 为 ( 任 写 一
个)____________________________。
(3)在蒸发操作中,用玻璃棒搅拌的作用是________________。
(4)如果称量Ⅰ中称得粗盐的质量为5g,称量Ⅱ中称得精盐的质量为5.1g,则下列分析
正确的是________。(多选少选均不给分)
A.精盐的产率一定为98.4%
B.粗盐的产率一定为102%
C.蒸发操作中可能有水分没有蒸干
D.溶解操作中可能有粗盐没有溶解
E.除杂质过程中有NaCl生成
20.(2016上海)实验室有氧化铜和铁的混合粉末,为提炼其中的铜,取等质量样品,分
别进行了两个实验。
实验一
第20题图1
①分离得到溶液C的操作名称是________。
②写出步骤Ⅱ中反应的化学方程式______________________。
③上述步骤________(选填步骤编号)所包含的反应体现了铁的活动性比铜强。
实验二
第20题图2④写出步骤Ⅳ中反应的化学方程式________________________。
⑤D、E是同一种溶质形成的溶液,请写出该溶质的名称、判断能否得出D、E溶液中
该 溶 质 质 量 的 大 小 关 系 并 说 明 理 由 :
____________________________________________________________________________。
21.(2016内江)为了除去铜粉中混有的铁粉,并用提纯的铜粉制取胆矾(CuSO ·5H O)。
4 2
某课外活动小组的同学按如下流程进行实验。(反应中部分生成物已略去)
第21题图
已知:Cu+2HSO (浓)=====CuSO +SO ↑+2HO。
2 4 4 2 2
回答下列有关问题:
(1)操作 a 的名称是__________;除去铜粉中的铁粉,最简便的实验方法是
________________。
(2)FeCl 溶 液 中 通 入 Cl 发 生 化 合 反 应 , 写 出 该 反 应 的 化 学 方 程 式
2 2
_______________________________。
(3)由 Cu 制 CuSO 溶液的途径Ⅱ中,若不通入 O ,反应将不会发生,原因是
4 2
__________________________________________。途径Ⅱ与途径Ⅰ相比较,其显著的优点
是____________________________(回答一点即可)。
(4)FeCl 溶液可腐蚀铜以制作印刷线路板,反应只生成两种常见的盐,则该反应的化学
3
方程式为______________________________________。
类型6 水的净化
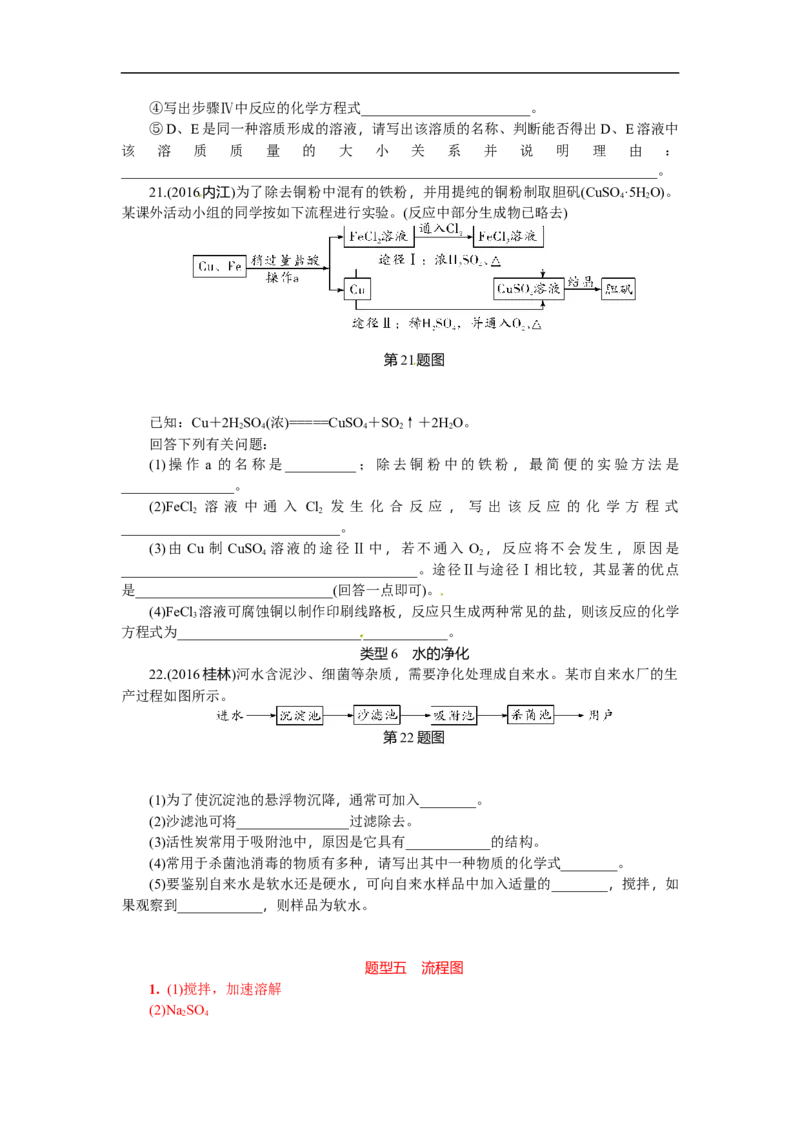
22.(2016桂林)河水含泥沙、细菌等杂质,需要净化处理成自来水。某市自来水厂的生
产过程如图所示。
第22题图
(1)为了使沉淀池的悬浮物沉降,通常可加入________。
(2)沙滤池可将________________过滤除去。
(3)活性炭常用于吸附池中,原因是它具有____________的结构。
(4)常用于杀菌池消毒的物质有多种,请写出其中一种物质的化学式________。
(5)要鉴别自来水是软水还是硬水,可向自来水样品中加入适量的________,搅拌,如
果观察到____________,则样品为软水。
题型五 流程图
1. (1)搅拌,加速溶解
(2)Na SO
2 4(3)CaCl 和BaCl
2 2 [来源:学科网]
(4)否
2. (1)CaO+HO=== Ca(OH) Ca(OH) +MgCl === Mg(OH) ↓+CaCl
2 2 2 2 2 2
(2)H 盐酸
2
(3)CaCl
2
3. (1)红
(2)蒸发结晶
(3)吸收更多的二氧化碳
(4)做发酵粉(或治疗胃酸过多,合理即可)
(5)2NaHCO ===== NaCO+HO+CO↑ 分解
3 2 3 2 2
4. (1)烧杯(或玻璃棒、漏斗等合理即可) 增大
(2)二氧化锰(或MnO )
2
(3)4KOH+2MnO +O===== 2KMnO +2HO
2 2 2 4 2
5. (1)Zn+2HCl=== ZnCl +H↑
2 2
(2)复分解反应
(3)过滤 滤纸破损(合理即可)
(4)CO CO
2
6. (1)+1
(2)大
(3)研磨
(4) 2Cu O+C===== 4Cu+CO↑ ①
2 2
(5)CO 作燃料(合理即可)
(6)表面变黑的是黄铜,不变色的是黄金
7. (1)+4
(2)FeCl
3
(3)化合反应
(4)作保护气 2Mg+TiCl ===== Ti+2MgCl
4 2
8. (1)Al O+3HSO === Al (SO )+3HO
2 3 2 4 2 4 3 2
(2)过滤
(3)作氮肥
(4)O C
2
9. (1)Fe O + 6HCl=== 2FeCl + 3HO(或CuO + 2HCl === CuCl + HO或
2 3 3 2 2 2
MgO + 2HCl === MgCl + HO)
2 2
(2)Cu2+、Fe3+、Mg2+、H+ (3)6.7~9.1 (4)过滤
(5)MgCl +Ca(OH) === Mg(OH) ↓+CaCl
2 2 2 2
10. (1)化合反应
(2) 2NaOH+ZnS O=== NaSO+Zn(OH) ↓
2 4 2 2 4 2
(3)过滤
(4)Na SO 在碱性溶液中稳定 降低NaSO 在水中的溶解度
2 2 4 2 2 4
(5)130
11. (1)氢氧化钠和碳酸钠
(2)+4
(3)2NaClO+SO === NaSO +2ClO
3 2 2 4 2
(4)温度过高,高氯酸钠易分解;温度过低,干燥不充分(或75 ℃~95 ℃,干燥充分且高氯酸钠晶体不易分解)
12. (1)2 3O 2 2
2
(2)使各反应物充分接触、加快反应速率
(3)C、Fe、Zn
(4)电解槽、底吹炉
13. (1)Zn和Cu(或锌和铜) 漏斗
(2)Zn+HSO === ZnSO+H↑
2 4 4 2
(3)不断搅拌,防止因局部温度过高,造成液滴飞溅
14. (1)过滤
(2)将废铁屑中铁完全反应
(3)4FeCO +O===== 2Fe O+4CO
3 2 2 3 2
15. (1)1∶1 (2)2H SO +O=== 2HSO (3)B
2 3 2 2 4
16. (1)CuSO
4
(2)BaCl +NaCO=== BaCO ↓+2NaCl
2 2 3 3
(3)Na CO 、KOH KCl 取少量无色溶液A于试管中,加入足量的稀硝酸,然后滴加
2 3
硝酸银溶液,产生白色沉淀,则固体中一定含有KCl,否则不含KCl
17. (1)漏斗 引流
(2)CaCO、Mg(OH) NaOH、BaCl BaCO
3 2 2 3
(3)MgCl
2
18.(1)K+、H+
(2)2Fe(OH) +3HSO === Fe (SO )+6HO
3 2 4 2 4 3 2
(3)2Cu+O===== 2CuO
2
(4)K CO、Fe(OH) 和Cu
2 3 3
19. (1)过滤
(2)NaOH+HCl=== NaCl+HO(或NaCO+2HCl=== 2NaCl+CO↑+HO)
2 2 3 2 2
(3)使液体受热均匀(或防止液体外溅)
(4)CE
20. ① 过滤
② Fe + HSO === FeSO + H↑、
2 4 4 2
Fe + CuSO === FeSO + Cu
4 4
③ Ⅱ、Ⅲ
④H+CuO ===== Cu + HO
2 2
⑤硫酸亚铁,D中FeSO 是步骤Ⅱ中多余的铁与稀硫酸反应所得,E中FeSO 是原混合
4 4
物中铁与稀硫酸反应所得,二者的大小关系不能确定
21. (1)过滤 用磁铁吸引
(2)2FeCl +Cl=== 2FeCl
2 2 3
(3)铜在金属活动性顺序表中排在氢的后面,不能和硫酸发生置换反应 不产生污染物
SO
2
(4)2FeCl +Cu=== 2FeCl +CuCl
3 2 2
22. (1)明矾
(2)泥沙
[来源:Z|xx|k.Com]
(3)疏松多孔
(4)ClO(或Cl)
2 2
(5)肥皂水 泡沫丰富