文档内容
第十讲 复分解反应
模块一 复分解反应的含义
知识精讲
1.复分解反应
NaCO + Ca(OH) == CaCO ↓ + 2NaOH
2 3 2 3
化合物 + 化合物 = 化合物 + 化合物
AB + CD = AD + BC
由两种化合物相互交换成分,生成另外两种化合物的反应,叫复分解反应。
复分解反应的特点
① 反应物、生成物只有两种化合物;
② 发生反应的两种化合物相互交换成分;
③ 各元素的化合价在反应前后均不改变。
思考与交流
判断下列反应是否属于复分解反应
(1)Fe+2HCl===FeCl +H ↑ ( )
2 2
△
(2)CO+CuO===CO+Cu( )
2
(3)NaOH+HCl═==NaCl+H O( )
2
(4)CuSO +2NaOH=Na SO +Cu(OH) ↓( )
4 2 4 2
(5)2NaOH+CO=Na CO+HO( )
2 2 3 2
(6)CaCO + 2HCl=CaCl +HO+CO↑( )
3 2 2 2
【答案】 √√ √
×× ×
及时小练
【练1】下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )A.用赤铁矿炼铁:FeO +4CO 3Fe+4CO 置换反应
3 4 2
B.用盐酸除铁锈:Fe O + 6HCl = 2FeCl +3H O 复分解反应
2 3 3 2
C.电解水发生的化学反应:2HO 2H↑+O ↑ 分解反应
2 2 2
D.熟石灰处理硫酸厂的污水:Ca(OH) + H SO = CaSO +2H O 中和反应
2 2 4 4 2
【答案】B
【练2】(2020·广东广州改编)叠氮酸(HN )常温下是一种无色液体,其水溶液具有酸性,可与NaOH
3
溶液反应得到叠氮化钠(NaN )。某些汽车安全气囊中装有叠氮化钠。
3
(1)试着写出叠氮酸与NaOH溶液的反应方程式: _______。
(2)叠氮酸与NaOH溶液的反应属于________(填反应类型)。
【答案】(1)HN+NaOH ==NaN +H O (2)复分解反应
3 3 2
【练3】漂白粉的主要成分为次氯酸钙[Ca(ClO) ]和氯化钙,即可用作漂白剂,又可用作消毒剂。漂白粉中
2
有效成分是[Ca(ClO) ],漂白的原理是:Ca(ClO) 在空气中发生反应
2 2
Ca(ClO) +CO +H O=CaCO +2HClO
2 2 2 3 ;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能
使品红等有色物质褪色。
(1)漂白粉是一种____________(填“纯净物”或“混合物”);
2HClO=2HCl+O
(2)HClO在常温下分解,反应为 2 。某瓶HClO溶液放置一段时间后,溶液的pH值
____________(填“增大”或“减小”或“不变”);
(3)在漂白粉中滴加盐酸,能加快漂白的速率。写出漂白粉中加入盐酸反应的化学方程式
_______________。该反应的基本反应类型是____________反应;
Ca(ClO) +2HCl=CaCl +2HClO
【答案】混合物 减小 2 2 复分解
【练4】我国第四套人民币硬币中含有金属镍(Ni),镍及其化合物能发生下列反应:
Ni+2HCl=NiCl +H
① 2 2 ;
NiO+2HCl=NiCl +H O
② 2 2 ;
NiO +4HCl=NiCl +Cl +2H O
③ 2 2 2 2
分析化学方程式,回答以下问题:
(1)金属镍(Ni)与硝酸银溶液反应的化学方程式为________。
(2)反应②属于基本反应类型中的_________反应。
(3)反应③中Ni的化合价在反应前后_______(填“不变”、“升高′“降低”)。
【答案】Ni+2AgNO ═Ni(NO )+2Ag 复分解 降低
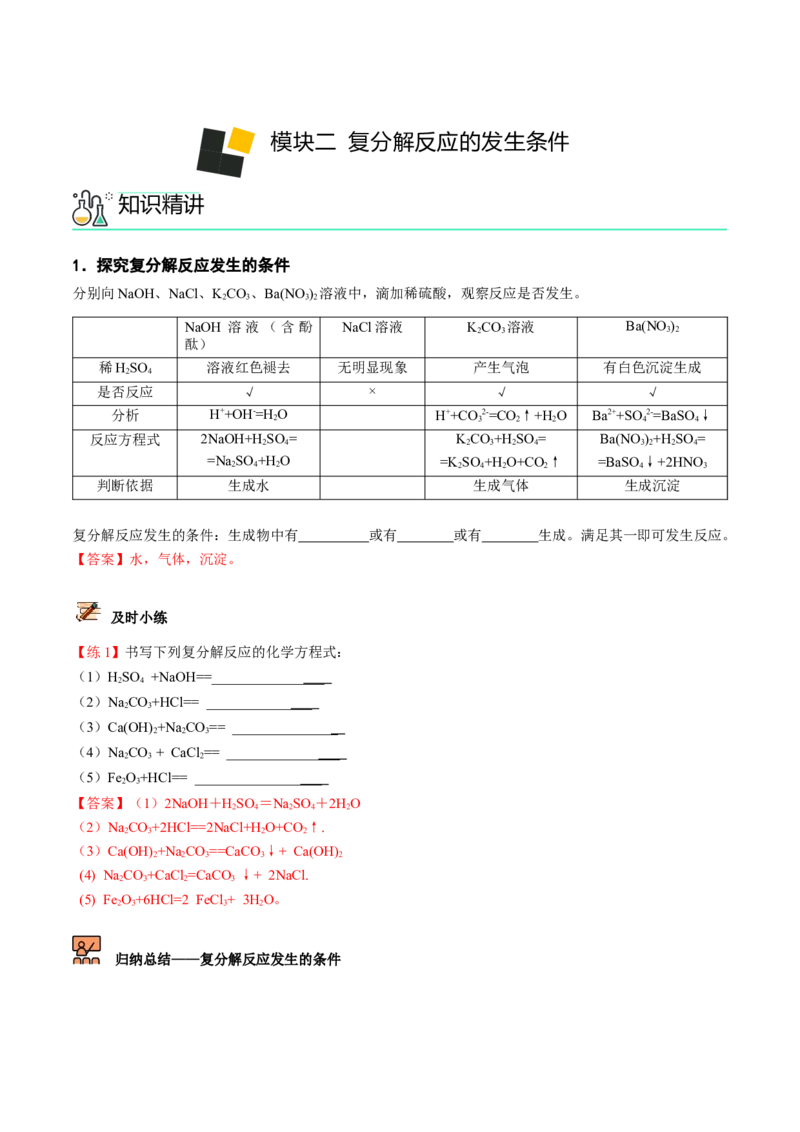
3 3 2模块二 复分解反应的发生条件
知识精讲
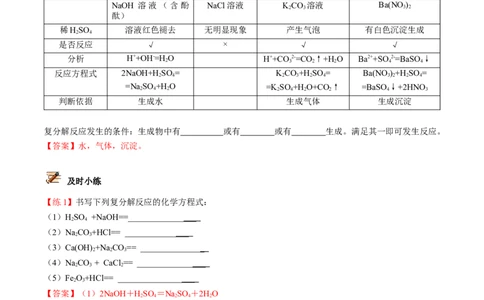
1.探究复分解反应发生的条件
分别向NaOH、NaCl、KCO、Ba(NO ) 溶液中,滴加稀硫酸,观察反应是否发生。
2 3 3 2
NaOH 溶液(含酚 NaCl溶液 KCO 溶液 Ba(NO )
2 3 3 2
酞)
稀HSO 溶液红色褪去 无明显现象 产生气泡 有白色沉淀生成
2 4
是否反应 √ × √ √
分析 H++OH-=H O H++CO 2-=CO ↑+H O Ba2++SO2-=BaSO ↓
2 3 2 2 4 4
反应方程式 2NaOH+H SO = KCO+H SO = Ba(NO )+H SO =
2 4 2 3 2 4 3 2 2 4
=Na SO +H O =KSO +H O+CO↑ =BaSO ↓+2HNO
2 4 2 2 4 2 2 4 3
判断依据 生成水 生成气体 生成沉淀
复分解反应发生的条件:生成物中有 或有 或有 生成。满足其一即可发生反应。
【答案】水,气体,沉淀。
及时小练
【练1】书写下列复分解反应的化学方程式:
(1)HSO +NaOH==________________
2 4
(2)NaCO+HCl== _______________
2 3
(3)Ca(OH) +Na CO== _______________
2 2 3
(4)NaCO + CaCl == ________________
2 3 2
(5)Fe O+HCl== __________________
2 3
【答案】(1)2NaOH+HSO =NaSO +2HO
2 4 2 4 2
(2)NaCO+2HCl==2NaCl+H O+CO↑.
2 3 2 2
(3)Ca(OH) +NaCO==CaCO ↓+ Ca(OH)
2 2 3 3 2
(4) NaCO+CaCl =CaCO ↓+ 2NaCl.
2 3 2 3
(5) Fe O+6HCl=2 FeCl+ 3HO。
2 3 3 2
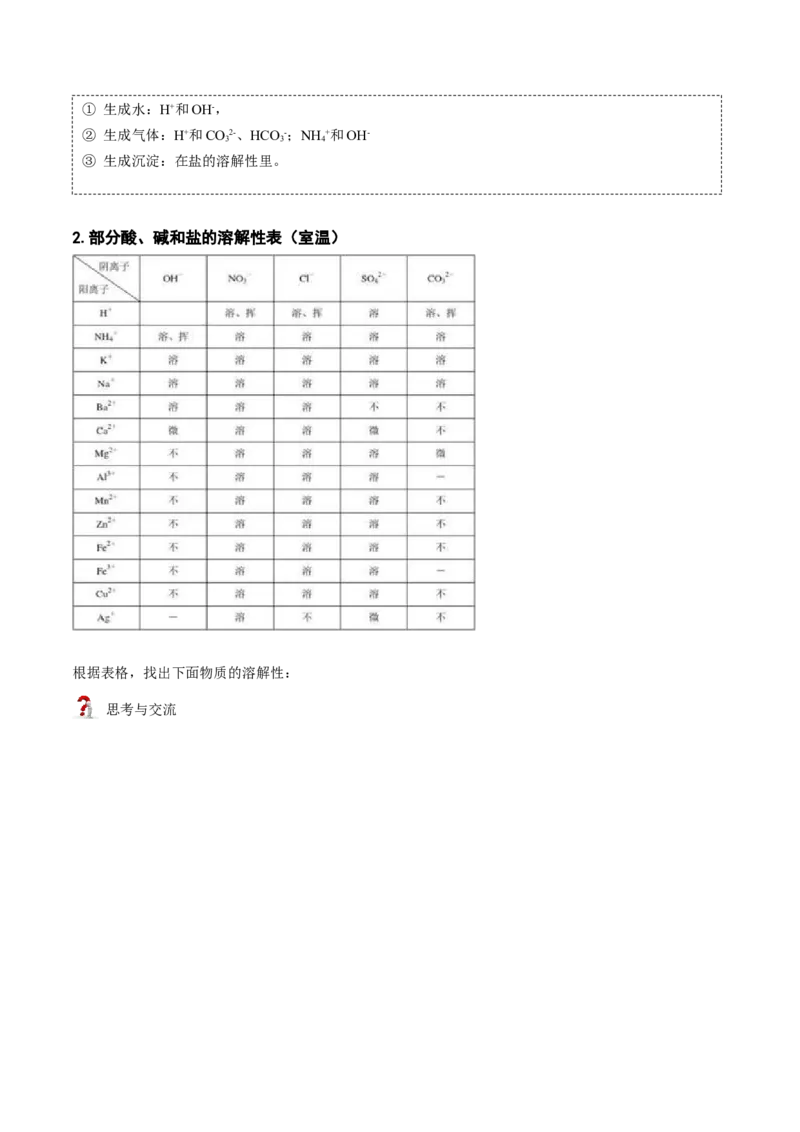
归纳总结——复分解反应发生的条件① 生成水:H+和OH-,
② 生成气体:H+和CO2-、HCO -;NH +和OH-
3 3 4
③ 生成沉淀:在盐的溶解性里。
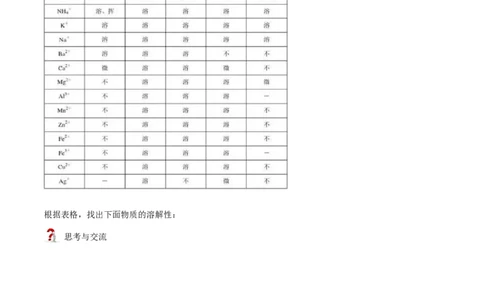
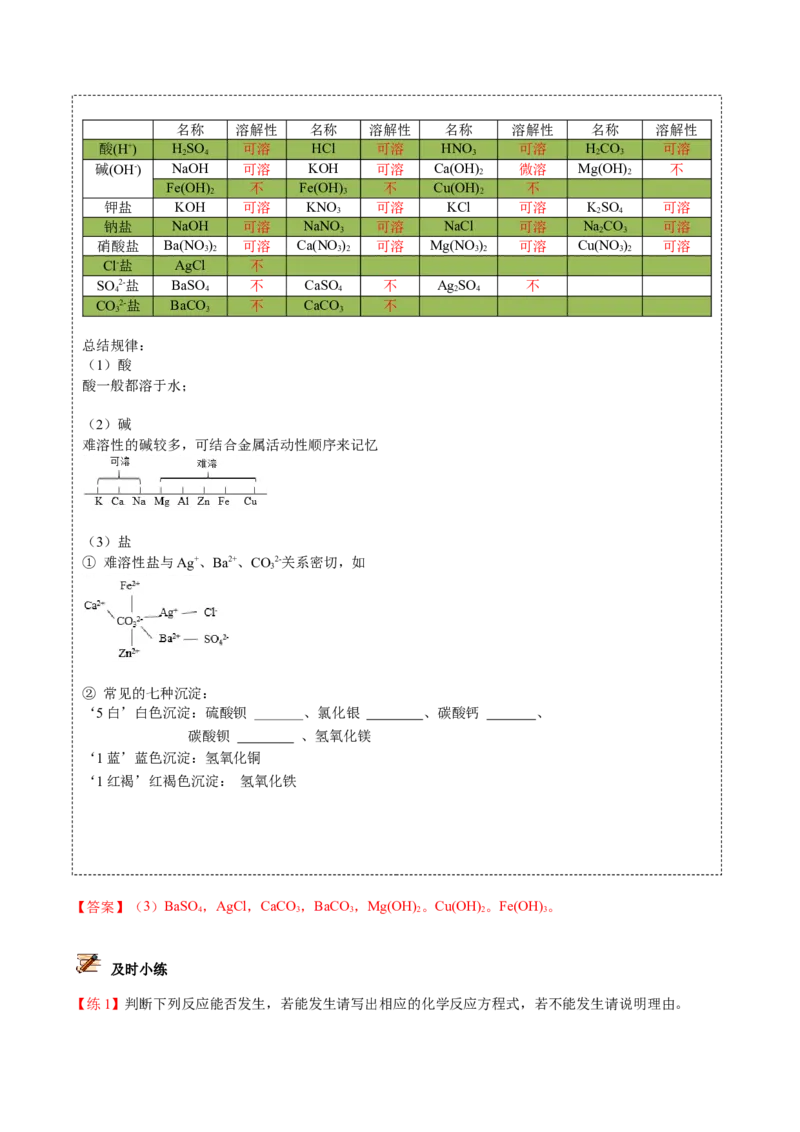
2.部分酸、碱和盐的溶解性表(室温)
根据表格,找出下面物质的溶解性:
思考与交流名称 溶解性 名称 溶解性 名称 溶解性 名称 溶解性
酸(H+) HSO 可溶 HCl 可溶 HNO 可溶 HCO 可溶
2 4 3 2 3
碱(OH-) NaOH 可溶 KOH 可溶 Ca(OH) 微溶 Mg(OH) 不
2 2
Fe(OH) 不 Fe(OH) 不 Cu(OH) 不
2 3 2
钾盐 KOH 可溶 KNO 可溶 KCl 可溶 KSO 可溶
3 2 4
钠盐 NaOH 可溶 NaNO 可溶 NaCl 可溶 NaCO 可溶
3 2 3
硝酸盐 Ba(NO ) 可溶 Ca(NO ) 可溶 Mg(NO) 可溶 Cu(NO ) 可溶
3 2 3 2 3 2 3 2
Cl-盐 AgCl 不
SO 2-盐 BaSO 不 CaSO 不 AgSO 不
4 4 4 2 4
CO2-盐 BaCO 不 CaCO 不
3 3 3
总结规律:
(1)酸
酸一般都溶于水;
(2)碱
难溶性的碱较多,可结合金属活动性顺序来记忆
(3)盐
① 难溶性盐与Ag+、Ba2+、CO2-关系密切,如
3
② 常见的七种沉淀:
‘5白’白色沉淀:硫酸钡 、氯化银 、碳酸钙 、
碳酸钡 、氢氧化镁
‘1蓝’蓝色沉淀:氢氧化铜
‘1红褐’红褐色沉淀: 氢氧化铁
【答案】(3)BaSO,AgCl,CaCO ,BaCO ,Mg(OH) 。Cu(OH) 。Fe(OH) 。
4 3 3 2 2 3
及时小练
【练1】判断下列反应能否发生,若能发生请写出相应的化学反应方程式,若不能发生请说明理由。1. AgNO + NaCl ==
3
2. Cu(OH) + HCl ==
2
3. KNO + CuSO ==
3 4
4. KOH + Na SO ==
2 4
5. NaCl + H SO ==
2 4
6. FeCl + NaCl ==
3
【答案】(1)AgCl +NaNO ;(2)CuCl + H O;(3)不反应;
3 2 2
(4)不反应;(5)不反应;(6)不反应。
【练2】根据复分解反应原理完成下列方程式:
(1)NaCl+ == +NaNO (2)CuSO + == +CuCl
3 4 2
(3)HSO + ==Na SO + + (4) + HCl== + H O
2 4 2 4 2
(5) + NaOH== + Fe(OH) ↓ (6)_______ + ______ = AgCl↓ + ______
3
(7)NaCO + ________ = NaOH + _________
2 3
【答案】(1)AgNO ,AgCl↓;(2)BaCl,BaSO↓;(3)NaOH,HO;
3 2 4 2
(4)NaOH,NaCl;(5)FeCl,NaCl;(6)AgNO ,NaCl,NaNO ;(7)Ca(OH) ,CaCO↓。
3 3 3 2 3
【练3】下列复分解反应不能发生的是( )
A.氯化钾和硫酸钠 B.氯化钡和硫酸钠 C.硝酸银和氯化钾 D.氯化钙和碳酸钠
【答案】A
【练4】利用所给的物质写出满足要求的如下反应方程式:
硫酸铜溶液 氢氧化钠溶液 氯化钡溶液 稀硫酸 氯化铁溶液 碳酸钠溶液
(1)有蓝色沉淀产生的是 。
(2)有红褐色沉淀产生的是 。
(3)有白色沉淀产生的是 。
(4)有水生成的是 。
(5)有气体生成的是 。
【答案】(1)CuSO +2NaOH=Cu(OH) ↓+Na SO ;(2)FeCl+3NaOH=Fe(OH) ↓+3NaCl;
4 2 2 4 3 3
(3)BaCl+Na CO=BaCO ↓+2NaCl;(4)2NaOH+H SO =Na SO4+2H O;
2 2 3 3 2 4 2 2
(5)NaCO+H SO =Na SO +H O+CO↑
2 3 2 4 2 4 2 2
经典例题
复分解反应的原理
【例1】(2017·广东广州)向KCO 溶液中滴入Ba(OH) 溶液至恰好完全反应。
2 3 2
(1)可以观察到的实验现象是________________。
(2)下图表示该反应前后溶液中存在的主要离子,写出每种图形代表的离子。(填离子符号)________ ________ ________
(3)下列物质能与KCO 溶液反应产生类似上述实验现象的是________。
2 3
A.Ca(OH) B.HCl C.BaCl D.(NH )SO
2 2 4 2 4
【答案】有白色沉淀生成 K+ CO2- OH- AC
3
【详解】
(1)碳酸钾和氢氧化钡反应生成白色沉淀碳酸钡和氢氧化钾溶液,因此可以观察到的实验现象是产生白色沉
淀;
(2) 碳酸钾和氢氧化钡反应生成白色沉淀碳酸钡和氢氧化钾溶液,反应后溶液中没有钡离子和碳酸根离子,
由图中信息可知,, 表示 K+, 表示CO2-, 表示 OH-;
3
(3)碳酸钾能和氢氧化钙反应生成白色沉淀碳酸钙和氢氧化钾溶液,和氯化钡反应生成白色沉淀碳酸钡和氯
化钾溶液,因此下列物质能与KCO 溶液反应产生类似上述实验现象的是Ca(OH) 和BaCl 。
2 3 2 2
故选AC。
【例2】(2018·广东广州)将下列各组中的两种溶液混合(溶液中的原有的水分子忽略不写):
编号 反应物1 反应物2 混合后存在的粒子
A 稀盐酸(H+、Cl-) 氢氧化钾溶液(K+、OH-) K+、Cl-、HO
2
B Na+、SO 2-、Cu(OH)
4 2
C 氯化钠溶液(Na+、Cl-) 稀硫酸(H+、SO 2-) H+、SO 2- 、Na+、Cl-
4 4
(1)A组发生化学变化,化学方程式为____________________。实质是反应物1中的_____(填粒子符号,下
同)与反应物2中的_____结合形成______。
(2)B组发生化学变化,且B组反应物1是盐的水溶液,反应物2是碱的水溶液,则B组中反应物1是
___________(填名称,下同),反应物2是__________________;
(3)C组没有发生化学反应,原因是(微观角度解释):______________________________。
【答案】HCl + KOH = KCl + H O H+ OH- H O 硫酸铜溶液 氢氧化钠溶液 混合前
2 2
后溶液中的离子没有结合成新的分子【例3】用一种试剂就能把NaCl、NH Cl、NaSO 三种溶液区别开,这种试剂是( )
4 2 4
A.AgNO 溶液 B.NaOH溶液 C.BaCl 溶液 D.Ba(OH) 溶液
3 2 2
【答案】D
【例4】下列物质混合后能发生反应,且实验现象明显的是( )
A.向碳酸钙中滴入氯化钡溶液 B.向氢氧化钾溶液中滴入氯化钡溶液
C.向铁粉中滴入氢氧化钠溶液 D.向氧化铝中滴入稀硝酸
【答案】D
【详解】
A.碳酸钙与氯化钡不发生化学反应,则向碳酸钙中滴入氯化钡溶液,无明显现象,故A错误;
B.氢氧化钾与氯化钡不发生化学反应,则向氢氧化钾溶液中滴入氯化钡溶液,无明显现象,故B错误;
C.铁粉能与酸反应,不能与碱反应,则向铁粉中滴入氢氧化钠溶液,无明显现象,故C错误;
D.金属氧化物能与酸反应生成盐和水,则氧化铝能与硝酸反应生成硝酸铝和水,现象为白色固体溶解,故
D正确;
综上所述,答案为D。
【例5】下列各组物质中,能发生复分解反应且反应前后溶液总质量变小的是( )
A.硝酸钡和氯化钾 B.硫酸和氢氧化钠
C.稀盐酸和碳酸钠 D.锌和硫酸铜
【答案】C
【详解】
A、硝酸钡和氯化钾不能反应,不符合题意;
B、硫酸和氢氧化钠反应生成硫酸钠和水,反应前后溶液总质量不变,不符合题意;
C、稀盐酸和碳酸钠反应生成氯化钠、二氧化碳和水,有气体跑出,所以溶液总质量减小,符合题意;
D、锌和硫酸铜反应生成硫酸锌和铜,化学方程式为: ,该反应属于置换反应,
不符合题意。故选C。
【例6】盐酸溶液中含有H+,能使石蕊溶液变红。在滴有紫色石蕊的稀盐酸中,分别加入过量的下列物质,
溶液仍为红色的是( )
A.CaO B.NaOH C.NaCO D.AgNO
2 3 3
【答案】D
【详解】
A、由于氧化钙过量,CaO会先和稀盐酸反应生成氯化钙和水,再和水反应生成氢氧化钙,最终溶液显碱
性,溶液红色会变为蓝色,不符合题意;
B、过量的NaOH会和稀盐酸发生中和反应生NaCl和水,氢氧化钠过量,最终溶液显碱性,溶液红色会变
为蓝色,不符合题意;
C、过量的NaCO 与稀盐酸反应生NaCl、二氧化碳和水,NaCO 溶液水解显碱性,溶液会变蓝,不符合
2 3 2 3
题意;D、过量的AgNO 与稀盐酸反应生成AgCl沉淀和硝酸,硝酸银过量但显中性,硝酸显酸性,最终溶液显
3
酸性,溶液仍然呈红色,符合题意。故选D。
复分解反应的类型
【例1】(2020·广东广州市·中考真题)下列实验中有化学反应发生,且能观察到明显现象的是( )
A.向氯化钾溶液中滴入稀硫酸
B.向硫酸钠溶液中滴入氯化锌溶液
C.向氧化铜粉末中滴入氢氧化钠溶液
D.高温下向氧化铁粉末中通入一氧化碳
【答案】D
【详解】
A、向氯化钾溶液中滴入稀硫酸,不反应,无明显现象,故选项错误;
B、向硫酸钠溶液中滴入氯化锌溶液,不反应,无明显现象,故选项错误;
C、向氧化铜粉末中滴入氢氧化钠溶液,不反应,无明显现象,故选项错误;
D、高温下向氧化铁粉末中通入一氧化碳,一氧化碳和氧化铁反应生成铁和二氧化碳,红棕色固体会变成
黑色,故选项正确。
故选D。
【例2】(2020·广东深圳市)如图,将胶头滴管中的物质X 滴入装有物质Y 的试管中,两物质充分反应。
下列说法错误的是( )
A.X 为稀硫酸,若反应有气泡产生,则生成的气体一定是H
2
B.X 为AgNO 溶液,Y 为Cu片,根据现象可判断金属活动性:Cu>Ag
3
C.X 为BaCl 溶液,Y 为NaSO 溶液,反应产生白色沉淀
2 2 4
D.X 为稀盐酸,Y 为Al(OH) ,该反应可应用于治疗胃酸过多症
3
【答案】A
【详解】
A、稀硫酸和碳酸盐反应能生成气体二氧化碳,生成的气体不一定是氢气,A错。
B、活动性强的金属可知置换活动性弱的金属,X 为AgNO 溶液,Y 为Cu片,铜可以置换出银,根据现
3
象可判断金属活动性:Cu>Ag,B正确。
C、氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,现象是产生白色沉淀,C正确。
D、氢氧化铝和稀盐酸反应生成氯化铝和水,该反应是氢氧化铝治疗胃酸的反应,D正确。
故选:A。【例3】下列关于氢氧化钠的认识,正确的是( )
A.组成:含有钠单质和氢氧根离子
B.性质:与氢氧化钡相似,能与硫酸钾溶液反应
C.用途:与硫酸铜等配制成具有杀菌作用的波尔多液
D.制备:通过氢氧化钙溶液与碳酸钠溶液反应制得
【答案】D
【详解】
A、氢氧化钠是由钠离子和氢氧根离子构成的,不含钠单质,故选项说法错误。
B、与氢氧化钡相似,但不能与硫酸钾溶液反应,因为与硫酸钾溶液混合没有沉淀、气体或水生成,故选
项说法错误。
C、氢氧化钠不能与硫酸铜等配制成具有杀菌作用的波尔多液,氢氧化钙能与硫酸铜等配制成具有杀菌作
用的波尔多液,故选项说法错误。
D、氢氧化钙溶液与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,可通过氢氧化钙溶液与碳酸钠溶液反应
制得氢氧化钠,故选项说法正确。
故选:D。
【例4】下列各组物质分别加入足量的水中,能得到透明溶液的是( )
A.FeCl 、NaOH、NaCl
3
B.NaSO 、HCl、BaCl
2 4 2
C.CuSO 、KCl、MgCl
4 2
D.NaCO、MgCl 、NaSO
2 3 2 2 4
【答案】C
【详解】
A、 氯化铁和氢氧化钠反应生成氢氧化铁沉淀和氯化钠,不符合题意;
B、硫酸钠和氯化钡反应生成硫酸钡沉淀和氯化钠,不符合题意;
C、这三种物质不反应,溶液是透明溶液,符合题意;
D、 碳酸钠和氯化镁反应生成碳酸镁沉淀和氯化钠,不符合题意。故选C。
专项训练
【训1】下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )
A.金属铝放罝在空气中形成氧化膜4Al+3O ═2A1 O 氧化反应
2 2 3
B.用氢氧化铝治疗胃酸过多症A1(OH) +3HCl=A1Cl +H O复分解反应
3 3 2
C.比较铜和银的活动性强弱Cu+2AgCl=CuCl +2Ag置换反应
2
D.用盐酸除铁锈Fe O+6HC1=2FeCl +3H O复分解反应
2 3 3 2
【答案】D【训2】下列试剂中,能将Ca(OH) 、HSO 、NaSO 三种溶液一次鉴别出来的是( )
2 2 4 2 4
A.酚酞溶液 B.MgCl 溶液
2
C.Ba(OH) 溶液 D.NaCO 溶液
2 2 3
【答案】D
【详解】
A、酚酞溶液遇Ca(OH) 、HSO 、NaSO 三种溶液,分别显红色、无色、无色,不会出现三种不同现象,
2 2 4 2 4
无法鉴别,故A不符合题意;
B、MgCl 溶液与Ca(OH) 溶液反应生成氢氧化镁白色沉淀,与HSO 、NaSO 溶液均不反应,不会出现三
2 2 2 4 2 4
种不同现象,无法鉴别,故B不符合题意;
C、Ba(OH) 溶液与Ca(OH) 溶液不反应,与HSO 、NaSO 溶液反应均生成硫酸钡白色沉淀,不会出现三
2 2 2 4 2 4
种不同现象,无法鉴别,故C不符合题意;
D、NaCO 溶液与氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,与稀硫酸反应生成硫酸钠、水和二氧化
2 3
碳,与硫酸钠溶液不反应,无明显现象,会出现三种不同现象,可以鉴别出来,故D符合题意。
故选D。
【训3】将下列各组物质分别同时加入到水中,得到无色透明溶液的是( )
A.CuSO Na SO NaOH B.KSO Ba(OH) HNO
4 2 4 2 4 2 3
C.KOH MgSO KNO D.KCl K SO KNO
4 3 2 4 3
【答案】D
【详解】
A、CuSO 能与NaOH溶液反应生成氢氧化铜蓝色沉淀,溶液变浑浊不能得到无色透明溶液,故选项错误;
4
B、KSO 、Ba(OH) 在溶液反应生成不溶于酸的硫酸钡白色沉淀,溶液变浑浊不能得到无色透明溶液,
2 4 2
故选项错误;
C、MgSO 能与KOH在溶液反应生成氢氧化镁白色沉淀,溶液变浑浊,不能得到无色透明溶液,故选项错
4
误;
D、三者之间不反应且不存在有色离子符合无色透明的要求,故选项正确;
故选D。
【训4】下列物质混合没有明显现象的是( )
A.向稀盐酸中加入澄清石灰水
B.氧化铜粉末中加入稀硫酸
C.向碳酸钾溶液中滴入足量的氯化镁溶液
D.烧碱固体中加入水
【答案】A
【详解】
A、向稀盐酸中加入澄清石灰水,氢氧化钙与稀盐酸反应生成氯化钙和水,无明显现象,符合题意;
B、氧化铜粉末中加入稀硫酸,氧化铜与稀硫酸反应生成硫酸铜和水,黑色粉末逐渐溶解,溶液由无色变
为蓝色,不符合题意;C、向碳酸钾溶液中滴入足量的氯化镁溶液,碳酸钾与氯化镁反应生成碳酸镁,碳酸镁微溶于水,会产生
白色沉淀,不符合题意;
D、烧碱是氢氧化钠的俗称,氢氧化钠固体溶于水放出大量的热,使溶液温度升高,不符合题意。
故选A。
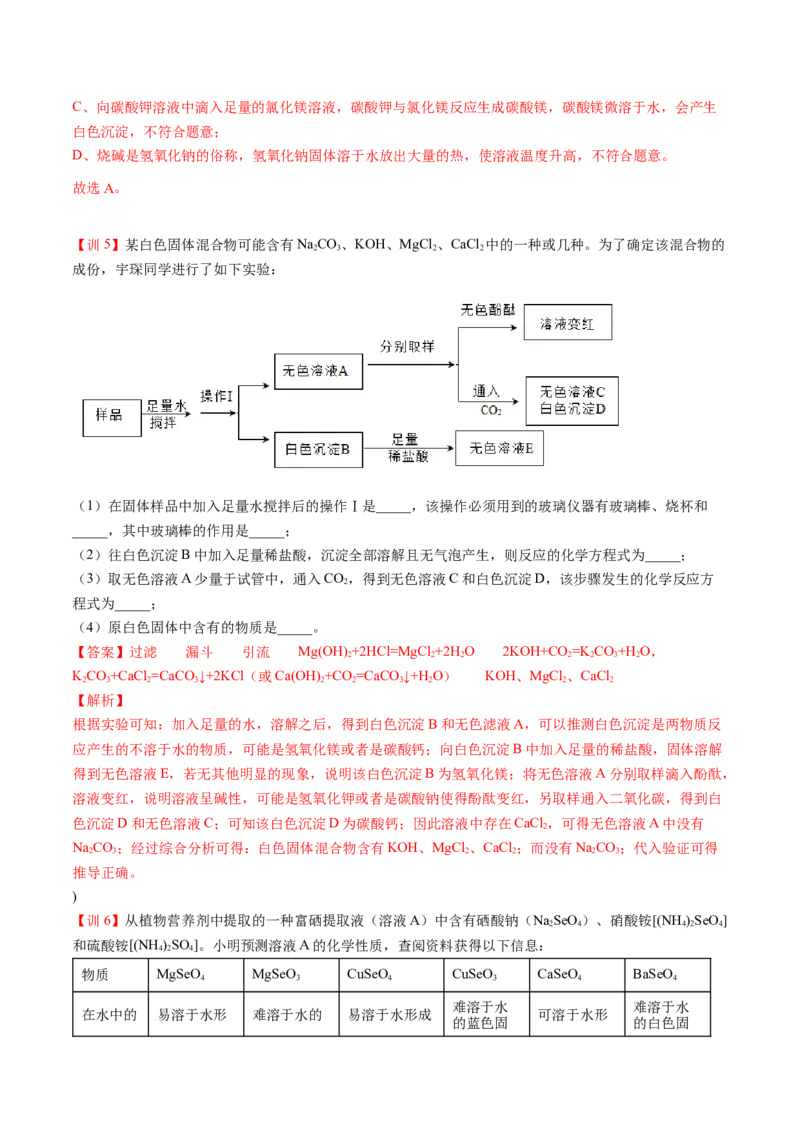
【训5】某白色固体混合物可能含有NaCO、KOH、MgCl 、CaCl 中的一种或几种。为了确定该混合物的
2 3 2 2
成份,宇琛同学进行了如下实验:
(1)在固体样品中加入足量水搅拌后的操作Ⅰ是_____,该操作必须用到的玻璃仪器有玻璃棒、烧杯和
_____,其中玻璃棒的作用是_____;
(2)往白色沉淀B中加入足量稀盐酸,沉淀全部溶解且无气泡产生,则反应的化学方程式为_____;
(3)取无色溶液A少量于试管中,通入CO,得到无色溶液C和白色沉淀D,该步骤发生的化学反应方
2
程式为_____;
(4)原白色固体中含有的物质是_____。
【答案】过滤 漏斗 引流 Mg(OH) +2HCl=MgCl +2H O 2KOH+CO =K CO+H O,
2 2 2 2 2 3 2
KCO+CaCl =CaCO ↓+2KCl(或Ca(OH) +CO =CaCO ↓+H O) KOH、MgCl 、CaCl
2 3 2 3 2 2 3 2 2 2
【解析】
根据实验可知:加入足量的水,溶解之后,得到白色沉淀B和无色滤液A,可以推测白色沉淀是两物质反
应产生的不溶于水的物质,可能是氢氧化镁或者是碳酸钙;向白色沉淀B中加入足量的稀盐酸,固体溶解
得到无色溶液E,若无其他明显的现象,说明该白色沉淀B为氢氧化镁;将无色溶液A分别取样滴入酚酞,
溶液变红,说明溶液呈碱性,可能是氢氧化钾或者是碳酸钠使得酚酞变红,另取样通入二氧化碳,得到白
色沉淀D和无色溶液C;可知该白色沉淀D为碳酸钙;因此溶液中存在CaCl ,可得无色溶液A中没有
2
NaCO;经过综合分析可得:白色固体混合物含有KOH、MgCl 、CaCl ;而没有NaCO;代入验证可得
2 3 2 2 2 3
推导正确。
)
【训6】从植物营养剂中提取的一种富硒提取液(溶液A)中含有硒酸钠(NaSeO)、硝酸铵[(NH )SeO]
2 4 4 2 4
和硫酸铵[(NH )SO ]。小明预测溶液A的化学性质,查阅资料获得以下信息:
4 2 4
物质 MgSeO MgSeO CuSeO CuSeO CaSeO BaSeO
4 3 4 3 4 4
难溶于水 难溶于水
在水中的 易溶于水形 难溶于水的 易溶于水形成 可溶于水形
的蓝色固 的白色固溶解性 成无色溶液 白色固体 蓝色溶液 体 成无色溶液 体
小明预测溶液A能与含Cu2+的可溶性盐反应,判断该预测是否合理并说明理由:_____。
请根据所学知识及限选试剂,继续预测溶液A其他化学性质,说明预测的依据,并设计实验验证。限选试
剂:溶液A、CuSO 溶液、Mg(NO ) 溶液、Ca(NO ) 溶液、BaCl 溶液。
4 3 2 3 2 2
预测 预测的依据 验证预测的实验操作与预期现象
能够与_____(填物质类 取少量溶液A于试管中,_____,如果观察
_____。
别)反应 到_____,则预测成立。
【答案】不合理,理由是:CuSeO 是易溶于水的蓝色溶液,不符合复分解反应发生的条件; 含Ba2+的
4
可溶性盐 BaSeO 是难溶于水的白色沉淀 滴加BaCl 溶液 产生白色沉淀
4 2
模块三 复分解反应的应用
知识精讲
1.检验
常见离子的检验
物质 试剂、方法 实验现象
酸(H+) ①滴加紫色石蕊试液;②pH试纸;③加入Zn粒 ①变 红 ;②pH<7;③产生 气泡
①滴加紫色石蕊试液;②滴加无色酚酞试液;
碱(OH-) ①变 蓝 ;②变 红 ;③pH>7
③pH试纸
Cl- 加入AgNO 溶液和稀硝酸 产生白色沉淀,且白色沉淀不溶解
3
SO 2- 加入稀盐酸酸化后再加入BaCl 溶液 酸化后无现象,加入BaCl 后产生白色沉淀
4 2 2
CO2- 加入稀盐酸,将产生的气体通入澄清的石灰水中 有无色无味气体产生,石灰水变浑浊
3
加入强碱,加热,将产生的气体用湿润红色石蕊
NH + 产生有刺激性气味的气体,试变蓝
4 试纸检验
Fe3+ 加入强碱溶液 产生红褐色沉淀
Cu2+ 插入铁丝(或加入强碱溶液) 铁丝附有红色物质(或产生蓝色沉淀)经典例题
检验
【例1】有一包白色固体样品,可能含有氯化钠、碳酸钠、硫酸钾、氢氧化钡中的一种或几种,为确定其
组成,进行如下实验:
步骤Ⅰ:取少量样品于烧杯中,加足量水,充分搅拌,静置,有固体剩余。
步骤Ⅱ:取步骤Ⅰ所得上层清液于试管中,滴入几滴酚酞溶液,溶液变红色;再滴入足量稀硫酸,无气泡
或沉淀产生,溶液由红色逐渐变成无色。
步骤Ⅲ:取步骤I所得固体于试管中,滴入稀盐酸溶液,有气泡产生,固体无剩余。
回答下列问题:
(1)步骤Ⅰ中发生反应的化学方程式是___;步骤Ⅱ中发生反应的化学方程式是__。
(2)综合以上实验,可以推知样品中肯定没有_____,可能有_____(填化学式)。
(3)若要进一步确定样品的组成,还需进行的实验是_____。
【答案】 KSO
2 4
NaCl 取步骤I所得上层清液于试管中,加入足量稀硝酸,再滴入硝酸银,振荡,观察现象。若有白色
沉淀,则样品组成中有NaCl;若没有明显现象,则样品组成中没有NaCl
【详解】
解:步骤Ⅰ:取少量样品于烧杯中,加足量水,充分搅拌,静置,有固体剩余,因此固体可能是碳酸钡或
硫酸钡或碳酸钡和硫酸钡的混合物;
步骤Ⅱ:取步骤I所得上层清液于试管中,滴入几滴酚酞溶液,溶液变红色;再滴入足量稀硫酸,无气泡
或沉淀产生,红色逐渐褪去,得到无色溶液,因此上层清液中有氢氧化钠,没有碳酸钠;
步骤Ⅲ:取步骤I所得固体于试管中,滴入稀盐酸,有气泡产生,固体无剩余,说明固体只有碳酸钡,原
固体样品一定有碳酸钠和氢氧化钡,不含有硫酸钾,氯化钠不能确定。
(1)综上所述分析:步骤Ⅰ中说明含有氢氧化钡和碳酸钠;反应的化学方程式为NaCO+Ba(OH)
2 3
═BaCO ↓+2NaOH;步骤Ⅱ中发生反应是氢氧化钠和稀硫酸反应生成硫酸钠和水,反应的化学方程式是
2 3
2NaOH+H SO ═NaSO +2H O;
2 4 2 4 2
(2)综合以上实验,可以推知样品中肯定没有KSO ;可能含有NaCl;
2 4
(3)若要进一步确定样品的组成,还需进行的实验是取步骤I所得上层清液于试管中,加入足量稀硝酸,
再滴入硝酸银,振荡,观察现象。若有白色沉淀,则样品组成中有NaCl;若没有明显现象,则样品组成中
没有NaCl。
【例2】小明配制了两瓶溶液,分别为碳酸钾溶液和氢氧化钾溶液,却忘记贴标签。为了鉴别这两种溶液,
小明同学过进行了以下实验:
(1)分别取少量溶液于两支试管中,各加入少量氯化钡溶液,观察到一支试管中出现白色浑浊,此试管中反
应的化学方程式为_________。
(2)小明将步骤(1)反应后的两支试管中的物质一并倒入烧杯中,充分混合后进行过滤,随后对滤液的成分进
行了如下探究。①小明推测滤液一定有的物质是_____________,可能含有的离子是______________;
②小明为了验证滤液中是否存在 ,取少量滤液于一支试管中,滴入几滴盐酸,没有明显现象,因此
得到结论,滤液中没有 。你认为是否合理:_________;说明你判断的依据________。
【答案】 氢氧化钾、氯化钾 或 不合理 滤
液中含有氢氧化钾,加入稀盐酸后,酸碱中和反应优先进行,不能判断出滤液中没有
【分析】
碳酸钾溶液中加入少量氯化钡溶液产生白色沉淀是碳酸钡沉淀;氢氧化钾溶液中加入少量氯化钡溶液没有
反应;滤液中有的是碳酸钾和氯化钡反应后的溶液为氯化钾溶液,还有不反应的氢氧化钾溶液,若氯化钡
少量则碳酸钾过量,若氯化钡过量,则碳酸钾完全反应;滤液中含有氢氧化钾,滴入几滴盐酸会优先和氢
氧化钾反应,由此分析。
【详解】
(1)碳酸钾溶液和氢氧化钾溶液各加入少量氯化钡溶液,碳酸钾和氯化钡反应生成碳酸钡和氯化钾,反应的
化学方程式为 ;
(2)①碳酸钾和氯化钡反应生成碳酸钡和氯化钾,氢氧化钾溶液氯化钡不反应,滤液一定有的物质是氯化钾
和氢氧化钾;若氯化钡少量则碳酸钾过量,则溶液中含有碳酸钾;若氯化钡过量,则碳酸钾完全反应,则
溶液种含有氯化钡;故可能含有的离子是 或 ;
②滤液中一定含有氯化钾和氢氧化钾,取少量滤液于一支试管中,滴入几滴盐酸,盐酸会优先和溶液中的
氢氧化钾反应生成氯化钾和水,没有明显现象,不能验证滤液中是否存在 ,结论不合理。
【例3】(2020·广东广州)某固体粉末可能含有KOH、KCO、KSO 中的一种或几种,为了确定其成分,
2 3 2 4
进行如下实验:
根据上述实验,回答下列问题:
(1)上述实验中,“产生气泡”的化学方程式为______。
(2)分析实验现象,推断原固体粉末的成分是____(填化学式)。
(3)能区别KCO 溶液和NaCl溶液的试剂是______(填标号)。
2 3A NaOH溶液
B 盐酸
C 酚酞溶液
D NaNO 溶液
3
【答案】 KCO BC
2 3
【分析】
取样溶解,滴加酚酞溶液,溶液变红,说明溶液显碱性,至少含有碳酸钾或氢氧化钾中的一种,另一份溶
液加入过量氯化钡溶液,生成白色沉淀,加入过量盐酸,产生气泡,固体完全溶解,说明含有碳酸钾,不
含有硫酸钾,加入氯化钡溶液过滤,滴加酚酞溶液,无明显现象,说明不含氢氧化钾。
【详解】
(1)实验中,“产生气泡”的反应是碳酸钡和盐酸生成氯化钡、水和二氧化碳,故反应的化学方程式为
。
(2)两份固体粉末的溶液,一份滴加酚酞溶液,溶液变红,说明溶液显碱性,至少含有碳酸钾或氢氧化
钾中的一种,另一份加入过量氯化钡溶液,生成白色沉淀,加入过量盐酸,产生气泡,固体完全溶解,说
明含有碳酸钾,不含有硫酸钾,过滤,滴加酚酞溶液,无明显现象,说明不含氢氧化钾,故原固体粉末的
成分是碳酸钾,化学式为KCO。
2 3
(3)A、NaOH溶液和碳酸钾、氯化钠均不反应,不能区别,故A不正确;
B、盐酸和碳酸钾反应生成氯化钾、水和二氧化碳,有气泡产生,盐酸和氯化钠不反应,可以区别,故B
正确;
C、碳酸钾溶液显碱性,能使酚酞溶液变红色,氯化钠显中性,不能使酚酞溶液变红色,可以区别,故C
正确;
D、NaNO 溶液和碳酸钾、氯化钠均不反应,不能区别,故D不正确。故选BC。
3
2.推断
【例1】(2020·广东)下列各组物质不能实现如图所示的转化关系的是( )
选项 甲 乙
A Fe O 稀硫酸
2 3B SO NaOH溶液
3
C 稀盐酸 Ca(OH) 溶液
2
D 稀盐酸 AgNO 溶液
3
【答案】D
【详解】
A、氧化铁和稀硫酸反应生成硫酸铁和水,硫酸铁属于盐,符合图中转化关系,不符合题意;
B、三氧化硫和氢氧化钠反应生成硫酸钠和水,硫酸钠属于盐,符合图中转化关系,不符合题意;
C、稀盐酸和氢氧化钙反应生成氯化钙和水,氯化钙属于盐,符合图中转化关系,不符合题意;
D、稀盐酸与硝酸银反应生成氯化银沉淀和硝酸,不符合图中转化关系,符合题意。故选D。
【例2】(2019·广东)五种物质之间的转化关系如图所示,回答下列有关问题:
(1)③反应的基本类型是_____。
(2)完成①转化中,可在NaCO 溶液中加入的物质类别是_____(选填序号,A.氧化物B.酸C.碱
2 3
D.盐)。
(3)写出转化中属于中和反应的化学方程式_____。
(4)⑧反应时一定发生的现象是_____;若④反应出现蓝色沉淀,则反应的化学方程式是_____;
(5)①~⑧能够逆向转化的有_____(填序号)。
【答案】复分解反应 BD NaOH+HNO =NaNO +H O 产生白色沉淀 CuCl +2NaOH=Cu
3 3 2 2
(OH)↓+2NaCl ②⑤
2
【解析】
(1)碳酸钠能与硫酸反应生成硫酸钠、二氧化碳和水,该反应是由两种化合物相互交换成分生成了两种
新的化合物,属于复分解反应;故填:复分解反应;
(2)碳酸钠能与盐酸(属于酸)反应生成氯化钠、水和二氧化碳;碳酸钠能与氯化钙(属于盐)反应生
成氯化钠和碳酸钙白色沉淀;故填:BD;
(3)中和反应是指酸与碱作用生成盐和水的反应,即氢氧化钠与硝酸反应生成硝酸钠和水;故填:
NaOH+HNO =NaNO +H O;
3 3 2(4)硫酸钠能与硝酸钡反应生成硫酸钡白色沉淀和硝酸钠,所以会观察到有白色沉淀产生;氢氧化钠能
与氯化铜反应生成氢氧化铜蓝色沉淀和氯化钠;故填:产生白色沉淀;CuCl +2NaOH=Cu(OH)
2
↓+2NaCl;
2
(5)碳酸钠能与氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠;硫酸钠能与氢氧化钡反应生成硫酸钡白
色沉淀和氢氧化钠;故填:②⑤。
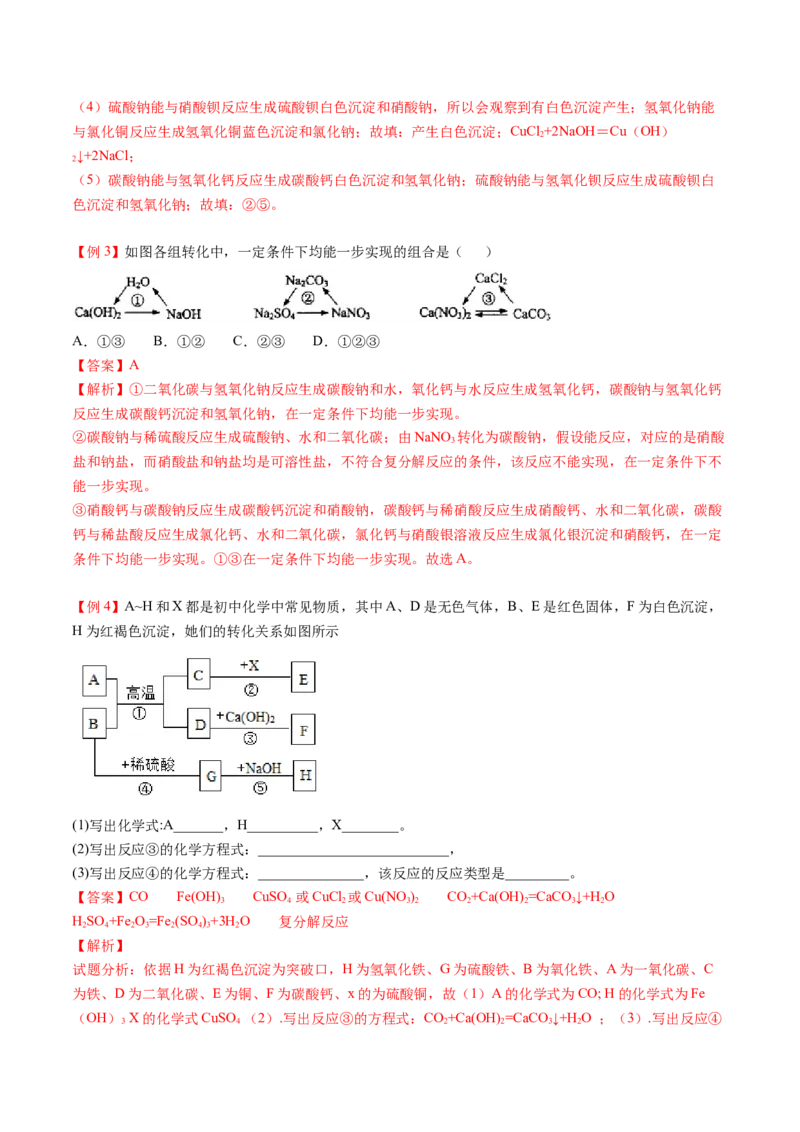
【例3】如图各组转化中,一定条件下均能一步实现的组合是( )
A.①③ B.①② C.②③ D.①②③
【答案】A
【解析】①二氧化碳与氢氧化钠反应生成碳酸钠和水,氧化钙与水反应生成氢氧化钙,碳酸钠与氢氧化钙
反应生成碳酸钙沉淀和氢氧化钠,在一定条件下均能一步实现。
②碳酸钠与稀硫酸反应生成硫酸钠、水和二氧化碳;由NaNO 转化为碳酸钠,假设能反应,对应的是硝酸
3
盐和钠盐,而硝酸盐和钠盐均是可溶性盐,不符合复分解反应的条件,该反应不能实现,在一定条件下不
能一步实现。
③硝酸钙与碳酸钠反应生成碳酸钙沉淀和硝酸钠,碳酸钙与稀硝酸反应生成硝酸钙、水和二氧化碳,碳酸
钙与稀盐酸反应生成氯化钙、水和二氧化碳,氯化钙与硝酸银溶液反应生成氯化银沉淀和硝酸钙,在一定
条件下均能一步实现。①③在一定条件下均能一步实现。故选A。
【例4】A~H和X都是初中化学中常见物质,其中A、D是无色气体,B、E是红色固体,F为白色沉淀,
H为红褐色沉淀,她们的转化关系如图所示
(1)写出化学式:A_______,H__________,X________。
(2)写出反应③的化学方程式:___________________________,
(3)写出反应④的化学方程式:_______________,该反应的反应类型是_________。
【答案】CO Fe(OH) CuSO 或CuCl 或Cu(NO ) CO +Ca(OH) =CaCO ↓+H O
3 4 2 3 2 2 2 3 2
HSO +Fe O=Fe (SO )+3H O 复分解反应
2 4 2 3 2 4 3 2
【解析】
试题分析:依据H为红褐色沉淀为突破口,H为氢氧化铁、G为硫酸铁、B为氧化铁、A为一氧化碳、C
为铁、D为二氧化碳、E为铜、F为碳酸钙、x的为硫酸铜,故(1)A的化学式为CO; H的化学式为Fe
(OH) X的化学式CuSO (2).写出反应③的方程式:CO+Ca(OH) =CaCO ↓+H O ;(3).写出反应④
3 4 2 2 3 2的方程式Fe O+3H SO =Fe (SO )+3H O;该反应的反应类型是复分解反应。
2 3 2 4 2 4 3 2
【例5】甲乙丙有如图所示的转化关系(“→”表示反应一步实现,部分反应物和反应条件略去),下列各组物
质按照甲乙丙的顺序不符合要求的是( )
A.Cu(OH) 、CuCl 、Cu(NO )
2 2 3 2
B.CuO、Cu、Cu(NO )
3 2
C.HO、O、HO
2 2 2 2
D.C、CO、CO
2
【答案】A
【详解】
A、氢氧化铜与稀盐酸反应生成氯化铜和水,氯化铜能与硝酸银溶液反应生成氯化银沉淀和硝酸铜,硝酸
铜不能一步转化为氯化铜, 因为若生成物是氯化铜和硝酸盐,均易溶于水,不符合复分解反应的条件,
故选项A不符合要求。
B、氧化铜与氢气在加热条件下反应生成铜和水,和硝酸反应生成硝酸铜,铜与硝酸银溶液反应生成硝酸
铜溶液和银,铁与硝酸铜溶液反应生成硝酸亚铁溶液和铜,按照甲乙丙的顺序符合要求,故选项B符合要
求。
C、过氧化氢分解生成水和氧气,氧气和氢气反应生成水,水通电分解生成氧气,按照甲乙丙的顺序符合
要求,故选项C符合要求。
D、碳充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳,二氧化碳与碳在高温下反应生成一氧化碳,一
氧化碳燃烧生成二氧化碳,按照甲乙丙的顺序符合要求,故选项D符合要求。
故选: A。
【例6】下列各组变化中,每一转化在一定条件下均能一步实现的是( )
A.①和② B.②和③ C.①和④ D.③和④
【答案】C
【详解】
①碳在氧气不充足的条件时燃烧生成一氧化碳,碳在氧气充足的条件时燃烧生成二氧化碳,二氧化碳在高
温条件下与碳反应生成一氧化碳;故①可以一步实现。
②氢氧化钠与盐酸反应可以生成氯化钠,氯化钠不能直接生成碳酸钠,故②不可以一步转化;③氧化铜不可以一步转化成氢氧化铜,故③不能一步转化;
④氢氧化钙可以和碳酸钠反应生成碳酸钙,碳酸钙和盐酸反应生成氯化钙,氢氧化钙与盐酸反应生成氯化
钙,故④可以一步转化;故满足条件的是①和④
故选C
专项训练
【训1】某校化学兴趣小组在课外活动中,对某溶液进行了多次检验,其中3次检验的结果如表所示。
序 溶液中检验溶液中检验出的物
号 质
1 KCl、KOH、NaCO
2 3
2 NaCl、Ba(OH) 、KCO
2 2 3
3 NaOH、KCl、KCO
2 3
(1)表中第__________次结果肯定不准确,原因是____________________(以化学方程式作答)。
(2)为验证其他两次检验结果中是否存在OH-、CO2- 和C1-,该小组设计了如下实验,请帮助他们完成实验
3
报告。
提示:①KCO 的化学性质与NaCO 相似;②Ag+不能与OH-共存,⑨本实验情境下,微溶物以沉淀形式出
2 3 2 3
现。
限选试剂:稀硝酸、稀盐酸、硝酸银溶液、氯化钡溶液、硝酸钡溶液
实验操作 预期现象与结论
步骤1:取待测溶液少许,加入足量的__________溶 现象_______________,说明
液。 溶液存在CO2-
3
现象______________,说明
步骤2:继续往步骤1溶液中滴加几滴酚酞试液。
溶液存在OH-。
现象_____________,说明溶
步骤3:__________________________。
液存在Cl-。
为了确认溶液中存在的阳离子:该小组同学查阅资料,发现可以利用焰色反应来确定溶液中存在的阳离子,
最终确定出该溶液中确实存在Na+、Cl-、OH-、CO2-。
3
【答案】2 Ba(OH) +K CO===2KOH+BaCO ↓ Ba(NO ) 有白色沉淀产生 溶液由无色变为红
2 2 3 3 3 2
色 先加入足量HNO 再加入AgNO 溶液 溶液由红色变无色,有白色沉淀产生
3 3
【训2】除去下列物质中的少量杂质,所选用试剂及操作方法均正确的是( )
选项 物质(括号内为杂质) 选用试剂 操作方法
A CO(CO) 适量O 点燃
2 2
B NaCl溶液(NaCO) 过量CaCl 溶液 过滤
2 3 2C KNO 溶液(KSO 溶液) 适量Ba(NO ) 溶液 过滤
3 2 4 3 2
D KC1溶液(CuCl 溶液) 足量NaOH溶液 过滤
2
【答案】C
【详解】
A、除去二氧化碳中的一氧化碳不能够通氧气点燃,这是因为除去气体中的气体杂质不能使用气体,否则
会引入新的气体杂质,故选项所采取的方法错误。
B、NaCO 能与过量CaCl 溶液反应生成碳酸钙沉淀和氯化钠,能除去杂质但引入了新的杂质氯化钙(过
2 3 2
量的),不符合除杂原则,故选项所采取的方法错误。
C、KSO 溶液与适量Ba(NO ) 溶液反应生成硫酸钡沉淀和硝酸钾,再过滤,能除去杂质且没有引入新
2 4 3 2
的杂质,符合除杂原则,故选项所采取的方法正确。
D、CuCl 溶液与足量NaOH溶液反应生成氢氧化铜沉淀和氯化钠,能除去杂质但引入了新的杂质氯化钠,
2
不符合除杂原则,故选项所采取的方法错误。
故选:C。
【训3】除去下列物质中混有的少量杂质所选用的操作方法,正确的是( )
选项 物质 操作方法
CO 中混有水蒸气 将气体通过装有生石灰的干燥管,干燥
2
B 铜粉中混有木炭 将混合物在空气中灼烧
C NaCl 溶液中混有CaCl 加入过量NaCO 溶液、过滤
2 2 3
D Cu(NO ) 溶液中混有CuCl 加入适量AgNO 溶液、过滤
3 2 2 3
【答案】D
【详解】
A.二氧化碳能与氧化钙反应,水能与氧化钙反应,不但能把杂质除去,也会把原物质除去,不符合除杂
原则,故选项A不符合题意;
B.铜与氧气在加热的条件下生成氧化铜,碳与氧气反应生成二氧化碳,不但能把杂质除去,也会把原物
质除去,不符合除杂的原则,故选项B不符合题意;
C.加入过量NaCO 溶液,氯化钙能与碳酸钠反应生成碳酸钙和氯化钠,过滤,除去碳酸钙,虽然除去了
2 3
杂质,但是引入了新的杂质碳酸钠(过量的),不符合除杂原则,故选项C不符合题意;
D.加入适量AgNO 溶液,氯化铜能与硝酸银反应生成硝酸铜和氯化银,过滤,除去氯化银,可得硝酸铜,
3
符合除杂原则,故选项D符合题意。
故选D。
【训4】镉镍电池属于有害垃圾。当环境受到镉污染后,镉可在生物体内富集,通过食物链进入人体引起
慢性中毒。镉的回收一般先将废镉镍电池进行处理以制得硫酸镉(CdSO )溶液。
4请预测硫酸镉(CdSO )的化学性质,说明预测的依据,并设计实验验证。
4
已知:(1)金属镉(Cd)的活动性与锌相似,锌的金属活动性比镉强。
(2)镉(Cd)从溶液中析出时呈海绵状固体。
(3)经查阅资料,镉的化合物相关性质如下表:
物质 Cd(OH) CdCO CdSO
2 3 4
20℃时的溶解度(g) 2.97×10-4 3.932×10-5 76.6
颜色与状态 白色固体 白色固体 白色固体,其水溶液是无色液体
限选试剂:CdSO 溶液、NaCO 溶液、Ba(NO ) 溶液、KOH溶液、稀盐酸、锌片、铜片。
4 2 3 3 2
预测 预测的依据 验证预测的实验操作与预期现象
①能够与含Ba2+的可溶性盐 CdSO 溶液中含 取少量CdSO 溶液于试管中,_____,如果观察
4 4
反应 SO 2- 到_____,则预测成立
4
②能够与_____(填物质类 取少量CdSO 溶液于试管中,_____,如果观察
_____ 4
别)反应 到_____,则预测成立
③能够与_____(填物质类 取少量CdSO 溶液于试管中,_____,如果观察
_____ 4
别)反应 到_____,则预测成立
④能够与_____(填物质类 取少量CdSO 溶液于试管中,_____,如果观察
_____ 4
别)反应 到_____,则预测成立
【答案】加入Ba(NO ) 溶液 有白色沉淀产生 含CO2-的可溶性盐 CdSO 溶液中含Cd2+
3 2 3 4
加入NaCO 溶液 有白色沉淀产生 可溶性碱 CdSO 溶液中含Cd2+ 然后加入KOH溶液
2 3 4
有白色沉淀产生 比Cd活泼的金属 CdSO 溶液中含Cd2+ 加入锌片 海绵状固体析出
4
【详解】
①硫酸镉属于硫酸盐,硫酸盐能与钡盐溶液反应生成硫酸钡沉淀,取少量CdSO 溶液于试管中,滴加Ba
4
(NO ) 溶液,观察到产生白色沉淀,说明CdSO 能与可溶性钡盐反应,则预测成立。
3 2 4
②根据镉的化合物在20℃的溶解度数据,CdCO 的溶解度很小,难溶于水,可预测能与可溶性碳酸盐反应,
3
预测的依据是可溶性镉盐能与可溶性碳酸盐反应,生成碳酸镉沉淀;取少量CdSO 溶液于试管中,滴加
4
NaCO 溶液,振荡,如果观察到产生白色沉淀,则预测成立。
2 3
③根据镉的化合物在20℃的溶解度数据,Cd(OH) 的溶解度很小,难溶于水,可预测能与可溶性碱反应,
2
预测的依据是可溶性镉盐能与可溶性碱反应,生成氢氧化镉沉淀;可取少量CdSO 溶液于试管中,滴加
4
KOH溶液,如果观察到产生白色沉淀,则预测成立。
④或根据金属镉(Cd)的活动性与锌相似,锌的金属活动性比镉强,预测锌能与镉发生置换反应,取少量
CdSO 溶液于试管中,加入锌片,锌片表面出现海绵状固体,则预测成立。
4
提分作业1.下列实验中有明显现象的是( )
A.铜丝浸入稀硫酸中 B.向BaCO 中滴入NaSO 溶液
3 2 4
C.向氧化铜滴加氢氧化钠溶液 D.稀硫酸滴入变质的氢氧化钾溶液
【答案】D
【详解】
A、铜金属活动性在氢之后,和稀硫酸不反应,故A错误。
B、碳酸钡和硫酸钠不反应,无现象,B错误。
C、氧化铜和氢氧化钠不反应,无现象C错误。
D、氢氧化钾变质生成碳酸钾,碳酸钾和稀硫酸反应生成硫酸钾二氧化碳和水,有现象,D正确。
故选:D。
2.下列除去杂质的方法不正确的是( )
物质(括号内为杂
选项 除去杂质的方法
质)
A NaCl溶液(CuSO ) 加适量NaOH溶液
4
B N(O) 通过灼热的铜网
2 2
C CaCl (CaCO ) 加水、过滤、蒸发
2 3
D HNO 溶液(HCl) 加适量AgNO 溶液、过滤
3 3
【答案】A
【详解】
A、CuSO 能与适量NaOH溶液反应生成氢氧化铜沉淀和硫酸钠,能除去杂质但引入了新的杂质硫酸钠,
4
不符合除杂原则,故选项所采取的方法错误;
B、氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的
杂质,符合除杂原则,故选项所采取的方法正确;
C、CaC1 易溶于水,CaCO 难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,故选项所采取
2 3
的方法正确;
D、HCl能与适量AgNO 溶液反应生成氯化银沉淀和硝酸,再过滤,能除去杂质且没有引入新的杂质,符
3
合除杂原则,故选项所采取的方法正确。
故选A。
3.为除去下列物质中的杂质(括号内是杂质),下列操作方法正确的是( )
选项 物质 操作方法
A NaCl溶液(NaCO) 先加过量稀盐酸,再滴加NaOH溶液调节pH=7
2 3
B 铜粉(铁粉) 加入过量AgNO 溶液,过滤
3
C NaOH溶液[Ca(OH) 溶液] 通入过量CO 气体,充分反应后过滤
2 2D BaSO(NaOH) 加足量水溶解,再滴加足量稀HSO
4 2 4
【答案】A)
【详解】
A、NaCO 能与过量稀盐酸反应生成氯化钠、水和二氧化碳,再滴加NaOH溶液调节pH=7,能除去杂质
2 3
且没有引入新的杂质,符合除杂原则,故选项正确;
B、铁粉和铜粉均能与过量AgNO 溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,
3
故选项错误;
D、Ca(OH) 溶液和NaOH溶液均能与CO 气体反应,不但能把杂质除去,也会把原物质除去,不符合
2 2
除杂原则,故选项错误;
D、NaOH易溶于水,BaSO 难溶于水,可采取加入足量的水,充分溶解后过滤的方法进行分离除杂,故选
4
项错误。故选A。
4.下列实验中无明显现象的是( )
A.铝丝浸入硫酸铜溶液中
B.向Mg(NO ) 溶液中滴加NaSO 溶液
3 2 2 4
C.将浓硫酸加入水中并不断搅拌
D.将生锈的铁钉放入稀盐酸中
【答案】B
【详解】
A、铝丝浸入CuSO 溶液中,能置换出铜,有红色固体析出,现象明显,不符合题意;
4
B、Mg(NO ) 和NaSO 不反应,没有现象,符合题意;
3 2 2 4
C、浓硫酸加入蒸馏水中并不断搅拌,会放出大量的热,不符合题意;
D、铁锈和盐酸反应生成氯化铁和水,氯化铁溶液是黄色,所以观察到的现象是溶液由无色变为黄色,不
符合题意。故选B。
5.如图表示的是物质A~G相互间的关系(“ →” 表示物质间存在的转化关系,“—”表示两端的物质
能发生化学反应)A、F都是单质;F是使用最多的金属材料; B是导致温室效应的主要气体;在工业上,
C广泛用于玻璃、造纸、纺织和洗涤剂的生产等;E是一种蓝色溶液。请回答:
(1)C的化学式______________,G可能是______________。
(2)写出E的一种用途________________。
(3)写出标号①、②的化学反应方程式:
①__________。
②_________,反应的类型属于____________。
【答案】NaCO 盐酸 (或硫酸) 配制农药波尔多液 NaCO+Ca(OH) =2NaOH+CaCO ↓(其他合
2 3 2 3 2 3理答案也可) Fe+CuSO=FeSO+Cu ; 置换反应
4 4
【分析】
B是导致温室效应的主要气体,所以B为二氧化碳;A是单质,且A能与B(二氧化碳)反应,则A为碳
或氧气;在工业上,C广泛用于玻璃、造纸、纺织和洗涤剂的生产等,则C为碳酸钠;E是一种蓝色溶液,
则E为硫酸铜溶液;由图可知,D与C(碳酸钠)、E(硫酸铜)均能反应,则D可能为氢氧化钙或氯化
钡等;F是使用最多的金属材料,则F为铁;由图可知,G与C(碳酸钠)、F(铁)均能反应,根据盐和
金属的化学性质可知,G应为酸,即盐酸 或硫酸。