文档内容
第十一单元 盐 化肥
课题 1 生活中常见的盐
(第一课时)
教学目标
知识和技能:通过资料收集和实验探究,认识生活中常见的盐的种类和用途。
过程和方法:初步学会粗盐提纯的方法和步骤。
情感态度和价值观:充分认识到生活中处处有化学、了解我国科学家做出的杰出贡献,从而
激发爱国热情和学习激情。
教学重点和难点
重点:粗盐的提纯。
难点:提纯过程的操作要点。
实验准备
① 粗盐的提纯:烧杯、漏斗、量筒(10 mL)、玻璃棒、蒸发皿、酒精灯、药匙、铁架台(带铁圈)、
滤纸、剪刀、托盘天平、粗盐、水。
② 多媒体电脑及投影仪。
教学过程
课前准备
学生多渠道收集四方面的资料:
① 日常生活中,你所见到的氯化钠、碳酸钠、碳酸氢钠、高锰酸钾、碳酸钙等实物。
② 食盐与人体健康的关系,工业用盐主要成分。
③ 氯化钠、碳酸钠、碳酸氢钠、碳酸钙等几种常见的盐,在日常生活及工农业生产中的用途。
④ ④氯化钠、碳酸钙在自然界的存在情况,我县境内的碳酸钙的含量如何?人们是怎样从
自然界中获取氯化钠、碳酸钙的?
创设情境引入:
多媒体投影播放电影《盐》(节选),让学生在轻音乐声中,观赏美丽的风光,了解盐的历史,
初知盐的用途等。
学生活动一:
报:1.交换观察、交流信息:在日常生活中搜集到的常见盐的实物,简述其外观及性质;交流
课外阅读或网上查找的文字、图片等信息资料。
2.集体交流:各组代表汇报相互交流情况。(教师作必要的补充,给予恰当的点评)
练:阅读课本,整理资料,完成下表。
氯化钠 碳酸钠 碳酸氢钠 碳酸钙化学式
主要用途
组成上的共同
点
日常生活中所说的盐是指:
结论
化学中所说的盐是指:
讲:出示:一瓶食盐,一瓶粗盐,一瓶食盐的水溶液,一瓶粗盐的水溶液。
报:①固体食盐与粗盐的外观差异;
②食盐与粗盐的水溶液的外观差异。
讲:提出问题:“如何将粗盐转化为精盐?”“怎样除去粗盐中不溶性杂质和可溶性杂
质?”今天的学习任务:活动与探究──粗盐的初步提纯。
学生活动二:
讲:分组讨论:(教师深入实验小组,了解情况、发现问题、发现典型)
① 通过观察、比较固体食盐与粗盐的外观和食盐与粗盐的水溶液的外观,你得出什么结果?
②除去粗盐中不溶性杂质,你采取什么方法?
③粗盐提纯的基本步骤有哪些,怎样设计?
④每个步骤,应该注意哪些问题?
报:交流讨论结果:
粗盐提纯实验仪器:药匙、烧杯、玻璃棒、蒸发皿、漏斗、滤纸、量筒、酒精灯、铁架台、托盘
天平
实验步骤:1.溶解 2.过滤 3.蒸发 4.称量并计算粗盐的产率
过滤:分离没溶于液体的固体和液体的混合物的操作。要点是“一贴二低三靠”:
一贴:滤纸紧贴漏斗的内壁。
二低:过滤时滤纸的边缘应低于漏斗的边缘,漏斗内液 体的液面低于滤纸的边缘。
三靠:倾倒液体的烧杯嘴紧靠引流的玻璃棒,玻璃棒的末端轻轻靠在三层滤纸的一边,漏
斗的下端紧靠接收的烧杯。
讲:教师示范
1.制作过滤器。
2.简要说明过滤操作注意事项。
练:学生活动
分组实验:分工协作,分步操作,记录现象及数据。(教师巡回指导,了解情况、发现问题、发
现典型)
报:交流实验结果:各组代表汇报实验结果,交流实验的得与失。
提:(教师适时点评,告诉精盐产率的理论值)报:学生评议,提出疑问:
①我们小组得出的精盐产率大于理论值,为什么?
② 我们小组得出的精盐产率远低于理论值,为什么?
分组讨论:
①造成实验误差的原因,可能有哪些?
②根据实验误差的原因,你在操作中,还应该注意什么?怎样改进?
5.交流讨论结果:尽可能多找出造成实验误差可能出现的原因。(学生可以进行争论,教师给
以引导)
教学小结
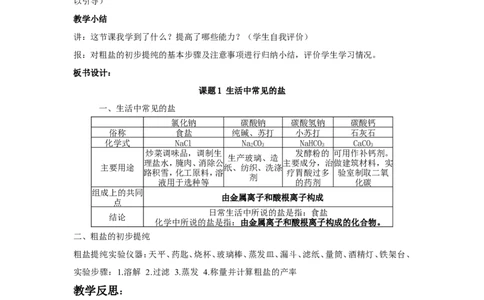
讲:这节课我学到了什么?提高了哪些能力?(学生自我评价)
报:对粗盐的初步提纯的基本步骤及注意事项进行归纳小结,评价学生学习情况。
板书设计:
课题1 生活中常见的盐
一、生活中常见的盐
氯化钠 碳酸钠 碳酸氢钠 碳酸钙
俗称 食盐 纯碱、苏打 小苏打 石灰石
化学式 NaCl NaCO NaHCO CaCO
2 3 3 3
炒菜调味品,调制生 发酵粉的 可用作补钙剂。
生产玻璃、造
理盐水,腌肉、消除公 主要成分,治做建筑材料,实
主要用途 纸、纺织、洗涤
路积雪,化工原料,溶 疗胃酸过多 验室制取二氧
剂
液用于选种等 的药剂 化碳
组成上的共同
由金属离子和酸根离子构成
点
日常生活中所说的盐是指:食盐
结论
化学中所说的盐是指:由金属离子和酸根离子构成的化合物。
二、粗盐的初步提纯
粗盐提纯实验仪器:天平、药匙、烧杯、玻璃棒、蒸发皿、漏斗、滤纸、量筒、酒精灯、铁架台、
实验步骤:1.溶解 2.过滤 3.蒸发 4.称量并计算粗盐的产率
教学反思:
本节课在介绍常见的盐的基础上总结出盐的概念,他不是单单指生活中的食盐。分组
实验粗盐的提纯,主要操作是溶解、过滤,学生之前都有学过,故知识容易掌握,要求学生通
过亲自实验懂得基本的实验步骤,为以后实验考试做好准备。课程时间安排比较紧,对于常
见的盐的俗称和用途还需强化记忆。
(第2课时)
教学目标
知识与技能:了解碳酸钠、碳酸氢钠、碳酸钙的组成、性质及生活中的用途,学会碳酸根离子的检验;认识部分酸碱盐的溶解性,能应用复分解反应概念判断该反应类型,能应用复分解
反应的发生条件判断酸碱盐之间能否发生反应。
过程与方法:通过碳酸盐及酸碱盐之间的混合实验,探索并归纳碳酸盐的检验方法,盐类物
质的性质、复分解反应的条件。
情感态度价值观:利用纯碱用途简介为我国制碱工业作出巨大贡献的侯德榜先生的事迹,增
强爱国主义情感教育。
教学重难点:应用复分解反应的条件判断酸碱盐之间能否发生反应
教学准备:侯德榜先生的视频材料
相关的仪器和药品
教学过程:
练:完成新课堂的复习导学,识记常见的盐类的俗称
报:学生汇报答案
新课学习:
练:完成新课堂92页中导学1碳酸盐和盐酸反应的方程式,并试着找出相似点进行分析
报:学生报告答案
讲:教师演示实验【实验探究1】碳酸钠和碳酸氢钠与盐酸反应,是否都能产生CO2 ?实验步
骤:向盛有0.5g碳酸钠的试管里加入2mL盐酸,迅速用带有导管的塞子塞进管口,并将导管
的另一端通入盛有澄清石灰水的试管中,观察现象。用碳酸氢钠代替碳酸钠进行上述实验,
并分析。
报:学生能说出碳酸盐检验的步骤,现象,结论。
练:完成新课堂中相应的练习
讲:【实验探究2】向盛有少量碳酸钠溶液的试管中滴入澄清石灰水,观察现象。
报:实验现象,写化学方程式
讲:复分解反应的概念:
书写规律:AB+CD=AD+CB
是不是所有的酸碱盐都能发生复分解反应呢?
报:只有生成物有水或沉淀或气体的复分解反应才能发生。
讲:酸碱盐的溶解性表和口诀
练:学生完成新课堂导学
报:汇报答案,教师点评
讲:现在大家来归纳一下盐的化学性质报:盐+活泼金属=新盐+金属单质
盐+碱=新盐+新碱
盐+酸=新盐+新酸
盐+盐=两种新盐
练:完成新课堂练习
报:汇报答案
提:这节课我们学习了很多重要的知识,请大家回忆总结
报:1、碳酸盐的检验
2、复分解反应的条件
3、盐的化学性质
板书:
1、碳酸盐的检验:取样,加入稀盐酸,有气泡生成,将生成的气体通入澄清石灰水,变浑
浊,则该样品中含有碳酸盐。
2、复分解反应的条件:生成物中必须有沉淀(难溶物)或水或气体。
3、盐的化学性质
教学反思:
课题 2 化学肥料
教学目标
1.知识与技能
(1)了解化学元素对植物生长的重要性及常见化肥的种类和作用;
(2)了解化肥、农药对环境的影响。
2.过程与方法
(1)学会如何成功地、有效地完成探究实验和探究报告;
(2)学习用分析、归纳的方法对有关信息进行加工;
(3)学习运用所学知识和技能解决实际问题的能力;
(4)能主动与他人进行交流和讨论,清楚的表达自己的观点,逐步形成良好的学习习惯和
学习方法。
(5)善于用辩证的方法看待问题。
3.情感态度与价值观
(1)知道化肥、农药在农业生产中的重要地位,懂得“科学种田”的道理;
(2)通过分析化肥、农药对环境的利弊,树立关注环境、热爱自然、合理使用化学物质的意识。
(3)赞赏化学对改善个人生活和促进社会发展的积极作用,关注与化学有关的社会问题,
初步形成主动参与社会决策的意识。
(4)发展善于合作、勤于思考、严谨求实、勇于创新和实践的科学精神。
教学重点:如何运用所学知识解决实际问题。
教学难点:对几种常见化肥的鉴别
教学方法:通过对化肥知识的调查研究和课堂讨论交流,培养学生的自学能力及运用所学知
识和技能解决实际问题的能力。通过对几种常见化肥签别的探究,培养和发展学生的探究能
力。
教学过程:
讲:农作物的生长需要养分,土壤提供的养分是有限的。随着世界人口的增长,人类对农产品
的需求量不断增大,那么人类是如何在有限的土地上上获得足够多的农产品的呢?
农作物生长需要的营养元素中N、P、K是三大营养元素,因此氮肥、磷肥、钾肥是最主要的化
肥。
练:学生阅读课本教材,完成新课堂相关练习
报:汇报作答情况,并进行小结
展示各组实验成果,归纳氮肥、磷肥、钾肥对植物所起的作用及缺少时的症状。
营养元素——氮、磷、钾。
复合肥料——含两种或两种以上营养元素的肥料。
对植物所起
常见种类 缺少时的症状
的作用
铵态氮肥:
NH4Cl、NH4HCO3
硝态氮肥: 促进茎叶生 植株矮小瘦弱,叶片发黄,严重时叶
氮肥
NHNO、NaNO 长 脉呈淡棕色——叶色黄。
4 3 3
有机态氮肥:
CO(NH)
2 2
磷矿粉, 促进根系发 植株特别矮小,叶片呈暗绿色,并出
磷肥
过磷酸钙 达 现紫——叶瘦黄而细小。
茎秆软弱,容易倒伏,叶片边缘和尖
钾肥 KCl ,KSO 使茎杆粗壮 端呈褐色,并逐渐焦枯
2 4
——叶片边缘黄色。
复合 KNO, NHHPO, 上述所有作
3 4 2 4 讲:师生
肥 (NH)HPO 用
4 2 4
讨论使用
化肥的利和弊
报:1.使用化肥的利与弊:
利——提高家作物产量
弊——1.对水的污染 2.土壤的污染3.对大气的污染4.对人类健康的危害。
2.使用农药的利与弊:
利——促进农业的高产丰收。
弊——污染环境、危害人体健康
3.怎样减少污染和危害呢?
1.合理使用
2.有机肥与化肥混合使用
3.减少剧毒农药的使用,开发高效低毒农药4.大力发展无土栽培植物 ……
讲:化肥的简易鉴别
[实验探究一]:比较氮肥(氯化铵、碳酸氢铵)、磷肥(磷矿粉、过磷酸钙) 和钾肥(硫酸钾、氯
化钾)的外观、气味和在水中的溶解性。
氮肥 磷肥 钾肥
碳酸氢铵 氯化铵 磷矿粉 过磷酸钙 硫酸钾 氯化钾
外观 白色晶体 灰白色粉状 白色晶体
气味 强烈氨味 加碱有氨 无气味
味
溶解性 溶于水 大多数不溶或部分溶 溶于水
[实验探究二]:取研细的氮肥(硫酸铵、氯化铵)、钾肥(硫酸钾、 氯化钾)各0.5克,分别放
在铁片上灼烧, 观察现象. 再取上述化肥各少量,分别加入少
量熟石灰粉末,混合、研磨,能否嗅到气味?
氮肥 钾肥
硫酸铵 氯化铵 硫酸钾 氯化钾
灼烧 熔化起泡或冒烟 不燃烧、跳动或有爆裂声
加熟石灰研磨 有刺激性氨味 无氨味气体生成
练:完成新课堂相关练习:
报:汇报结果
提:这节课我们学到了哪些知识?
氮肥 钾肥 磷肥
看外观 白色晶体 灰白色粉末
加水 全部溶解 大多数不溶或
部分溶
灼烧 可燃烧、熔化起 不燃烧、跳动或 无现象
泡或冒烟 有爆裂声
加熟石灰 放出具有刺激 无具有刺激性 无现象
性气味的氨气 气味的氨气放
出
[投影]农村中常用的鉴别化肥的方法.
在农村,人们总结出以下鉴别化肥的简易方法。
一看:液态化肥,有刺激性氨臭气味的是氨水;像鱼卵的白色固体,一般是尿素;灰色粉未或
颗粒,一般是过磷酸钙;黄褐色或灰褐色粉未一般是磷矿粉;白色晶体可能是硫铵、碳
铵、氯化钾等。
二闻:直接闻,有明显氨臭味的是碳铵(易分解放出氨气);用拇指和食指将石灰与白色晶体
混合揉搓,有氨臭气味的是硫铵或硝铵。
三溶:灰色粉未部分溶于水,且溶液有酸味的是过磷酸钙;黄褐色或灰褐色粉未不溶于水的
是磷矿粉。
练:某同学帮父亲去一家生产资料公司购买化肥,该公司化肥售价表如下:
化肥 CO(NH) Ca(PO) NHNO NHHCO 过磷酸钙 硫酸钾 氯化钾
2 2 3 4 2 4 3 4 3
价格(元/t) 1200 150 1000 350 250 800 650
他知道自己家的庄稼生长不茂盛、叶色淡绿、茎叶细小,也出现了倒伏情况。能供买化肥的钱
只有300元,该同学稍作思考便购买了两个品种的化肥,而且花钱最少,购得所需的营养元素总的含量最多,试问:
(1)该同学家的庄稼缺两种营养元素,它们是 (填“N”“P”“K”或“微量元素”)
(2)该同学买了碳酸氢铵化肥,则他买的另一种化肥是 。
板书设计:
一、化肥简介
农作物生长需要的营养元素中N、P、K是三大营养元素,
因此氮肥、磷肥、钾肥是最主要的化肥。
复合肥料——含两种或两种以上营养元素的肥料。
二、化肥的简易鉴别
氮肥 磷肥 钾肥
碳酸氢铵 氯化铵 磷矿粉 过磷酸钙 硫酸钾 氯化钾
外观 白色晶体 灰白色粉状 白色晶体
气味 强烈氨味 加碱有氨 无气味
味
溶解性 溶于水 大多数不溶或部分溶 溶于水
氮肥 钾肥
硫酸铵 氯化铵 硫酸钾 氯化钾
灼烧 熔化起泡或冒烟 不燃烧、跳动或有爆裂声
加熟石灰研磨 有刺激性氨味 无氨味气体生成
教学反思: