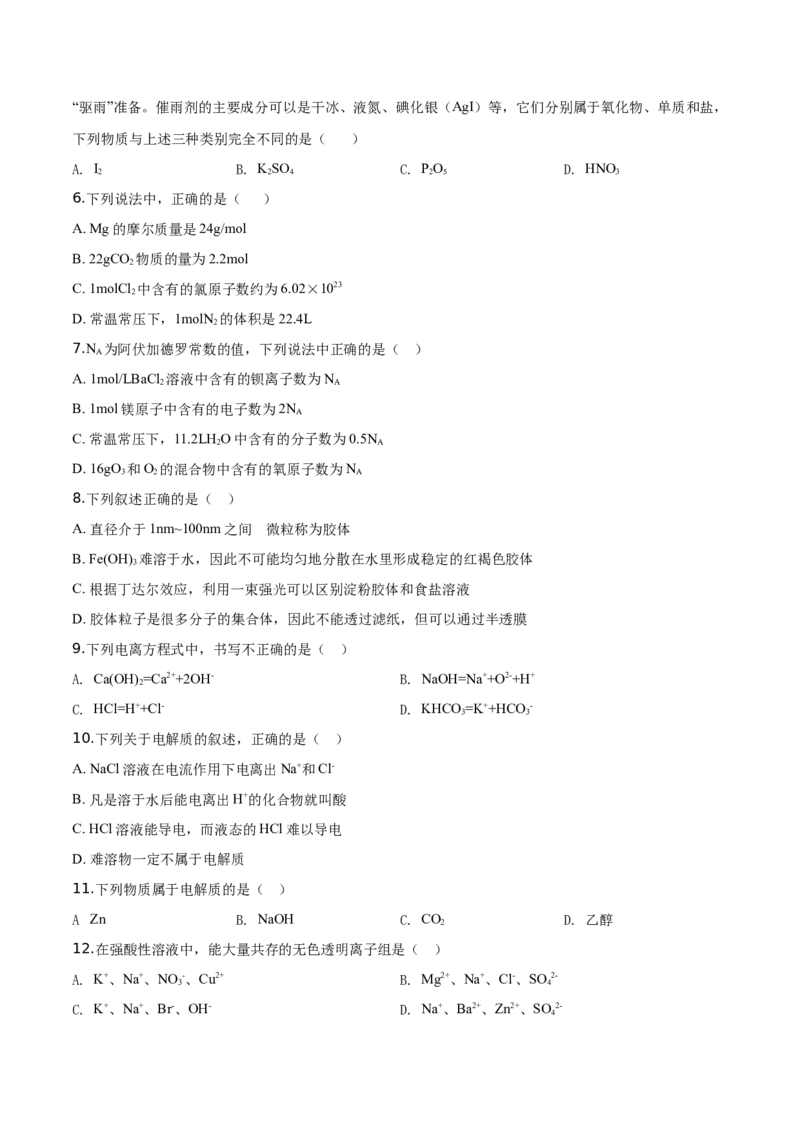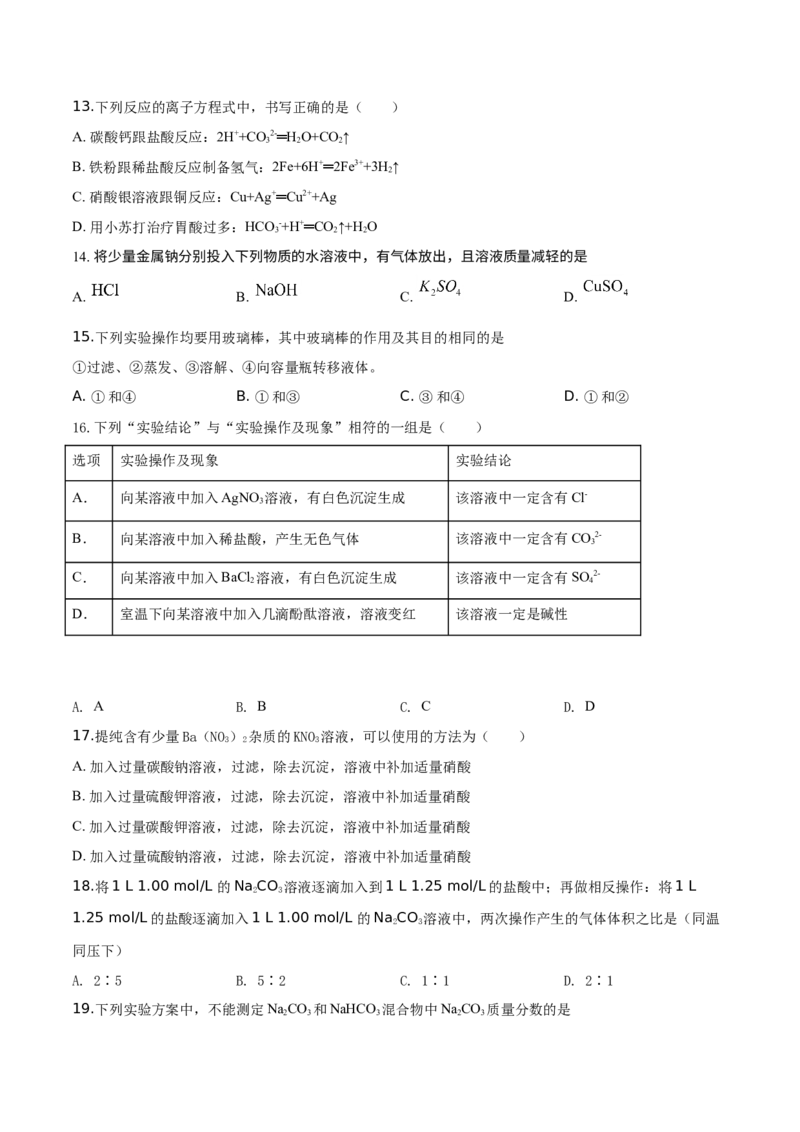文档内容
2019 北京人大附中高一(上)期中
化学
可能用到的相对原子质量:H—1;C—12;N—14;O—16;Na—23;Mg—24;S—32;Cl
—35.5;K—39;Cu—64
第I卷(共40分)
每小题只有一个选项符合题意
1.下列我国古代的技术应用中,其工作原理不涉及化学反应的是( )
A.火药使用 B.粮食酿酒 C.转轮排字 D.铁 的冶炼
A. A B. B C. C D. D
2.我国科技创新成果斐然,下列成果中获得诺贝尔奖的是( )
A. 徐光宪建立稀土串级萃取理论 B. 屠呦呦发现抗疟新药青蒿素
C. 闵恩泽研发重油裂解催化剂 D. 海域天然气水合物试采连续60天
3.下列行为不符合安全要求 的是( )
A. 实验结束后,将废液倒入指定容器中
B. 做实验剩余的金属钠不得直接丢弃在废液缸中
C. 大量氯气泄漏时,迅速离开现场并尽量应往低处去
D. 配制稀硫酸时,将浓硫酸缓慢倒入水中并不断搅拌
4.我们日常生活中出现了“加碘食盐”、“增铁酱油”、“富硒茶叶”和“含氟牙膏”等商品。这里的碘、铁、硒、
氟应理解为( )
A. 元素 B. 单质 C. 分子 D. 氧化物
5.2017年9月厦门金砖国家峰会期间,气象部门的科技人员为了保证峰会有关活动的正常进行,一直做好“驱雨”准备。催雨剂的主要成分可以是干冰、液氮、碘化银(AgI)等,它们分别属于氧化物、单质和盐,
下列物质与上述三种类别完全不同的是( )
A. I B. KSO C. PO D. HNO
2 2 4 2 5 3
6.下列说法中,正确的是( )
A. Mg的摩尔质量是24g/mol
B. 22gCO 物质的量为2.2mol
2
C. 1molCl 中含有的氯原子数约为6.02×1023
2
D. 常温常压下,1molN 的体积是22.4L
2
7.N 为阿伏加德罗常数的值,下列说法中正确的是( )
A
A. 1mol/LBaCl 溶液中含有的钡离子数为N
2 A
B. 1mol镁原子中含有的电子数为2N
A
C. 常温常压下,11.2LH O中含有的分子数为0.5N
2 A
D. 16gO 和O 的混合物中含有的氧原子数为N
3 2 A
8.下列叙述正确的是( )
A. 直径介于1nm~100nm之间 的微粒称为胶体
B. Fe(OH) 难溶于水,因此不可能均匀地分散在水里形成稳定的红褐色胶体
3
C. 根据丁达尔效应,利用一束强光可以区别淀粉胶体和食盐溶液
D. 胶体粒子是很多分子的集合体,因此不能透过滤纸,但可以通过半透膜
9.下列电离方程式中,书写不正确的是( )
A. Ca(OH) =Ca2++2OH- B. NaOH=Na++O2-+H+
2
C. HCl=H++Cl- D. KHCO =K++HCO-
3 3
10.下列关于电解质的叙述,正确的是( )
A. NaCl溶液在电流作用下电离出Na+和Cl-
B. 凡是溶于水后能电离出H+的化合物就叫酸
C. HCl溶液能导电,而液态的HCl难以导电
D. 难溶物一定不属于电解质
11.下列物质属于电解质的是( )
.
A Zn B. NaOH C. CO D. 乙醇
2
12.在强酸性溶液中,能大量共存的无色透明离子组是( )
A. K+、Na+、NO -、Cu2+ B. Mg2+、Na+、Cl-、SO 2-
3 4
C. K+、Na+、Br-、OH- D. Na+、Ba2+、Zn2+、SO 2-
413.下列反应的离子方程式中,书写正确的是( )
A. 碳酸钙跟盐酸反应:2H++CO 2-═H O+CO↑
3 2 2
B. 铁粉跟稀盐酸反应制备氢气:2Fe+6H+═2Fe3++3H ↑
2
C. 硝酸银溶液跟铜反应:Cu+Ag+═Cu2++Ag
D. 用小苏打治疗胃酸过多:HCO -+H+═CO ↑+H O
3 2 2
14. 将少量金属钠分别投入下列物质的水溶液中,有气体放出,且溶液质量减轻的是
A. B. C. D.
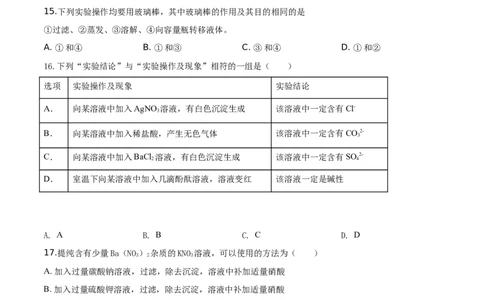
15.下列实验操作均要用玻璃棒,其中玻璃棒的作用及其目的相同的是
①过滤、②蒸发、③溶解、④向容量瓶转移液体。
A. ①和④ B. ①和③ C. ③和④ D. ①和②
16.下列“实验结论”与“实验操作及现象”相符的一组是( )
选项 实验操作及现象 实验结论
A. 向某溶液中加入AgNO 溶液,有白色沉淀生成 该溶液中一定含有Cl-
3
B. 向某溶液中加入稀盐酸,产生无色气体 该溶液中一定含有CO2-
3
C. 向某溶液中加入BaCl 溶液,有白色沉淀生成 该溶液中一定含有SO 2-
2 4
D. 室温下向某溶液中加入几滴酚酞溶液,溶液变红 该溶液一定是碱性
A. A B. B C. C D. D
17.提纯含有少量Ba(NO) 杂质的KNO 溶液,可以使用的方法为( )
3 2 3
A. 加入过量碳酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
B. 加入过量硫酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
C. 加入过量碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
D. 加入过量硫酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
18.将1 L 1.00 mol/L 的NaCO 溶液逐滴加入到1 L 1.25 mol/L的盐酸中;再做相反操作:将1 L
2 3
1.25 mol/L的盐酸逐滴加入1 L 1.00 mol/L 的NaCO 溶液中,两次操作产生的气体体积之比是(同温
2 3
同压下)
A. 2∶5 B. 5∶2 C. 1∶1 D. 2∶1
19.下列实验方案中,不能测定NaCO 和NaHCO 混合物中NaCO 质量分数的是
2 3 3 2 3A. 取a克混合物充分加热,固体质量减轻b克
B. 取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C. 取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
D. 取a克混合物与足量Ba(OH) 溶液充分反应,过滤、洗涤、烘干,得b克固体。
2
20.室温下,向容积不变的密闭容器中充入HS和SO 的混合气体(2HS+SO=3S↓ +2HO),充分反应后,
2 2 2 2 2
恢复至室温,容器内压强变为原来的1/4(忽略水的挥发)。则原混合气体中HS和SO 的体积比可能是(
2 2
)
A. 1:2 B. 2:1 C. 3:1 D. 4:1
第II卷(共60分)
21.阅读短文,回答问题。
平昌冬奥会闭幕式上,“2022,相约北京”文艺表演蕴含了丰富的中国文化,展现了新时代中国形象。
熊猫木偶:熊猫木偶高2.35m,质量仅为10kg,用铝合金管材和碳纤维条做框架,配合LED灯制作而成。
其中,碳纤维是含碳量高于90%的新型材料,密度比铝小,强度比钢大。
智能机器人:中国新一代智能机器人与轮滑舞者共舞、互动,在导航精准性、动作复杂性和灵活性等方面,
实现了人工智能领域的升级创新。
石墨烯智能发热服:这种智能发热服可在−20℃的条件下持续发热4h。石墨烯是一种由碳原子构成的六角
型二维碳纳米材料,具有超高硬度、强度和导热系数等特性。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
(1)熊猫木偶、智能机器人、石墨烯智能发热服展现了“中国智慧”。_____。
(2)碳纤维具有优良的性能,将有广泛的应用前景。_____。
(3)中国新一代智能机器人在动作、导航等方面实现了人工智能领域的升级创新。_____。
(4)石墨烯和石墨由同种元素组成,但它们的物理性质差异较大。_____。
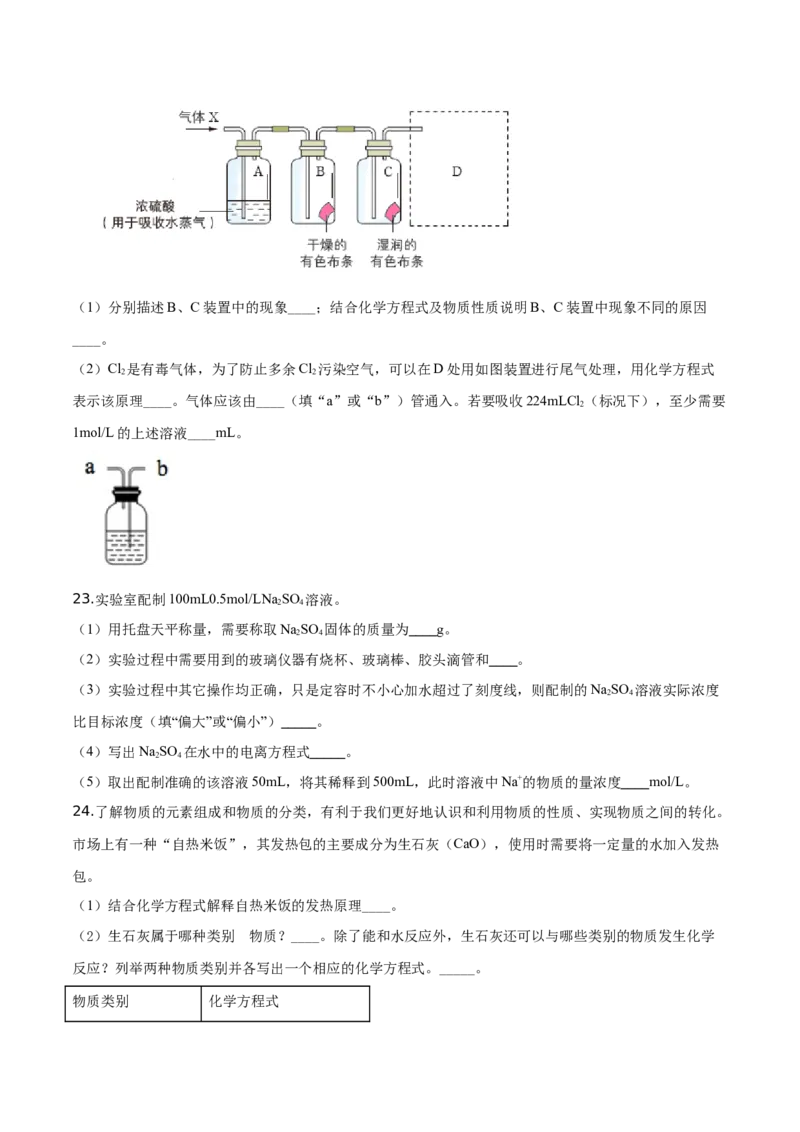
22.某学习小组用如图装置研究气体X的性质,气体X的主要成分是Cl,其中含有少量水蒸气。请回答下
2
列问题:(1)分别描述B、C装置中的现象____;结合化学方程式及物质性质说明B、C装置中现象不同的原因
____。
(2)Cl 是有毒气体,为了防止多余Cl 污染空气,可以在D处用如图装置进行尾气处理,用化学方程式
2 2
表示该原理____。气体应该由____(填“a”或“b”)管通入。若要吸收224mLCl (标况下),至少需要
2
1mol/L的上述溶液____mL。
23.实验室配制100mL0.5mol/LNa SO 溶液。
2 4
(1)用托盘天平称量,需要称取NaSO 固体的质量为____g。
2 4
(2)实验过程中需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和____。
(3)实验过程中其它操作均正确,只是定容时不小心加水超过了刻度线,则配制的NaSO 溶液实际浓度
2 4
比目标浓度(填“偏大”或“偏小”)_____。
(4)写出NaSO 在水中的电离方程式_____。
2 4
(5)取出配制准确的该溶液50mL,将其稀释到500mL,此时溶液中Na+的物质的量浓度____mol/L。
24.了解物质的元素组成和物质的分类,有利于我们更好地认识和利用物质的性质、实现物质之间的转化。
市场上有一种“自热米饭”,其发热包的主要成分为生石灰(CaO),使用时需要将一定量的水加入发热
包。
(1)结合化学方程式解释自热米饭的发热原理____。
(2)生石灰属于哪种类别 的物质?____。除了能和水反应外,生石灰还可以与哪些类别的物质发生化学
反应?列举两种物质类别并各写出一个相应的化学方程式。_____。
物质类别 化学方程式(3)生活中生石灰还可以用作食品干燥剂。若选用生石灰做干燥剂,请判断其能否循环利用并说明理由。
_____。
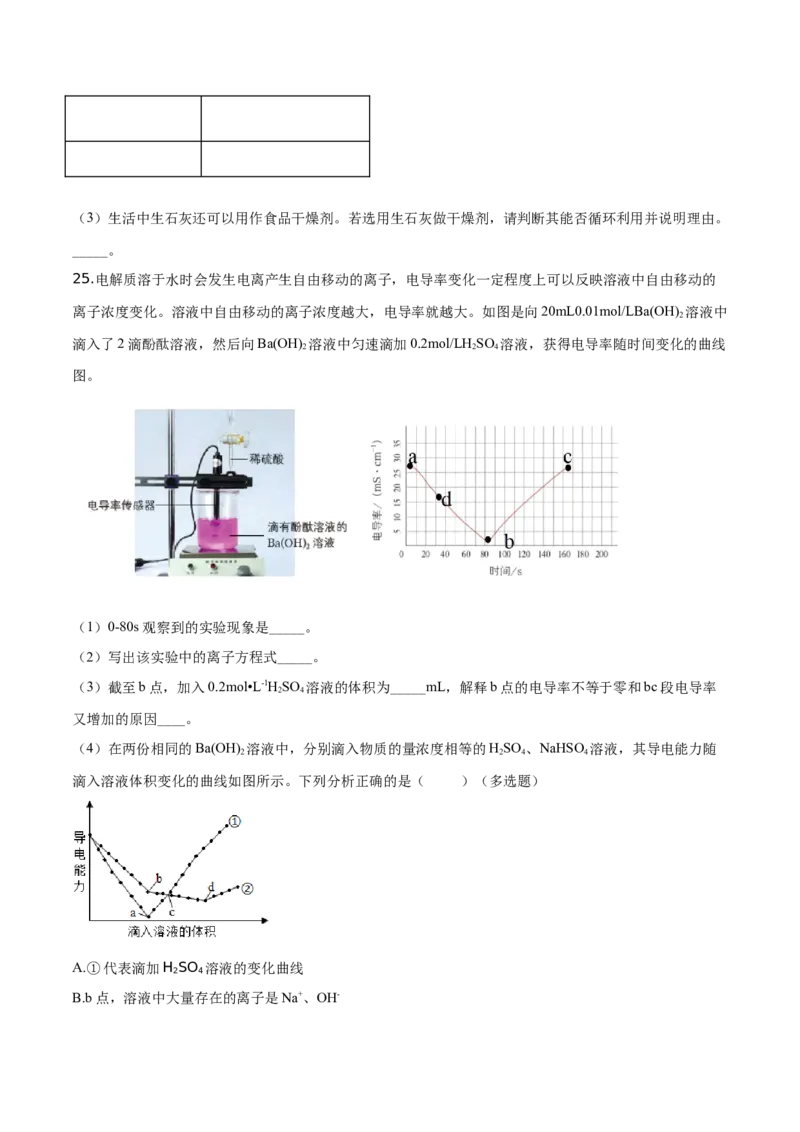
25.电解质溶于水时会发生电离产生自由移动的离子,电导率变化一定程度上可以反映溶液中自由移动的
离子浓度变化。溶液中自由移动的离子浓度越大,电导率就越大。如图是向20mL0.01mol/LBa(OH) 溶液中
2
滴入了2滴酚酞溶液,然后向Ba(OH) 溶液中匀速滴加0.2mol/LH SO 溶液,获得电导率随时间变化的曲线
2 2 4
图。
(1)0-80s观察到的实验现象是_____。
(2)写出该实验中的离子方程式_____。
(3)截至b点,加入0.2mol•L-1HSO 溶液的体积为_____mL,解释b点的电导率不等于零和bc段电导率
2 4
又增加的原因____。
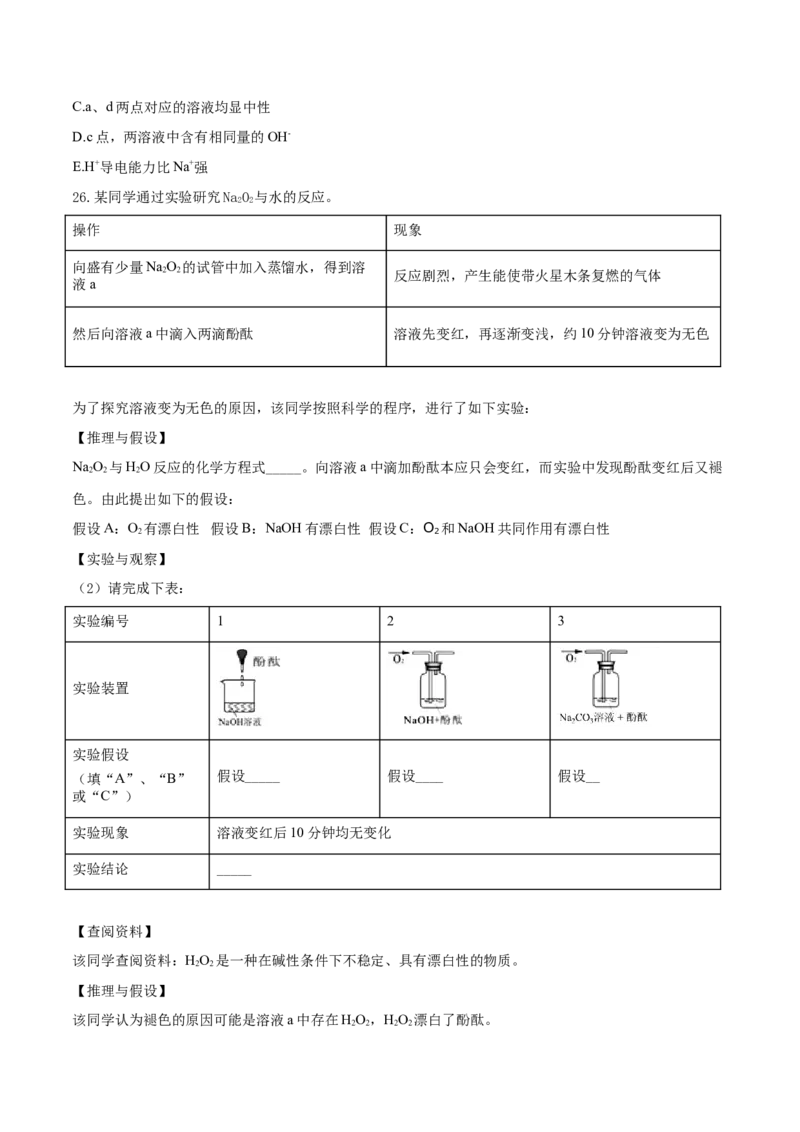
(4)在两份相同的Ba(OH) 溶液中,分别滴入物质的量浓度相等的HSO 、NaHSO 溶液,其导电能力随
2 2 4 4
滴入溶液体积变化的曲线如图所示。下列分析正确的是( )(多选题)
A.①代表滴加H SO 溶液的变化曲线
2 4
B.b点,溶液中大量存在的离子是Na+、OH-C.a、d两点对应的溶液均显中性
D.c点,两溶液中含有相同量的OH-
E.H+导电能力比Na+强
26.某同学通过实验研究NaO 与水的反应。
2 2
操作 现象
向盛有少量NaO 的试管中加入蒸馏水,得到溶
2 2 反应剧烈,产生能使带火星木条复燃的气体
液a
然后向溶液a中滴入两滴酚酞 溶液先变红,再逐渐变浅,约10分钟溶液变为无色
为了探究溶液变为无色的原因,该同学按照科学的程序,进行了如下实验:
【推理与假设】
NaO 与HO反应的化学方程式_____。向溶液a中滴加酚酞本应只会变红,而实验中发现酚酞变红后又褪
2 2 2
色。由此提出如下的假设:
假设A:O 有漂白性 假设B:NaOH有漂白性 假设C:O 和NaOH共同作用有漂白性
2 2
【实验与观察】
(2)请完成下表:
实验编号 1 2 3
实验装置
实验假设
(填“A”、“B” 假设_____ 假设____ 假设__
或“C”)
实验现象 溶液变红后10分钟均无变化
实验结论 _____
【查阅资料】
该同学查阅资料:HO 是一种在碱性条件下不稳定、具有漂白性的物质。
2 2
【推理与假设】
该同学认为褪色的原因可能是溶液a中存在HO,HO 漂白了酚酞。
2 2 2 2【实验与观察】
(3)通过实验证实了HO 的存在:取少量溶液a,加入黑色粉末____(填化学式),快速产生了能使带
2 2
火星木条复燃的气体。该同学进一步通过实验证实了溶液a中滴入酚酞后,HO 与酚酞发生了化学反应。
2 2
实验方案:取少量溶液a于试管中,_____。
【解释与结论】
(4)由以上实验结果可知,NaO 与HO反应的化学方程式如果分两步书写,应为_____;但课本上没有
2 2 2
写出中间产物HO,可能的原因是___。
2 2