文档内容
丽水外国语实验学校高中部 2020 学年第一学期第三次月考
高一化学试卷
考生须知:
1.本卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,第Ⅰ卷第1题至第25题,第Ⅱ卷第26
题至第30题。全卷满分100分,考试时间90分钟。
2.本卷答案必须写在答题卷的相应位置上,写在试题卷上无效。
3.可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 S-32 Cl-35.5 K-39
Mn-55 Fe-56 Ba-137 N-14 Al-27
第Ⅰ卷(选择题,共50分)
一、选择题(本题包括25小题,每小题2分,共50分。每小题只有一个选项符合题意)
1. 下列属于氧化物的是
A. HO B. NaOH C. O D. NaCO
2 2 2 3
2. 下列分散系具有丁达尔效应的是
A. 蒸馏水 B. 氯化钠溶液
C. 氢氧化铝胶体 D. 硫酸铜溶液
3. 下列物质属于纯净物的是
A. 生铁 B. 碱石灰 C. 液氯 D. 漂白粉
4. 仪器名称为“容量瓶”的是
A. B. C. D.
5. 属于氧化还原反应的是
A. 2NaOH+H SO =Na SO +2H O B. 2NaCl+2H O 2NaOH+H ↑+Cl↑
2 4 2 4 2 2 2 2
C. NaCO+CO +H O=2NaHCO D. CaCO CO↑+CaO
2 3 2 2 3 3 2
6. 下列说法不正确的是( )
A. 核素23Na的中子数是12
B. 16O和18O互为同位素
C. 三种核素1H、2H、16O可构成3种水分子
学科网(北京)股份有限公司D. S2-结构示意图:
7. 下列物质属于共价化合物的是
A. NaCl B. CO C. CaCl D. NHCl
2 2 4
8. 下列说法中正确的是
A. Cl 有毒性,Cl-也有毒性
2
B. 氯水呈黄绿色,含Cl-的溶液也呈黄绿色
的
C. 纯净 H 在氯气中能安静地燃烧,发出苍白色火焰
2
D. Cl 不溶于水,所以可用排水法收集
2
9. 下列元素中,原子半径最大的是
A. H B. Li C. Na D. K
10. 下列离子方程式书写正确的是( )
A. 用FeCl 溶液腐蚀铜线路板:Cu+Fe3+=Cu2++Fe2+
3
B. Na O 固体与HO反应产生O:2NaO+2H O=4Na++4OH-+O ↑
2 2 2 2 2 2 2 2
C. Ba(OH) 溶液中加入稀硫酸:Ba2++OHˉ+H++SO =BaSO ↓+H O
2 4 2
D. 稀HSO 与铁粉反应:2Fe+6H+=2Fe3++3H ↑
2 4 2
11. 下列说法正确的是
A. 焰色反应的铂丝可用稀硫酸洗涤
B. 常温下铁遇浓硫酸会发生钝化
C. 工业上用氯气和石灰水为原料制漂白粉
.
D 氯化铁溶液中加入硫氰化钾溶液产生血红色沉淀
12. 下列溶液中氯离子浓度最大的是
A. 250mL0.5mol·L-1的MgCl 溶液 B. 100mL1mol·L-1的AlCl 溶液
2 3
C. 200mL1.5mol·L-1的NaCl溶液 D. 150mL3mol·L-1的KClO 溶液
3
13. 下列化学反应中溴元素仅被氧化的是
A. 2NaBr+Cl=2NaCl+Br B. Br+2NaI=2NaBr+I
2 2 2 2
C. 3Br+6NaOH 5NaBr+NaBrO+3HO D. HBr+NaOH=NaBr+HO
2 3 2 2
14. 某实验需要0.2mol/L 的CuSO 溶液490mL,配制时应选用的容量瓶的规格和称取硫酸铜晶体
4
(CuSO ·5H O)的质量分别是
4 2
A. 500mL 25g B. 490mL 24.5g
C. 490mL 25g D. 500mL 24.5g
学科网(北京)股份有限公司15. 铯(Cs)在自然界中只有一种稳定同位素 Cs,核泄漏事故中会产生人工放射性同位素 Cs、 Cs。
下列有关说法正确的是
A. 铯元素的相对原子质量约为133 B. Cs、 Cs的化学性质相同
C. Cs的电子数为79 D. Cs、 Cs互为同素异形体
16. 用一定方法可除去下列物质所含的少量杂质(括号内为杂质),其中所加物质能达到除杂目的的是
.
A Cl(HCl)用NaOH溶液
2
B. NaCO(NaHCO )固体用HCl溶液
2 3 3
C. 溶液NaHCO (Na CO)通入足量二氧化碳
3 2 3
D. CO(HCl)用饱和碳酸钠溶液
2
17. 如图,将潮湿的Cl 通过甲装置后再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所
2
盛试剂不可能是( )
A. 饱和食盐水 B. 浓硫酸 C. FeCl 溶液 D. NaOH溶液
2
18. 将一小块金属钠加入CuSO 溶液中不可能观察到的实验现象是( )
4
A. 有无色无味气体产生 B. 溶液中析出红色固体
C. 溶液中产生蓝色沉淀 D. 钠块在溶液表面四处游动
19. 下列各组化合物中,化学键的类型完全相同的是( )
①CaCl 和NaS ②NaO和NaO ③CO 和CS ④HCl和NaOH
2 2 2 2 2 2 2
A. ①② B. ①③ C. ②③ D. ②④
20. 下列离子在水溶液中能大量共存的是
A. Na+、K+、Cl-、HCO B. Na+、Ca2+、NO 、CO
C. NH 、Fe3+、SO 、OH- D. Ag+、Cu2+、Cl-、SO
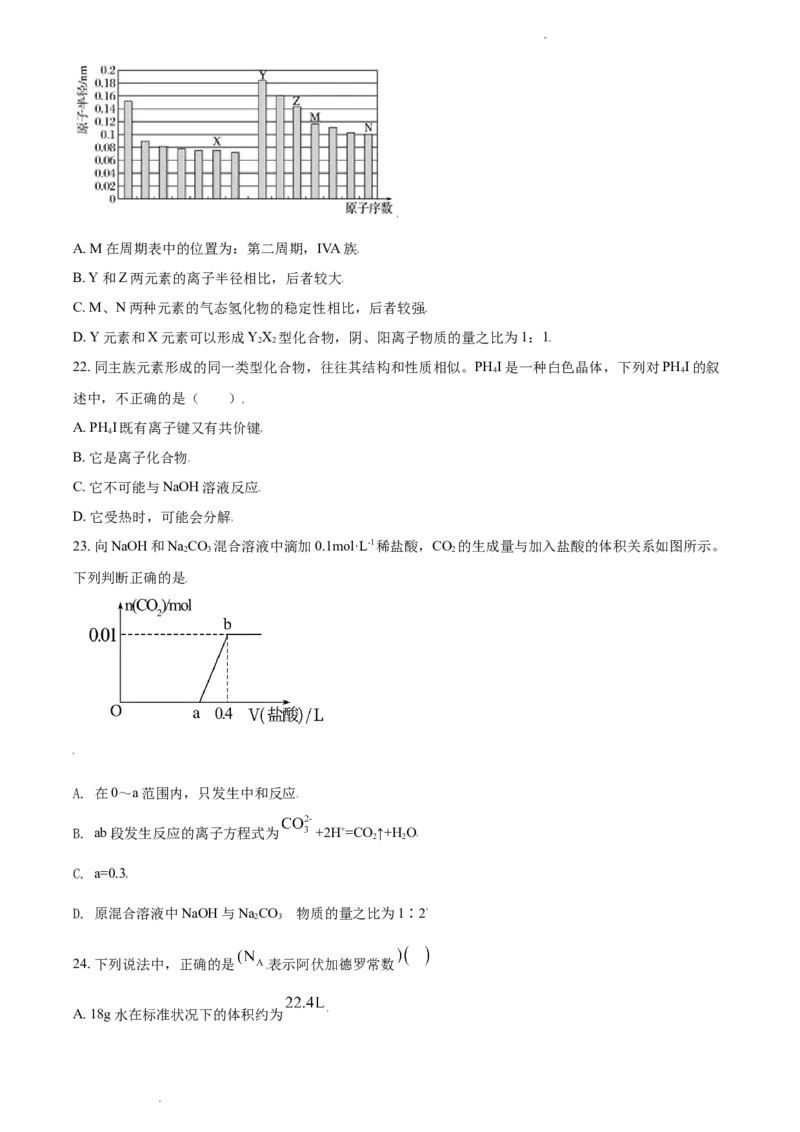
21. 如图所示是部分短周期元素原子半径与原子序数的关系,则下列说法正确的是( )
学科网(北京)股份有限公司A. M在周期表中的位置为:第二周期,IVA族
B. Y和Z两元素的离子半径相比,后者较大
C. M、N两种元素的气态氢化物的稳定性相比,后者较强
D. Y元素和X元素可以形成YX 型化合物,阴、阳离子物质的量之比为1:1
2 2
22. 同主族元素形成的同一类型化合物,往往其结构和性质相似。PH I是一种白色晶体,下列对PH I的叙
4 4
述中,不正确的是( )
A. PH I既有离子键又有共价键
4
B. 它是离子化合物
C. 它不可能与NaOH溶液反应
D. 它受热时,可能会分解
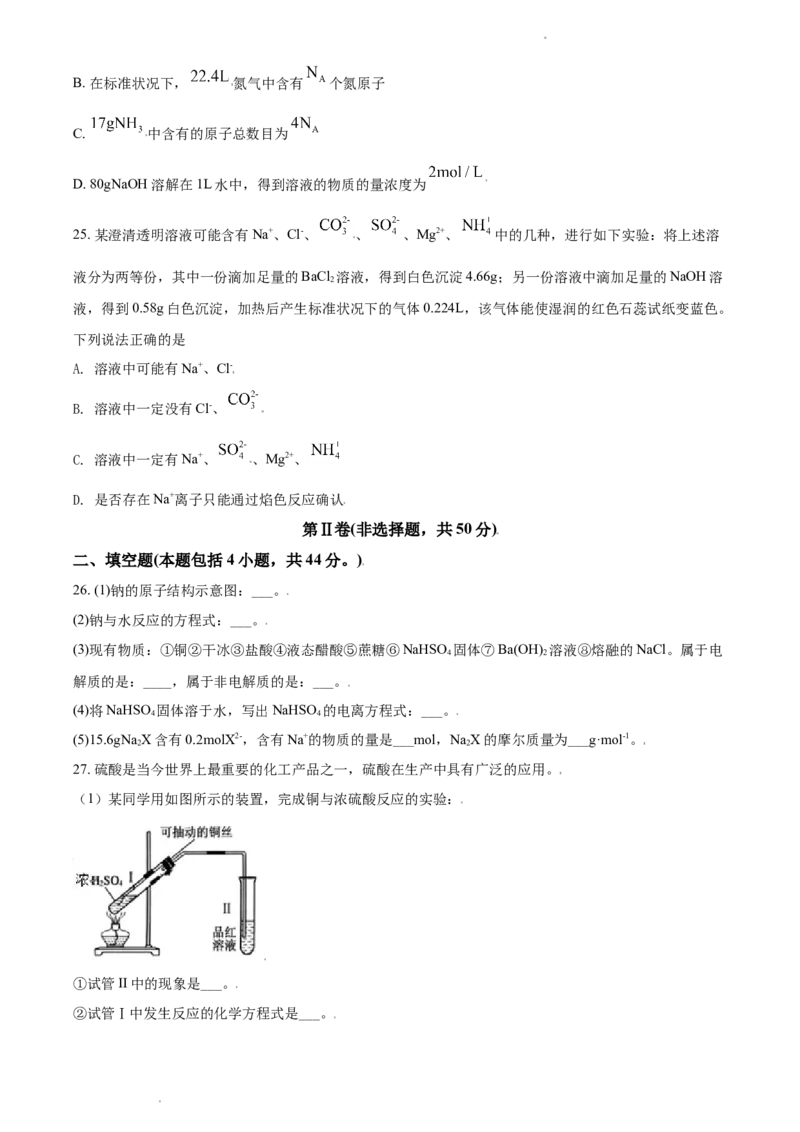
23. 向NaOH和NaCO 混合溶液中滴加0.1mol·L-1稀盐酸,CO 的生成量与加入盐酸的体积关系如图所示。
2 3 2
下列判断正确的是
A. 在0~a范围内,只发生中和反应
B. ab段发生反应的离子方程式为 +2H+=CO ↑+H O
2 2
C. a=0.3
的
D. 原混合溶液中NaOH与NaCO 物质的量之比为1∶2
2 3
24. 下列说法中,正确的是 表示阿伏加德罗常数
A. 18g水在标准状况下的体积约为
学科网(北京)股份有限公司B. 在标准状况下, 氮气中含有 个氮原子
C. 中含有的原子总数目为
D. 80gNaOH溶解在1L水中,得到溶液的物质的量浓度为
25. 某澄清透明溶液可能含有Na+、Cl-、 、 、Mg2+、 中的几种,进行如下实验:将上述溶
液分为两等份,其中一份滴加足量的BaCl 溶液,得到白色沉淀4.66g;另一份溶液中滴加足量的NaOH溶
2
液,得到0.58g白色沉淀,加热后产生标准状况下的气体0.224L,该气体能使湿润的红色石蕊试纸变蓝色。
下列说法正确的是
A. 溶液中可能有Na+、Cl-
B. 溶液中一定没有Cl-、
C. 溶液中一定有Na+、 、Mg2+、
D. 是否存在Na+离子只能通过焰色反应确认
第Ⅱ卷(非选择题,共50分)
二、填空题(本题包括4小题,共44分。)
26. (1)钠的原子结构示意图:___。
(2)钠与水反应的方程式:___。
(3)现有物质:①铜②干冰③盐酸④液态醋酸⑤蔗糖⑥NaHSO 固体⑦Ba(OH) 溶液⑧熔融的NaCl。属于电
4 2
解质的是:____,属于非电解质的是:___。
(4)将NaHSO 固体溶于水,写出NaHSO 的电离方程式:___。
4 4
(5)15.6gNa X含有0.2molX2-,含有Na+的物质的量是___mol,NaX的摩尔质量为___g·mol-1。
2 2
27. 硫酸是当今世界上最重要的化工产品之一,硫酸在生产中具有广泛的应用。
(1)某同学用如图所示的装置,完成铜与浓硫酸反应的实验:
①试管II中的现象是___。
②试管Ⅰ中发生反应的化学方程式是___。
学科网(北京)股份有限公司③请你指出该实验装置的不足之处___。
(2)在实际应用中,人们常根据需要,把浓硫酸稀释成不同浓度的稀硫酸。现用18.4mol·L-1的浓HSO
2 4
配制100mL1.00mol·L-1的稀HSO 。
2 4
①用量筒量取浓硫酸的体积是___mL。
②下列操作会使所配溶液浓度偏低的是___。
A.将溶液转移到未干燥的容量瓶中
B.转移时,忘记洗涤烧杯和玻璃棒
C.将未冷却的溶液转移到容量瓶中
D.定容时,仰视刻度线
28. 元素周期表是化学学习和化学研究的重要工具。下表为元素周期表的一部分,表中①~⑩分别代表一
种元素。回答下列问题:
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
1 ①
2 ② ③ ④ ⑤ ⑥ ⑦
3 ⑧ ⑨ ⑩
的
(1)上述元素中,有一种是地壳中含量最多 元素,该元素在周期表中的位置是_________。
(2)⑦、⑧、⑨元素的离子半径由大到小的顺序为_________(用离子符号表示)。
(3)由①、⑥、⑩组成的一种化合物有强氧化性,具有杀菌漂白的能力,则该化合物的电子式为_______。
(4)由⑤、⑥两元素组成的气态化合物常见的有两种,其中有一种不能用排水法收集,试用化学方程式解
释原因________。
(5)上述元素中有一种元素的氧化物和氢氧化物都是两性化合物,画出该元素的原子结构示意图______,
且该元素的单质可以溶解在氢氧化钠溶液中,写出该过程发生的离子方程式_____。
(6)不同卤素原子之间可形成卤素互化物,如I和Br形成的互化物IBr,其性质与卤素单质相近。⑩和Br
形成的互化物可以和SO 在水溶液中发生反应,该反应的化学方程式为___________。
2
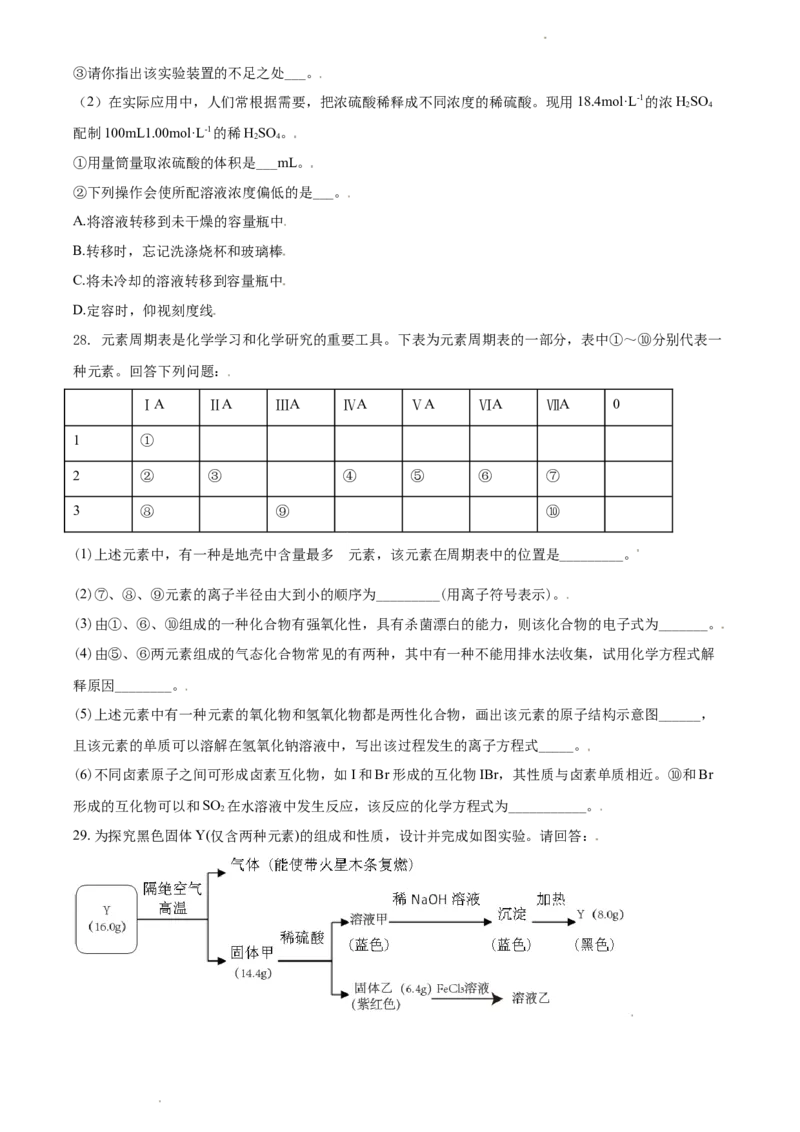
29. 为探究黑色固体Y(仅含两种元素)的组成和性质,设计并完成如图实验。请回答:
学科网(北京)股份有限公司(1)Y的化学式是___;
(2)固体乙与FeCl 溶液反应的化学方程式是___;
3
(3)固体甲与稀硫酸反应的离子方程式是___。
三、计算题(6分)
30. 将一定质量的镁和铝的合金投入100 mL,一定物质的量浓度的盐酸中,恰好反应,共产生气体5.6
L(标准状况下),向所得溶液中滴加5mol·L-1NaOH溶液至过量,最终产生白色沉淀13.6 g。请计算:
(1)原合金中镁和铝的质量分别是________。
(2)原盐酸溶液的物质的量浓度________。
学科网(北京)股份有限公司学科网(北京)股份有限公司