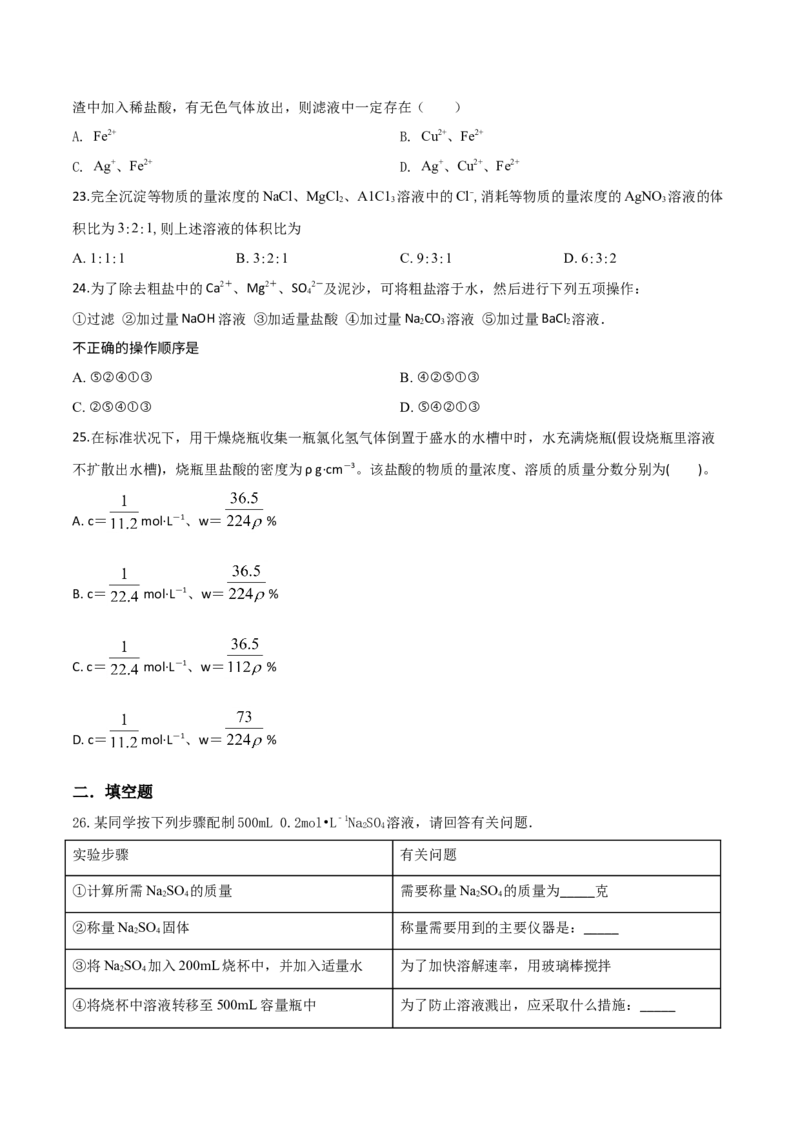文档内容
2019~2010 学年 高一第一学期期中试卷
化学
(清华附中高19级)
可能用到的相对原子质量H-1; C-2; N-14;O-16;Na-23; Mg-24; Al-27; Cl-35.5; Fe-56; Cu-64;
Ag-108; Ba-137; Zn-65.
一.选择题(单选题,25个,每个2分,共50分)
1.下列科研成果不是由我国发明或创造的是( )
A. 世界上第一个由人工合成的、具有生理活性的蛋白质﹣﹣结晶牛胰岛素
B. 黑火药和造纸
C. 发现元素周期律
D. 青蒿素的合成
2.我国女科学家屠呦呦发现青蒿素(青蒿素的化学式:C H O),它是一种用于治疗疟疾的药物,曾经挽
15 22 5
救了数百万人的生命,2015年获得诺贝尔生理与医学奖,成为我国获得诺贝尔科学奖的第一人.下列关于
青蒿素的叙述错的是( )
A. 青蒿素的一个分子中含有42个原子
B. 青蒿素是一种有机物
C. 青蒿素的摩尔质量为282
D. 青蒿素中碳元素的质量分数约为63.8%
3.下列叙述不正确的是( )
A. 切开的金属Na暴露在空气中,光亮的表面逐渐变暗2Na+O═Na O
2 2 2
B. 将少量Na投入到CuSO 溶液中,有红色固体生成
4
C. Na与HO反应的离子方程式为2Na+2HO═2Na++2OH﹣+H ↑
2 2 2
D. 金属钠着火时,使用泡沫灭火器灭
4. 下列物质能使干燥的蓝色石蕊试纸先变红后褪色的是( )
①氯气 ②液氯 ③新制氯水 ④氯气 的四氯化碳溶液 ⑤盐酸 ⑥盐酸与少量漂白粉的混合溶液
A. ①②③ B. ①②③⑥ C. ③⑥ D. ③④⑥
5.下列物质中,与氯气、盐酸都能发生反应且生成不同氯化物的是
A. Fe B. Al C. Cu D. Zn
6.在氯水中存在多种分子和离子,它们在不同的反应中表现各自的性质.下列实验现象和结论一致且正确的是( )
A. 加入有色布条,一会儿有色布条褪色,说明溶液中有Cl 存在
2
B. 溶液呈黄绿色,说明有Cl 分子存在
2
C. 向氯水中加入NaOH粉末,有气泡产生,说明氯水中含有HClO
D. 加入AgNO 溶液,出现白色沉淀,说明有ClO﹣存在
3
7.下列溶液中Cl﹣浓度由大到小的顺序是( )
①200mL 2mol/L MgCl 溶液
2
②1000mL 2.5mol/L NaCl溶液
③300mL 5mol/L KCl溶液
④250mL 1mol/L FeCl 溶液。
3
A. ③①④② B. ④①②③ C. ③②①④ D. ②③①④
8.下列物质分类的正确组合是( )
碱 酸 盐 碱性氧化物 酸性氧化物
A Cu (OH)CO HSO NaHCO SiO CO
2 2 3 2 4 3 2 2
B NaOH HCl NaCl NaO CO
2
C NaOH NH CaCl MgO SO
3 2 2
D KOH HNO CaCO CaO SO
3 3 3
A. A B. B C. C D. D
9.下列各组物质中分子数相同的是( )
A. 2L CO和2L CO B. 9g HO和标准状况下11.2L CO
2 2 2
C. 标准状况下1mol O 和22.4L HO D. 0.2mol H 和4.48L HCl气体
2 2 2
10.下列叙述中,正确的是( )
A. 1.6g O 和O 的混合物含有氧原子的数目为0.1 N
2 3 A
B. 2 L 0.3mol•L﹣1 硫酸钾溶液中钾离子的物质的量为0.6mol
C. 标准状况下,22.4L H O 中的分子数为N
2 A
D. 11.2L CO 所含有的碳原子数为 0.5N
2 A
11.磁流体是电子材料的新秀,它是由直径为纳米量级(1到10 nm之间)的磁性固体颗粒、基载液以及界面活性剂三者混合而成的分散系,既具有固体的磁性,又具有液体的流动性,下列关于纳米Fe O 磁流体的
3 4
说法中不正确的是( )
A. 纳米Fe O 磁流体分散系属于溶液
3 4
B. 纳米Fe O 磁流体可以通过半透膜得到提纯
3 4
C. 当一束可见光通过该磁流体时会出现光亮的通路
D. 纳米Fe O 磁流体比较稳定
3 4
12.下列各项说法正确的是( )
的
①“卤水点豆腐”、“黄河入海口处 沙洲形成”都与胶体的聚沉有关
②若将Fe(OH) 胶体提纯,可以采用的方法是过滤
3
③沸水中滴加适量饱和FeCl 溶液,形成带电的微粒,水导电能力增强
3
④明矾能作净水剂是因为铝离子与水作用生成氢氧化铝胶体具有吸附悬浮杂质的作用
⑤在制备Fe(OH) 胶体实验中,可以长时间加热
3
为
⑥向Fe(OH) 胶体中加入过量稀硫酸,先有红褐色沉淀生成,然后沉淀溶解 黄色溶液
3
A. 3个 B. 4个 C. 5个 D. 6个
13.下列叙述中正确的是( )
A. 强电解质溶液的导电性一定比弱电解质溶液的导电性强
B. 稀盐酸溶液能导电,所以稀盐酸是电解质
C. 二氧化硫溶于水能导电,故二氧化硫属于电解质
D. 硫酸钡虽然难溶于水,但硫酸钡属于电解质
14.下列物质在水溶液中的电离方程式书写错误的是( )
A. NaHSO=Na++H++SO2﹣
4 4
B. A1 (SO )=2A13++3SO2﹣
2 4 3 4
C. Ba(OH)=Ba2++2OH﹣
2
D. NaHCO =Na++H++CO 2﹣
3 3
15.下列离子方程式中,不正确的是( )
A. 氯气溶于水:Cl+H O═2H++Cl﹣+ClO﹣
2 2
B. 盐酸与氢氧化钡溶液:H++OH﹣═H O
2
C. 碳酸钙与稀硝酸:CaCO +2H+═Ca2++CO ↑+H O
3 2 2
D. 硫酸铜和氢氧化钡溶液:Cu2++SO2﹣+Ba2++OH﹣═BaSO ↓+Cu(OH)↓
4 4 2
16.在pH=1的溶液中,可以大量共存的离子是( )A. K+、Na +、SO 2﹣、SO 2﹣
4 3
B. Na +、K +、HCO ﹣、Cl ﹣
3
C. NH +、Mg 2+、SO 2﹣、Cl ﹣
4 4
.
D K +、Na +、OH﹣ 、NO ﹣
3
17.下列离子方程式中书写正确的是( )
A. 氧化亚铁与稀盐酸反应:FeO+2H+=Fe3++H O
2
B. 碳酸钙和醋酸反应:CaCO +2H+=Ca2++CO ↑+H O
3 2 2
C. 钠与水反应:Na+HO=Na++OH-+H ↑
2 2
D. 将氢氧化铁胶体放入过量的盐酸:Fe(OH)+3H+=Fe3++3H O
3 2
18. 某无色溶液中加入氯化钡后有白色沉淀,再加稀硝酸沉淀不消失,则该溶液中
A. 一定含有SO 2- B. 一定含有Ag+
4
C. 可能含有SO 2-或Ag+ D. 一定含有Ag+、SO 2-
4 4
19.向含有下列离子的溶液中分别加入SO 固体后,溶液中下列离子个数不变的是( )
3
A. Mg2+ B. CO2﹣ C. Ba2+ D. SO 2﹣
3 3
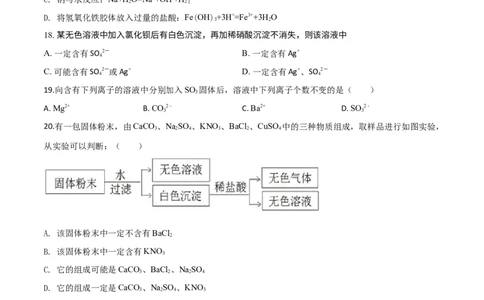
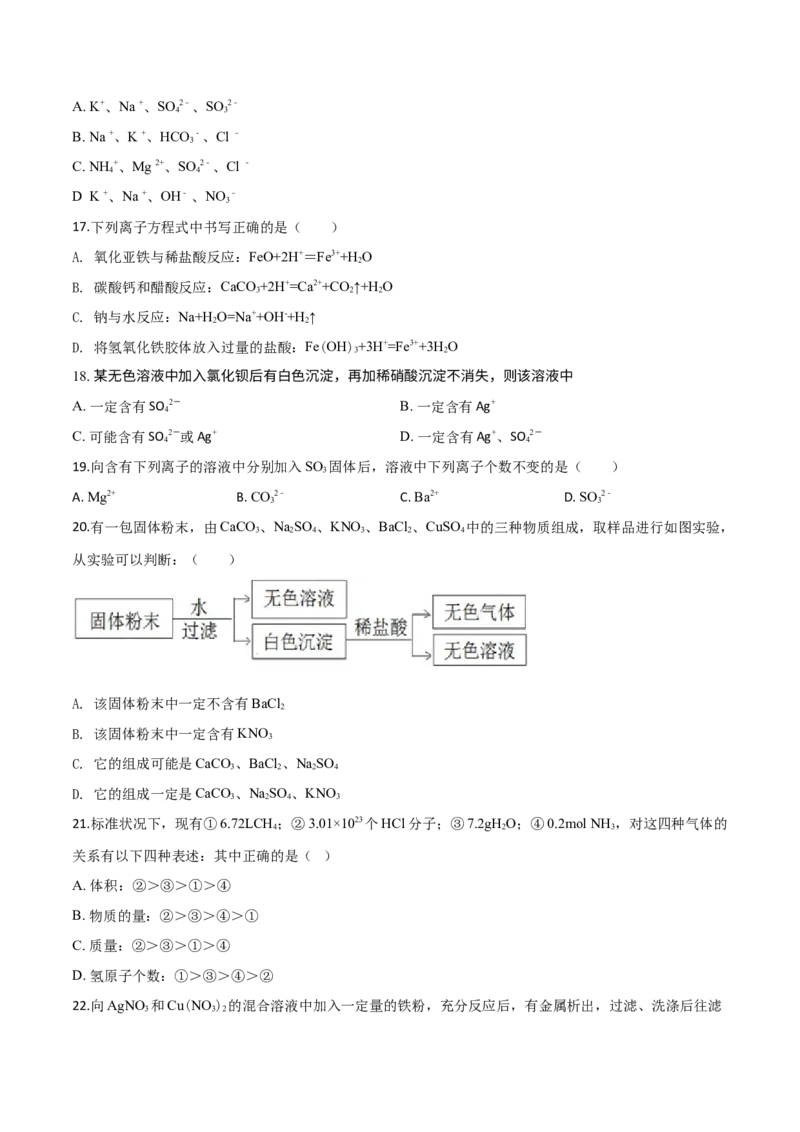
20.有一包固体粉末,由CaCO 、NaSO 、KNO、BaCl 、CuSO 中的三种物质组成,取样品进行如图实验,
3 2 4 3 2 4
从实验可以判断:( )
A. 该固体粉末中一定不含有BaCl
2
B. 该固体粉末中一定含有KNO
3
C. 它的组成可能是CaCO 、BaCl 、NaSO
3 2 2 4
D. 它的组成一定是CaCO 、NaSO 、KNO
3 2 4 3
21.标准状况下,现有①6.72LCH ;②3.01×1023个HCl分子;③7.2gH O;④0.2mol NH ,对这四种气体的
4 2 3
关系有以下四种表述:其中正确的是( )
A. 体积:②>③>①>④
B. 物质的量:②>③>④>①
C. 质量:②>③>①>④
D. 氢原子个数:①>③>④>②
22.向AgNO 和Cu(NO ) 的混合溶液中加入一定量的铁粉,充分反应后,有金属析出,过滤、洗涤后往滤
3 3 2渣中加入稀盐酸,有无色气体放出,则滤液中一定存在( )
A. Fe2+ B. Cu2+、Fe2+
C. Ag+、Fe2+ D. Ag+、Cu2+、Fe2+
23.完全沉淀等物质的量浓度的NaCl、MgCl 、A1C1 溶液中的Cl-,消耗等物质的量浓度的AgNO 溶液的体
2 3 3
积比为3:2:1,则上述溶液的体积比为
A. 1:1:1 B. 3:2:1 C. 9:3:1 D. 6:3:2
24.为了除去粗盐中的Ca2+、Mg2+、SO 2-及泥沙,可将粗盐溶于水,然后进行下列五项操作:
4
①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na CO 溶液 ⑤加过量BaCl 溶液.
2 3 2
不正确的操作顺序是
A. ⑤②④①③ B. ④②⑤①③
C. ②⑤④①③ D. ⑤④②①③
25.在标准状况下,用干燥烧瓶收集一瓶氯化氢气体倒置于盛水的水槽中时,水充满烧瓶(假设烧瓶里溶液
不扩散出水槽),烧瓶里盐酸的密度为ρ g·cm-3。该盐酸的物质的量浓度、溶质的质量分数分别为( )。
A. c= mol·L-1、w= %
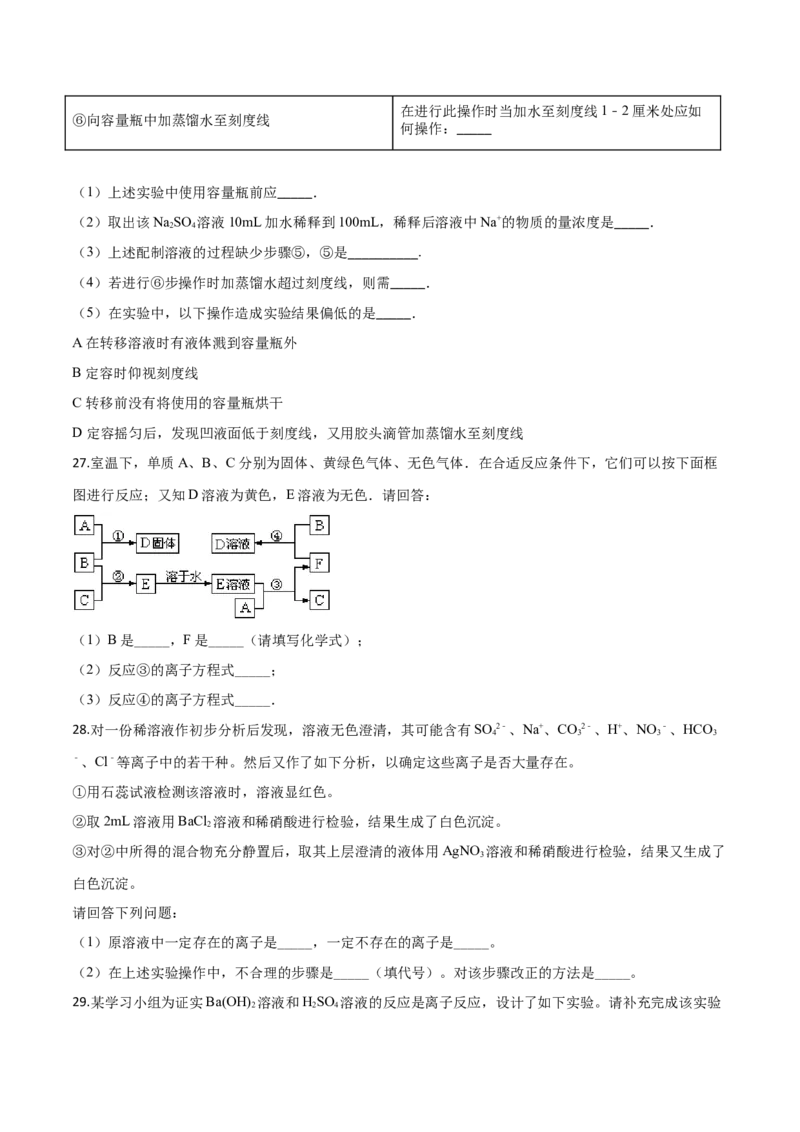
B. c= mol·L-1、w= %
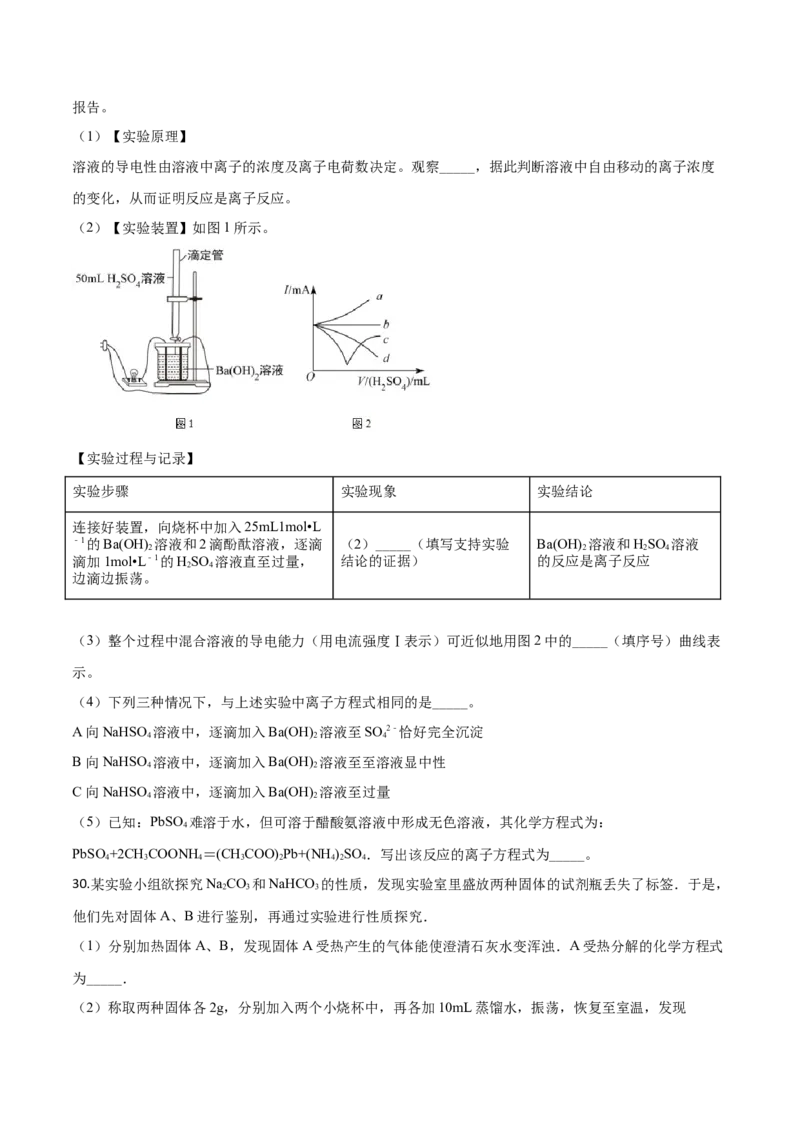
C. c= mol·L-1、w= %
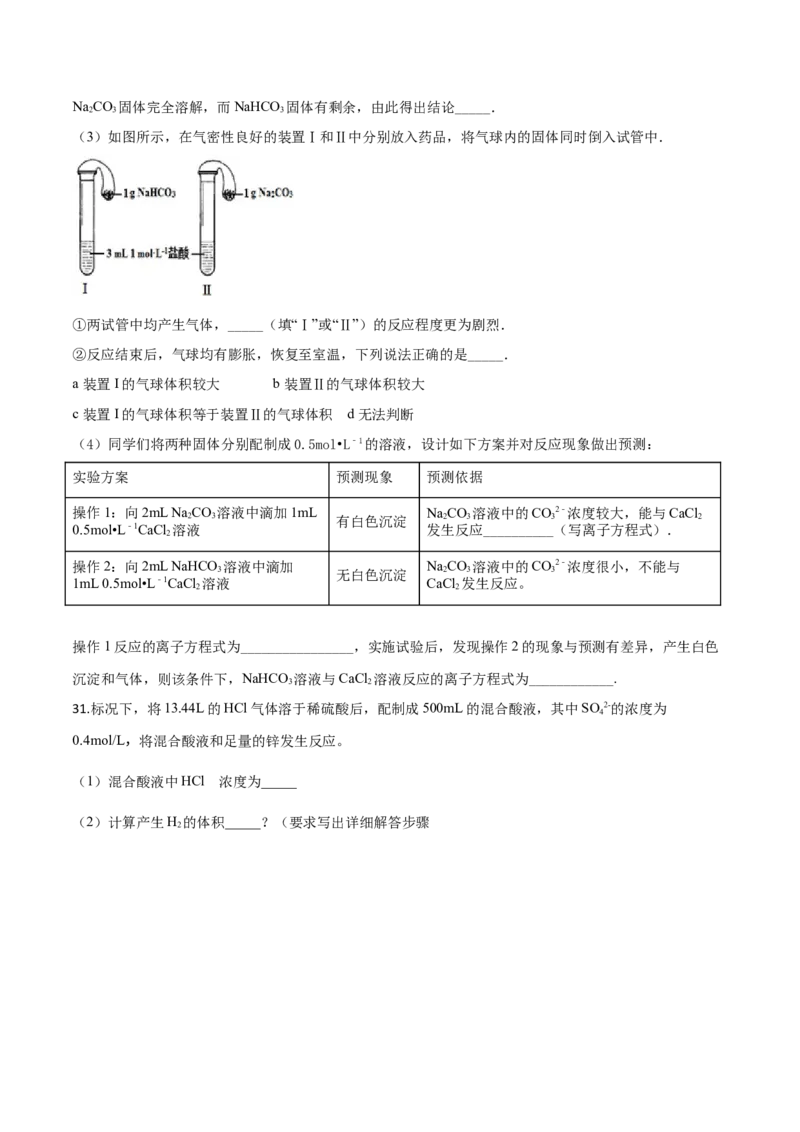
D. c= mol·L-1、w= %
二.填空题
26.某同学按下列步骤配制500mL 0.2mol•L﹣1NaSO 溶液,请回答有关问题.
2 4
实验步骤 有关问题
①计算所需NaSO 的质量 需要称量NaSO 的质量为_____克
2 4 2 4
②称量NaSO 固体 称量需要用到的主要仪器是:_____
2 4
③将NaSO 加入200mL烧杯中,并加入适量水 为了加快溶解速率,用玻璃棒搅拌
2 4
④将烧杯中溶液转移至500mL容量瓶中 为了防止溶液溅出,应采取什么措施:_____在进行此操作时当加水至刻度线1﹣2厘米处应如
⑥向容量瓶中加蒸馏水至刻度线
何操作:_____
(1)上述实验中使用容量瓶前应_____.
(2)取出该NaSO 溶液10mL加水稀释到100mL,稀释后溶液中Na+的物质的量浓度是_____.
2 4
(3)上述配制溶液的过程缺少步骤⑤,⑤是__________.
(4)若进行⑥步操作时加蒸馏水超过刻度线,则需_____.
(5)在实验中,以下操作造成实验结果偏低的是_____.
A 在转移溶液时有液体溅到容量瓶外
B 定容时仰视刻度线
C 转移前没有将使用的容量瓶烘干
D 定容摇匀后,发现凹液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
27.室温下,单质A、B、C分别为固体、黄绿色气体、无色气体.在合适反应条件下,它们可以按下面框
图进行反应;又知D溶液为黄色,E溶液为无色.请回答:
(1)B是_____,F是_____(请填写化学式);
(2)反应③的离子方程式_____;
(3)反应④的离子方程式_____.
28.对一份稀溶液作初步分析后发现,溶液无色澄清,其可能含有SO 2﹣、Na+、CO2﹣、H+、NO ﹣、HCO
4 3 3 3
﹣、Cl﹣等离子中的若干种。然后又作了如下分析,以确定这些离子是否大量存在。
①用石蕊试液检测该溶液时,溶液显红色。
②取2mL溶液用BaCl 溶液和稀硝酸进行检验,结果生成了白色沉淀。
2
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO 溶液和稀硝酸进行检验,结果又生成了
3
白色沉淀。
请回答下列问题:
(1)原溶液中一定存在的离子是_____,一定不存在的离子是_____。
(2)在上述实验操作中,不合理的步骤是_____(填代号)。对该步骤改正的方法是_____。
29.某学习小组为证实Ba(OH) 溶液和HSO 溶液的反应是离子反应,设计了如下实验。请补充完成该实验
2 2 4报告。
(1)【实验原理】
溶液的导电性由溶液中离子的浓度及离子电荷数决定。观察_____,据此判断溶液中自由移动的离子浓度
的变化,从而证明反应是离子反应。
(2)【实验装置】如图1所示。
【实验过程与记录】
实验步骤 实验现象 实验结论
连接好装置,向烧杯中加入25mL1mol•L
﹣1的Ba(OH) 溶液和2滴酚酞溶液,逐滴 (2)_____(填写支持实验 Ba(OH) 溶液和HSO 溶液
2 2 2 4
滴加1mol•L﹣1的HSO 溶液直至过量, 结论的证据) 的反应是离子反应
2 4
边滴边振荡。
(3)整个过程中混合溶液的导电能力(用电流强度Ⅰ表示)可近似地用图2中的_____(填序号)曲线表
示。
(4)下列三种情况下,与上述实验中离子方程式相同的是_____。
A 向NaHSO 溶液中,逐滴加入Ba(OH) 溶液至SO 2﹣恰好完全沉淀
4 2 4
B 向NaHSO 溶液中,逐滴加入Ba(OH) 溶液至至溶液显中性
4 2
C 向NaHSO 溶液中,逐滴加入Ba(OH) 溶液至过量
4 2
(5)已知:PbSO 难溶于水,但可溶于醋酸氨溶液中形成无色溶液,其化学方程式为:
4
PbSO +2CH COONH=(CHCOO) Pb+(NH )SO .写出该反应的离子方程式为_____。
4 3 4 3 2 4 2 4
30.某实验小组欲探究NaCO 和NaHCO 的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签.于是,
2 3 3
他们先对固体A、B进行鉴别,再通过实验进行性质探究.
(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊.A受热分解的化学方程式
为_____.
(2)称取两种固体各2g,分别加入两个小烧杯中,再各加10mL 蒸馏水,振荡,恢复至室温,发现NaCO 固体完全溶解,而NaHCO 固体有剩余,由此得出结论_____.
2 3 3
(3)如图所示,在气密性良好的装置Ⅰ和Ⅱ中分别放入药品,将气球内的固体同时倒入试管中.
①两试管中均产生气体,_____(填“Ⅰ”或“Ⅱ”)的反应程度更为剧烈.
②反应结束后,气球均有膨胀,恢复至室温,下列说法正确的是_____.
a 装置 I的气球体积较大 b 装置Ⅱ的气球体积较大
c 装置 I的气球体积等于装置Ⅱ的气球体积 d 无法判断
(4)同学们将两种固体分别配制成0.5mol•L﹣1的溶液,设计如下方案并对反应现象做出预测:
实验方案 预测现象 预测依据
操作1:向2mL Na CO 溶液中滴加1mL NaCO 溶液中的CO2﹣浓度较大,能与CaCl
2 3 有白色沉淀 2 3 3 2
0.5mol•L﹣1CaCl 溶液 发生反应__________(写离子方程式).
2
操作2:向2mL NaHCO 溶液中滴加 NaCO 溶液中的CO2﹣浓度很小,不能与
3 无白色沉淀 2 3 3
1mL 0.5mol•L﹣1CaCl 溶液 CaCl 发生反应。
2 2
操作1反应的离子方程式为________________,实施试验后,发现操作2的现象与预测有差异,产生白色
沉淀和气体,则该条件下,NaHCO 溶液与CaCl 溶液反应的离子方程式为____________.
3 2
31.标况下,将13.44L的HCl气体溶于稀硫酸后,配制成500mL的混合酸液,其中SO 2-的浓度为
4
0.4mol/L,将混合酸液和足量的锌发生反应。
的
(1)混合酸液中HCl 浓度为_____
(2)计算产生H 的体积_____?(要求写出详细解答步骤
2