文档内容
第 1 3 课时 质量守恒定律 化学方程式
考点1 质量守恒定律
1.下列对质量守恒定律的理解,正确的是( )[来源:学.科.网Z.X.X.K]
A.将5 g铁和5 g铜混合加热后,物质的总质量为10 g,遵循质量守恒定律
B.化学反应前后,分子的总数一定不会发生变化
C.5 g硫和5 g氧气完全反应后,生成物质量为10 g
D.镁条燃烧后质量增加,不遵循质量守恒定律
2.现有32 g某可燃物在密闭容器中完全燃烧后,测得生成88 g二氧化碳和72 g水,关于
该可燃物的说法正确的是( )
A.一定是氧化物
B.只含有碳、氢两种元素
C.一定含有碳、氢、氧三种元素
D.一定含有碳、氢元素,可能含有氧元素
3.某市空气受到SO 的严重污染,环保部门立即派出飞机喷洒X粉末,快速降低空气中
2
SO 含量,该过程发生的化学方程式是2X+2SO +O===2CaSO +2CO,X的化学式是( )
2 2 2 4 2
A.HO B.NaCO C.CaO D.CaCO
2 2 3 3
4.用下列装置来验证质量守恒定律(托盘天平未画出),能达到目的的是( )
图K13-1
5.高纯硅是信息产业最基础的原材料。制备高纯硅的主要生产过程如下,请回答:
图K13-2
(1)一个SiHCl 分子中含有氯原子的个数为____________。
3
(2)制备高纯硅的反应原理:SiHCl (纯)+H=====Si+3X,则X的化学式为________。
3 2
考点2 化学方程式
6.下列关于S+O=====SO 的理解不正确的是( )
2 2
A.表示硫与氧气在点燃条件下反应生成二氧化硫
B.参加反应的硫与氧气的质量比是2∶1
C.反应前后硫原子、氧原子的个数均不变
D.参加反应的氧气与生成的二氧化硫的分子个数比为1∶1
7.下列表中的叙述、对应的化学方程式和所属反应类型都正确的是( )
选项 叙述 化学反应方程式 反应类型[来源:学科网]
拉瓦锡研究空气成分[来
A 2HgO=====2Hg+O 分解反应
源:学科网ZXXK] 2
B 探究一氧化碳的还原性 CO+CuO=====Cu+ 置换反应CO
2
用二氧化碳制作碳酸饮
C CO+HO===H CO 化和反应
料 2 2 2 3
服用含氢氧化铝的药物 Al(OH) +3HCl===AlCl 复分解
D 3 3
治疗胃酸过多 +3HO 反应
2
考点3 根据化学方程式的简单计算
8.早在西汉时期的《淮南万毕术》中就记载的“曾青得铁则化为铜”,成为现代湿法冶金
的先驱。现有含1.6 kg硫酸铜的工业废液,加入铁粉回收铜,请计算:[来源:学科网ZXXK]
(1)硫酸铜中铜元素的质量分数。
(2)理论上与硫酸铜反应消耗铁粉的质量。
1.把一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间,
测得反应后各物质的质量如下,则下列说法中错误的是( )
物质 甲 乙 丙 丁
反应前的质量/g 7.6 2.0 0.2 0
反应后的质量/g 3.2 x 5.8 0.4
A.x=0.4
B.丁一定是单质
C.甲和乙是反应物
D.反应中的甲、丙发生改变的质量比是11∶14[来源:学,科,网Z,X,X,K]
2.如图K13-3是某反应的微观粒子示意图。
图K13-3
(1)根据化学反应的本质,反应物的方框内还应补充的粒子及数目是________。
A.一个 B.两个 C.一个 D.两个
(2)两种生成物分子的共同之处是____________________,该反应属于基本反应类型中的
________反应。
3.请对下表中的化学方程式进行评价(填写评价序号),并注明化学反应类型。
[来源:学。科。网Z。X。X。K]
化学方程式 评价 化学反应类型
MgCl =====Mg+Cl↑
2 2Al+O=====Al O
2 2 3
HCl+NaOH===NaCl+HO
2
2Fe+6HCl===2FeCl +3H↑
3 2
评价序号:①完全正确;②反应条件不正确;③没有配平;④违背客观事实。
4.用适当的化学方程式说明或解释下列问题。
(1)铜的金属活动性比铁弱:____________________________________________。
(2)工业上煅烧石灰石制生石灰:_______________________________________。
(3)用石灰浆粉刷墙面,干燥后变得坚硬:_________________________________。
(4)服用含Al(OH) 的药丸治疗胃酸过多症: ______________________。
3
5.以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究并帮忙填写空
格(包括表中的空格)。
[提出问题] 化学反应前后各物质的质量总和是否相等?
[猜想与假设] 猜想1:不相等;
猜想2:相等。
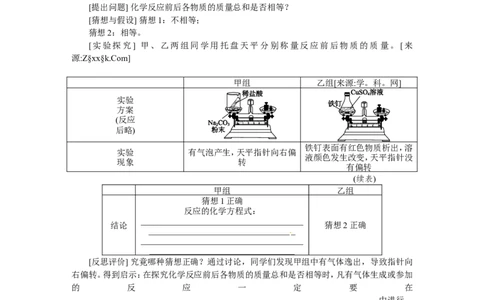
[实验探究] 甲、乙两组同学用托盘天平分别称量反应前后物质的质量。[来
源:Z§xx§k.Com]
甲组 乙组[来源:学。科。网]
实验
方案
(反应
后略)
铁钉表面有红色物质析出,溶
实验 有气泡产生,天平指针向右偏
液颜色发生改变,天平指针没
现象 转
有偏转
(续表)
甲组 乙组
猜想1正确
反应的化学方程式:
______________________________________
结论 猜想2正确
__________________________________
______________________________________
__________________________________
[反思评价] 究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体逸出,导致指针向
右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加
的 反 应 一 定 要 在
________________________________________________________________________中进行。
[优化装置] 同学们对甲组左盘中的反应装置进行了如下三种改进,你认为最佳装置是___
_____( 填 序 号 ) , 从 另 外 两 种 装 置 中 任 选 一 种 指 出 其 不 足
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。图K13-4
[得出结论] 同学们利用改进后的最佳装置进行再次探究,均得出猜想2正确。进一步分析
发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,最终得出结论:
________________________的各物质的质量总和等于反应后生成的各物质的质量总和。
[解释应用] 解释:化学反应前后,原子的种类、数目、质量均不变,所以质量守恒。
应用:某固体物质受热会发生分解反应,生成氧化铜、水和二氧化碳三种物质,则该固体
物 质 一 定 由 __________________________________________________________________
______种元素组成。
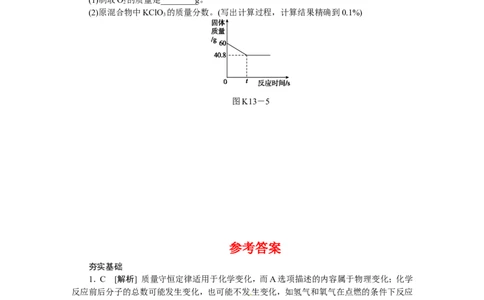
6.某学习小组在实验室中用加热KClO 和MnO 混合物的方法制取O,反应过程中固体
3 2 2
质量变化如图K13-5所示,请计算:[来源:Zxxk.Com]
(1)制取O 的质量是________g。
2
(2)原混合物中KClO 的质量分数。(写出计算过程,计算结果精确到0.1%)
3
图K13-5
参考答案
夯实基础
1.C [解析] 质量守恒定律适用于化学变化,而A选项描述的内容属于物理变化;化学
反应前后分子的总数可能发生变化,也可能不发生变化,如氢气和氧气在点燃的条件下反应
后分子个数变少;任何化学反应均遵循质量守恒定律。
2.B 3.D
4.D [解析] A中有气体生成,装置也不是密闭容器,不能验证;B中两种物质不反应,不
能验证;C中镁带在空气中燃烧,反应后固体质量会明显增大,不能验证;D中铁与硫酸铜反
应生成铜与硫酸亚铁,反应物中没有气体参加,生成物中也没有气体生成,装置可不密闭,可
以验证。
5.(1)3 (2)HCl[来源:学科网ZXXK]
6.B [解析] 参加反应的硫与氧气的质量比是32∶(16×2)=1∶1。
7.D
8.解:(1)硫酸铜中铜元素的质量分数为×100%=40%。(2)设理论上与硫酸铜反应消耗铁粉的质量为x。
Fe+CuSO ===Cu+FeSO
4 4
56 160
x 1.6 kg
= x=0.56 kg
答:(1)硫酸铜中铜元素的质量分数为 40%;(2)理论上与硫酸铜反应消耗铁粉的质量为
0.56 kg。
能力提升
1.B [解析] x=7.6+2+0.2-3.2-5.8-0.4=0.4;甲、乙质量减少,是反应物,丙、丁质量
增加,是生成物,丁不一定为单质;反应中的甲、丙发生改变的质量比是(7.6-3.2)∶(5.8-0.2)
=11∶14。
2.(1)C (2)各含有两个相同的原子 分解
[解析] (1)在化学反应前后原子种类、数目不变,生成物共有两种原子共6个,对比反应前
后原子种类和个数可知还应补充的粒子为C。(2)由微观结构图可以看出两种生成物的共同之
处是:每个分子都含有两个相同的原子;该反应的反应物是一种,生成物是两种,属于分解反
应。
3.② 分解反应 ③ 化合反应 ① 复分解反应 ④ 置换反应
4.(1)Fe+CuSO ===FeSO+Cu
4 4
(2)CaCO=====CaO +CO↑
3 2
(3)Ca(OH) +CO===CaCO ↓+HO
2 2 3 2
(4)Al(OH) +3HCl===AlCl +3HO
3 3 2
5.[实验探究] Na CO+2HCl===2NaCl+HO+CO↑
2 3 2 2
[反思评价] 密闭容器(或封闭体系等合理答案)
[优化装置] B A装置中反应产生气体,气球膨胀,浮力增大,导致称量结果不准(或C装
置中反应产生气体,瓶内气压增大,可能导致瓶塞弹出)(合理即可)
[得出结论] 参加化学反应(或参加反应)
[解释应用] 四(或4或C、H、O、Cu四)
[解析] [实验探究] 碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,根据质量守恒定律,参
加反应的碳酸钠与氯化氢的质量和等于生成的氯化钠、水和二氧化碳的质量和,因有二氧化
碳气体逸出,故反应后总质量比反应前总质量减少,观察到天平不平衡。[反思评价] 通过讨论,
同学们发现甲组中有气体逸出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的
质量总和是否相等时,凡有气体生成或参加的反应一定要在密闭容器中进行。[优化装置] 最
佳装置是B,A中碳酸钠与盐酸反应生成二氧化碳,二氧化碳充满气球,使整个装置所受空气
浮力增大,因此反应后天平不能平衡。C中碳酸钠粉末与盐酸反应太快,橡胶塞易弹出。[得出
结论] 参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。[解释应用]
因为化学反应前后元素的种类不变,氧化铜、二氧化碳和水含有铜、碳、氧、氢四种元素,所以
该化合物中也含有这四种元素。
6.(1)19.2
(2)解:设原混合物中KClO 的质量为x。
3
2KClO=====2KCl+3O↑
3 2
245 96
x 19.2 g
= x=49 g
原混合物中KClO 的质量分数为×100%≈81.7%。
3答:原混合物中KClO 的质量分数为81.7%。
3