文档内容
自主广场
我夯基 我达标
1.(2005江苏南京中考,10)在实验操作中如果不慎将浓硫酸沾到皮肤上,应立即用布擦拭并
用大量的水冲洗,然后涂上4%左右的碳酸氢钠溶液。配制200 g质量分数为4%的碳酸氢钠
溶液,需要碳酸氢钠的质量为( )
A.4 g B.8 g C.192 g D.200 g
思路解析:根据公式:溶质质量=溶液质量×溶质质量分数计算,即可得出结果。
答案:B
2.根据你对溶液组成的认识,判断下列说法正确的是( )
A.溶液的质量等于溶质与溶剂的质量之和
B.20 mL浓硫酸与80 mL水相混合后得到100 mL稀硫酸
C.20 g氯化钠完全溶解于100 g水中,所得溶液的质量分数为20%
D.20 mL酒精放入盛有80 mL水的烧杯中,所得酒精溶液的质量分数为20%
思路解析:溶液质量可以相加,溶液的体积不能相加,溶液中溶质质量分数是溶质质量与溶
液质量的比值。
答案:A
3.40 ℃时,200 g硝酸钾饱和溶液,蒸发掉20 g水后,仍然冷却到40 ℃,则蒸发前后保持不
变的是( )
①溶液的质量;②溶液中溶质的质量分数;③溶剂的质量;④溶质的质量;⑤硝酸钾的溶解度
A.①② B.②③ C.②⑤ D.②④
思路解析:温度不变,物质的溶解度不变,饱和溶液的溶质质量分数也不变。
答案:C
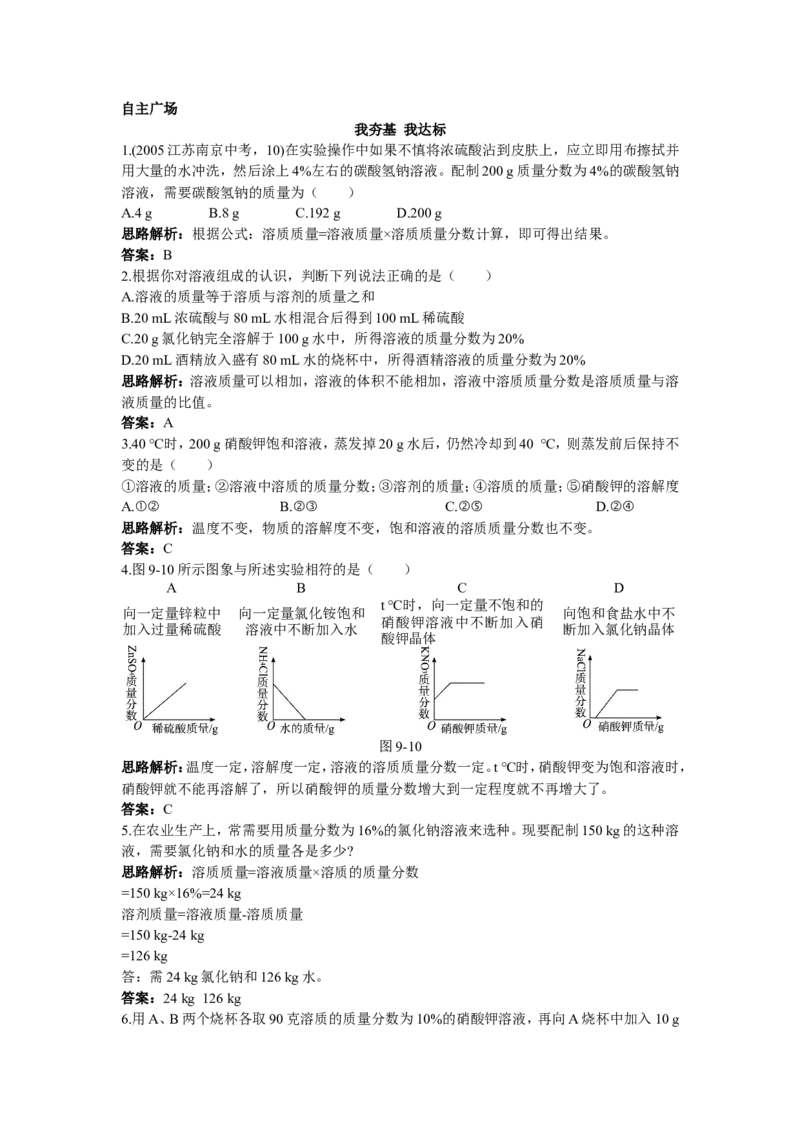
4.图9-10所示图象与所述实验相符的是( )
A B C D
t ℃时,向一定量不饱和的
向一定量锌粒中 向一定量氯化铵饱和 向饱和食盐水中不
硝酸钾溶液中不断加入硝
加入过量稀硫酸 溶液中不断加入水 断加入氯化钠晶体
酸钾晶体
图9-10
思路解析:温度一定,溶解度一定,溶液的溶质质量分数一定。t ℃时,硝酸钾变为饱和溶液时,
硝酸钾就不能再溶解了,所以硝酸钾的质量分数增大到一定程度就不再增大了。
答案:C
5.在农业生产上,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150 kg的这种溶
液,需要氯化钠和水的质量各是多少?
思路解析:溶质质量=溶液质量×溶质的质量分数
=150 kg×16%=24 kg
溶剂质量=溶液质量-溶质质量
=150 kg-24 kg
=126 kg
答:需24 kg氯化钠和126 kg水。
答案:24 kg 126 kg
6.用A、B两个烧杯各取90克溶质的质量分数为10%的硝酸钾溶液,再向A烧杯中加入10 g硝酸钾,向B烧杯中加入10 g水,并用玻璃棒搅拌至全部溶解。
[讨论]
(1)原溶液中溶质的质量是多少?溶液的质量是多少?溶剂的质量是多少?
(2)向原溶液中增加10克硝酸钾(全部溶解)或增加10克水后,溶液中溶质质量、溶剂质量、
溶液质量各是多少?
思路解析:(1)溶液的质量=90克
溶质的质量=溶液质量×溶质的质量分数
=90克×10%=9克
溶剂的质量=溶液质量-溶质质量
=90克-9克=81克
(2)①增加10克硝酸钾后:
溶质质量=9克+10克=19克
溶剂质量=81克(不变)
溶液质量=19克+81克=100克(增加10克)
或90克+10克=100克
则可知:(1)增加10克溶质后:
溶质的质量分数= ×100%
= ×100%=19%
注:若新增的10克溶质未完全溶解,则上述计算错误。
②加入10克水后:
溶质质量=9克(不变)
溶剂质量=81克+10克=91克(增加)
溶液质量=9克+91克=100克(增加10克)
或90克+10克=100克
则可知:增加10克水后:
溶质的质量分数= ×100%
= ×100%=9%
答案:(1)9 g 90 g 81 g
(2)①加10 g KNO 时,19 g,81 g,100 g
3
②加10 g HO时,9 g,91 g,100 g
2
7.5 g食盐溶解在95 g水中,计算所得溶液的溶质的质量分数。
思路解析:A%= ×100%=5%
答案:5%
8.15 ℃时,食盐的溶解度是35 g,求此时食盐溶液的溶质的质量分数。
思路解析:A%= ×100%≈25.9%
答案:25.9%
我综合 我发展
9.(2006江苏徐州中考,22)溶液在生产和科研中具有广泛的用途。在农业上,为了选种子,需要配制15%的盐溶液。现有30 kg食盐固体,可配制食盐溶液_____________kg。配制食盐溶
液的一般步骤为①__________________________;②__________________________;③溶解。
思路解析:根据质量分数公式计算出溶液的质量=30 kg÷15%=200 kg。配制溶液的步骤一般
为:①计算;②称量固体和量取液体;③溶解。
答案:200 计算 称量固体和量取液体
10.浓度为98%,密度为1.84 g·cm-3的浓硫酸和水按1∶5的体积比配制硫酸溶液,求所得硫酸
溶液的溶质的质量分数。
思路解析:设水为5 mL,浓HSO 为1 mL。
2 4
溶质质量=1×1.84×98%≈1.8 g
溶液质量=1×1.84+5×1=6.84 g
A%= ×100%=26.9%
答案:26.9%
11.侯德榜是我国著名的化学家。由他发明的侯氏制碱法制得的纯碱中可能含有少量氯化钠。
现取仅含氯化钠杂质的纯碱样品33.2 g,加入到130 g稀盐酸中,恰好完全反应,得氯化钠溶
液150 g。
求:(1)该纯碱样品中NaCO 的质量。
2 3
(2)反应后所得溶液中溶质的质量分数。
思路解析:本题综合性较强,运用质量守恒定律(质量守恒法)求得生成CO 的质量是解题的
2
关键。
设样品中含NaCO 质量为x,生成NaCl的质量为y,依题意知产生CO 的质量为33.2 g+130
2 3 2
g-150 g=13.2 g。则:
NaCO+2HCl====2NaCl+CO ↑+H O
2 3 2 2
106 117 44
x y 13.2 g
x= g
y= g
原样品中含NaCl:33.2 g-31.8 g=1.4 g
×100%=24.3%
答案:(1)该纯碱样品中NaCO 为31.8 g
2 3
(2)所得溶液中溶质的质量分数为24.3%
12.长久使用的热水壶底部有一层水垢,主要成分是CaCO 和Mg(OH) 。某学校化学研究性学
3 2
习小组的同学通过实验测定水垢中的CaCO 含量,取200 g水垢,加入过量的稀盐酸,同时测
3
量5分钟内生成CO 的质量,结果如下表:
2
时间/分钟 1 2 3 4 5
质量/g 30 50 60 66 66
试完成下列问题:
(1)4分钟后,水垢中CaCO 是否反应完全?
3
(2)该水垢中的CaCO 质量分数是多少?
3
思路解析:此题是一道数据分析题,解题的关键是从表中数据分析出在第4次实验后水垢已
反应完全。答案:(1)已反应完全
(2)由表可知,完全反应后,生成的CO 为66 g。设水垢中CaCO下标3 的质量为x
2
2HCl+CaCO ====CaCl +H O +CO ↑
3 2 2 2
100 100 44
X x 66 g
x=150 g
水垢中CaCO 的质量分数为150 g/200 g×100%=75%
3
13.在“非典”期间,某市售过氧乙酸(化学式为CHCOOOH),其标签上的部分文字说明如
3
下。请完成下列问题:
过氧乙酸
(质量:500 g/瓶)
成分名称 化学式 质量分数
过氧乙酸 C HO 40%
2 4 3
水 HO 55%
2
双氧水 HO 5%
2 2
性 质:强氧化性、酸性
主要用途:强氧化性、酸性
储存方法:密封、避光、避热,不可与可燃物混合存放,防猛烈撞击。
(1)从标签上的文字说明可以推知:过氧乙酸之所以避热储存,是因为过氧乙酸受热时像双
氧水一样,容易发生分解,生成乙酸和一种单质气体。过氧乙酸加热分解的化学方程式是
__________________________________________________。
(2)一瓶这种溶液中含过氧乙酸溶质________________g。
(3)0.5%的过氧乙酸溶液可以杀死细菌和SARS病毒。某医院需配制0.5%的过氧乙酸,一瓶
这种过氧乙酸需加多少克水?
思路解析:本题是一道紧密联系实际的商品标签试题。标签上提供了瓶装过氧乙酸的成分、
性质、主要用途和储存方法。由于试题已明确告知过氧乙酸分解时生成乙酸和一种单质气体,
且分解时像双氧水一样。显然题目在暗示这种单质气体是氧气。其实,即使题目中除掉“像
双氧水一样”字眼,同样可以根据质量守恒定律来推测这种单质气体。由于含过氧乙酸的溶
液质量分数为40%,则一瓶这种溶液中含过氧乙酸溶质质量:500 g×40%=200 g。第(3)问可
以这样变换:某医院用500 g 40%的过氧乙酸溶液来配制0.5%的过氧乙酸,需加水多少克?
经过这样的变换,就成了一道有关溶液稀释的计算题。在稀释前后,溶质过氧乙酸质量不会
改变。
设应加水的质量为x,
稀释前溶质质量 稀释后溶质质量
解得:x=39 500 g
答案:
(1)2CHCOOOH △ 2 C HCOOH+O ↑
3 3 2
(2)200
(3)39 500 g