文档内容
丽水外国语实验学校高中部 2020 学年第一学期第三次月考
高一化学试卷
考生须知:
1.本卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,第Ⅰ卷第1题至第25题,第Ⅱ卷第26
题至第30题。全卷满分100分,考试时间90分钟。
2.本卷答案必须写在答题卷的相应位置上,写在试题卷上无效。
3.可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 S-32 Cl-35.5 K-39
Mn-55 Fe-56 Ba-137 N-14 Al-27
第Ⅰ卷(选择题,共50分)
一、选择题(本题包括25小题,每小题2分,共50分。每小题只有一个选项符合题意)
1. 下列属于氧化物的是
A. HO B. NaOH C. O D. NaCO
2 2 2 3
【答案】A
【解析】
【分析】氧化物是只有两种元素,且必须有氧元素,据此分析判断。
【详解】A.HO中有两种元素,其中一种为氧元素,属于氧化物,故A选;
2
B.NaOH中有三种元素,不属于氧化物,故B不选;
C.O 是由氧元素组成的单质,不属于氧化物,故C不选;
2
D.NaCO 中有三种元素,不属于氧化物,故D不选;
2 3
故选A。
2. 下列分散系具有丁达尔效应的是
A. 蒸馏水 B. 氯化钠溶液
C. 氢氧化铝胶体 D. 硫酸铜溶液
【答案】C
【解析】
【分析】丁达尔效应是胶体特有 的性质,分散质粒子直径介于1-100nm分散系为胶体,据此判断。
【详解】A.蒸馏水是纯液体,无丁达尔效应,故A不选;
B.氯化钠溶液属于溶液,不能产生丁达尔效应,故B不选;
C.氢氧化铝胶体属于胶体,能产生“丁达尔效应”,故C选;
D.硫酸铜溶液属于溶液,不能产生丁达尔效应,故D不选;
学科网(北京)股份有限公司故选C。
3. 下列物质属于纯净物的是
A. 生铁 B. 碱石灰 C. 液氯 D. 漂白粉
【答案】C
【解析】
【分析】
【详解】A.生铁是铁和碳的混合物,故A不选;
B.碱石灰是固体氢氧化钠和氧化钙的混合物,故B不选;
C.液氯是液态的氯气,是纯净物,故C选;
D.漂白粉是主要成分为氯化钙和次氯酸钙的混合物,故D不选;
故选C。
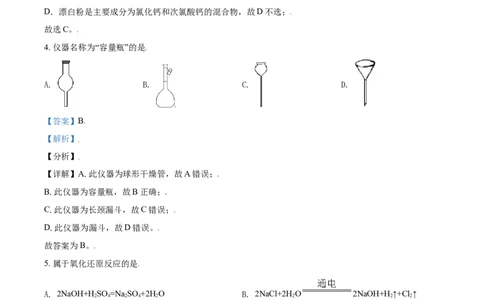
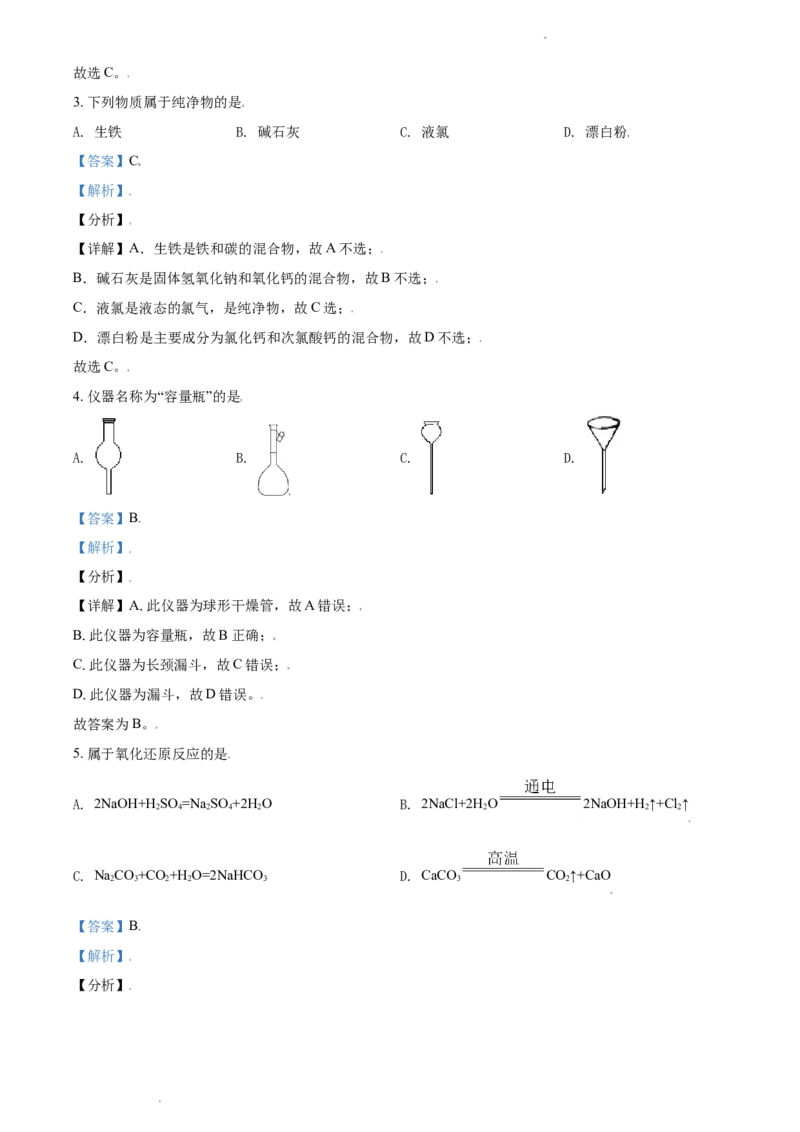
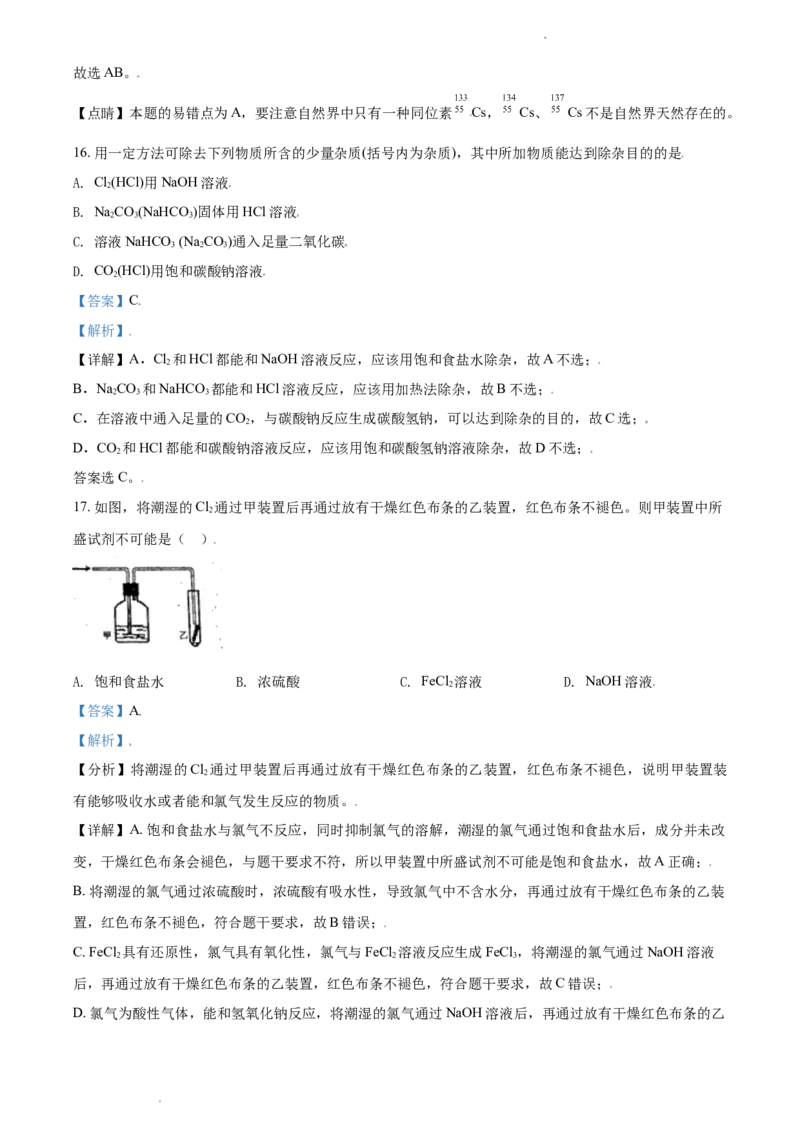
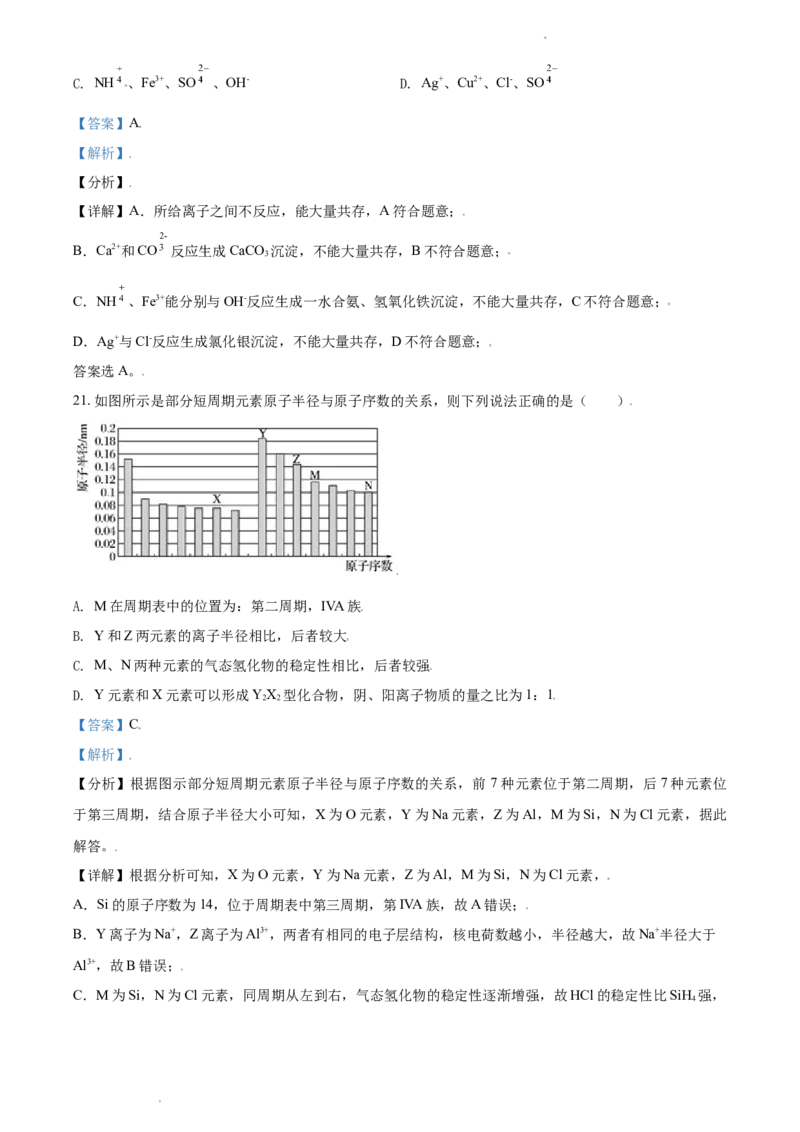
4. 仪器名称为“容量瓶”的是
A. B. C. D.
【答案】B
【解析】
【分析】
【详解】A.此仪器为球形干燥管,故A错误;
B.此仪器为容量瓶,故B正确;
C.此仪器为长颈漏斗,故C错误;
D.此仪器为漏斗,故D错误。
故答案为B。
5. 属于氧化还原反应的是
A. 2NaOH+H SO =Na SO +2H O B. 2NaCl+2H O 2NaOH+H ↑+Cl↑
2 4 2 4 2 2 2 2
C. NaCO+CO +H O=2NaHCO D. CaCO CO↑+CaO
2 3 2 2 3 3 2
【答案】B
【解析】
【分析】
学科网(北京)股份有限公司【详解】元素化合价发生变化的反应属于氧化还原反应,反应2NaCl+2H O 2NaOH+H ↑+Cl↑
2 2 2
中,氯元素化合价升高、氢元素化合价降低,则B满足;
答案选B。
6. 下列说法不正确的是( )
的
A. 核素23Na 中子数是12
B. 16O和18O互为同位素
C. 三种核素1H、2H、16O可构成3种水分子
D. S2-结构示意图:
【答案】D
【解析】
【详解】A.核素23Na的中子数=质量数-质子数=23−11=12,故A正确;
B.质子数相同而中子数不同的同一元素的不同原子互为同位素,16O和18O质子数相同,中子数不同,互
为同位素,故B正确;
C.因1个水分子是由两个氢原子和1个氧原子构成,则 与2个 , 与2个 、 与1个
和1个 共组成3种水分子,故C正确;
D.硫离子核外有18个电子、最外层有8个电子,其离子结构示意图为 ,故D错误;
答案选D。
7. 下列物质属于共价化合物的是
A. NaCl B. CO C. CaCl D. NH Cl
2 2 4
【答案】B
【解析】
【详解】A. 氯化钠中钠离子和氯离子之间只存在离子键,为离子化合物,故A错误;
B. CO 分子中C与O原子之间只存在共价键,为共价化合物,故B正确;
2
C. CaCl 中钙离子和氯离子之间只存在离子键,为离子化合物, 故C错误;
2
D. NHCl中铵根离子和氯离子之间存在离子键、N原子和H原子之间存在共价键,为离子化合物,故D错
4
误;
学科网(北京)股份有限公司故选:B。
8. 下列说法中正确的是
A. Cl 有毒性,Cl-也有毒性
2
B. 氯水呈黄绿色,含Cl-的溶液也呈黄绿色
C. 纯净的H 在氯气中能安静地燃烧,发出苍白色火焰
2
D. Cl 不溶于水,所以可用排水法收集
2
【答案】C
【解析】
【详解】A.Cl 有毒性,但Cl-无毒性,A说法错误;
2
B.氯水中溶有氯气,溶液呈黄绿色,含Cl-的溶液为无色,B说法错误;
C.纯净的H 在氯气中能安静地燃烧,发出苍白色火焰,生成HCl气体,C说法正确;
2
D.Cl 可溶于水,所以可用排饱和食盐水的方法收集,D说法错误;
2
为
答案 C。
9. 下列元素中,原子半径最大的是
A. H B. Li C. Na D. K
【答案】D
【解析】
【分析】
【详解】同主族从上到下半径递增,H、Li、Na和K均位于ⅠA,且核电荷数递增,则原子半径最大的是
K,故D正确;
答案:D。
10. 下列离子方程式书写正确的是( )
A. 用FeCl 溶液腐蚀铜线路板:Cu+Fe3+=Cu2++Fe2+
3
B. NaO 固体与HO反应产生O:2NaO+2H O=4Na++4OH-+O ↑
2 2 2 2 2 2 2 2
C. Ba(OH) 溶液中加入稀硫酸:Ba2++OHˉ+H++SO =BaSO ↓+H O
2 4 2
D. 稀HSO 与铁粉反应:2Fe+6H+=2Fe3++3H ↑
2 4 2
【答案】B
【解析】
【详解】A. 用FeCl 溶液腐蚀铜线路板得到氯化亚铁和氯化铜,Cu+Fe3+=Cu2++Fe2+电荷不守恒,正确的为
3
Cu+2Fe3+=Cu2++2Fe2+,A错误;
B. Na O 固体与HO反应产生O 和氢氧化钠溶液,离子方程式:2NaO+2H O=4Na++4OH-+O ↑,B正确;
2 2 2 2 2 2 2 2
学科网(北京)股份有限公司C. Ba(OH) 溶液中加入稀硫酸生成硫酸钡和水,正确的离子方程式应为 Ba2++2OHˉ+2H++SO
2
=BaSO ↓+2H O,C错误;
4 2
D. 稀HSO 与铁粉反应生成硫酸亚铁和氢气,正确的离子方程式应为: Fe+2H+=Fe2++H ↑,D错误;
2 4 2
答案选B。
11. 下列说法正确的是
A. 焰色反应的铂丝可用稀硫酸洗涤
B. 常温下铁遇浓硫酸会发生钝化
C. 工业上用氯气和石灰水为原料制漂白粉
D. 氯化铁溶液中加入硫氰化钾溶液产生血红色沉淀
【答案】B
【解析】
【分析】
【详解】A. 为了出去残留物,焰色反应的铂丝可用稀盐酸洗涤,A错误;
B.浓硫酸具有强氧化性, 常温下铁遇浓硫酸会发生钝化,B正确;
C. 熟石灰微溶,工业上用氯气和石灰乳为原料制漂白粉,C错误;
D. 氯化铁溶液中加入硫氰化钾溶液产生血红色溶液,D错误;
答案选B。
12. 下列溶液中氯离子浓度最大的是
A. 250mL0.5mol·L-1的MgCl 溶液 B. 100mL1mol·L-1的AlCl 溶液
2 3
C. 200mL1.5mol·L-1的NaCl溶液 D. 150mL3mol·L-1的KClO 溶液
3
【答案】B
【解析】
【分析】
【详解】A.0.5 mol/LMgCl 溶液中Cl-浓度为0.5mol/L×2=1mol/L;
2
B.1 mol•L-1AlCl 溶液氯离子浓度为1mol/L×3=3mol/L;
3
C.1.5mol•L-1NaCl溶液中氯离子的浓度为1.5mol/L;
D.3mol/LKClO 溶液中没有氯离子,只有氯酸根离子,氯离子浓度为0;
3
所以氯离子浓度最大的是100mL 1mol•L-1AlCl 溶液,故选B。
3
13. 下列化学反应中溴元素仅被氧化的是
A. 2NaBr+Cl=2NaCl+Br B. Br+2NaI=2NaBr+I
2 2 2 2
C. 3Br+6NaOH 5NaBr+NaBrO+3HO D. HBr+NaOH=NaBr+HO
2 3 2 2
学科网(北京)股份有限公司【答案】A
【解析】
【详解】A、溴化钠中溴元素化合价升高被氧化作还原剂,选项A符合;B、溴单质中溴元素化合价降低
被还原作氧化剂,选项B不符合;C、溴单质既 是氧化剂又是还原剂,被氧化生成溴酸钠,被还原生成溴
化钠,选项C不符合;D、反应属于中和反应,各元素化合价不变,不属于氧化还原反应,选项D不符合。
答案选A。
14. 某实验需要0.2mol/L 的CuSO 溶液490mL,配制时应选用的容量瓶的规格和称取硫酸铜晶体
4
(CuSO ·5H O)的质量分别是
4 2
A. 500mL 25g B. 490mL 24.5g
C. 490mL 25g D. 500mL 24.5g
【答案】A
【解析】
【详解】实验室没有 490mL 的容量瓶,选 500mL 的容量瓶,称取胆矾的质量 0.2mol/L 0.5L 250g/
mol=25.0g,故答案是A; × ×
故选A。
15. 铯(Cs)在自然界中只有一种稳定同位素 Cs,核泄漏事故中会产生人工放射性同位素 Cs、 Cs。
下列有关说法正确的是
A. 铯元素的相对原子质量约为133 B. Cs、 Cs的化学性质相同
C. Cs的电子数为79 D. Cs、 Cs互为同素异形体
【答案】AB
【解析】
【分析】
【详解】A.元素的相对原子质量是按各种天然同位素原子所占的一定百分比算出来的平均值,铯(Cs)在
自然界中只有一种稳定同位素 Cs,则铯元素的相对原子质量约为133,故A正确;
B. Cs、 Cs互为同位素,同位素的化学性质相同,物理性质有差别,故B正确;
C.电子数等于质子数, Cs的质子数为55,则电子数为55,故C错误;
D. Cs、 Cs是同种元素的不同原子,互为同位素,同素异形体是单质,故D错误;
学科网(北京)股份有限公司故选AB。
【点睛】本题的易错点为A,要注意自然界中只有一种同位素 Cs, Cs、 Cs不是自然界天然存在的。
16. 用一定方法可除去下列物质所含的少量杂质(括号内为杂质),其中所加物质能达到除杂目的的是
A. Cl(HCl)用NaOH溶液
2
B. NaCO(NaHCO )固体用HCl溶液
2 3 3
C. 溶液NaHCO (Na CO)通入足量二氧化碳
3 2 3
D. CO(HCl)用饱和碳酸钠溶液
2
【答案】C
【解析】
【详解】A.Cl 和HCl都能和NaOH溶液反应,应该用饱和食盐水除杂,故A不选;
2
B.NaCO 和NaHCO 都能和HCl溶液反应,应该用加热法除杂,故B不选;
2 3 3
C.在溶液中通入足量的CO,与碳酸钠反应生成碳酸氢钠,可以达到除杂的目的,故C选;
2
D.CO 和HCl都能和碳酸钠溶液反应,应该用饱和碳酸氢钠溶液除杂,故D不选;
2
答案选C。
17. 如图,将潮湿的Cl 通过甲装置后再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所
2
盛试剂不可能是( )
A. 饱和食盐水 B. 浓硫酸 C. FeCl 溶液 D. NaOH溶液
2
【答案】A
【解析】
【分析】将潮湿的Cl 通过甲装置后再通过放有干燥红色布条的乙装置,红色布条不褪色,说明甲装置装
2
有能够吸收水或者能和氯气发生反应的物质。
【详解】A. 饱和食盐水与氯气不反应,同时抑制氯气的溶解,潮湿的氯气通过饱和食盐水后,成分并未改
变,干燥红色布条会褪色,与题干要求不符,所以甲装置中所盛试剂不可能是饱和食盐水,故A正确;
B. 将潮湿的氯气通过浓硫酸时,浓硫酸有吸水性,导致氯气中不含水分,再通过放有干燥红色布条的乙装
置,红色布条不褪色,符合题干要求,故B错误;
C. FeCl 具有还原性,氯气具有氧化性,氯气与FeCl 溶液反应生成FeCl ,将潮湿的氯气通过NaOH溶液
2 2 3
后,再通过放有干燥红色布条的乙装置,红色布条不褪色,符合题干要求,故C错误;
D. 氯气为酸性气体,能和氢氧化钠反应,将潮湿的氯气通过NaOH溶液后,再通过放有干燥红色布条的乙
学科网(北京)股份有限公司装置,红色布条不褪色,符合题干要求,故D错误;
综上所述,正确答案为A。
【点睛】氯气没有漂白性,潮湿的氯气具有漂白性,发挥漂白性的物质是氯气与水反应后生成的次氯酸。
18. 将一小块金属钠加入CuSO 溶液中不可能观察到的实验现象是( )
4
A. 有无色无味气体产生 B. 溶液中析出红色固体
C. 溶液中产生蓝色沉淀 D. 钠块在溶液表面四处游动
【答案】B
【解析】
【分析】Na比较活泼,先跟水反应生成NaOH和H ,NaOH和CuSO 反应生成Cu(OH) 和NaSO ,据此
2 4 2 2 4
分析解答。
【详解】A.产生无色无味的氢气,A正确;
B.由分析可知,不生成红色固体,B错误;
C.产生了蓝色的Cu(OH) 沉淀,C正确;
2
D.该反应的现象为钠浮在水面上,熔化成一个小球,四处游动,发出“嘶嘶”的声音,产生蓝色沉淀,
D正确。
答案选B。
【点睛】钠与盐溶液反应,先与水反应,再看生成物NaOH是否能和盐溶质反应。
19. 下列各组化合物中,化学键的类型完全相同的是( )
①CaCl 和NaS ②NaO和NaO ③CO 和CS ④HCl和NaOH
2 2 2 2 2 2 2
A. ①② B. ①③ C. ②③ D. ②④
【答案】B
【解析】
【分析】一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键,据此判
断。
【详解】①CaCl 和NaS中都只有离子键,化学键类型完全相同;
2 2
②NaO中只有离子键,NaO 中有离子键和非极性共价键,化学键类型不完全相同;
2 2 2
③CO 和CS 中都只有极性共价键,化学键类型完全相同;
2 2
④HCl中只有共价键,NaOH中有离子键和极性共价键,化学键类型不完全相同;
化学键类型完全相同的是①③,答案选B。
20. 下列离子在水溶液中能大量共存的是
A. Na+、K+、Cl-、HCO B. Na+、Ca2+、NO 、CO
学科网(北京)股份有限公司C. NH 、Fe3+、SO 、OH- D. Ag+、Cu2+、Cl-、SO
【答案】A
【解析】
【分析】
【详解】A.所给离子之间不反应,能大量共存,A符合题意;
B.Ca2+和CO 反应生成CaCO 沉淀,不能大量共存,B不符合题意;
3
C.NH 、Fe3+能分别与OH-反应生成一水合氨、氢氧化铁沉淀,不能大量共存,C不符合题意;
D.Ag+与Cl-反应生成氯化银沉淀,不能大量共存,D不符合题意;
答案选A。
21. 如图所示是部分短周期元素原子半径与原子序数的关系,则下列说法正确的是( )
A. M在周期表中的位置为:第二周期,IVA族
B. Y和Z两元素的离子半径相比,后者较大
C. M、N两种元素的气态氢化物的稳定性相比,后者较强
D. Y元素和X元素可以形成YX 型化合物,阴、阳离子物质的量之比为1:1
2 2
【答案】C
【解析】
【分析】根据图示部分短周期元素原子半径与原子序数的关系,前 7种元素位于第二周期,后7种元素位
于第三周期,结合原子半径大小可知,X为O元素,Y为Na元素,Z为Al,M为Si,N为Cl元素,据此
解答。
【详解】根据分析可知,X为O元素,Y为Na元素,Z为Al,M为Si,N为Cl元素,
A.Si的原子序数为14,位于周期表中第三周期,第IVA族,故A错误;
B.Y离子为Na+,Z离子为Al3+,两者有相同的电子层结构,核电荷数越小,半径越大,故Na+半径大于
Al3+,故B错误;
C.M为Si,N为Cl元素,同周期从左到右,气态氢化物的稳定性逐渐增强,故HCl的稳定性比SiH 强,
4
学科网(北京)股份有限公司故C正确;
D.X为O元素,Y为Na元素,Na元素和O元素形成的Na O 中,阴离子为过氧根离子,则阴、阳离子
2 2
物质的量之比为1:2,故D错误;
答案选C。
【点睛】推断元素为解答关键,注意掌握元素周期律内容及常见元素化合物性质,试题侧重考查学生的分
析能力及逻辑推理能力。
22. 同主族元素形成的同一类型化合物,往往其结构和性质相似。PH I是一种白色晶体,下列对PH I的叙
4 4
述中,不正确的是( )
A. PH I既有离子键又有共价键
4
B. 它是离子化合物
C. 它不可能与NaOH溶液反应
D. 它受热时,可能会分解
【答案】C
【解析】
【分析】同主族元素形成的同一类型化合物,往往其结构和性质相似。N和P是同主族元素,I和Cl是同
主族元素,所以PH I和NH Cl结构和性质相似。
4 4
【详解】A.NH Cl既含离子键又含共价键,所以PH I也既含离子键,又含共价键,故A正确;
4 4
B.NH Cl是离子化合物,所以PH I也是一种离子化合物,故B正确;
4 4
C.NH Cl能与NaOH溶液反应生成一水合氨,所以PH I也能和NaOH溶液反应,故C错误;
4 4
D.NH Cl受热时会分解为氨气和HCl,所以PH I受热也可能分解,故D正确;
4 4
答案选C。
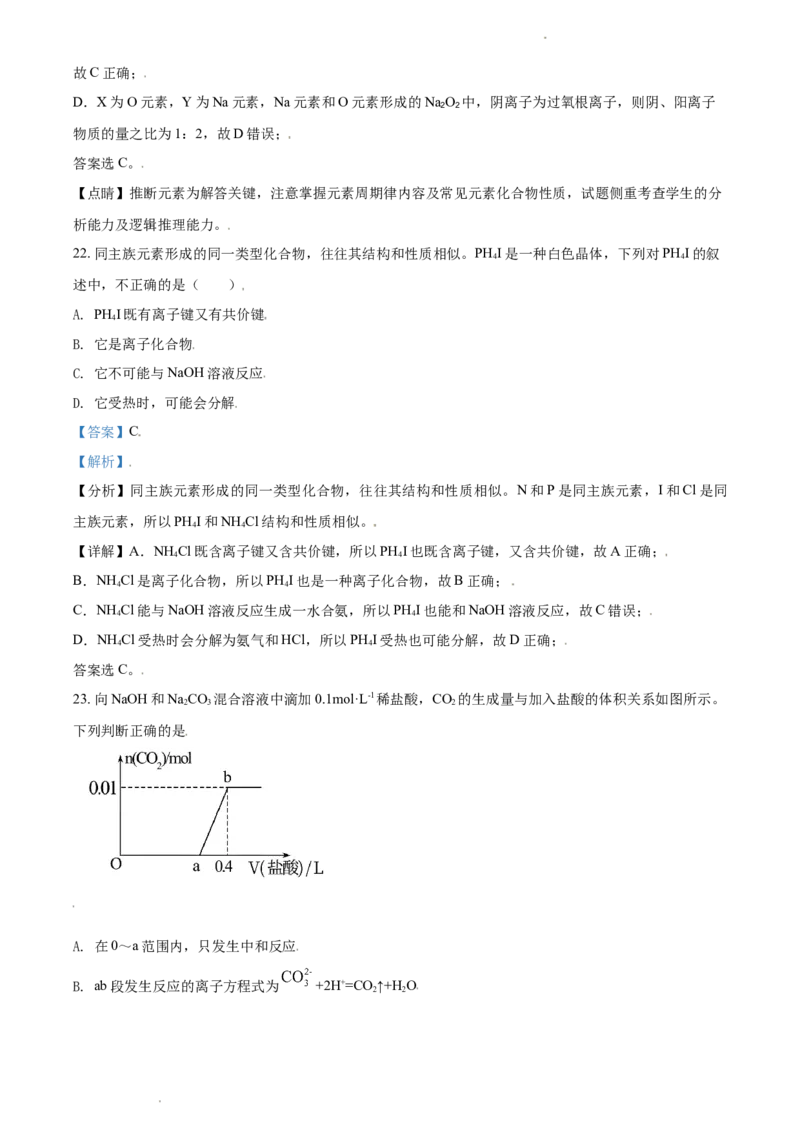
23. 向NaOH和NaCO 混合溶液中滴加0.1mol·L-1稀盐酸,CO 的生成量与加入盐酸的体积关系如图所示。
2 3 2
下列判断正确的是
A. 在0~a范围内,只发生中和反应
B. ab段发生反应的离子方程式为 +2H+=CO ↑+H O
2 2
学科网(北京)股份有限公司C. a=0.3
D. 原混合溶液中NaOH与NaCO 的物质的量之比为1∶2
2 3
【答案】C
【解析】
【分析】由图和题意可知0~a段先发生HCl和NaOH反应生成NaCl和HO,然后发生NaCO 和HCl反应
2 2 3
生成NaHCO 和NaCl,a~b段发生NaHCO 和HCl反应生成NaCl、HO和CO,据此解答。
3 3 2 2
【详解】A.在0~a范围内,发生 和 ,故A错误;
B.ab段发生反应 ,故B错误;
C.由 和二氧化碳的物质的量可知n( )=0.01mol,设a点对应的HCl的物
质的量为x,则 ,解得x=0.03mol,则a=0.03÷0.1=0.3,故C正确;
D .因为n( )=0.01mol,且n( )=n( )=0.01mol,再由 可得消耗的氢离
子为0.01mol,再由 可得n(OH-)=n(H+)= ,所以原混合
溶液中NaOH与NaCO 的物质的量之比为 2:1,故D错误;
2 3
故答案为C。
24. 下列说法中,正确的是 表示阿伏加德罗常数
A. 18g水在标准状况下的体积约为
B. 在标准状况下, 氮气中含有 个氮原子
C. 中含有的原子总数目为
D. 80gNaOH溶解在1L水中,得到溶液的物质的量浓度为
【答案】C
【解析】
【详解】A.标况下水为液态,故18g水的物质的量为1mol,但在标况下的体积小于22.4L,故A错误;
B.标况下,22.4L氮气的物质的量为1mol,而氮气为双原子分子,故1mol氮气中含2mol单原子即2N 个,
A
故B错误;
学科网(北京)股份有限公司C.17g氨气的物质的量为1mol,而氨气为4原子分子,故1mol氨气中含4mol氢原子即4N 个,故C正
A
确;
D.当氢氧化钠溶于1L水后,溶于体积大于1L,故溶液的浓度小于2mol/L,故D错误;
故答案为C。
【点睛】注意气体摩尔体积的使用范围和条件,①对象是否气体,标况下水、CCl 、HF等为液体,只有气
4
体才能使用;②温度和压强是否为标准状况,只指明体积无法求算物质的量,只有标准状况才能使用
22.4L/mol。
25. 某澄清透明溶液可能含有Na+、Cl-、 、 、Mg2+、 中的几种,进行如下实验:将上述溶
液分为两等份,其中一份滴加足量的BaCl 溶液,得到白色沉淀4.66g;另一份溶液中滴加足量的NaOH溶
2
液,得到0.58g白色沉淀,加热后产生标准状况下的气体0.224L,该气体能使湿润的红色石蕊试纸变蓝色。
下列说法正确的是
A. 溶液中可能有Na+、Cl-
B. 溶液中一定没有Cl-、
C. 溶液中一定有Na+、 、Mg2+、
D. 是否存在Na+离子只能通过焰色反应确认
【答案】C
【解析】
【详解】一份溶液中滴加足量的NaOH溶液,得到0.58g白色沉淀,白色沉淀为氢氧化镁,溶液中存在
Mg2+且物质的量为0.01mol;加热后产生标准状况下的气体0.224L,气体为氨气,溶液中含有 且物质
的量为0.01mol;根据离子共存原则,肯定不含有 ;一份滴加足量的BaCl 溶液,得到4.66 g白色沉
2
淀为硫酸钡,溶液中含有 且物质的量为0.02mol;根据电荷守恒,溶液中一定含有阳离子Na+,不一
定含有Cl−。由上分析知,溶液中一定有Na+、 、Mg2+、 ,一定没有 ,不确定有Cl−,故
选:C。
【点睛】本题考查了常见离子的检验方法及判断,侧重考查学生的分析能力和实验能力,注意掌握常见离
子的性质及检验方法。
第Ⅱ卷(非选择题,共50分)
学科网(北京)股份有限公司二、填空题(本题包括4小题,共44分。)
26. (1)钠的原子结构示意图:___。
(2)钠与水反应的方程式:___。
(3)现有物质:①铜②干冰③盐酸④液态醋酸⑤蔗糖⑥NaHSO 固体⑦Ba(OH) 溶液⑧熔融的NaCl。属于电
4 2
解质的是:____,属于非电解质的是:___。
(4)将NaHSO 固体溶于水,写出NaHSO 的电离方程式:___。
4 4
(5)15.6gNa X含有0.2molX2-,含有Na+的物质的量是___mol,NaX的摩尔质量为___g·mol-1。
2 2
【 答 案 】 ① . ②. 2Na+2HO=2NaOH+H ↑ ③. ④⑥⑧ ④. ②⑤ ⑤.
2 2
⑥. 0.4mol ⑦. 78
【解析】
【分析】
【详解】(1) 钠的原子序数是11,钠的原子结构示意图: 。
(2) 钠与水反应产生氢气和氢氧化钠,发生的反应为2Na+2HO=2NaOH+H ↑。
2 2
(3)①铜是金属单质,不是电解质; ②干冰,不含自由电子,不含自由移动的离子,不能导电,碳酸溶液
能导电、但离子是碳酸电离的结果、则干冰属于非电解质; ③盐酸是混合物,不是电解质; ④醋酸在水
溶液中能电离、醋酸的水溶液能导电、醋酸是电解质;⑤蔗糖属于有机物、蔗糖是非电解质; ⑥NaHSO
4
属于盐、是电解质; ⑦Ba(OH) 溶液 是混合物,不是电解质;⑧熔融的 NaCl含有自由移动的离子,能导
2
电,属于电解质;则属于电解质的是:④⑥⑧;属于非电解质的是:②⑤。
(4) 硫酸氢钠为强电解质,将NaHSO 固体溶于水,完全电离出钠离子、氢离子和硫酸根离子, NaHSO 的
4 4
电离方程式: 。
(5)15.6gNa X含有0.2molX2-,NaX的物质的量为0.2mol,含有Na+的物质的量是0.4mol,NaX的摩尔质
2 2 2
量 。
27. 硫酸是当今世界上最重要的化工产品之一,硫酸在生产中具有广泛的应用。
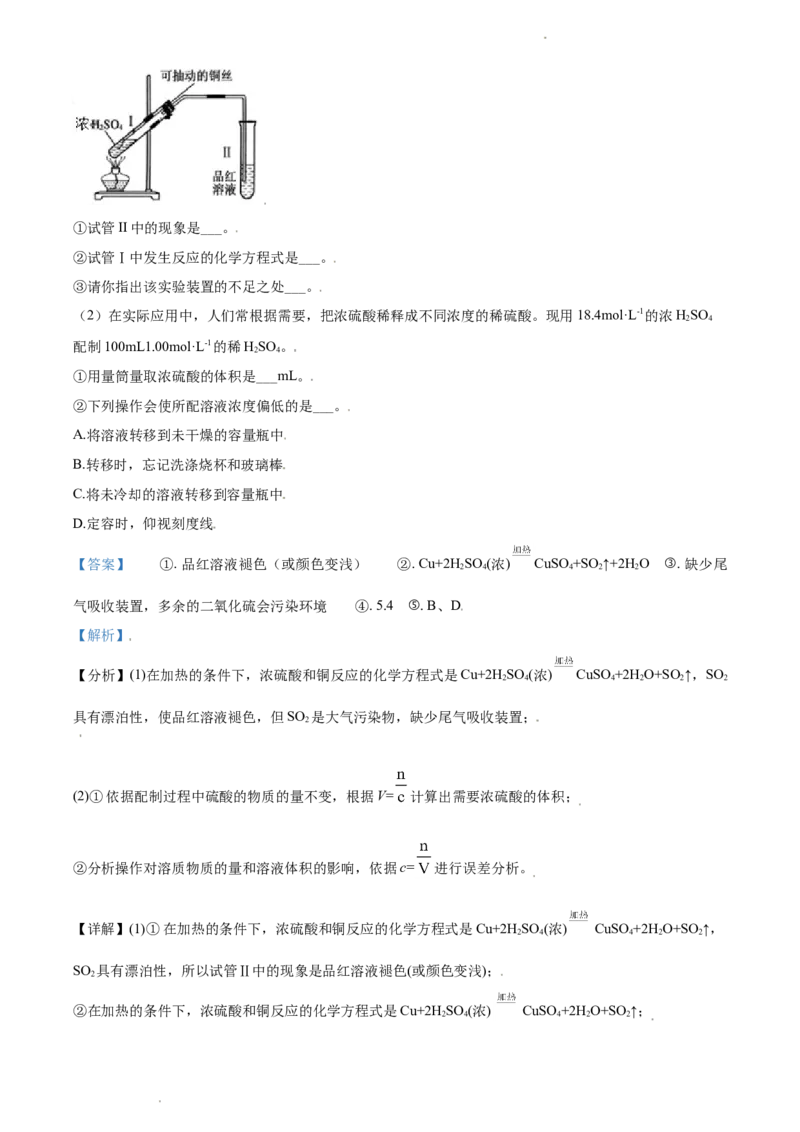
(1)某同学用如图所示的装置,完成铜与浓硫酸反应的实验:
学科网(北京)股份有限公司①试管II中的现象是___。
②试管Ⅰ中发生反应的化学方程式是___。
③请你指出该实验装置的不足之处___。
(2)在实际应用中,人们常根据需要,把浓硫酸稀释成不同浓度的稀硫酸。现用18.4mol·L-1的浓HSO
2 4
配制100mL1.00mol·L-1的稀HSO 。
2 4
①用量筒量取浓硫酸的体积是___mL。
②下列操作会使所配溶液浓度偏低的是___。
A.将溶液转移到未干燥的容量瓶中
B.转移时,忘记洗涤烧杯和玻璃棒
C.将未冷却的溶液转移到容量瓶中
D.定容时,仰视刻度线
【答案】 ①. 品红溶液褪色(或颜色变浅) ②. Cu+2H SO (浓) CuSO +SO↑+2H O ③. 缺少尾
2 4 4 2 2
气吸收装置,多余的二氧化硫会污染环境 ④. 5.4 ⑤. B、D
【解析】
【分析】(1)在加热的条件下,浓硫酸和铜反应的化学方程式是Cu+2H SO (浓) CuSO +2H O+SO ↑,SO
2 4 4 2 2 2
具有漂泊性,使品红溶液褪色,但SO 是大气污染物,缺少尾气吸收装置;
2
(2)①依据配制过程中硫酸的物质的量不变,根据V= 计算出需要浓硫酸的体积;
②分析操作对溶质物质的量和溶液体积的影响,依据c= 进行误差分析。
【详解】(1)①在加热的条件下,浓硫酸和铜反应的化学方程式是Cu+2H SO (浓) CuSO +2H O+SO ↑,
2 4 4 2 2
SO 具有漂泊性,所以试管Ⅱ中的现象是品红溶液褪色(或颜色变浅);
2
②在加热的条件下,浓硫酸和铜反应的化学方程式是Cu+2H SO (浓) CuSO +2H O+SO ↑;
2 4 4 2 2
学科网(北京)股份有限公司③SO 是大气污染物,所以实验装置的不足之处是缺少尾气吸收装置,多余的二氧化硫会污染环境;
2
(2)①配制过程中硫酸的物质的量不变,则V= = =5.4mL;
②A.将溶液转移到未干燥的容量瓶中,不影响溶液浓度,故A不符合题意;
B.转移时,忘记洗涤烧杯和玻璃棒,导致部分溶质损坏,溶质物质的量偏小,溶液浓度偏低,故B符合
题意;
C.将未冷却的溶液转移到容量瓶中,冷却后溶液体积偏小,溶液浓度偏高,故C不符合题意;
D.定容时,仰视刻度线,导致溶液体积偏大,溶液浓度偏小,故D符合题意;
答案选B、D。
28. 元素周期表是化学学习和化学研究的重要工具。下表为元素周期表的一部分,表中①~⑩分别代表一
种元素。回答下列问题:
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
1 ①
2 ② ③ ④ ⑤ ⑥ ⑦
3 ⑧ ⑨ ⑩
(1)上述元素中,有一种是地壳中含量最多的元素,该元素在周期表中的位置是_________。
(2)⑦、⑧、⑨元素的离子半径由大到小的顺序为_________(用离子符号表示)。
(3)由①、⑥、⑩组成的一种化合物有强氧化性,具有杀菌漂白的能力,则该化合物的电子式为_______。
(4)由⑤、⑥两元素组成的气态化合物常见的有两种,其中有一种不能用排水法收集,试用化学方程式解
释原因________。
(5)上述元素中有一种元素的氧化物和氢氧化物都是两性化合物,画出该元素的原子结构示意图______,
且该元素的单质可以溶解在氢氧化钠溶液中,写出该过程发生的离子方程式_____。
(6)不同卤素原子之间可形成卤素互化物,如I和Br形成的互化物IBr,其性质与卤素单质相近。⑩和Br
形成的互化物可以和SO 在水溶液中发生反应,该反应的化学方程式为___________。
2
【答案】 ①. 第二周期第VIA族 ②. F->Na+>Al3+ ③. ④. 3NO +HO=2HNO+NO
2 2 3
⑤. ⑥. 2Al+2OH-+2HO=2 +3H↑ ⑦. BrCl+2HO+SO =HSO +HCl+HBr
2 2 2 2 2 4
学科网(北京)股份有限公司【解析】
【分析】根据元素在周期表中的相对位置可知①~⑩分别是H、Li、Be、C、N、O、F、Na、Al、Cl。据
此解答。
【详解】(1)上述元素中,氧是地壳中含量最多的元素,该元素在周期表中的位置是第二周期第VIA族。
(2)⑦、⑧、⑨元素的离子具有相同的核外电子排布,离子半径随原子序数的增大而减小,则离子半径由
大到小的顺序为F->Na+>Al3+。
(3)由①、⑥、⑩组成的一种化合物有强氧化性,具有杀菌漂白的能力,该化合物是次氯酸,则该化合物
的电子式为 。
(4)由⑤、⑥两元素组成的气态化合物常见的有两种,其中有一种不能用排水法收集,该物质是二氧化氮,
由于二氧化氮能与水反应因此不能用排水法收集,化学方程式为3NO +HO=2HNO+NO。
2 2 3
(5)上述元素中有一种元素的氧化物和氢氧化物都是两性化合物,该元素是铝,其原子结构示意图为
,单质铝可以溶解在氢氧化钠溶液中,该过程发生的离子方程式为2Al+2OH-+2HO=2
2
+3H↑。
2
(6)卤素互化物的性质与卤素单质相近,则Cl和Br形成的互化物和SO 在水溶液中发生反应的化学方程式
2
为BrCl+2HO+SO =HSO +HCl+HBr。
2 2 2 4
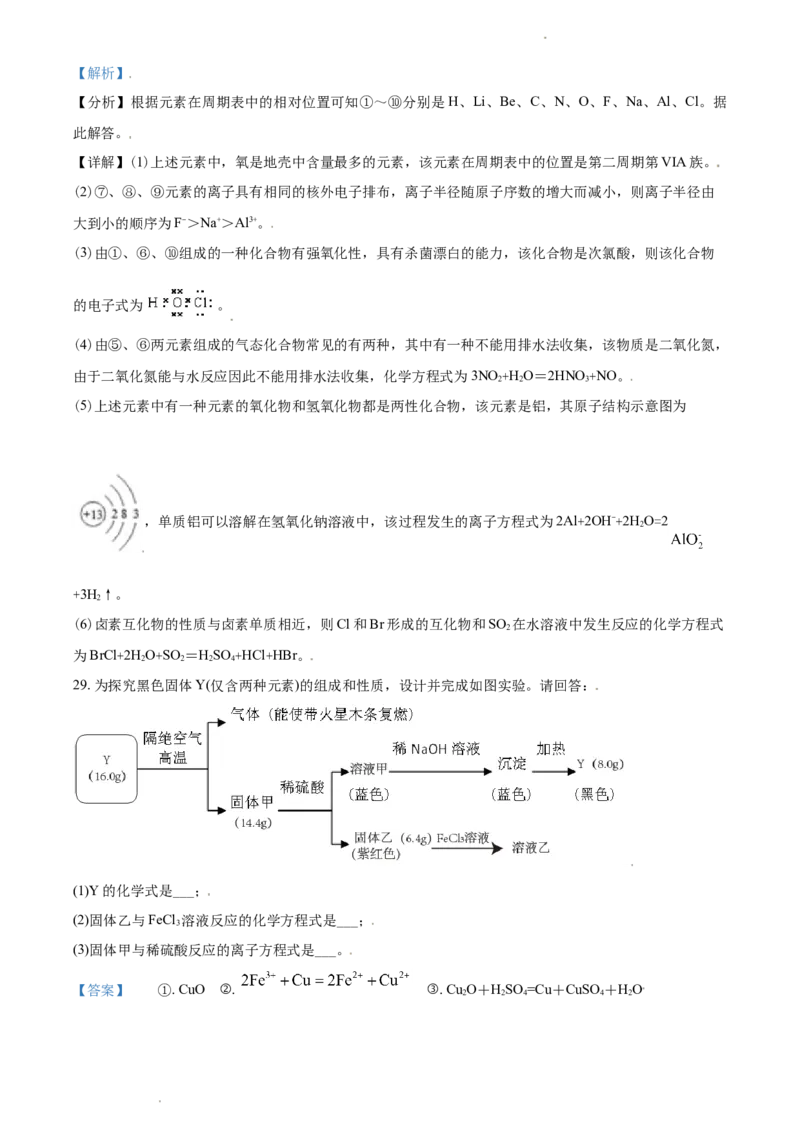
29. 为探究黑色固体Y(仅含两种元素)的组成和性质,设计并完成如图实验。请回答:
(1)Y的化学式是___;
(2)固体乙与FeCl 溶液反应的化学方程式是___;
3
(3)固体甲与稀硫酸反应的离子方程式是___。
【答案】 ①. CuO ②. ③. Cu O+HSO =Cu+CuSO +HO
2 2 4 4 2
学科网(北京)股份有限公司【解析】
【分析】流程中 16.0gX 隔绝空气加热分解放出了能使带火星的木条复燃的气体为氧气,质量:
16.0g-14.4g=1.6g,证明X中含氧元素,14.4g固体甲和稀硫酸溶液反应生成蓝色溶液,说明含铜离子,证
明固体甲中含铜元素,即X中含铜元素,甲溶液中加氢氧化钠溶液得到氢氧化铜沉淀、氢氧化铜受热分解
得到黑色固体氧化铜即Y,n(CuO)= =0.1mol,紫红色的固体乙能与氯化铁溶液反应、则固体乙为
Cu,结合质量守恒知,甲由铜、氧元素组成、其中铜元素质量为 0.1mol×64g/mol+6.4g =12.8g,氧元素质
量为14.4g-12.8g=1.6g,得到n(Cu):n(O)= 2:1,固体甲化学式为Cu O,由质量守恒知,Y隔绝空气加强热
2
放出氧气n(O )= =0.05mol,则Y中铜元素共甲12.8g,氧元素质量为16.0g-12.8g=3.2g,则物
2
质的量均为0.2mol,得到n(Cu):n(O)=0.2mol: 0.2mol=1:1,固体Y化学式为CuO,据此回答。
【详解】(1)分析可知X为CuO,故答案为CuO;
(2) 紫红色的固体乙即Cu能与氯化铁溶液反应生成氯化亚铁和氯化铜、则离子方程式为
;
(3)固体甲为Cu O,氧化亚铜和稀硫酸溶液发生反应生成铜、硫酸铜和水,反应的化学方程式为:Cu O+
2 2
HSO =Cu+CuSO +HO。
2 4 4 2
三、计算题(6分)
30. 将一定质量的镁和铝的合金投入100 mL,一定物质的量浓度的盐酸中,恰好反应,共产生气体5.6
L(标准状况下),向所得溶液中滴加5mol·L-1NaOH溶液至过量,最终产生白色沉淀13.6 g。请计算:
(1)原合金中镁和铝的质量分别是________。
(2)原盐酸溶液的物质的量浓度________。
【答案】 ①. m(Mg)=2.4 g,m(Al)=2.7 g ②. 5 mol/L
【解析】
【分析】金属Mg、Al是比较活泼的金属,与HCl反应产生Mg2+、Al3+进入溶液,Mg2+、Al3+与加入NaOH
电离产生的OH-结合形成Mg(OH) 、Al(OH) ,Mg、Al失去电子的物质的量与Mg2+、Al3+形成Mg(OH) 、
2 3 2
Al(OH) 结合的OH-的物质的量相等,等于盐酸中的H+完全转化为H 得到的电子的物质的量,结合H 的体
3 2 2
积及Mg(OH) 、Al(OH) 沉淀的质量计算。
2 3
学科网(北京)股份有限公司【详解】(1)n(H )= =0.25 mol,则一定质量的镁和铝的合金反应,转移的电子的物质的量
2
为 n(e-)=2n(H)=2×0.25mol=0.5 mol,向反应后的溶液中加入足量 NaOH 溶液,Mg2+、Al3+反应产生
2
Mg(OH) 、Al(OH) ,OH-的物质的量等于反应过程中金属失去电子的物质的量,n(OH-)=n(e-)=0.5 mol,则
2 3
m(OH-)=0.5 mol×17 g/mol=8.5 g,所以 Mg、Al 质量和为 m(Mg、Al)=13.6 g-8.5 g=5.1 g。假设混合物中
Mg、Al的物质的量分别是x、y,则24x+27y=5.1;2x+3y=0.5,解得x=0.1,y=0.1,所以混合物中Mg的质
量为m(Mg)=0.1 mol×24 g/mol=2.4 g;Al的质量为m(Al)=0.1 mol×27 g/mol=2.7 g;
(2)根据H元素守恒可知n(HCl)=2n(H)=2×0.25 mol=0.5 mol,则原盐酸溶液的物质的量浓度c(HCl)=
2
=5 mol/L。
【点睛】本题考查镁铝化合物性质、混合物的计算。掌握反应实质,利用电子守恒、元素守恒分析判断和
计算。
学科网(北京)股份有限公司学科网(北京)股份有限公司