文档内容
儋州市第一中学 2019-2020 学年高一上学期期中考试
化学
注意事项:
1.答题前在答题卡上填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上,答题卡密封线内不准答题
可能用到的相对原子质量:H:1,C:12,N:14,O:16,Na:23,S:32,Cl:35.5
第Ⅰ卷(40分)
一、选择题:本题共8小题,每小题2分,共16分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
1.下列说法正确的是( )
A. 化学是科学研究的内容,与普通百姓的生活没有多大关系
B. 化学研究只能认识分子,不能制造分子
C. 化学家可以制造出自然界中不存在的物质
D. 化学研究只会造成严重的环境污染,最终人类将毁灭在化学物质中
【答案】C
【解析】
【详解】A、我们生活环境中的药物、化纤、塑料、电池、计算机芯片,都来自化学家的研究成果,化学
与每个人息息相关,选项A不正确;
B、化学研究不只是认识分子,还能制造分子,化纤、塑料等高分子都是化学研究的成果,选项B不正确;
C、化学家可以制造出自然界中不存在的物质,选项C正确;
D、选项过于悲观,要相信我们一定能研制出对环境无害的化学用品和生活用品,通过对环境友好的方式
及优化环境的途径来提高生活质量,人类不会毁灭在化学物质中,选项D错误;
答案选C。
2.下列物质属于纯净物的是( )
A. 盐酸 B. 纯净无污染的空气 C. 泥水 D. 冰水
【答案】D
【解析】
【详解】A. 盐酸为HCl的水溶液,为混合物,与题意不符,A错误;
B. 纯净无污染的空气,为氮气、氧气等多种气体的混合物,与题意不符,B错误;C. 泥水为土与水的混合物,与题意不符,C错误;
D. 冰水为纯净的水,为纯净物,符合题意,D正确;
答案为D。
【点睛】盐酸为HCl的水溶液,为混合物。
3. 下列叙述中,正确的是( )
A. 氧化还原反应的本质是元素化合价发生了变化
B. 含化合价升高元素的反应物被氧化
C. 得到电子的物质被氧化
D. 氧化还原反应中,氧化剂和还原剂一定是两种物质
【答案】B
【解析】
试题分析:A、氧化还原反应 的特征是元素化合价发生了变化,其本质为电子的转移,错误;B、元素的化
合价升高,则失去电子,被氧化,发生氧化反应,正确;C、得到电子的物质为氧化剂,在反应中被还原,
错误;D、氧化还原反应中,同种元素可能既失去电子也得到电子,如氯气与水的反应,氧化剂、还原剂
可为同种物质,错误。
考点:考查氧化还原反应
4.下列电离方程式不正确的是( )
A. HSO =2H++SO2- B. MgCl =Mg2++2Cl-
2 4 4 2
C. NaCO=Na ++CO 2- D. Ba(OH) =Ba2++2OH-
2 3 2 3 2
【答案】C
【解析】
【详解】A. H SO 为强电解质,完全电离,则电离方程式为HSO =2H++SO2-,与题意不符,A错误;
2 4 2 4 4
B. MgCl 为强电解质,完全电离,则电离方程式为MgCl =Mg2++2Cl-,与题意不符,B错误;
2 2
C. Na CO 为强电解质,完全电离,则电离方程式为NaCO=2Na++CO 2-,符合题意,C正确;
2 3 2 3 3
D. Ba(OH) 为强电解质,完全电离,则电离方程式为Ba(OH) =Ba2++2OH-,与题意不符,D错误;
2 2
答案为C。
5.下列关于钠及其化合物的叙述中,正确的是( )
A. NaO、NaO 都属于碱性氧化物
2 2 2
B. 钠着火时可用干冰灭火
C. NaO、NaO 水溶液的成分相同
2 2 2
D. 向碳酸钠固体中滴加少量水,伴随着吸热现象【答案】C
【解析】
【详解】A. Na O属于碱性氧化物,NaO 属于过氧化物,与题意不符,A错误;
2 2 2
B. 钠着火时可用沙子灭火,钠与二氧化碳反应,不能用二氧化碳灭钠的着火,与题意不符,B错误;
C. Na O、NaO 水溶液均为NaOH溶液,成分相同,符合题意,C正确;
2 2 2
D. 向碳酸钠固体中滴加少量水,伴随着放热现象,与题意不符,D错误;
答案为C。
6.下列反应既属于离子反应又属于氧化还原反应的是( )
A. C+O =CO B. 2KClO=2KCl+3O ↑
2 2 3 2
C. HCl+NaOH=NaCl+H O D. Fe+CuSO=Cu+FeSO
2 4 4
【答案】D
【解析】
【详解】A. C+O =CO 化合价改变,属于氧化还原反应,不存在离子形式,不属于离子反应,与题意不符,
2 2
A错误;
B. 2KClO =2KCl+3O ↑化合价改变,属于氧化还原反应,不存在离子形式,不属于离子反应,与题意不符,
3 2
B错误;
C. HCl+NaOH=NaCl+H O化合价未变,属于非氧化还原反应,与题意不符,C错误;
2
D. Fe+CuSO =Cu+FeSO 化合价改变,属于氧化还原反应,可在溶液中进行,属于离子反应,符合题意,D
4 4
正确;
答案为D。
7.下列变化中,一定需加还原剂才能实现的是( )
A. CO→CO2- B. FeCl →FeCl C. C→CO D. NaO→O
2 3 3 2 2 2 2 2
【答案】B
【解析】
【分析】
还原剂化合价升高,需加入还原剂,则选项提供的变化为化合价降低。
【详解】A. CO →CO2-化合价未变,与题意不符,A错误;
2 3
B. FeCl →FeCl 化合价降低,符合题意,B正确;
3 2
C. C→CO 化合价升高,与题意不符,C错误;
2
D. Na O→O 化合价升高,与题意不符,D错误;
2 2 2
答案为B。【点睛】氧化还原反应中,还原剂化合价升高,则氧化剂化合价必然降低,且同时存在。
8.下列化学方程式中,不能用H++OH-=H O表示的是
2
A. 2NaOH+H SO =Na SO +2H O B. Ba(OH) +2HCl=BaCl +2H O
2 4 2 4 2 2 2 2
C. Cu(OH) +2HNO =Cu(NO)+2H O D. KOH+HCl=KCl+H O
2 3 3 2 2 2
【答案】C
【解析】
A、氢氧化钠是强碱,硫酸是强酸,硫酸钠是可溶性的盐,故A正确;B、氢氧化钡是强碱,盐酸是强酸,
氯化钡是可溶性的盐,故B正确;C、氢氧化铜是一种弱碱,其离子反应为Cu(OH)+2H+=2HO+Cu2+,故C错
2 2
误;D、氢氧化钾是强碱,盐酸是强酸,氯化钾是可溶性的盐,故D正确;故选C。
二、选择题:本题共6小题,每小题4分,共24分。每小题有一个或两个选项是符合题目要
求的。若正确答案只包括一个选项,多选得0分;若正确答案包括两个选项,只选一个且正
确得2分,选两个且都正确得4分,但只要选错一个就得0分。
9.用光洁的铂丝蘸取某无色溶液在无色火焰上灼烧,直接观察时看到火焰呈黄色,下列判断正确的是( )
A. 只含Na+ B. 可能含有Na+,可能还含有K+
C. 既含有Na+,又含有K+ D. 一定含Na+,可能含有K+
【答案】D
【解析】
【详解】钠元素的焰色是黄色,钾元素的焰色是紫色,但观察钾元素的焰色时要透过蓝色钴玻璃,以滤去
钠元素的黄光的干扰。做焰色反应实验时,直接观察时看到火焰呈黄色,说明肯定含有 Na+,不能判断
K+的存在与否,故D是正确的。
故选D。
10.下列关于物质的用途说法不正确的是( )
A. 碳酸氢钠作食品膨化剂 B. 过氧化钠作供氧剂
C. 氯气制漂白粉 D. 碳酸钠作胃药
【答案】D
【解析】
【详解】A. 碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,制作的食品疏松多孔,可作食品膨化剂,与题
意不符,A错误;
.
B 过氧化钠可与二氧化碳反应生碳酸钠和氧气,可作供氧剂,与题意不符,B错误;
C. 氯气与消石灰制漂白粉,与题意不符,C错误;
D. 碳酸钠水解后溶液碱性太强,不能作胃药,符合题意,D正确;答案为D。
11.下列有关胶体和溶液的说法正确的是( )
A. 制备Fe(OH) 胶体要用到饱和氯化铁溶液
3
B. 可通过观察溶液是否澄清透明来区别胶体和溶液
C. 胶体区别于其他分散系的本质特征是分散质的微粒直径在1~100nm之间
D. 氯化钠溶液可以产生丁达尔效应
【答案】AC
【解析】
【详解】A. 制备Fe(OH) 胶体时,操作为向沸水中滴加几滴饱和氯化铁溶液,至溶液呈红褐色,停止加热,
3
符合题意,A正确;
B. 胶体和溶液均为澄清的分散系,无法通过观察溶液是否澄清透明来区别,与题意不符,B错误;
C. 胶体区别于其他分散系的本质特征是分散质的微粒直径在1~100nm之间,符合题意,C正确;
D. 氯化钠溶液不 是胶体,不能产生丁达尔效应,与题意不符,D错误;
答案为AC。
12.将NaO 投入FeCl 溶液中, 可观察到的现象是( )
2 2 3
A. 生成白色沉淀 B. 生成红褐色沉淀
C. 有气泡产生 D. 无变化
【答案】BC
【解析】
【详解】将NaO 投入FeCl 溶液中,NaO 与水反应生成氢氧化钠、氧气和水,NaOH与FeCl 反应生成氢
2 2 3 2 2 3
氧化铁红褐色沉淀,则观察到的现象为:有气泡生成,有红褐色沉淀产生,答案为BC。
13.能大量共存的离子组是( )
A. Na+、Ag+、NO -、Cl- B. Cu2+、Na+、H+、OH-
3
C. K+、Ba2+、CO2-、Cl- D. K+、Na+、CO2-、NO -
3 3 3
【答案】D
【解析】
【详解】A. Ag+、Cl-可生成AgCl沉淀,不能大量共存,与题意不符,A错误;
.
B Cu2+、OH-可生成Cu(OH) 沉淀,不能大量共存,与题意不符,B错误;
2
C. Ba2+、CO2-可生成BaCO 沉淀,不能大量共存,与题意不符,C错误;
3 3
D. K+、Na+、CO2-、NO -可用大量共存,符合题意,D正确;
3 3
答案为D。14.除去下列物质中的杂质,所用试剂和方法正确的是( )
选项 物质 杂质 除杂质所用试剂和方法
A NaCO 固体 NaHCO 加热
2 3 3
B KNO KSO BaCl 溶液,过滤
3 2 4 2
C Cu CuO 稀硫酸,过滤
D CaCO CaO 盐酸,过滤
3
A. A B. B C. C D. D
【答案】AC
【解析】
【详解】A. 碳酸氢钠受热分解生成碳酸钠固体、二氧化碳气体和水,可用加热的方法除去碳酸钠中的碳酸
氢钠杂质,符合题意,A正确;
B. 硫酸钾与氯化钡反应生成硫酸钡沉淀和氯化钾,引入新的杂质离子,与题意不符,B错误;
C. CuO与硫酸反应生成硫酸铜溶液和水,而Cu与硫酸不反应,可用除去Cu中的CuO,符合题意,C正确;
D. 碳酸钙与盐酸反应生成氯化钙溶液,不符合除杂原则,与题意不符,D错误;
答案为AC。
【点睛】除杂时,除去杂质的同时不能引入新的杂质、不消耗非杂质物质。
第Ⅱ卷(60分)
15.下列物质中:①NaCl ②NaOH ③HCl ④CO ⑤NaHCO ⑥Fe ⑦金刚石 ⑧Cl ⑨澄清石灰水其中属
2 3 2
于电解质的有____;属于非电解质的有:____;能导电的有:____(填序号)
【答案】 (1). ①②③⑤ (2). ④ (3). ⑥⑨
【解析】
【详解】①NaCl中无自由移动的离子,不能导电,为化合物,其水溶液能导电,为电解质;
②NaOH中无自由移动的离子,不能导电,为化合物,其水溶液能导电,为电解质;
③HCl不能导电,为化合物,其水溶液能导电,为电解质;
④CO 不能导电,与水反应,其液态不能导电,为化合物,非电解质;
2
⑤NaHCO 中无自由移动的离子,不能导电,为化合物,其水溶液能导电,为电解质;
3
⑥Fe为单质,有自由移动的电子,能导电,既不是电解质,也不是非电解质;
⑦金刚石不能导电,为单质,既不是电解质,也不是非电解质;⑧Cl 不能导电,为单质,既不是电解质,也不是非电解质;
2
⑨澄清石灰水能导电,为混合物,既不是电解质,也不是非电解质;
综上所述,属于电解质的有①②③⑤;属于非电解质的有:④;能导电的有:⑥⑨。
16.3Cu+8HNO(稀)=3Cu(NO )+2NO↑+4HO
3 3 2 2
(1)用双线桥标明该反应中电子的转移及数目:___。
(2)还原剂是___;还原产物是___;被还原与未被还原N的个数比为___。
【答案】 (1). (2). Cu (3). NO
(4). 1:3
【解析】
【分析】
Cu与稀HNO 反应,Cu的化合价由0价变为+2价,化合价升高,作还原剂,生成的硝酸铜为氧化产物;
3
硝酸中的N原子化合价降低,由+5价变为+2价,作氧化剂,生成还原产物,则反应的最小公倍数为6。
【详解】Cu与稀HNO 反应,Cu的化合价由0价变为+2价,化合价升高,作还原剂,生成的硝酸铜为氧
3
化产物;硝酸中的N原子化合价降低,由+5价变为+2价,作氧化剂,生成还原产物,则反应的最小公倍
数为6,双线桥法为 ;被还原的N原子的个数为2,未被还原N的个数为
6,比值为1:3。
【点睛】还原剂失电子,化合价升高,被氧化,得到氧化产物;氧化剂得电子,化合价降低,被还原,得
到还原产物。
17.现有下列4组物质:
A.CuO、MgO、CO、NaO B.Cl、H、N、Na
2 2 2 2 2
C.O、Fe、Cu、Zn D.HCl、HO、HSO 、HNO
2 2 2 4 3
(1)填写下表空白___
组别 A组 B组 C组 D组分类标准 碱性氧化物 金属单质
不属于该类别的物质 Na HO
2
(2)若(1)表中的4种物质均为原料,用两种方法制取NaCO,请写出有关的化学反应方程式。
2 3
方法一:____。
方法二:____。
【答案】 (1).
组别 A组 B组 C组 D组
分类标准 碱性氧化物 非金属单质 金属单质 酸
不属于该类别的物质 CO Na O HO
2 2 2
(2). 4Na+O =2Na O、NaO+CO= Na CO (3). 2Na+2H O=2NaOH+H ↑、2NaOH+CO =Na CO +H O
2 2 2 2 2 3 2 2 2 2 3 2
【解析】
【详解】(1)A.CuO、MgO、NaO 都属于碱性氧化物,而CO 为酸性氧化物;
2 2
B.Cl、H、N 都属于气体或非金属单质,而Na 为固体,金属单质;
2 2 2
C. Fe、Cu、Zn为金属单质,O 为非金属单质;
2
D.HCl、HSO 、HNO 属于酸或强电解质,而HO不属于酸、属于弱电解质;
2 4 3 2
(2)表中的4种物质为CO、Na、O、HO,可用Na与氧气反应生成氧化钠,再与二氧化碳反应生成碳
2 2 2
酸钠;还可以Na与水反应生成NaOH,再与二氧化碳反应生成碳酸钠,涉及到的方程有4Na+O=2Na O、
2 2
NaO+CO= Na CO;2Na+2HO=2NaOH+H ↑、2NaOH+CO =Na CO +H O;
2 2 2 3 2 2 2 2 3 2
18.有一包白色固体,它可能是KCl、KCO、KNO 中的一种或几种,进行下列实验:
2 3 3
①溶于水,得无色溶液;
②在所得溶液中滴入AgNO 溶液,生成白色沉淀;
3
③再滴加稀硝酸,沉淀量减少但不完全消失,同时有气泡生成。
根据上述现象判断:
(1)白色固体一定含有的成分是___________,可能含有的成分是___________;
(2)请写出上述实验中有关反应的离子方程式:______________________。
【答案】(1)KCl 和 K CO KNO (2)Ag++Cl-====AgCl↓,2Ag++ ====Ag CO ↓,
2 3 3 2 3
Ag CO +2H+====2Ag++H O+CO ↑
2 3 2 2
【解析】由②产生白色沉淀知,可能含有K CO 和KCl中的一种或两种;由③沉淀量减少且有气泡生成知,一定含
2 3
有K CO ;又由沉淀不完全消失可知,一定含有KCl。
2 3
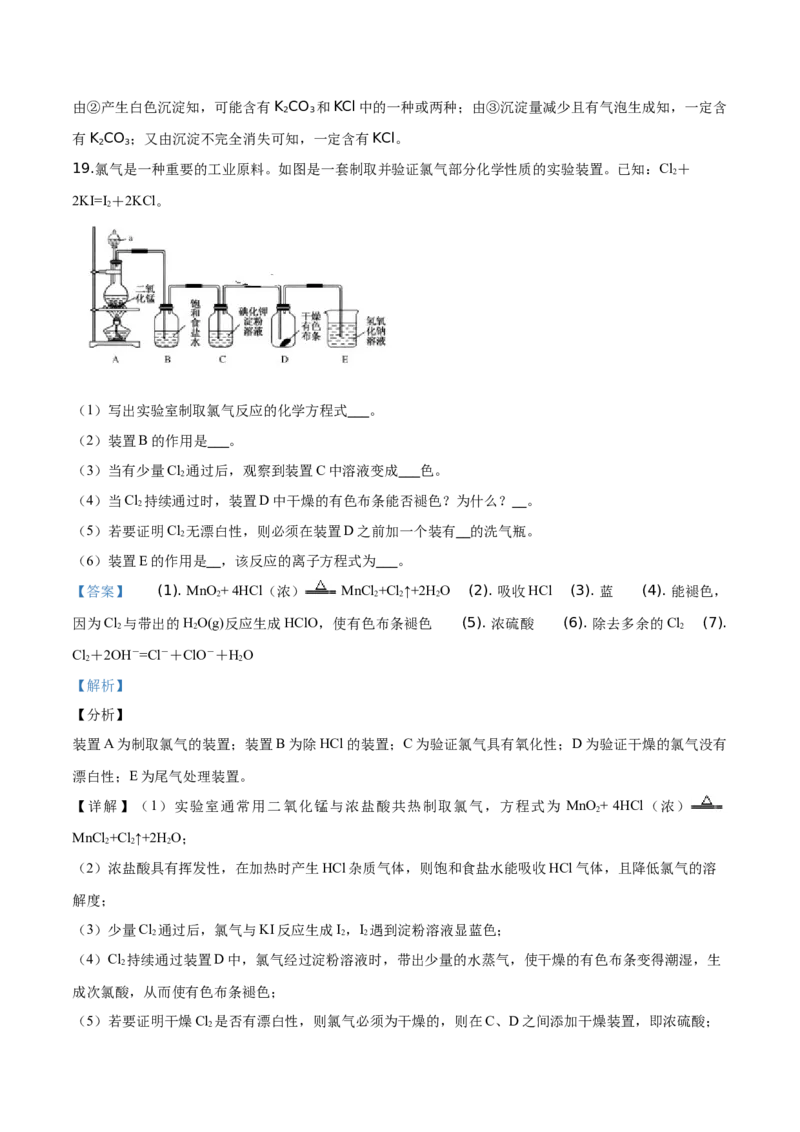
19.氯气是一种重要的工业原料。如图是一套制取并验证氯气部分化学性质的实验装置。已知:Cl+
2
2KI=I+2KCl。
2
(1)写出实验室制取氯气反应的化学方程式___。
(2)装置B的作用是___。
(3)当有少量Cl 通过后,观察到装置C中溶液变成___色。
2
(4)当Cl 持续通过时,装置D中干燥的有色布条能否褪色?为什么?__。
2
(5)若要证明Cl 无漂白性,则必须在装置D之前加一个装有__的洗气瓶。
2
(6)装置E的作用是__,该反应的离子方程式为___。
【答案】 (1). MnO + 4HCl(浓) MnCl +Cl↑+2H O (2). 吸收HCl (3). 蓝 (4). 能褪色,
2 2 2 2
因为Cl 与带出的HO(g)反应生成HClO,使有色布条褪色 (5). 浓硫酸 (6). 除去多余的Cl (7).
2 2 2
Cl+2OH-=Cl-+ClO-+HO
2 2
【解析】
【分析】
装置A为制取氯气的装置;装置B为除HCl的装置;C为验证氯气具有氧化性;D为验证干燥的氯气没有
漂白性;E为尾气处理装置。
【详解】(1)实验室通常用二氧化锰与浓盐酸共热制取氯气,方程式为 MnO + 4HCl(浓)
2
MnCl +Cl↑+2H O;
2 2 2
(2)浓盐酸具有挥发性,在加热时产生HCl杂质气体,则饱和食盐水能吸收HCl气体,且降低氯气的溶
解度;
(3)少量Cl 通过后,氯气与KI反应生成I,I 遇到淀粉溶液显蓝色;
2 2 2
(4)Cl 持续通过装置D中,氯气经过淀粉溶液时,带出少量的水蒸气,使干燥的有色布条变得潮湿,生
2
成次氯酸,从而使有色布条褪色;
(5)若要证明干燥Cl 是否有漂白性,则氯气必须为干燥的,则在C、D之间添加干燥装置,即浓硫酸;
2(6)氯气有毒,不能直接排放到大气中,则NaOH溶液为吸收未反应的氯气;反应生成氯化钠、次氯酸
钠和水,离子反应为Cl+2OH-=Cl-+ClO-+HO。
2 2
【点睛】氯气通过湿润的淀粉碘化钾溶液时,使溶液中的水蒸气进入干燥的有色布条的装置。