文档内容
海南中学 2019——2020 学年第一学期期末考试
高一化学试题
本试卷分选择题和非选择题两部分,全卷满分100分,考试时间90分钟
可能用到的相对原子质量:H-1 C-12 O-16 Cl-35.5 Na-23 Mg-24 Al-27
Fe-56
第Ⅰ卷选择题(共40分)
一、单项选择题(每小题只有一个选项符合题意,每小题2分,共16分)
1.下列物质中属于两性氧化物的是( )
A. CO B. NaO C. NaO D. Al O
2 2 2 2 2 3
2.经一束单色光照射,下列分散系中能出现明显丁达尔效应的是( )
.
A 澄清石灰水 B. 氢氧化铁红褐色液体
C. 饱和食盐水 D. 石灰浆
3.下列物质不属于合金材料的是( )
A. 赤铁矿 B. 硬铝 C. 304不锈钢 D. 青铜器
4.下列各组物质中,属于同位素的是( )
A. 金刚石、石墨、C B. 小苏打、苏打、大苏打(NaSO)
60 2 2 3
C. 12C、13C、14C D. 盐酸、次氯酸、高氯酸(HClO)
4
5.下列物质中,只含有非极性共价键的是( )
A. KOH B. HS C. Cl D. MgO
2 2
6.1869年2月,编制并公布了世界上第一张元素周期表的科学家是( )
A. 英国的舍勒 B. 俄国的门捷列夫
C. 瑞士的维尔纳 D. 意大利的阿伏伽德罗
7.已知反应6HCl+KClO =3Cl↑+KCl+3H O,下列说法错误的是( )
3 2 2
A. HCl既显酸性又显还原性
B. KClO 是氧化剂
3
C. 被氧化与被还原的氯元素的物质的量比为5:1
D. KCl是还原产物
8.焰色试验常用于检验试样中所含金属元素 的种类,灼烧下列物质时,火焰呈浅紫色的是( )
A. 碳酸钾 B. 硫酸铜 C. 氯化钙 D. 氯化钠
二、不定项选择题(每小题有1个或2个合理选项,全对得4分、答对但不全的2分、有错得0分;每小题4分,共24分)
9.漂白液、漂白粉和过氧化钙(CaO)均可用于漂白、杀菌或消毒。下列说法正确的是( )
2
A. 漂白粉的有效成分是Ca(ClO)
2
B. 漂白液能杀菌消毒,源于其本身具有毒性
C. 漂白粉投入适量的稀盐酸中可以提高漂白、杀菌的效率
D. 漂白液、漂白粉和过氧化钙均属于次氯酸盐
10.设N 为阿伏伽德罗常数,下列判断正确 的是( )
A
A. 22.4L氯气中含有的Cl数目为2N
A
B. 1.0mol/LCaCl 溶液中含有的Cl-数目为2N
2 A
C. 7.8gNa O 晶体中含有的Na+数目为0.1N
2 2 A
D. 2.0g重水(2H16O)中含有的中子数目为N
2 A
11.根据元素周期律判断,下列关系正确的是( )
A. 离子半径:O2->S2->Na+ B. 稳定性:CH>H O>NH
4 2 3
C. 酸性:HNO>H CO>H SiO D. 最高化合价:S>Cl>P
3 2 3 2 3
12.我国宋代的药物著作《开宝本草》中记载了有关中药材----铁华粉的制法为:取钢煅作叶,令表光净、
以盐水洒之并置于浓醋瓮中,阴处埋之百日,则铁上生衣,铁华成矣。由此判断铁华粉是指( )
A. 铁粉 B. 醋酸亚铁 C. 食盐 D. 氢氧化铁
13.下列离子方程式书写正确的是( )
A. 氧化亚铁与稀盐酸反应:FeO+2H+=Fe3++H O
2
B. 向氯化铁溶液中加入铜粉:Fe3++Cu=Fe2++Cu2+
C. 将足量的氢氧化钡溶液与少量的碳酸氢钠溶液混合:HCO -+Ba2++OH-=BaCO ↓+H O
3 3 2
D. 将铝粉投入到烧碱溶液中:2Al+2OH-+2H O=2AlO-+3H ↑
2 2 2
14.使用容量瓶配制溶液过程中,下列操作会使所配制的溶液浓度偏低的是( )
A. 溶液转移到容量瓶后,烧杯内壁及玻璃棒未用蒸馏水洗涤
B. 转移溶液前,容量瓶内存有少量蒸馏水
C. 定容时,俯视容量瓶的刻度线
.
D 定容后摇匀,发现液面降低,又补加少量蒸馏水重新达到刻度线
第Ⅱ卷非选择题(共60分)
15.根据下列实验过程,请回答:
(1)在常温下,将氯气通入氢氧化钠溶液中,所发生反应的离子方程式为:__;所得溶液具有漂白性,
其有效成分的名称为__。
(2)将上述呈碱性的溶液与FeCl 溶液混合,可制得一种新型绿色消毒剂——高铁酸钠(NaFeO),反
3 2 4应如下:3ClO-+2Fe3++10OH-=2FeO 2-+3Cl-+5H O则该反应中的氧化产物是__(填离子符号),当反应中转移
4 2
电子的数目是0.3N 时,所消耗的氧化剂的物质的量为__。
A
(3)证实最终所得溶液中含有Na+的操作是:进行焰色实验时,火焰呈现__色。
16.请直接用计算结果填空:
(1)标准状况下,测定1.32g某气体X的体积为0.672L,则X的摩尔质量为__。
(2)已知5.1g镁铝合金与100mL某浓度的盐酸恰好完全反应,得到5.6L氢气(标准状况下)。则:①生
成的H 分子的数目是__N 。
2 A
②该合金中镁和铝的物质的量之比为__。
③上述盐酸的物质的量浓度为__。
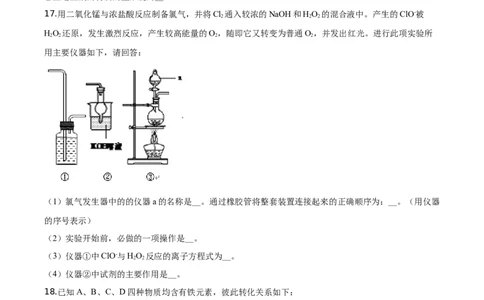
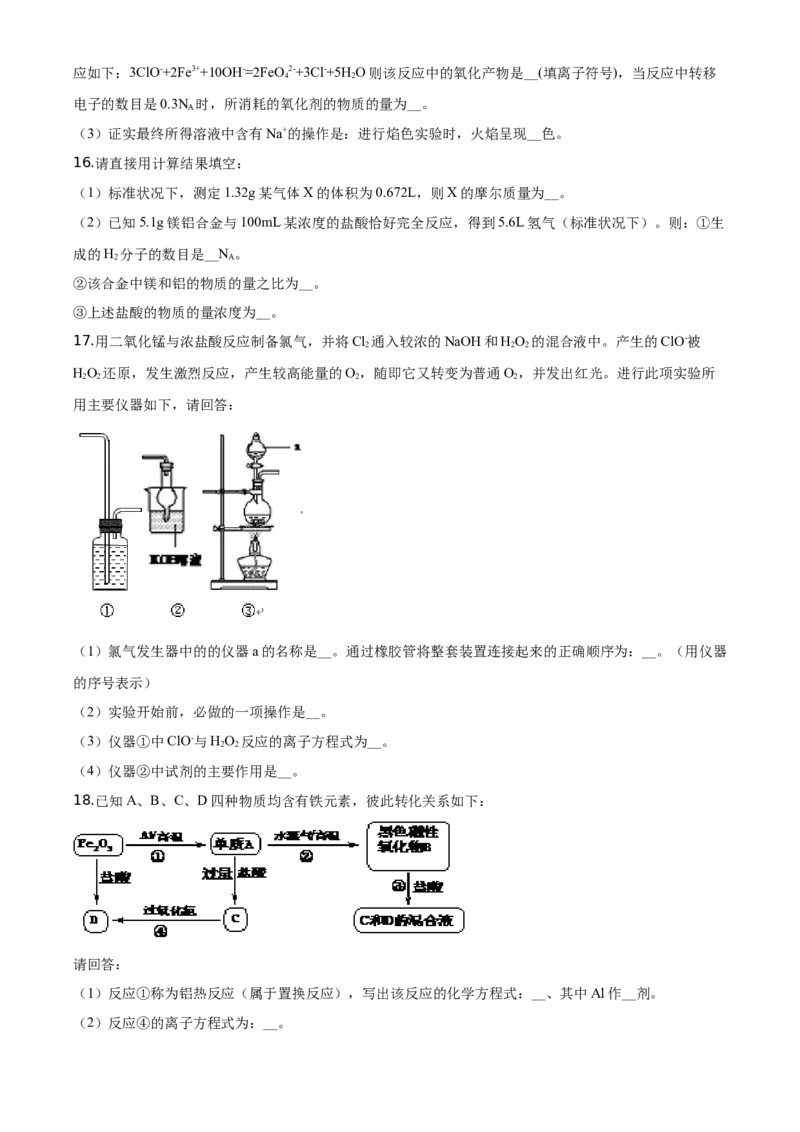
17.用二氧化锰与浓盐酸反应制备氯气,并将Cl 通入较浓的NaOH和HO 的混合液中。产生的ClO-被
2 2 2
HO 还原,发生激烈反应,产生较高能量的O,随即它又转变为普通O,并发出红光。进行此项实验所
2 2 2 2
用主要仪器如下,请回答:
(1)氯气发生器中的的仪器a的名称是__。通过橡胶管将整套装置连接起来的正确顺序为:__。(用仪器
的序号表示)
(2)实验开始前,必做的一项操作是__。
(3)仪器①中ClO-与HO 反应的离子方程式为__。
2 2
(4)仪器②中试剂的主要作用是__。
18.已知A、B、C、D四种物质均含有铁元素,彼此转化关系如下:
请回答:
(1)反应①称为铝热反应(属于置换反应),写出该反应的化学方程式:__、其中Al作__剂。
(2)反应④的离子方程式为:__。(3)新配制的C溶液中应加入__,以防止其转化为D。检验D溶液中阳离子的常用试剂是__(填化学
式),实验现象为__。
19.下表为元素周期表的一部分,请参照给定元素的位置,回答下列问题:
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
周期\族
1 ①
2 ② ③ ④
3 ⑤ ⑥ ⑦ ⑧
(1)元素④、⑤、⑥的原子半径由大到小的顺序为___(用元素符号表示)。
(2)元素③、⑦的最高价含氧酸的酸性由强到弱的顺序为__。(用化学式表示)
(3)碱性强弱比较:元素⑤的氢氧化物__⑥的氢氧化物(用<、=、>填空);两者相互反应的离子方程式
为__。
(4)由元素⑤和⑧共同组成的化合物的电子式为__、它属于__化合物。(填“共价”或“离子”)
(5)由元素①⑧形成的化合物A和由元素④⑤⑧的化合物B,可相互反应产生黄绿色气体单质,该反应
的离子方程式为__;该黄绿色气体单质会使得湿润淀粉碘化钾试纸变蓝色,表明生成了碘单质(I),由
2
此推测这两种元素的气态氢化物的稳定性强弱顺序为:__。(用化学式表示)
20.人们运用元素周期律和元素周期表,可以系统研究元素的性质。试回答:
(1)碱金属元素中,锂原子的结构示意图为__、其中6Li、7Li互为__,用电子式表示LiO的形成过程___。
2
(2)金属钾 K位于元素周期表中的第__周期、第__族;钾的氧化物有多种,其中过氧化钾(KO)和超氧化
19 2 2
钾(KO )常作供氧剂,写出过氧化钾与CO 反应的化学方程式:___;超氧化钾与水反应如下,请配平该反
2 2
应的化学方程式:
_KO +_HO=_KOH+_O↑+_HO
2 2 2 2 2
(3)第三周期元素中,酸性最强的HClO 中氯元素的化合价为__、可作半导体材料的元素是__(填名称),
4
当反应H+Cl 2HCl发生过程中,涉及到___键断裂和__键的形成。(填:离子键或极性键或非极性键)
2 2