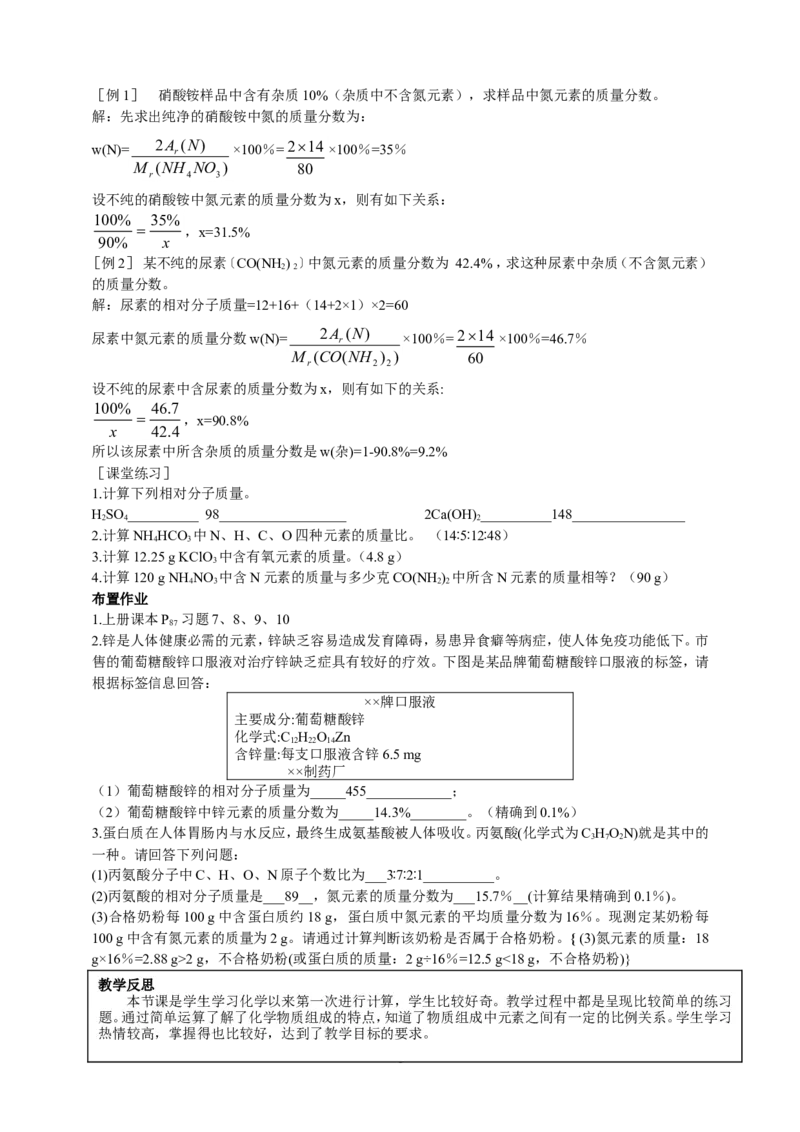文档内容
课题 4 化学式与化合价
教学目标
(1)了解什么是化学式及化学式的意义;
(2)熟记常见元素及原子团的化合价;
(3)能利用化学式简单推求化合价,进而能用化学式正确地表示常见物质的组成;
(4)学会简单化学式的读法。
教学重点
1.熟记常见元素及原子团的化合价;
2.用化学式表示某些物质的组成,并利用化合价推求化学式。
教学难点
1.化学式的书写;
2.利用化合价写化学式。
第一课时 化学式
1、下列符号分别代表某些物质,从组成中所含元素的种类判断各属哪一类物质(单质、化合物、氧化物)
Al、CuO、He、H、NH 、SO 、ZnO、NaCl、KMnO
2 3 2 4
一、化学式
1.定义:用元素符号和数字的组合表示物质组成的式子叫做化学式
[提问] 化学式有什么意义呢?我们以水的化学式“HO”为例进行学习。
2
2.注意:①纯净物的化学式是唯一的,混合物无化学式;
②书写化学式必须以事实为基础;
③由原子构成的单质的化学式与元素符号一样。
3、意义(以HO为例)
2
[提问] 水中是否含氢气、氧气?理解右下角小数字的正确含义。2HO表示什么?
2
[回答] 水中没有氢气和氧气;右下角的2表示一个水分子中有2个氢原子;2HO表示2个水分子。
2
[练习] 请以水的化学式表示的意义为参考,说说二氧化碳的化学式(CO)表示的意义。
2
[讨论] 符号H、2H、H、2H、2H+各具有几个意义?分别是什么?
2 2
3.化学式的写法和读法
(1)单质用元素符号表示:
①金属(铁Fe、铜Cu等)
②固态非金属(如碳C、磷P、硫S等)
③稀有气体(氦He、氖Ne、氩Ar等)
④双原子构成的分子:如氢气H、氧气O、氮气N、氟气F、氯气Cl、溴Br 、碘I 等。
2 2 2 2 2 2 2
(2)化合物(只研究两种元素组成的化合物)
①写法:a.氧化物:如CuO、PO,“氧在后”。
2 5
b.金属与非金属元素组成的化合物:如NaCl、ZnS,“金左,非右”。
(注意)1.化学式中原子个数为1时,“1”不标出。
2.化学式中右下方的小数字一般为最简整数比。
②读法:一般从右向左读作“某化某”,例如:ZnS读作硫化锌。非金属氧化物还要读出化学式中各种
1元素的原子个数,如PO。
2 5
板书设计
课题4 化学式与化合价
一、化学式
1.定义:用元素符号和数字的组合表示物质组成的式子叫做化学式
2.意义(以水为例)
(1)表示一种物制:水
宏观
(2)表示该物质的元素组成 :水由氢、氧两种元素组成
(3)表示物质的一个分子 :一个水分子
微观
(4)表示物质的分子构成 :每个水分子由两个氢原子和一个氧原子构成
3.化学式的写法和读法
[课堂练习]
1.上册课本P 习题 1.(1)(2)(3)(4)
87
2.2CO 表示( )
2
A.2个二氧化碳分子 B.2个碳原子和4个氧原子
C.2个碳原子和2个氧分子 D.2个碳原子和2个氧原子
第二课时 化合价
二、化合价
实验测知,化合物均有固定的组成,即形成化合物的元素有固定的原子个数比。
物质 HCl HO NaCl Fe O
2 2 3
原子个数比 1∶1 2∶1 1∶1 2∶3
通过观察我们可以得出:物质不同,原子个数比可能不同。
[分析] 原因是在形成化合物时,各原子为了使其结构达到稳定,即最外层电子数达到8,不同原子的
个数比是电子数目不同造成的。
1、化学上用“化合价”来表示原子之间相互化合的数目。化合价是元素化合时表现出来的性质。
看书本P85表4--2 常见元素和根的化合价
2、注意:①化合价有正价和负价之分,有些元素有多种化合价
②单质中元素化合价为0
③金属元素只有正价,非金属元素一般显负价
④在化合物中正负化合价的代数和为0
⑤氧元素通常显—2价,氢元素通常显+1价。
[观察] Ca( OH ) 、NaOH 、 CaCO、NaCO、CuSO 、 NH NO 、(NH )SO 这些化合物中加横线的部分
2 3 2 3 4 4 3 4 2 4
有什么特点?
3、原子团: 有些物质如Ca(OH)、CaCO 中的一些原子集团,作为整体参加化学反应,这样的原子集
2 3
团叫做原子团,也叫根,根也有化合价。
原子团 化学式 化合价 原子团 化学式 化合价
氢氧根 OH -1 硝酸根 NO -1
3
碳酸根 CO -2 硫酸根 SO -2
3 4
铵根 NH +1 高锰酸根 MnO -1
4 4
原子团的化合价是其组成元素的化合价的代数和。
4、化合价的书写:在元素符号的正上方先标“+”“—”,后标数值。
2+1 -2 +2 -2
H O Mg S
[练习] 请同学们标出下列物质中各元素的化合价。讨论常见化合物中,正、负化合价的代数和有什么
相同之处?
1 1 2 2 1 2 4 2 4 2
NaCl MgO H O SO MnO
2 2 2
[总结] 1.许多元素的原子在不同的条件下可显示不同的化合价。
2.在化合物里正负化合价的代数和为零。
3化合价口诀:
一价钾氯氢钾钠银,二价氧钡钙镁锌;三铝四硅五价磷,二三铁,二四碳,二四六硫都齐全
注意:Fe有+2、+3;Cu有+1、+2,高价时读作铁或铜,低价时读作亚铁或亚铜。
例如:FeCl 读作氯化亚铁,FeCl 读作氯化铁。Cu O读作氧化亚铜,CuO读作氧化铜。
2 3 2
[探究]化合价的表示与离子符号有何区别?
+3
如:+3价铁元素 Fe 铁离子 Fe3+ (两同两不同)
三、 化合价的应用
1.已知化合价书写化学式(知价写式)
[例题] 已知磷为+5价,氧为-2价,写出磷的氧化物的化学式。
解:(1)写出组成化合物的两种元素的符号,正价的写在左边,负价的写在右边。
P O
(2)求两种元素正、负化合价绝对值的最小公倍数。
5×2=10
(3)求各元素的原子数:
最小公倍数 正价数(或负价数 ) 原子数
P: 10 ÷5 =2
O: 10 ÷2 =5
(4)把原子数写在各元素符号的右下方,即得化学式:PO
2 5
(5)检查化学式,当正价总数与负价总数的代数和等于0时,化学式才算是正确的。
(+5)×2+(-2)×5=+10-10=0
答:这种磷的化合物的化学式是PO。
2 5
[小结] 知价写式一般步骤:
(1)写出元素符号,正价在左,负价在右。
(2)求两种元素正、负化合价绝对值的最小公倍数。
(3)求各元素的原子数。
(4)把原子数写在各元素符号的右下方,即得化学式。
(5)按正负化合价代数和为0的原则检查化学式。
[练习] 写出溴化钠、氧化钙、氧化铝、二氧化氮的化学式。
答案:NaBr、CaO、Al O、NO
2 3 2
[补充] 十字交叉法写化学式
一排序,二标价,三约简,四交叉,五检查
例如:写出下列物质的化学式
氧化铝 硫化氢 水 氯化镁
3 2 1 2 1 2 2 1
Al O N S H O MgCl
2 3 2 2 2
3练习:写出下列物质的化学式
氧化钠 氯化钡 氯化银
答案:NaO BaCl AgCl
2 2
2.已知化学式书写化合价(知式写价)
例:根据在化合物中,正、负化合价代数和为0的原则,已知氧元素为-2价,计算二氧化硫里硫的化合
价。
解:SO :根据正负化合价代数和为零可知:S元素的化合价为+4。
2
练习:标出下列加点元素的化合价:
S、SO、SO、HSO
2 3 2 4
NO、NO、NO、NHNO
2 2 5 4 3
答案:0 、 4 、 6 、 6 2 、 4 、 5 、 3 5
S SO SO H SO NO NO N O NH NO
2 3 2 4 2 2 5 4 3
[课堂小结]
通过本节课的学习,我们知道表示物质的组成可以用化学式,化学式既可以表示该物质中有哪几种元
素,又可表示出该物质中的一个分子中每种原子各有几个。化学式是通过实验测定的,除此以外我们
还可以通过化合价推求化学式。同时我们还知道了化合价表示原子之间相互化合的数目。
板书设计
课题4 化学式与化合价
二、化合价
1.化合价表示原子之间相互化合的数目
2.原子团:作为一个整体参加反应的原子集团,也叫根
3.注意事项:
4.应用
(1)已知化合价书写化学式
(2)已知化学式书写化合价
布置作业
1.上册课本P 习题3、5、6
87
2.某宝石的主要成分是SiO,SiO 中硅元素的化合价是( )
2 2
A.+1 B.+2 C.+3 D.+4
3.某含铁盐溶液能够在高浓度的碱性环境下长期稳定存在,且具有较强的灭菌消毒功能,该盐是一种
绿色、无污染的净水剂,其化学式为NaFeO。则其中铁元素的化合价是( )
2 3
A.+2 B.+3 C.+4 D.+6
4.我国科学家发现,亚硒酸钠能消除加速人体衰老的活性氧。亚硒酸钠中硒元素(Se)为+4价,氧元素
为-2价,则亚硒酸钠的化学式为( )
A.Na SeO B.Na SeO C.NaSeO D.Na SeO
2 3 2 4 3 2 2
答案:2.D 3.C 4.A
教学反思
通过本节课的教学,发现化合价概念较抽象使学生接受有一定的困难,所以应分散难点。前面的离子、
元素等知识的学习不容忽视,它是这节课的重要基础。记忆化合价十分枯燥,组织好本课的活动与探究,
让学生主动投入到学习活动中。在课下让学生编化合价的歌谣,利于学生记忆,有的学生编得挺不错!
4第三课时 根据化学式的计算
相对分子质量:就是化学式中各原子的相对原子质量的总和。(符号为Mr)
1.根据化学式计算相对分子质量
[例1] 计算HO的相对分子质量。
2
解:HO的相对分子质量=2×1+16×1=18
2
[练习] 计算3HNO、NH NO 、(NH )SO 的相对分子质量。
3 4 3 4 2 4
2.根据化学式计算组成物质的元素质量比
[例] 计算HO中H、O元素的质量比。
2
在物质中各元素的质量比就是同种原子的相对原子质量之和之比。
解:HO中H、O元素的质量比=(2×1)∶(16×1)=2∶16=1∶8(化为最简整数比)
2
计算二氧化碳中各元素的质量比m(C)∶m(O)=(12×1)∶(16×2)=12∶32=3∶8
计算硫酸中各元素的质量比:m(H)∶m(S)∶m(O)=(1×2)∶32∶(16×4) =1∶16∶32
计算硫酸铵中各元素的质量比:m(N)∶m(H)∶m(S)∶m(O)=(2×14)∶(1×8)∶32∶(16×4)=7∶2∶8∶16
[练习] 计算HNO、NH NO 中各元素的质量比。
3 4 3
3.计算物质中某一元素的质量分数。(质量分数又称为质量百分含量)
[例] 计算水中H元素的质量分数
氢原子的相对原子质量氢原子的个数 ×100%=12 ×100% =11.1%
水的相对分子质量 18
答:水中氢元素的质量分数为11.1%。
[练习] 计算NH NO 中各元素的质量分数。
4 3
4.根据化学式的其他计算
(1)计算化合物中的原子个数之比
如:Fe O 中,铁原子与氧原子个数比就是2∶3,CaCO 中钙、碳、氧原子个数比为1∶1∶3。
2 3 3
注意某些物质的化学式中,同种元素并不写在一起的,这时要注意原子个数。
如:NH NO 中,氮、氢、氧原子个数比应该为2∶4∶3
4 3
Cu (OH) CO 中,铜、碳、氢、氧原子个数比为2∶1∶2∶5
2 2 3
(2)计算一定质量的化合物中某元素的质量
某元素的质量=物质的质量×该元素在物质中的质量分数
[例1] 求 60 g MgSO 中含有氧的质量。
4
416
解:m(O)=m(MgSO )×w(O)=60 g× =32 g
4
2432416
[例2] 多少克碳酸氢铵( NH HCO )与 400 g 硝酸铵(NH NO )含氮元素质量相等?
4 3 4 3
解:根据所含氮元素质量相等来列等式
设需要碳酸氢铵的质量为 x,则质量为 x 的碳酸氢铵中含有氮元素的质量为 m (N)=x·
1
14
=17.7%·x
1451248
142
400 g硝酸铵中含有氮元素质量为m(N)=400× ×100%=400 g×35%
2
14241163
根据题意:17.7%·x=400 g×35%;x=790 g
(3)有关混合物中元素的质量分数的计算
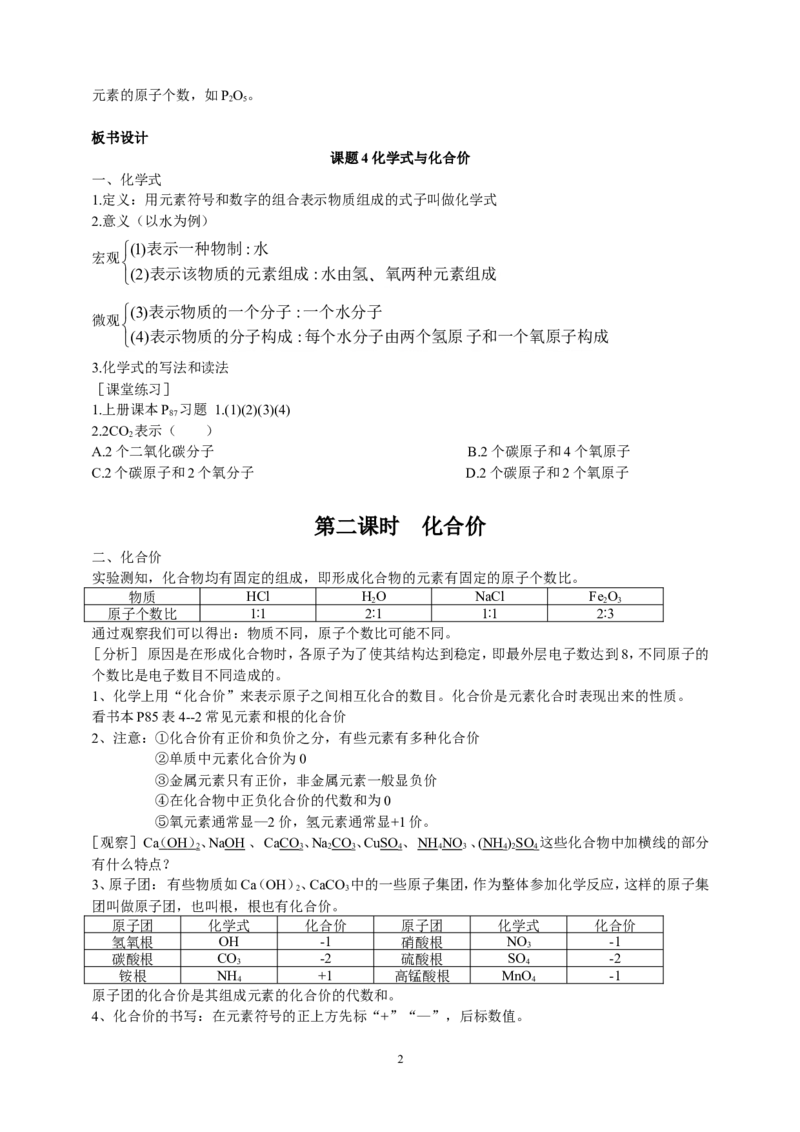
5[例1] 硝酸铵样品中含有杂质10%(杂质中不含氮元素),求样品中氮元素的质量分数。
解:先求出纯净的硝酸铵中氮的质量分数为:
w(N)= 2A r (N) ×100%= 214 ×100%=35%
M (NH NO ) 80
r 4 3
设不纯的硝酸铵中氮元素的质量分数为x,则有如下关系:
100% 35%
,x=31.5%
90% x
[例2] 某不纯的尿素〔CO(NH) 〕中氮元素的质量分数为 42.4% ,求这种尿素中杂质(不含氮元素)
2 2
的质量分数。
解:尿素的相对分子质量=12+16+(14+2×1)×2=60
尿素中氮元素的质量分数w(N)= 2A r (N) ×100%= 214 ×100%=46.7%
M (CO(NH ) ) 60
r 2 2
设不纯的尿素中含尿素的质量分数为x,则有如下的关系:
100% 46.7
,x=90.8%
x 42.4
所以该尿素中所含杂质的质量分数是w(杂)=1-90.8%=9.2%
[课堂练习]
1.计算下列相对分子质量。
HSO __________ 98__________________ 2Ca(OH) __________148________________
2 4 2
2.计算NH HCO 中N、H、C、O四种元素的质量比。 (14∶5∶12∶48)
4 3
3.计算12.25 g KClO 中含有氧元素的质量。(4.8 g)
3
4.计算120 g NH NO 中含N元素的质量与多少克CO(NH) 中所含N元素的质量相等?(90 g)
4 3 2 2
布置作业
1.上册课本P 习题7、8、9、10
87
2.锌是人体健康必需的元素,锌缺乏容易造成发育障碍,易患异食癖等病症,使人体免疫功能低下。市
售的葡萄糖酸锌口服液对治疗锌缺乏症具有较好的疗效。下图是某品牌葡萄糖酸锌口服液的标签,请
根据标签信息回答:
××牌口服液
主要成分:葡萄糖酸锌
化学式:C H O Zn
12 22 14
含锌量:每支口服液含锌6.5 mg
××制药厂
(1)葡萄糖酸锌的相对分子质量为_____455____________;
(2)葡萄糖酸锌中锌元素的质量分数为_____14.3%________。(精确到0.1%)
3.蛋白质在人体胃肠内与水反应,最终生成氨基酸被人体吸收。丙氨酸(化学式为C HON)就是其中的
3 7 2
一种。请回答下列问题:
(1)丙氨酸分子中C、H、O、N原子个数比为___3∶7∶2∶1__________。
(2)丙氨酸的相对分子质量是___89__,氮元素的质量分数为___15.7%__(计算结果精确到0.1%)。
(3)合格奶粉每100 g中含蛋白质约18 g,蛋白质中氮元素的平均质量分数为16%。现测定某奶粉每
100 g中含有氮元素的质量为2 g。请通过计算判断该奶粉是否属于合格奶粉。{ (3)氮元素的质量:18
g×16%=2.88 g>2 g,不合格奶粉(或蛋白质的质量:2 g÷16%=12.5 g<18 g,不合格奶粉)}
教学反思
本节课是学生学习化学以来第一次进行计算,学生比较好奇。教学过程中都是呈现比较简单的练习
题。通过简单运算了解了化学物质组成的特点,知道了物质组成中元素之间有一定的比例关系。学生学习
热情较高,掌握得也比较好,达到了教学目标的要求。
6