文档内容
一、选择题(本大题共10小题,每小题2分,共20分,在四个选项中只有一项符合题意)
1.下列属于化学变化的是( )
A.西瓜榨汁 B.给球打气 C.蜡烛燃烧 D.电灯发光
【答案】C
考点:化学变化和物理变化的判别
2.下列实验操作正确的是( )
A.熄灭酒精灯 B.量筒的读数 C.加热液体 D.用高锰酸钾制氧气
【答案】B
考点:加热器皿-酒精灯;测量容器-量筒;给试管里的液体加热;氧气的制取装置
3.下列空气的组成物质中属于氧化物的是( )
A.氮气 B.氧气 C.二氧化碳 D.稀有气体
【答案】C考点:从组成上识别氧化物
4.电热水袋中的水加热后袋子膨胀,是因为袋内的水( )
A.分子体积增大 B.分子质量增大 C.分子个数增多 D.分子间隔增大
【答案】D
考点:利用分子与原子的性质分析和解决问题
5.下列有关溶液的说法错误的是( )
A.溶液一定是无色透明的
B.溶液由溶质和溶剂组成
C.溶质可以是固体、液体和气体
D.稀溶液也可能是饱和溶液
【答案】A
考点:溶液的概念、组成及其特点;浓溶液、稀溶液跟饱和溶液、不饱和溶液的关系6.下列有关资源、能源的叙述正确的是( )
A.太阳能、核能、风能属于化石能源
B.目前氢能没有广泛推广的主要原因是淡水资源缺乏
C.使用清洁能源不能减少PM
2.5
D.海底蕴藏着丰富的资源,如“可燃冰”等
【答案】D
考点:化石燃料及其综合利用;防治空气污染的措施;海洋中的资源;氢气的用途和氢能的优缺点
7.人体结石有多种,其中一种含有较多的草酸钙(CaC O),CaC O 中碳元素的化合价是( )
2 4 2 4
A.+1 B.+2 C.+3 D.+4
【答案】C
考点:有关元素化合价的计算
8.某反应的微观示意图如图(一种小球代表一种元素的原子),下列说法错误的是( )
A.该反应是置换反应
B.该反应的本质是原子的重新组合
C.该反应前后分子的种类改变
D.该反应中的生成物都是化合物
【答案】A考点:微粒观点及模型图的应用;单质和化合物的判别;化学反应的实质;反应类型的判定
9.关于质量守恒定律的理解,错误的是( )
A.宏观:实际参加反应的反应物总质量等于生成物总质量
B.微观:反应前后原子种类和个数不变
C.X+3HO=2HPO 中的X为PO
2 3 4 2 5
D.煤燃烧后灰渣质量小于煤,不能用质量守恒定律解释
【答案】D
考点:质量守恒定律及其应用
10.认真分析测定相对原子质量的示意图,推断A原子的相对原子质量约为( )
A.12 B.16 C.5 D.10【答案】B
考点:相对原子质量的概念及其计算方法
二、填空题(本大题共5小题,15题(2)小题1分,其余每空1分,共16分)
11.写出化学用语所表示的意义或用化学用语填空.
(1)Cl﹣ ;
(2)两个铁原子 ;
(3)人体中含量较高的金属元素 .
【答案】氯离子;2Fe;Ca
考点:化学符号及其周围数字的意义
12.如图是元素周期表的一部分,请按要求填空.
(1)由表中空格处元素组成的单质在空气中燃烧的化学方程式是 .
(2)表中不同元素最本质的区别是 (填字母).
A.各元素原子的质子数不同 B.各元素原子的中子数不同 C.各元素相对原子质量不同(3)钠元素原子的结构示意图为 ,该原子在化学反应中易 (填“得到”或“失去”)电子,
元素的化学性质主要由其原子的 决定.
(4)化学反应总是伴随着能量变化,锂是制作手机电池的原料,手机通话时电池中贮存的化学能转化为
.
【答案】(1)2Mg+O 2MgO;(2)A;(3)失去;最外层电子数;(4)电能
2
考点:元素周期表的特点及其应用;核外电子在化学反应中的作用;原子结构示意图与离子结构示意图;
物质发生化学变化时的能量变化;书写化学方程式、文字表达式、电离方程式
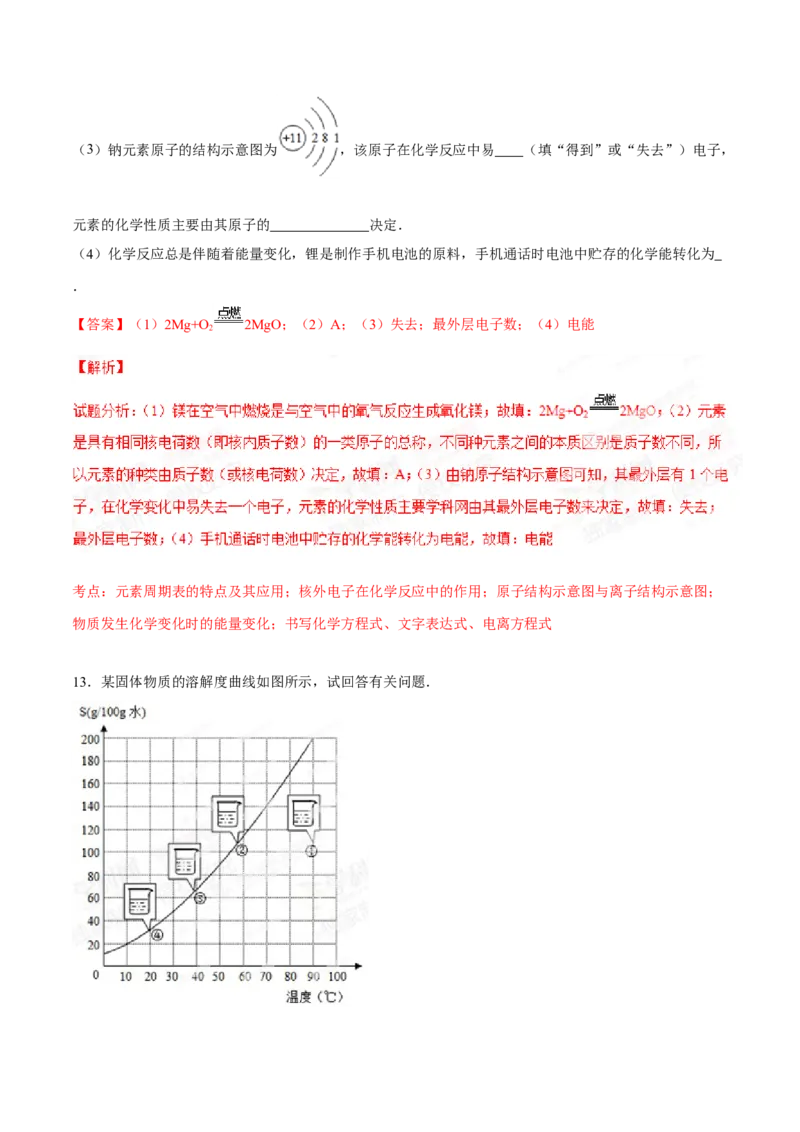
13.某固体物质的溶解度曲线如图所示,试回答有关问题.(1)估计90℃下该固体的溶解度为 克.
(2)②点可表示将①点溶液降温到约 ℃,溶液刚好达到饱和状态.
(3)③点可表示将②点溶液降温到40℃左右,有 析出.
(4)③点溶液中溶质的质量分数 (填“大于”或“小于”或“等于”④点溶液中溶质的质量分
数.
【答案】(1)190;(2)60;(3)固体;(4)大于
考点:固体溶解度曲线及其作用;晶体和结晶的概念与现象;溶质的质量分数
14.过氧乙酸与过氧化氢化学性质有相似之处.为了预防禽流感的发生,养殖人员常用15%的过氧乙酸溶
液给鸡、鸭舍进行消毒.过氧乙酸的化学式为CHCOOOH.完成下列空白:
3
(1)过氧乙酸由 元素组成.
(2)过氧乙酸中碳元素和氢元素的质量比为 .
【答案】(1)碳、氢、氧;(2)6:1
【解析】
试题分析:(1)由过氧乙酸的化学式为CHCOOOH,则该物质是由碳、氢、氧三种元素组成,故填:碳、
3
氢、氧;(2)过氧乙酸中碳、氢、氧三种元素的质量比为C:H:O=(12×2):(1×4)=6:1;故填:
6:1
考点:化学式的书写及意义;元素质量比的计算
15.认真分析示意图并填空:(1)如图1所示,将一个用导热性能良好的粗金属丝(如铜丝或铝丝)绕成的线圈罩在一支蜡烛的火焰上,
火焰会熄灭.用燃烧的条件解释此现象 .
(2)根据中和反应的实质,结合图2补充完成式子:H++ = .这种用实际参加反应的离子来表示化
学反应的式子,叫离子方程式.它也属于国际通用的化学语言.
【答案】(1)冷的金属丝快速吸热,使温度降到了蜡烛的着火点以下;(2)OH﹣;HO
2
考点:燃烧与燃烧的条件;中和反应及其应用
三、实验与探究(本大题共2小题,每空1分,共15分)
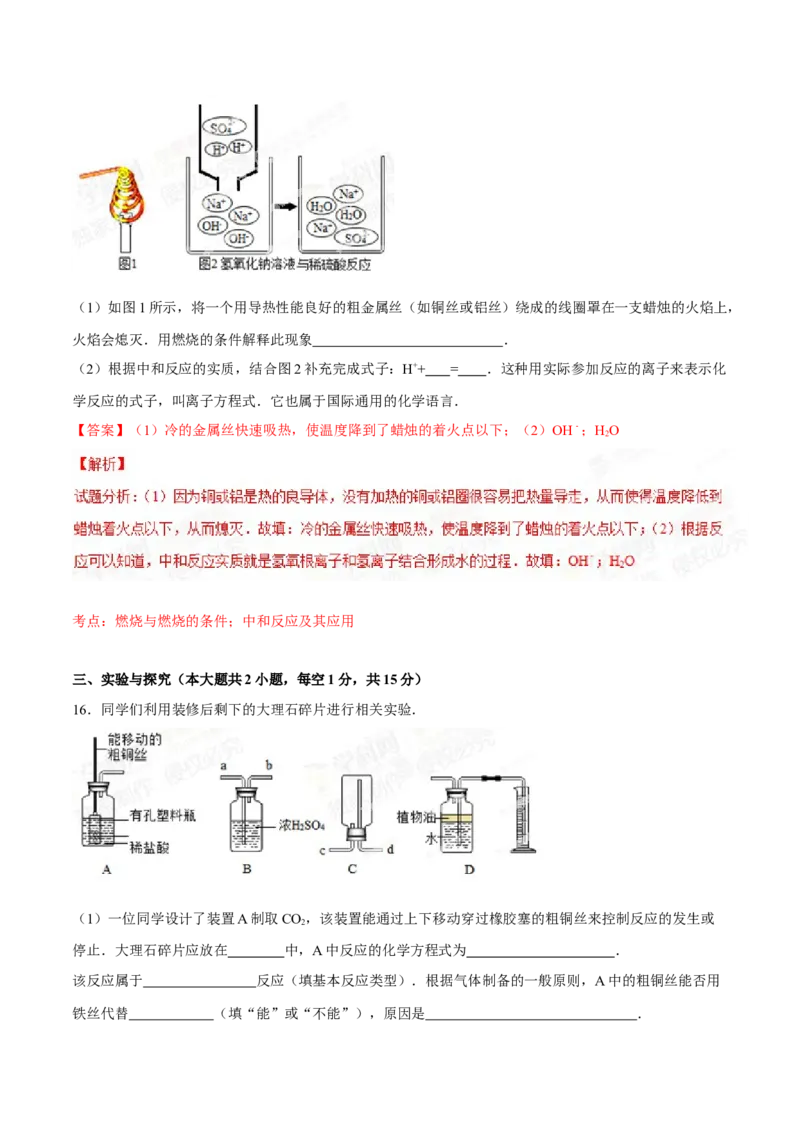
16.同学们利用装修后剩下的大理石碎片进行相关实验.
(1)一位同学设计了装置A制取CO,该装置能通过上下移动穿过橡胶塞的粗铜丝来控制反应的发生或
2
停止.大理石碎片应放在 中,A中反应的化学方程式为 .
该反应属于 反应(填基本反应类型).根据气体制备的一般原则,A中的粗铜丝能否用
铁丝代替 (填“能”或“不能”),原因是 .(2)浓HSO 具有强烈的吸水性,可作为干燥剂除去某些气体中的水份.如用装置B干燥CO,则CO 应
2 4 2 2
从 (填字母)端口通入.
(3)如用装置C收集CO,则CO 应从 (填字母)端口通入.
2 2
(4)装置D用于通入CO 将水压入量筒中以测量CO 的体积,植物油的作用是 .
2 2
【答案】(1)有孔塑料袋;CaCO +2HCl═CaCl +H O+CO↑;复分解;不能;铁能和稀盐酸反应生成氯化
3 2 2 2
亚铁和氢气;(2)a;(3)c;(4)防止二氧化碳溶于水
考点:二氧化碳的实验室制法;量气装置;浓硫酸的性质及浓硫酸的稀释;金属的化学性质;反应类型的
判定;书写化学方程式、文字表达式、电离方程式
17.王林同学对一位高中同学说的“盐溶液不一定显中性”的观点产生了强烈的质疑,同时为了给农民做
技术指导,于是利用所学知识对碳酸钾(KCO)、氯化铵(NH Cl)两种化肥的相关性质进行探究,请你
2 3 4
帮助他补充“①②③④⑤⑥⑦”处的内容,以完成实验报告:【结论与运用】
取下列物质分别于KCO 和NH Cl溶液混合,根据实验现象不能将二者鉴别开的是 (填字母).
2 3 4
A.稀HCl B.水 C.CaCl 溶液 D.酚酞溶液
2
KCO 与NH Cl两种化肥 (填“能”或“不能”)混用,理由是 .
2 3 4
【答案】(从上到下)碱;酸;有气泡产生;有气泡产生且有刺激性气味;【结论与运用】B;不能;碳
酸钾溶液呈碱性,与硫酸铵混合施用,产生NH ,降低肥效
3
【解析】试题分析:【实验探究】:②碳酸钾与纯碱具有相似的化学性质,呈碱性,使石蕊试液变蓝,氯化铵呈酸
性使石蕊试液变红,碳酸钾与硫酸反应生成硫酸钾、水和二氧化碳,氢氧化钠和氯化铵反应生成氯化钠、氨气和水,所以
【结论与运用】A、碳酸钾和盐酸反应会生成二氧化碳,故A正确;B、水不会与碳酸钾、氯化铵反应,
故B错误;C、氯化钙会与碳酸钾反应生成碳酸钙沉淀,故C正确;D、无色酚酞遇碱性物质碳酸钾变红,
遇酸性的氯化铵不显色,故D正确;故选:B;铵态氮肥和显碱性物质混合能生成氨气,从而降低肥效.故答案为:
【结论与运用】B;不能,碳酸钾溶液呈碱性,与硫酸铵混合施用,产生NH ,降低肥效.
3
考点:实验探究物质的性质或变化规律;盐的化学性质
四、化学与社会发展(本大题共1小题,每空1分,共4分)
18.(1)2006年公布的“中国居民营养与健康状况调查”结果显示,中国儿童的钙摄入量仅为标准的,
青少年贫血问题普遍,营养不良与超重肥胖同时存在.下列认识错误的是 (填字母).
A.贫血与人体摄入和吸收铁元素不足有关 B.应根据实际情况多样化地选择食物
C.白开水没有营养,建议多喝饮料
(2)下列是制取CuSO 的两种流程,按照绿色化学的理念,你认为合理的是 (填字母).
4
A.Cu CuSO (友情提示:Cu+2H SO (浓) CuSO +SO↑+2H O)
4 2 4 4 2 2
光 点燃 点燃 浓硫酸 Δ H+ Cu 170℃ O hυ 催化剂
——→ ——→ ———→ ————→ ————→ ——→ ——→ ————→ ———2—→ ————→ ————→
Δ Δ 浓硫B酸.Cu CuO CuSO
4
(3)下列关于有机物的认识正确的是 (填字母).
A.一个有机物分子中可以有一个或多个碳原子 B.有机物只含有碳、氢、氧三种元素
C.分子中含有碳原子的化合物一定是有机物(4)随着经济社会的发展,人们使用的各类电池越来越多,针对我国现状,请你对废旧电池的处理提出
一条合理化建议: .
【答案】(1)C;(2)B;(3)A;(4)实行垃圾分类
【解析】
考点:人体的元素组成与元素对人体健康的重要作用;绿色化学;有机物的特征、分类及聚合物的特性;
物质的相互转化和制备;生命活动与六大营养素;常见污染物的来源、危害及治理
五、计算题(本大题共1小题,共5分)
19.通常认为CO 是引起温室效应的主要气体,但它也是一种重要的资源,关键是人类要采取适当技术对
2
其进行利用,变废为宝.生产车用甲醇汽油中甲醇(CHO)的反应之一为:CO+3H =CH O+HO.如按此
4 2 2 4 2
反应,消耗88吨CO,可生产多少吨甲醇?
2
【答案】64吨考点:根据化学反应方程式的计算高考一轮复习微课视频手机观看地址:
http://xkw.so/wksp