文档内容
一、选择题
1.物质世界充满着变化,下列生活中的变化属于化学变化的是( )
A.食品解冻 B.拉面条 C.鲜奶变酸 D.苹果削皮
【答案】C
【解析】
考点:化学变化和物理变化的判别
2.化学使生活变得更美好,下列做法不可行的是( )
A.为了卫生常用一次性筷子 B.用食醋清除保温瓶中的水垢
C.服用小苏打治疗胃酸过多 D.利用洗涤精清洗餐具上的油污
【答案】A
【解析】
试题分析:A、常用一次性筷子会增加树木的砍伐,不利用保护环境,错误,B、水垢的主要成分是碳酸钙,
能与酸反应,故可用食醋清除保温瓶中的水垢,正确,C、小苏打:碳酸氢钠能与酸反应,不服用小苏打
治疗胃酸过多,正确,D、洗涤精具有乳化功能,可利用洗涤精清洗餐具上的油污,正确,故选A
考点:化学与生活
3.下列实验基本操作正确的是( C )
【答案】C
【解析】
试题分析:A、托盘天平应遵守“左物右码”的原则,错误,B、稀释浓硫酸时:应把浓硫酸沿烧杯壁慢慢
注入水里,并不断搅动使产生的热量迅速扩散,切不可把水直接倒入浓硫酸中,错误,C、进行蒸发操作时,应用玻璃棒搅拌,防止局部受热而导致液体飞溅,正确,D、滴加液体时,滴管应悬空垂直放在试管
口上方,以免污染滴管,滴管管口不能伸入受滴容器(防止滴管沾上其他试剂),错误,故选C.
考点:基本实验操作
4.下列做法不正确的是( )
A.绿色出行,提倡低碳生活 B.鸡饲料中添加抗生素使鸡快速生长
C.燃气泄漏,关闭阀门,开窗通风 D.合理使用化肥,提高粮食产量
【答案】B
【解析】
试题分析:A、绿色出行,提倡低碳生活,可以保护环境,正确,B、鸡饲料中添加抗生素使鸡快速生长,
在鸡肉中会残留,进而对人身体健康产生影响,错误,C、燃气泄漏,关闭阀门,开窗通风,以防止中毒
甚至爆炸,正确,D、合理使用化肥,提高粮食产量,可以防止水污染,正确,故选B
考点:化学与生活、环境
5.下列物质与对应用途不合理的是( )
A.熟石灰——改良酸性土壤 B.石墨——制电极
C.稀硫酸——金属除锈 D.氧气——做燃料
【答案】B
【解析】
考点:常见的性质及用途
6.下列物质按混合物、氧化物、单质顺序进行分类的是( )
A.生理盐水 干冰 臭氧 B.石灰石 熟石灰 金刚石
C.冰水共存物 铁锈 氮气 D.空气 五氧化二磷 生铁
【答案】A
【解析】
试题分析:混合物由多种物质组成,如:空气、自然界的水、溶液等,纯净物分为单质和化合物,单质:
由同种元素组成的纯净物;氧化物:由两种元素组成,其中一种是氧元素的化合物。A、正确,B、石灰石
是混合物,熟石灰是碱,金刚石是单质,错误,C、冰水共存物是氧化物,铁锈的主要成分是氧化铁,是
混合物,氮气是单质,错误,D、空气是混合物,五氧化二磷是氧化物,生铁是合金,是混合物,错误,故选A
考点:物质的分类
7.化学用语是最简单的国际通用语言。下列化学用语表示正确的是( )
A.两个氢原子——H B.氧化铁——FeO
2
C.两个铵根离子——2NH + D.正二价的铜元素——Cu2+
4
【答案】C
【解析】
考点:化学用语的书写
8.2010年12月,由瑞典皇家工学院物理化学教授托尔·布林克和同事在氮的氧化物中发现一种可替代目前
火箭燃料的新物质三硝基胺[N(NO)]。N(NO) 有关说法错误的是( )
2 3 2 3
A.N(NO) 是由氮、氧两种元素组成 B.N(NO) 中氮、氧元素质量比为2:3
2 3 2 3
C.N(NO) 的相对分子质量152 D.N(NO) 中氮元素的质量分数约为36.8%
2 3 2 3
【答案】B
【解析】
试题分析:A、物质由元素组成,N(NO) 是由氮、氧两种元素组成,正确,B、N(NO) 中氮、氧元素原子
2 3 2 3
个数比为2:3,而不是元素的质量比,错误,C、N(NO) 的相对分子质14×4+16×6=152,正确,D、根据元
2 3
素质量分数计算的表达式,N(NO) 中氮元素的质量分数约为36.8%,正确,故选B
2 3
考点:物质的宏观组成,根据化学式进行的计算
9.分类归纳是学习化学的重要方法之一。下列是小李整理的一些化学规律,其中 错误的是( )
【答案】D
【解析】
试题分析:A、根据金属活动性顺序表判断,正确,B、根据元素化合价的一般规律:在化合物中,正负化
合价的代数和为0,在NaCl中Na的化合价为+1,Cl的化合价为-1;Cl 单质中元素化合价为0;在HClO中
2Na的化合价为+1,O的化合价为-2,故Cl的化合价为+1;在ClO 中O的化合价为-2,Cl的化合价为+4;
2
氯元素的化合价由低到高,正确,C、H的原子序数为1,O的原子序数为,8,Ne的原子序数为10,Mg的
原子序数为24,正确,D、烧杯不能直接加热,应垫上石棉网,错误,故选D.
考点:金属活动性顺序,元素化合价的一般规律,元素的原子序数,常见仪器的使用注意事项
10.在“宏观——微观——符号”之间建立联系,是化学学科特有的思维方式。下图是某反应的微观示意
图,下列说法正确的是( )
A.该反应中有四种化合物 B.参加反应的甲、乙分子个数比为1:3
C.该反应属于置换反应 D.参加反应的甲、乙物质的质量比为28:32
【答案】B
【解析】
考点:物质的微观构成,化学反应基本类型,化学方程式的意义
二、填空题
11.化学就在我们身边。通过一年的学习,我有了许多收获:
(1)我认识了许多化学之最(用化学用语回答)
①空气中含量最多的气体单质是_______________
②最简单的有机物____________________
③地壳中含量最高的金属元素___________________
(2)我知道了许多鉴别物质的方法
①我会用________鉴别软水和硬水
②我会用____________鉴别二氧化碳和一氧化碳
③我会用______________法来鉴别合成纤维制品和羊毛制品
【答案】(1)①N ②CH ③Al (2)①肥皂水 ②澄清石灰水 ③灼烧
2 4【解析】
考点:空气的成分,有机物, 地壳中元素的含量,物质的鉴别
12.元素周期表是学习和研究化学的重要工具。回答下列问题:
(1)元素周期表中不同元素的本质区别是____________(填序号)
A.质子数不同 B.电子数不同 C.中子数不同 D.相对原子质量不同
(2)元素周期表中有关硫元素的信息如下图所示,下列说法正确的是_______(填序号)
A.硫属于金属元素
B.硫的相对原子质量是32.06g
C.硫的原子序数是16
(3)根据下列粒子结构示意图,回答问题。
①B与C形成化合物的化学式为_________________。
②化学性质相似的是________(填序号)
【答案】(1)A (2)C (3)①NaCl ②AD
【解析】考点:元素的概念,分类,元素最外层电子数与元素性质的关系
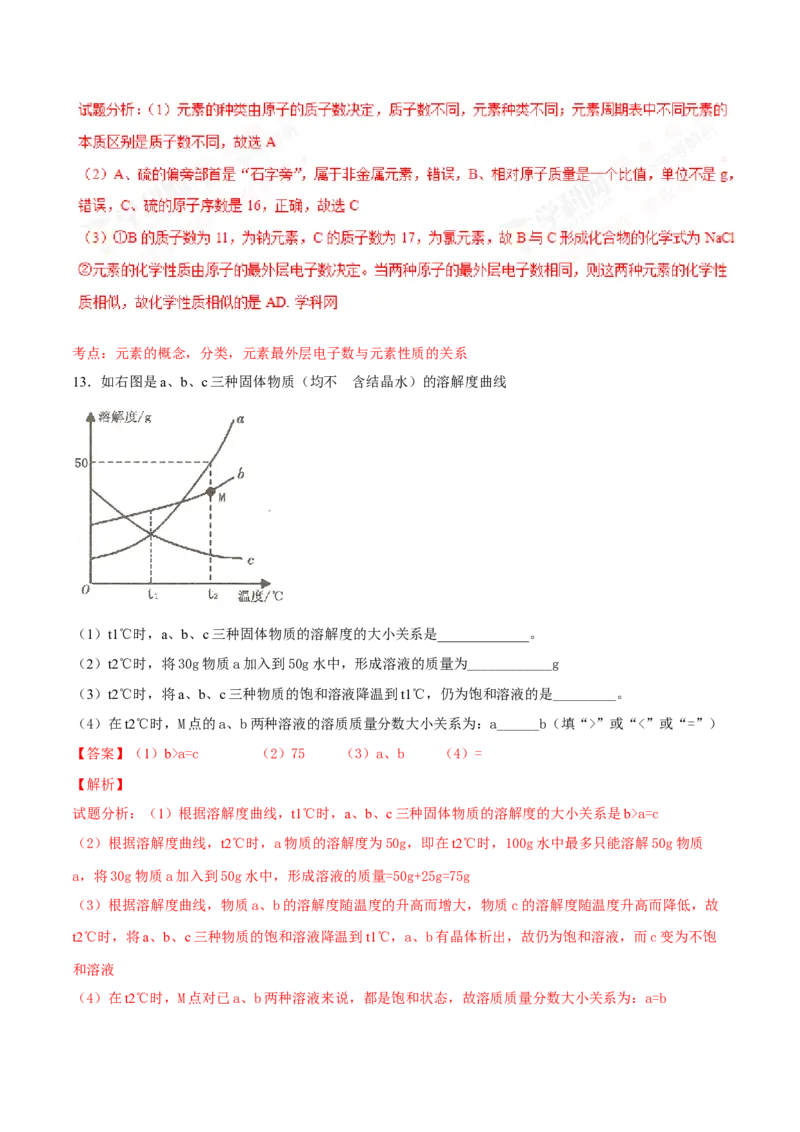
13.如右图是a、b、c三种固体物质(均不 含结晶水)的溶解度曲线
(1)t1℃时,a、b、c三种固体物质的溶解度的大小关系是_____________。
(2)t2℃时,将30g物质a加入到50g水中,形成溶液的质量为____________g
(3)t2℃时,将a、b、c三种物质的饱和溶液降温到t1℃,仍为饱和溶液的是_________。
(4)在t2℃时,M点的a、b两种溶液的溶质质量分数大小关系为:a______b(填“>”或“<”或“=”)
【答案】(1)b>a=c (2)75 (3)a、b (4)=
【解析】
试题分析:(1)根据溶解度曲线,t1℃时,a、b、c三种固体物质的溶解度的大小关系是b>a=c
(2)根据溶解度曲线,t2℃时,a物质的溶解度为50g,即在t2℃时,100g水中最多只能溶解50g物质
a,将30g物质a加入到50g水中,形成溶液的质量=50g+25g=75g
(3)根据溶解度曲线,物质a、b的溶解度随温度的升高而增大,物质c的溶解度随温度升高而降低,故
t2℃时,将a、b、c三种物质的饱和溶液降温到t1℃,a、b有晶体析出,故仍为饱和溶液,而c变为不饱
和溶液
(4)在t2℃时,M点对已a、b两种溶液来说,都是饱和状态,故溶质质量分数大小关系为:a=b考点:溶解度曲线的意义,溶解度的理解,溶质质量分数的计算
14.化学式一把“双刃剑”,有益也有弊。请从利与弊两个方面举例说明二氧化碳与人类生活的关系(各
答一列即可)
利:_________________________________________________________
弊:________________________________________________________
【答案】利:用于灭火等 弊:空气中的二氧化碳含量增加,会加剧温室效应
【解析】
考点:二氧化碳的利与弊
三、实验探究题
15.某同学设计了如图A—F气体制取与性质的组合装置。打开活塞K,很快看到F装置中蜡烛由下至上依
次熄灭。请根据下图回答问题
(1)仪器①的名称为:___________
(2)小华用G装置加热高锰酸钾制取氧气时,发现试管位置过高,他调节试管高度需要操作的旋钮是
_____________
(3)利用A装置制取气体的优点___________________
A装置中发生的化学反应方程式为:______________________
(4)B装置中观察到的现象为:______________________
(5)D装置中发生的化学反应方程式为:______________________-
(6)E装置中观察到石蕊试液变红,用化学反应方程式解释产生该现象的原因:__________
(7)F装置中蜡烛熄灭的原因是:____________________________
【答案】(1)长颈漏斗 (2)③
(3)可时反应随时发生,随时停止 2HO MnO2HO+O↑
2 2 2 2
(4)导管口有气泡冒出,白磷燃烧 (5)CaCO +2HCl=CaCl +HO+CO↑
3 2 2 2
(6)CO+HO=HCO (7)二氧化碳不能燃烧,不能支持燃烧,密度比空气大
2 2 2 3【解析】
试题分析:(1)常见仪器的识记:长颈漏斗
(5)D装置中发生的化学反应方程式为:CaCO +2HCl=CaCl +HO+CO↑
3 2 2 2
(6) E装置中观察到石蕊试液变红的原因是二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊试液变红,化学
反应方程式为:CO+HO=HCO
2 2 2 3
(7) F装置中蜡烛熄灭的原因是:二氧化碳不能燃烧,不能支持燃烧,密度比空气大
考点:常见仪器的识记,化学方程式的书写,燃烧的条件以及二氧化碳的性质探究
16.将一小块银白色的金属钠放置在空气中会发生下列变化:
【提出问题】常温下钠与氧气反应的产物有哪些?
【查阅资料】(1)钠的氧化物有氧化钠(NaO)和过氧化氢(NaO),钠的氧化物都能与水反应其化学
2 2 2
方程式为:NaO+HO=2NaOH 2Na O+2H O=4NaOH+O ↑
2 2 2 2 2 2
(2)CaCl 溶液呈中性
2
【作出猜想】常温下钠与氧气反应的产物可能为:
猜想一:________________;猜想二:NaO;猜想三:NaO 和NaO
2 2 2 2 2
【实验探究一】
实验操作 实验现象 实验结论
取少量上述钠的氧化物,加入适量的蒸馏水 _________________ 猜想一正确
【继续探究】钠在空气中放置较长时间发生反应生成的白色固体
【作出猜想】生成的白色固体可能是:1是NaCO 2是NaCO 和NaOH
2 3 2 3
【实验研究二】
实验操作 实验现象 实验结论
①取少量白色固体配成溶液,加入足量CaCl _____________ 白色固体为NaCO
2 2 3
的溶液 和NaOH
[
②将上述反应后的溶液过滤,取少量滤液滴加 ________________________
【反思拓展】1.也可以用稀盐酸区别NaO 和NaO,NaO 与稀盐酸反应的方程式为:
2 2 2 2 2
2NaO+4HCl=4NaCl+2H O+X↑,X的化学式为________________________
2 2 2
2.实验结束后,废液缸中溶液呈碱性,请你设计一个实验方案处理废液_____________
【答案】猜想一:NaO 【实验探究一】固体溶于水,无气泡冒出
2
【实验研究二】①产生白色沉淀 ②酚酞试液 酚酞试液变红
【反思拓展】1、O 2、加入适量的酸,将pH调为7
2
【解析】
试题分析:根据资料:钠的氧化物有氧化钠(NaO)和过氧化氢(NaO),故猜想一:NaO
2 2 2 2
②将上述反应后的溶液过滤,取少量滤液滴加酚酞试液,现象:酚酞试液变红;说明还含有NaOH
【反思拓展】1、根据质量守恒定律的微观解释:在化学反应前后,原子的种类、数目都不变,结合化学
反应:2NaO+4HCl=4NaCl+2H O+X↑,可以推出化学式为O
2 2 2 2
2、根据中和反应的原理:实验结束后,废液缸中溶液呈碱性,加入适量的酸,将pH调为7.
考点:反应后物质成分的判断,NaCO 和NaOH的化学性质,废液的处理方法
2 3
四、化学与社会发展
17.(1)六盘水市四创主题之一是“创建生活适宜居城市”,下列符合该主题的是( )
A.植树造林、美化城市
B.为解决白色污染,将塑料袋回收利用
C.鼓励使用太阳能热水器
(2)先进的交通工具可以出行更便捷。沪昆高铁是国家铁路交通的重要组成部分,预计2016年年底建成
车,六盘水市将步入“高铁时代”
列车制造离不开下列材料:A.金属材料 B.合成材料 C.复合材料
根据要求选择填空(填序号):
①列车制造中需要大量的钢铁,钢铁属于_________________
②高铁座椅需要用到耐磨、耐腐蚀鹅涤纶等材料,涤纶属于_______________
(3)水是生命之源,万物之基,是人类宝贵的自然资源。我们每个人都要珍惜水、爱护水、节约用水。
请举一例说明生活中你是如何节约用水的:__________________。【答案】(1)A、B、C (2)①A ②B (3)一水多用或用淘米水浇花等
【解析】
考点:化学与环境、材料,爱护水资源
五、计算题
18.小苏打常用作焙制高点的发酵剂。为测定某小苏打样品的纯度,现取样品10g 加热到质量不再减少
(杂质不参加反应),共收集到二氧化碳2.2g,求样品中小苏打的纯度。
提示:碳酸氢钠受热分解的化学方程式:2NaHCO ΔNaCO+HO+CO↑
3 2 3 2 2
【答案】84%
【解析】
试题分析:根据化学方程式:2NaHCO ΔNaCO+HO+CO↑中NaHCO 与CO 的质量关系 ,可先计算出
3 2 3 2 2 3 2
NaHCO 的质量,再计算样品中小苏打的纯度
3
解:设样品中的小苏打碳酸氢钠的质量为x
2NaHCO ΔNaCO+HO+CO↑
3 2 3 2 2
168 44
x 2.2g
168:44=x:2.2g
x=0.84g
样品中小苏打的纯度为: ×100%=84%
考点:根据化学方程式进行计算高考一轮复习微课视频手机观看地址:
http://xkw.so/wksp