文档内容
【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
化学部分
可能用到的相对原子质量:
一、选择题(本题共7个小题,每小题2分,共14分。每小题只有一个选项符合题目要求)。
1. 良好的生态环境是贵州最大的发展优势。下列做法有利于保护生态环境的是
A. 随意开采矿产资源 B. 直接排放工业废气 C. 滥砍乱伐森林树木 D. 分类回收生活垃圾
【答案】D
【解析】
【详解】A、矿产资源属于不可再生资源,随意开采会导致资源枯竭、生态破坏(如山体滑坡、土壤流
失)等,故A错误;
B、工业废气含污染物(如二氧化硫、氮氧化物),直接排放会污染空气,会引发酸雨等环境问题,故B
错误;
C、森林具有保持水土、调节气候的作用,滥伐会导致水土流失、生物多样性减少,故C错误;
D、垃圾分类可提高资源利用率,减少污染,故D正确。
故选D。
2. 下列实验操作中,正确的是
A. 熄灭酒精灯 B. 加固体粉末 C. 加热液体 D. 测溶液酸碱度
【答案】B
【解析】
【详解】A、酒精灯的熄灭方法是用灯帽盖灭,不能用嘴吹灭,故A错误;
B、取用粉末状药品,先将试管横放,用钥匙或纸槽把药品送到试管底部,故B正确;
C、给试管中的液体加热时,液体不能超过试管容积的 ,且试管夹应夹在距管口 处,同时使用酒精灯
火焰的外焰部分加热,试管口向上倾斜,与桌面约成45°,故C错误;
D、用pH试纸测定溶液的pH时,正确的操作方法为在白瓷板或玻璃片上放一小片pH试纸,用玻璃棒蘸
取待测液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,读出pH,不能将pH试纸直接伸入待测
1【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
液,防止污染试剂,故D错误。
故选B。
3. 净化水时,可用活性炭除去水中的色素和异味,利用了活性炭的性质是
A. 熔点高 B. 吸附性 C. 可燃性 D. 导电性
【答案】B
【解析】
【详解】活性炭具有吸附性,能吸附异味和色素,故净化水时放入活性炭除去色素、异味。故选B。
4. 氧化铟( )在触摸屏等设备中被广泛使用。 的物质类别是
A. 酸 B. 碱 C. 盐 D. 氧化物
【答案】D
【解析】
【分析】氧化物是仅含两种元素且其中一种为氧的化合物;
酸是电离时产生的阳离子都是氢离子的化合物;
碱是电离时产生的阴离子都是氢氧根离子的化合物;
盐是由金属离子(或铵根离子)与酸根离子构成的化合物。
【详解】InO 是由In、O两种元素组成的化合物,属于氧化物,故选D。
2 3
5. 合理晒太阳,有利于人体内特定的物质转化为维生素 ,促进身体健康。下列有关维生素
方的说法正确的是
A. 由碳、氢、氧三种元素组成 B. 由72个原子构成
C. 氧元素质量分数最高 D. 一个分子中含有22个氢分子
【答案】A
【解析】
【详解】A、由化学式C H O可知,其是由碳、氢、氧三种元素组成,故A正确;
27 44
B、分子由原子构成,则1个C H O分子中含有27+44+1=72个原子,故B错误;
27 44
C、C H O中碳、氢、氧三种元素质量比为 ,则碳元素的质量分数最
27 44
高,故C错误;
D、分子由原子构成,则1个C H O分子中含有44个氢原子,不含氢分子,故D错误。
27 44
故选A。
2【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
6. 下列实验方案,不能达到实验目的的是
选
实验目的 实验方案
项
A 证明分子之间有间隔 将 水与 酒精混合,观察体积变化
B 验证质量守恒定律 测定铜和氧气反应前后密闭装置的总质量
C 比较高锰酸钾和碘的溶解性 高锰酸钾加入水中,碘加入酒精中,比较溶解质量
D 探究水的组成 电解水,检验是否只生成氢气和氧气
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A、将100mL水与100mL酒精混合后体积小于200mL,说明分子之间存在间隔,故A不符合题
意;
B、铜与氧气在密闭装置中反应生成氧化铜,反应前后总质量不变,符合质量守恒定律,可验证质量守恒
定律,故B不符合题意;
C、比较高锰酸钾和碘的溶解性时,需在相同溶剂中进行。若高锰酸钾溶于水、碘溶于酒精,因溶剂不同,
无法直接比较两者溶解性,故C符合题意;
D、电解水生成氢气和氧气,氢气是由氢元素组成,氧气是由氧元素组成,根据质量守恒定律,说明水由
氢、氧元素组成,可探究水的组成,故D不符合题意。
故选C。
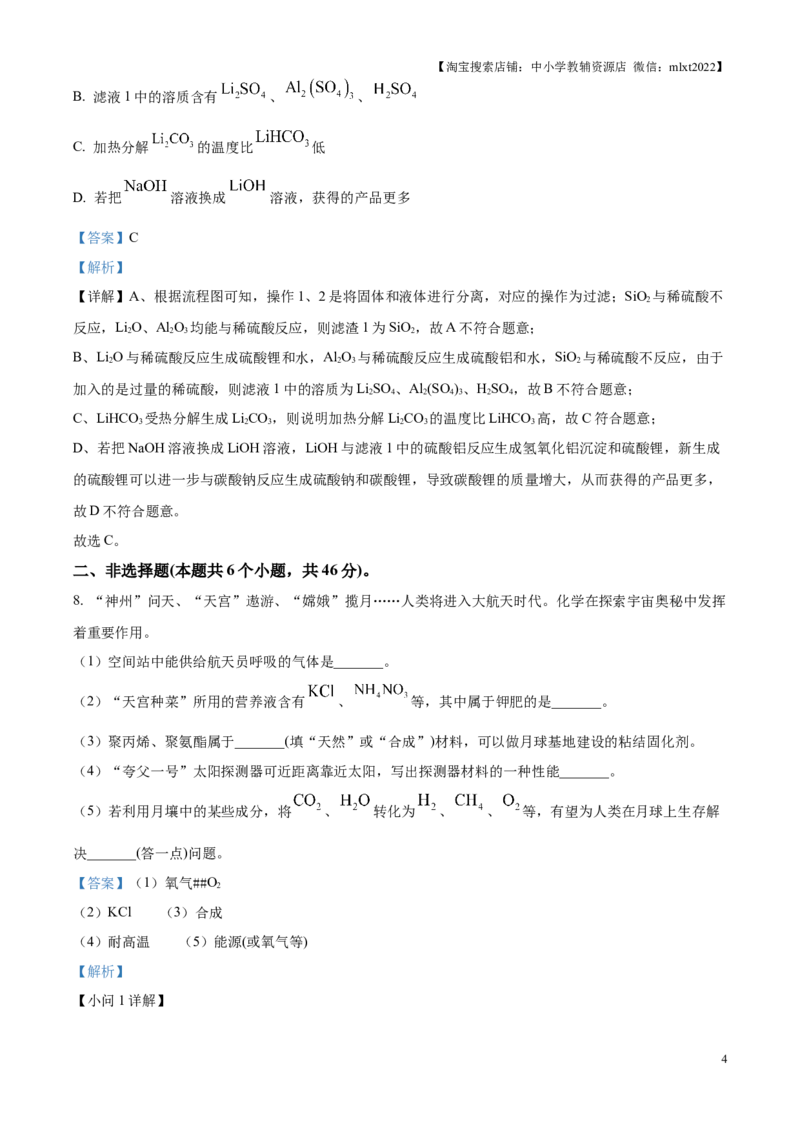
7. 碳酸锂( )是制备新能源汽车电池的重要原料。利用锂辉石(成分为 、 、 )制备
的流程如下:
已知 难溶于水,不与稀 反应; 。下列说法不正确的是
A. 操作1、2是过滤,滤渣1是
3【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
B. 滤液1中的溶质含有 、 、
C. 加热分解 的温度比 低
D. 若把 溶液换成 溶液,获得的产品更多
【答案】C
【解析】
【详解】A、根据流程图可知,操作1、2是将固体和液体进行分离,对应的操作为过滤;SiO 与稀硫酸不
2
反应,LiO、Al O 均能与稀硫酸反应,则滤渣1为SiO,故A不符合题意;
2 2 3 2
B、LiO与稀硫酸反应生成硫酸锂和水,Al O 与稀硫酸反应生成硫酸铝和水,SiO 与稀硫酸不反应,由于
2 2 3 2
加入的是过量的稀硫酸,则滤液1中的溶质为LiSO 、Al (SO )、HSO ,故B不符合题意;
2 4 2 4 3 2 4
C、LiHCO 受热分解生成LiCO,则说明加热分解LiCO 的温度比LiHCO 高,故C符合题意;
3 2 3 2 3 3
D、若把NaOH溶液换成LiOH溶液,LiOH与滤液1中的硫酸铝反应生成氢氧化铝沉淀和硫酸锂,新生成
的硫酸锂可以进一步与碳酸钠反应生成硫酸钠和碳酸锂,导致碳酸锂的质量增大,从而获得的产品更多,
故D不符合题意。
故选C。
二、非选择题(本题共6个小题,共46分)。
8. “神州”问天、“天宫”遨游、“嫦娥”揽月……人类将进入大航天时代。化学在探索宇宙奥秘中发挥
着重要作用。
(1)空间站中能供给航天员呼吸的气体是_______。
(2)“天宫种菜”所用的营养液含有 、 等,其中属于钾肥的是_______。
(3)聚丙烯、聚氨酯属于_______(填“天然”或“合成”)材料,可以做月球基地建设的粘结固化剂。
(4)“夸父一号”太阳探测器可近距离靠近太阳,写出探测器材料的一种性能_______。
(5)若利用月壤中的某些成分,将 、 转化为 、 、 等,有望为人类在月球上生存解
决_______(答一点)问题。
【答案】(1)氧气##O
2
(2)KCl (3)合成
(4)耐高温 (5)能源(或氧气等)
【解析】
【小问1详解】
4【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
氧气能供给呼吸,则空间站中能供给航天员呼吸的气体是氧气,故填:氧气或者O;
2
【小问2详解】
的
KCl中含有氮、磷、钾三种营养元素中 钾元素,属于钾肥;NH NO 中含有氮、磷、钾三种营养元素中
4 3
的氮元素,属于氮肥,故填:KCl;
【小问3详解】
聚丙烯、聚氨酯是人工合成的有机高分子材料,属于合成材料,故填:合成;
【小问4详解】
“夸父一号”太阳探测器可近距离靠近太阳,太阳探测器需承受极高温度,则材料需耐高温、耐辐射等,
故填:耐高温;
【小问5详解】
产物O 可供呼吸,H 和CH 可作为燃料,解决月球生存的氧气或能源需求,故填:能源(或氧气等)。
2 2 4
9. 燃料的使用推动了人类社会的发展。
(1)燃料变迁过程:木柴(热值 )→煤(热值 )→天然气(热值 )。
①木柴的热值比煤_______(填“高”或“低”)。
②为使煤充分燃烧,可采取的一种方法是_______。
③用电火花引燃气态燃料,为燃料燃烧提供的条件是_______。
④从达成“碳中和”的目标分析,用天然气( )替代煤(C)作燃料的理由是_______。
(2)氢气是未来理想的能源。
①2024年6月,我国首次实现利用海上风电电解海水制氢。电解 的水,理论上能得到氢气的质量为
_______ 。
②用单壁碳纳米管可储存氢气如图1,该过程中不变的微观粒子是_____。另一种储氢方式如图2,
与 的质量比是_____(填最简整数比)。
③从不同视角思考,设计一种理想燃料,需要考虑的因素有_______(答两点)。
5【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
【答案】(1) ①. 低 ②. 将煤制成蜂窝煤(合理即可) ③. 使温度达到燃料的着火点 ④.
要得到同样的热量,需要消耗的煤更多,产生的二氧化碳更多
(2) ①. 2 ②. 碳原子和氢原子 ③. 14:15 ④. 热值大、对环境污染小或无污染(合理即
可)
【解析】
【小问1详解】
①根据题干信息可知,木柴的热值比煤低,故填:低;
②为使煤充分燃烧,可采取的方法有将煤制成蜂窝煤(或者磨成煤粉,增大可燃物与空气的接触面积,使
燃烧更成分)、鼓风(增大氧气的含量)等,故填:将煤制成蜂窝煤(合理即可);
③用电火花引燃气态燃料,是为了使温度达到可燃物的着火点,故填:使温度达到燃料的着火点;
④根据题干信息“煤(热值34kJ/g)→天然气(热值55kJ/g)”,则用天然气(CH)替代煤(C)作燃料的理由是要
4
得到同样的热量,需要消耗的煤更多,产生的二氧化碳更多,故填:要得到同样的热量,需要消耗的煤更
多,产生的二氧化碳更多;
【小问2详解】
①根据 可知,水与氢气的质量比为 ,则电解18kg的水,
理论上能得到氢气的质量为 ,故填:2;
②根据质量守恒定律,反应前后原子的种类、个数不变,则该过程中不变的微观粒子是碳原子和氢原子;
结合图2,反应的化学方程式为 ,则 与 的质量比为
,故填:碳原子和氢原子;14:15;
③从不同视角思考,设计一种理想燃料,需要考虑的因素有热值大、对环境污染小或无污染、运输是否安
全和方便等,故填:热值大、对环境污染小或无污染(合理即可)。
10. 自然界氧循环对维持人类生活与生态平衡具有重要意义。
(1)用图1装置制取 和
6【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
①用大理石( )和稀 制取 的化学方程式为_______,收集装置是_______,验满的方法是
_______。
②用B作发生装置产生 ,反应的化学方程式为_______,检验氧气的方法是_______。
(2)探究鱼缸中氧循环
①图2鱼缸中 和含氧量比一周前明显下降。 下降的原因可能是_______(用化学方程式表示)。
②用图3进行实验,测得4小时后a中含氧量为 ,b中含氧量为 。从氧循环的角度分析,
氧含量不同的原因是_______。
③若要恢复鱼缸中的正常氧循环,可以采取的一种做法是_______。
【答案】(1) ①. ②. D ③. 将然着的木条放在集
气瓶口,若木条熄灭,则二氧化碳已收集满 ④. ⑤. 将带火星的木条
伸入集气瓶中,若木条复燃,证明该气体为氧气
(2) ①. ②. 水草经光合作用,将二氧化碳转化为氧气 ③. 补充光照
【解析】
7【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
【小问1详解】
①碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为
;
二氧化碳密度比空气大,能溶于水且与水反应,应采用向上排空气法进行收集,即收集装置选D;
二氧化碳不燃烧也不支持燃烧,则验满的方法为将然着的木条放在集气瓶口,若木条熄灭,则二氧化碳已
收集满;
②B装置适用于固-液常温型,可用于过氧化氢制氧气,过氧化氢在二氧化锰的催化作用下分解生成水和氧
气,反应的化学方程式为 ;
氧气具有助燃性,则检验氧气的方法是将带火星的木条伸入集气瓶中,若木条复燃,证明该气体为氧气;
【小问2详解】
①鱼缸中的鱼呼吸产生二氧化碳,二氧化碳与水反应生成碳酸( ),碳酸显酸性,
会导致鱼缸中水的pH下降;
②水草经光合作用,将二氧化碳转化为氧气,导致a、b中的含氧量不同;
③结合②,若要恢复鱼缸中的正常氧循环,可以补充光照。
11. 氯化钠是维持人的正常生理活动必不可少的物质。高盐饮食与心血管疾病密切相关,科学摄入氯化钠
有益健康。
查阅资料: 在睡液中溶解,钠离子转移到味蕾,使人们感知咸味。 粒径越小,钠离子能越快
转移到味蕾,从而避免 摄入过多。 结晶时,水分蒸发速度越快,晶体粒径越小。
(1)味蕾通过 溶液中的_______离子感知咸味。
(2)减小 晶体的粒径,其溶解速度变化是_______。
(3)提纯 常采用蒸发结晶的方法,当析出晶体时,过滤,滤液是 的_______(填“饱和”或
“不饱和”)溶液。
(4) 时,配制 质量分数为 的 溶液,需要 _______g。
(5)将含有大量 、少量的 和 的固体混合物放入饱和 溶液中,搅拌,过滤,
8【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
能得到纯净的 。解释用该方法提纯 的原因是_______。
(6)按下图实验,拉动注射器,有晶体析出。同温同体积的饱和 溶液在真空下蒸干和自然蒸干,判
断哪一种方式析出的小粒径晶体更多并说明理由_______。
【答案】(1)钠 (2)加快
(3)饱和 (4)16
(5)少量MgCl 和MgSO 固体会溶解在饱和NaCl溶液中,NaCl固体不会再溶解,得到的是纯净的NaCl
2 4
(6)真空蒸干析出小粒径晶体更多,因为真空状态下,系统压强减小,水的沸点降低,蒸发速度更快
【解析】
【小问1详解】
根据题干信息可知,NaCl在睡液中溶解,钠离子转移到味蕾,使人们感知咸味,故填:钠;
【小问2详解】
减小NaCl晶体的粒径,可以是其溶解速度加快,故填:加快;
【小问3详解】
析出固体后的原溶液为该物质的饱和溶液。则提纯NaCl常采用蒸发结晶的方法,当析出晶体时,过滤,
滤液是NaCl的饱和溶液,故填:饱和;
【小问4详解】
20℃时,配制100g质量分数为16%的NaCl溶液,需要NaCl的质量为 ,故填:16;
【小问5详解】
将含有大量NaCl、少量的MgCl 和MgSO 的固体混合物放入饱和NaCl溶液中,少量MgCl 和MgSO 固体
2 4 2 4
会溶解在饱和NaCl溶液中,NaCl固体不会再溶解,从而可以得到的是纯净的NaCl,故填:少量MgCl 和
2
MgSO 固体会溶解在饱和NaCl溶液中,NaCl固体不会再溶解,得到的是纯净的NaCl;
4
【小问6详解】
结合题干信息“NaCl结晶时,水分蒸发速度越快,晶体粒径越小”,真空状态下,系统压强减小,水的沸
点降低,蒸发速度更快,使得晶体粒径越小,故填:真空蒸干析出小粒径晶体更多,因为真空状态下,系
统压强减小,水的沸点降低,蒸发速度更快。
12. 在推进中国式现代化建设的进程中,桥梁是贵州一张亮丽的名片。金属材料在桥梁建造中发挥着重要
作用。
9【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
(1)桥梁的金属材料
①建造桥梁使用的金属材料主要有铁、锌、铝、钢丝、镀锌钢丝、镀锌铝钢丝等。其中属于合金的是
_______(选填一种)。
②将赤铁矿( )、焦炭和石灰石一起加入高炉。在高温下,炉内 和 反应得到 ,反应的化学
方程式为_______。
(2)金属材料的制造
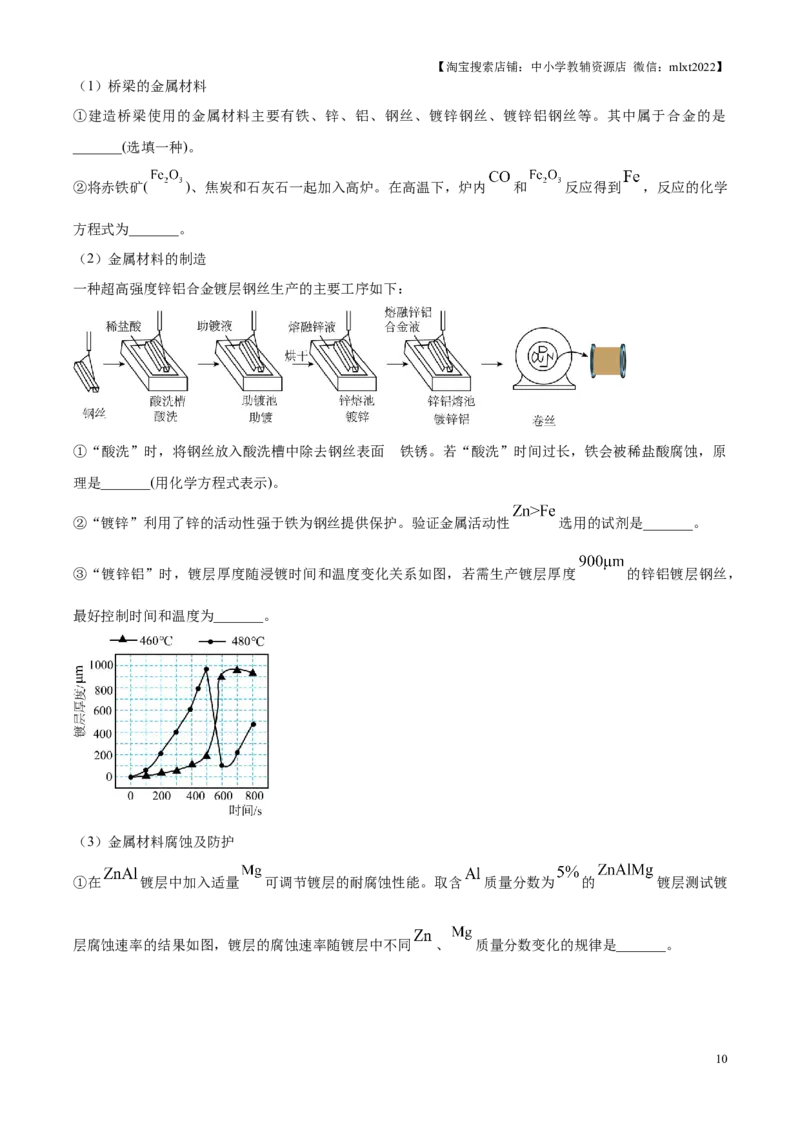
一种超高强度锌铝合金镀层钢丝生产的主要工序如下:
①“酸洗”时,将钢丝放入酸洗槽中除去钢丝表面 铁的锈。若“酸洗”时间过长,铁会被稀盐酸腐蚀,原
理是_______(用化学方程式表示)。
②“镀锌”利用了锌的活动性强于铁为钢丝提供保护。验证金属活动性 选用的试剂是_______。
③“镀锌铝”时,镀层厚度随浸镀时间和温度变化关系如图,若需生产镀层厚度 的锌铝镀层钢丝,
最好控制时间和温度为_______。
(3)金属材料腐蚀及防护
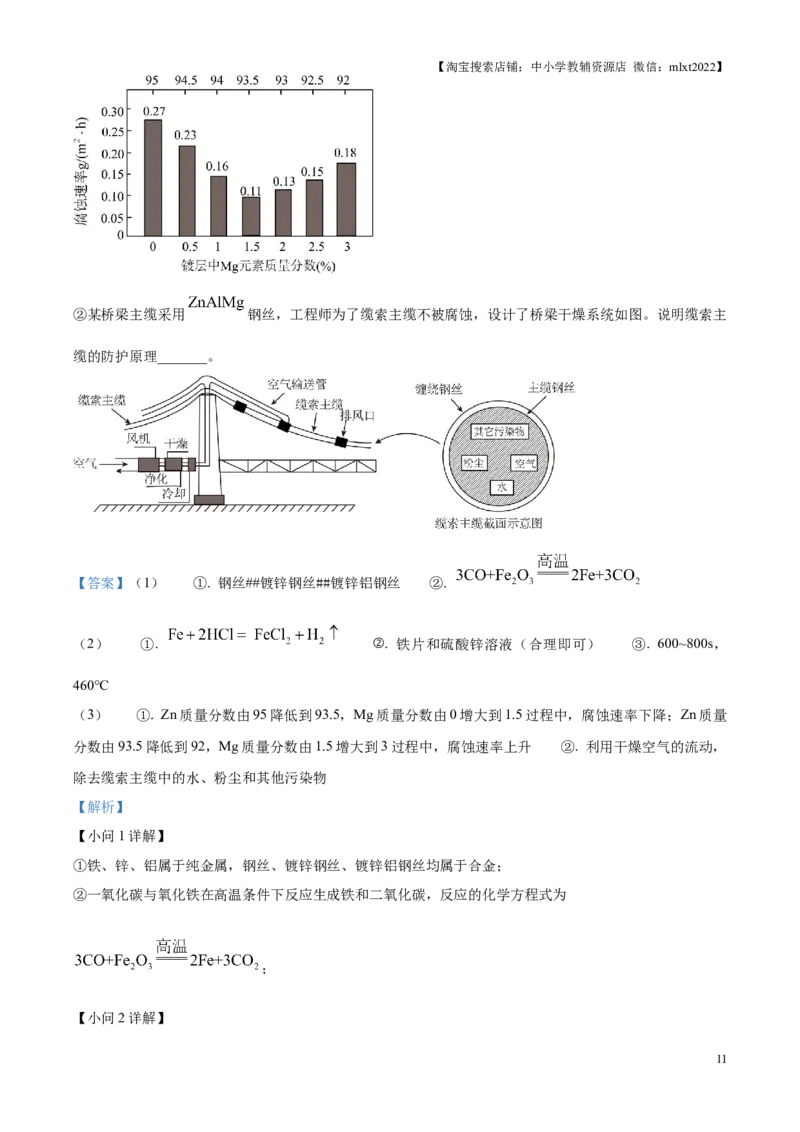
①在 镀层中加入适量 可调节镀层的耐腐蚀性能。取含 质量分数为 的 镀层测试镀
层腐蚀速率的结果如图,镀层的腐蚀速率随镀层中不同 、 质量分数变化的规律是_______。
10【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
②某桥梁主缆采用 钢丝,工程师为了缆索主缆不被腐蚀,设计了桥梁干燥系统如图。说明缆索主
缆的防护原理_______。
【答案】(1) ①. 钢丝##镀锌钢丝##镀锌铝钢丝 ②.
(2) ①. ②. 铁片和硫酸锌溶液(合理即可) ③. 600~800s,
460℃
(3) ①. Zn质量分数由95降低到93.5,Mg质量分数由0增大到1.5过程中,腐蚀速率下降;Zn质量
分数由93.5降低到92,Mg质量分数由1.5增大到3过程中,腐蚀速率上升 ②. 利用干燥空气的流动,
除去缆索主缆中的水、粉尘和其他污染物
【解析】
【小问1详解】
①铁、锌、铝属于纯金属,钢丝、镀锌钢丝、镀锌铝钢丝均属于合金;
②一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳,反应的化学方程式为
;
【小问2详解】
11【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
①若“酸洗”时间过长,铁会被稀盐酸腐蚀,铁与稀盐酸反应生成氯化亚铁和氢气,反应的化学方程式为
;
②活泼金属可以将不活泼金属从其盐溶液中置换出来,则验证金属活动性Zn>Fe,可选用的试剂是铁片和
硫酸锌溶液、锌片和硫酸亚铁溶液等;
③由镀层厚度随浸镀时间和温度变化关系图可知,若需生产镀层厚度900μm的锌铝镀层钢丝,最好控制时
间和温度为600~800s,460℃;
【小问3详解】
①分析图像可知,Zn质量分数由95降低到93.5,Mg质量分数由0增大到1.5过程中,腐蚀速率下降;Zn
质量分数由93.5降低到92,Mg质量分数由1.5增大到3过程中,腐蚀速率上升;
②分析桥梁干燥系统图可知,其是利用干燥空气的流动,除去缆索主缆中的水、粉尘和其他污染物,从而
达到对缆索主缆防护的目的。
13. 在“科普周”活动中,同学们走进某科研机构,了解到光催化转化CO 是一种实现“双碳”目标的途
2
径。在研究员的指导下,参与了光催化转化实验。
任务一:初步了解光催化转化CO
2
研究员介绍:在光照条件下,用某纳米笼作催化剂,可将CO 转化为CO、CH 等多种含碳物质;最新研究
2 4
成果是,向上述纳米笼中添加Cu O形成“纳米笼-Cu O”催化剂,反应后生成的含碳物质中CO接近100%,
2 2
获得的CO可直接用于合成化工产品。
任务二:制备“纳米笼- ”催化剂
(1)路径如下: ,小组同学认为,用 与
制取 ,需检验 是否变质。进行下列实验。
实验现象或方
实验操作 结论
程式
①取样,溶于水,滴加过量稀 现象_______ 已经变质
②取样,溶于水,加入过量 溶液,过 方 程 式 部分变质为
_______
滤,向滤液中加入_______
取提纯的 配制成一定浓度的溶液,依次加入 溶液、维生素C,发生反应生成 。让
12【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
纳米颗粒生长在纳米笼上,得到“纳米笼- ”。(已知 在潮湿的空气中容易发生反应:
)
任务三:深度认识光催化转化CO
2
(2)小组同学了解转化原理参与实验。先向透明玻璃反应容器中通入 ,放入“纳米笼- ”催化剂,
加入 ,再通入 ,排尽 ,反应容器中CO 的质量为 ,密闭光照。一段时间后,检测到只有
2
气体生成,且生成的含碳物质中 接近 。实验后反应容器中混合气体的质量为 。实验过程中
通入 的作用是_______。
小组同学讨论后,根据所学知识对上述实验进行探究。
【探究目的】
上述容器中CO 是否发生反应,且生成的气体中含碳物质是否只有 。
2
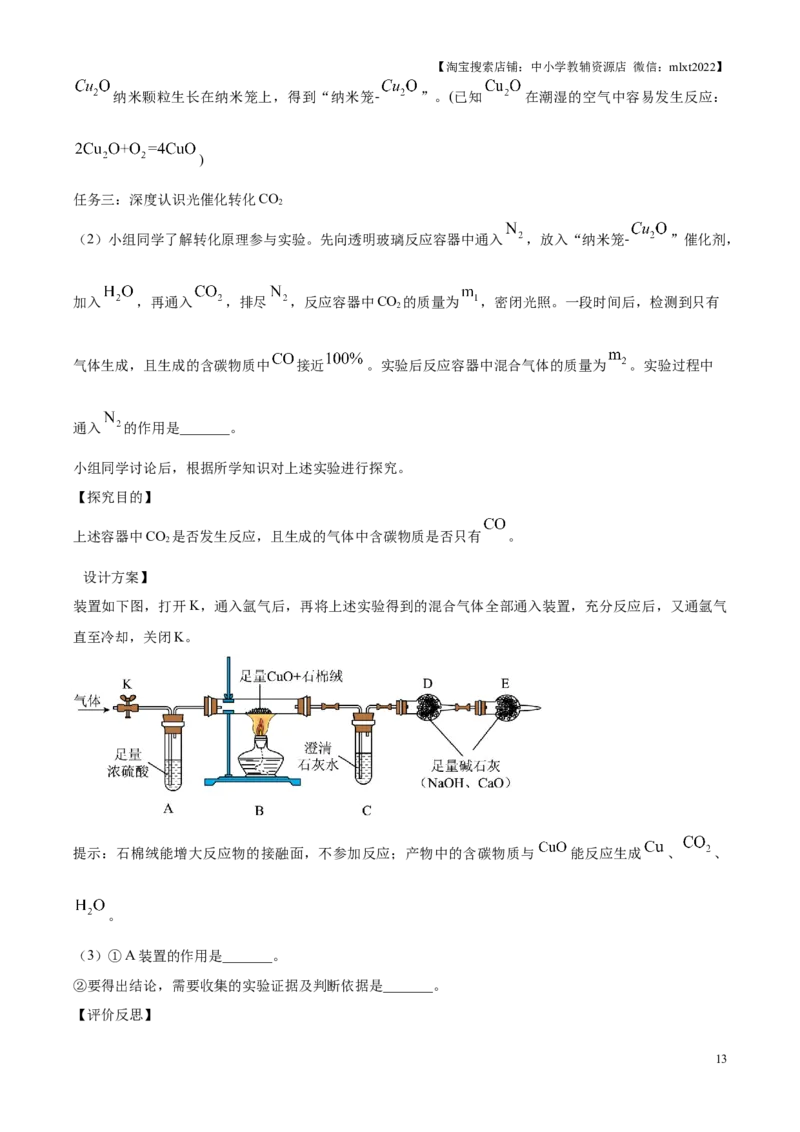
【设计方案】
装置如下图,打开K,通入氩气后,再将上述实验得到的混合气体全部通入装置,充分反应后,又通氩气
直至冷却,关闭K。
提示:石棉绒能增大反应物的接融面,不参加反应;产物中的含碳物质与 能反应生成 、 、
。
(3)①A装置的作用是_______。
②要得出结论,需要收集的实验证据及判断依据是_______。
【评价反思】
13【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
(4)通过上述探究学习,同学们对催化剂调控化学反应的新认识是_______。
(5)同学们讨论认为,从反应条件视角,得出光照条件、“纳米笼- ”作催化剂才能使生成的含碳
物质中 接近 的结论,还需补充的实验是_______。
【答案】(1) ①. 有气泡产生 ②. 酚酞溶液 ③.
(2)排尽装置中的空气,避免Cu O在潮湿环境下与氧气反应生成CuO
2
(3) ①. 吸收混合气体中的水(合理即可) ②. 方法1:收集证据:反应前后A装置质量;判断依据:
若 ,则生成的气体中含碳物质只有CO,若不相等,则生成的气体中含碳物质不
全为CO##方法2:收集证据:反应前后A、C、D装置质量;判断依据:若C、D装置增加的质量等于
,则生成的气体中含碳物质只有CO,若不相等,则生成的气体中含碳物质不全为
CO
(4)通过对催化剂改良(或添加其他物质),可控制生成物的种类
(5)增加对照组,实验条件为“光照、纳米笼作催化剂”(合理即可)
【解析】
【小问1详解】
①氢氧化钠变质是因为能和空气中的二氧化碳反应生成碳酸钠,稀硫酸和碳酸钠反应生成二氧化碳气体,
所以现象是有气泡产生;
②碳酸钠和氯化钡溶液反应生成碳酸钡沉淀和氯化钠,反应的化学方程式为:
;过滤,向滤液中加入酚酞溶液,溶液变红,说明有氢氧化钠,因
此氢氧化钠部分变质;
【
小问2详解】
的
已知 在潮湿 空气中容易发生反应: 。所以实验过程中通入 的作用是:排
尽装置中的空气,避免Cu O在潮湿环境下与氧气反应生成CuO;
2
【小问3详解】
14【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
①浓硫酸具有吸水性,所以A装置的作用是吸收混合气体中的水;
②方法1:通过测定反应前后A装置质量变化,然后利用质量守恒定律可得:
若 ,则生成的气体中含碳物质只有CO,若不相等,则生成的气体中含碳物质不
全为CO;
方法2:通过测定反应前后A、C、D装置质量变化(C、D装置增加的质量为一氧化碳和氧化铜反应生成
二氧化碳的质量),然后利用质量守恒定律可得:
若C、D装置增加的质量等于 ,则生成的气体中含碳物质只有CO,若不相等,则生
成的气体中含碳物质不全为CO;
【小问4详解】
由以上实验探究可知,通过对催化剂改良(或添加其他物质),可控制生成物的种类;
【小问5详解】
光照条件、“纳米笼- ”作催化剂才能使生成的含碳物质中 接近 。而本实验只是探究在密
闭光照、纳米笼- ”催化剂的作用下能使生成的含碳物质中 接近 ,所以需要设计对照实验,
即增加对照组,实验条件为“光照、纳米笼作催化剂”。
15