文档内容
2025—2026学年度第一学期芜湖市高中教学质量监控
高三年级化学试题卷
本试题卷共8页,满分100分,考试用时75分钟
注意事项:
1.答卷前,务必将自己的姓名、学校、考场/座位号、班级、准考证号填写在答题卷上,将条形码
横贴在答题卷右上角“条形码粘贴处”。
2.作答选择题时,选出每小题答案后,用2B铅笔在答题卷上对应题目选项的答案信息点涂黑;
如需改动,用橡皮擦干净后,再选涂其他答案。 答案不能答在试题卷上。
3.非选择题必须用黑色宇述的钢笔或签字笔作答,答案必须写在答题卷各题目指定区域内 ;
如需改动,先划掉原来的答案,然后再写上新答案;不准使用铅笔和涂改液,不按以上要求
作答无效。
4.考生必须保证答题卷的整洁,考试结束后,将试题卷和答题卷一并交回。
可能用到的相对原子质量:H1 C12 N14 016 Cl35.5 Fe56 Zn65 Ga70 Te 128
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题
目要求。
1,化学是一门实用的学科。 下列说法正确的是
A.碳纳米管属于胶体分散系,该材料具有超强的吸附能力
B.“福建舰”海水浸泡区的铝基可保障船体不易腐蚀,利用了牺牲阳极法
C.汽车尾气净化器通常使用贵金属为催化剂,能提高有害气体的平衡转化率
D.“歼-20S”等隐身战机的隐身涂层材料之一为石墨烯,石墨烯是一种有机纤维
2.下列化学用语或表述正确的是
A.
2p.电子云图:
B. 的名称;2-甲基-3-戊烯
C.基态S价电子的轨道表示式:
D.用电子式表示HCI的形成过程:
化学试题卷第 1 页(共8页)3.设N,为阿伏加德罗常数的值,下列说法错误的是
A. 4.6gCH O完全燃烧,转移电子数为1.2N
₄ ₄
B.Na”ClO与H*Cl反应,每产生71gCl₂,转移的电子数小于N₄
C.0.1mol AICl受热熔融时产生的离子数目为0.4N₄
D.含0.2mol H₂SO₁的浓硫酸与足量镁反应,转移的电子数大于0.2N₄
4.下列选项中的物质能按图示路径一步转化,且甲和丙不能直接反应生成乙的是
选项 甲 乙 丙
Na:CO
A NaOH NaHCO
B Fe FeCl₃ FeCl ₃
C HS SO ₃ H SO₂
D AlCl Al ( OH₂ ) |NaIAl₂ (OH₄ )。]
₃ ₂
5.穿 心莲内酯是一种天然抗生素,其结构简式如图,
下列关于穿心莲内酯说法正确的是
A.分子式为C₀HO₃
B.分子中含有5个手性碳原子
C.存在5个C-Oσ键
D.能发生加成反应、消去反应和加聚反应
阅读下列材料,完成下面6-7题。
铁、钴、镍被称为铁系元素,应用广泛。 高铁酸钾(K、FeO₄)是一种环境友好型水处理剂,可先
用Fe(OH);和NaClO在碱性条件下反应生成NaFeO.,再与KOH反应制备。 铁系元素能形成多
种化合物,如(NH)-Fe(SO₁):6H₂O、[Co(NH)]Cl、Ni(CO),等,其中(NHL)₂Fe(SO₁):6HO能溶
于水,具有较强的还原性;[Co(NHb)”很稳定;Ni(CO);常温下为液态,熔点低,易溶于四氯化碳、
苯等有机溶剂 。
6.下列说法正确的是
A.Ni(CO)₂属于极性分子 B.离子半径:(K)>r(Cr)>r(Na¹)
.
C H- N -H的键角:[Co(NH) *> NH D.基态原子未成对电子数:C>N>0
₃ ₀ ₃
7.下列有关反应的离子方程式错误的是
A. 制备N a FeO ::2F e (OH) +3ClO
~
=2FeO ²+3CI+4H'+H O
₂ ₃ ₃ ₂
B. [ Co(NH )]Cl 溶液与少量AgNO 溶液反应 : CI+Ag'=AgC!
₃ ₃ ₃
C.用Cl₂与NaOH溶液制备NaC1O:Cl+20H=CI+C1O~+H₂O
D.(NH₁)₂Fe(SO₃)₂·6H₂O与酸性K₂Cr₂O₇溶液反应:6Fe*+14H'+Cr₂O²~=6Fe”+2Ct”+
7H O
₂
化学试题卷第 2 页(共8页)8.下列溶液中,所给粒子组的共存判断及反应的离子方程式错误的是
选项 溶液 粒子组 粒子共存判断及反应的离子方程式
A 反 Fe 应 和 后 过 的 量 废 稀 液 盐酸 F e” 、 NO ; 、AP 、 SO3- 3 不 F e 能 *+ 大 NO 量 T 共 +2 存 H , O 3Fe²+4H^+NO5=
₃
通入少量SO₂气体 不能大量共存,2ClO +SO +H O=
B K²、Na²、ClO 、SO}- ~
₂ ₂
后的溶液 ~ 2HCIO+SO3-
常温下由水电离
K*、NH ·H O、Cr、
C 出c(H')=1×10² ₃ ₂ 可能大量共存
[AI(OH)。
mol
·
L”的溶液
e c
D 含F ”的溶液 Na°、NHi、 SO3 ~、 r 能大量共存
9.化合物甲是一种重要的化工原料,其结构如图所示,X、Y、Z、W、E是原子序数依次增大的短
周期主族元素,Y是空气中含量最多的元素,XZ是一种常见的溶剂,Z和E同主族。 下列说
法正确的是
A.元素电负性:X
<
WK (A g l)
₉ ₂
0.1 mol·L*KI溶液,有黄色沉淀生成
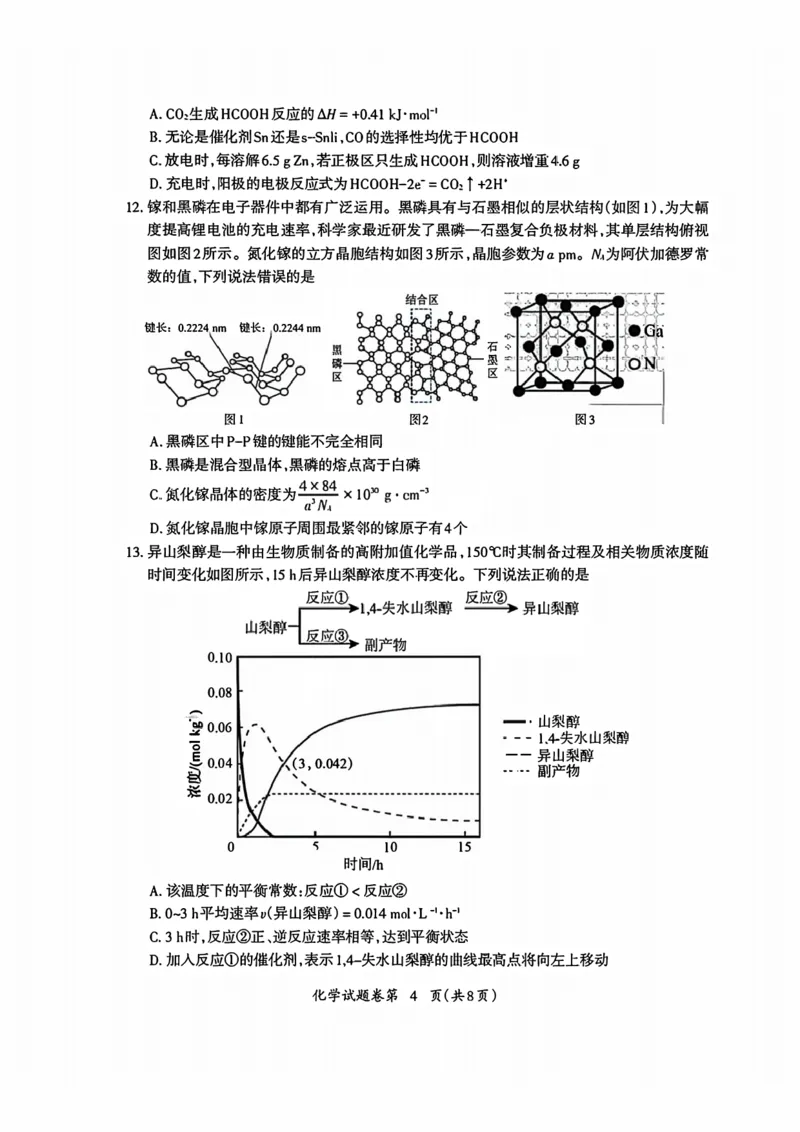
11.科学家近年发明了一种新型Zn—CO:水介质电池。 电极为金属锌和选择性催化材料,电池
工作时双极隔膜中的水解离为H'和OH-并分别向两极移动,电池工作原理和某电极反应的
催化机理如图所示。 下列说法正确的是
CO 1.4]
- ① - L 相 1 1 . 2 0- ] S s n SaLi ·COoH
CO 对
俭 0.8
电解质溶液1电解质溶液 2 × O ₂ 放电 M e 0.6] co
zn Z nl ộH) ₂ …→充电 v 0.4 032 HCOOH
·H O
0
2
0.38
H
₂
COOH
a.0 CO
₂ 003
oclo
双极隔膜
反应路径
化学试题卷第 3 页(共8页)A.CO₂生成HCOOH反应的△H=+0.41 kJ·mol¹
B.无论是催化剂Sn还是s-Snli,CO的选择性均优于HCOOH
C.放电时,每溶解6.5gZn,若正极区只生成HCOOH,则溶液增重4.6g
D.充电时,阳极的电极反应式为HCOOH-2e²=CO₂↑+2H'
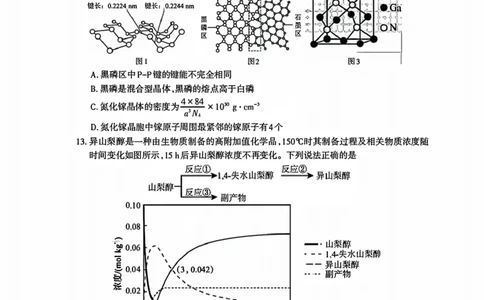
12.镓和黑磷在电子器件中都有广泛运用。 黑磷具有与石墨相似的层状结构(如图1),为大幅
度提高锂电池的充电速率,科学家最近研发了黑磷一石墨复合负极材料,其单层结构俯视
图如图2所示。 氮化镓的立方晶胞结构如图3所示,晶胞参数为a pm。 N,为阿伏加德罗常
数的值,下列说法错误的是
键长: 0.2224nm 键长: 0.2244nm _Ga
之
石 心
墨 0
区
图1 图2 图3
A.黑磷区中P-P键的键能不完全相同
B.黑磷是混合型晶体,黑磷的熔点高于白磷
c.氮化镓晶体的密度为
D.氮化镓晶胞中镓原子周围最紧邻的镓原子有4个
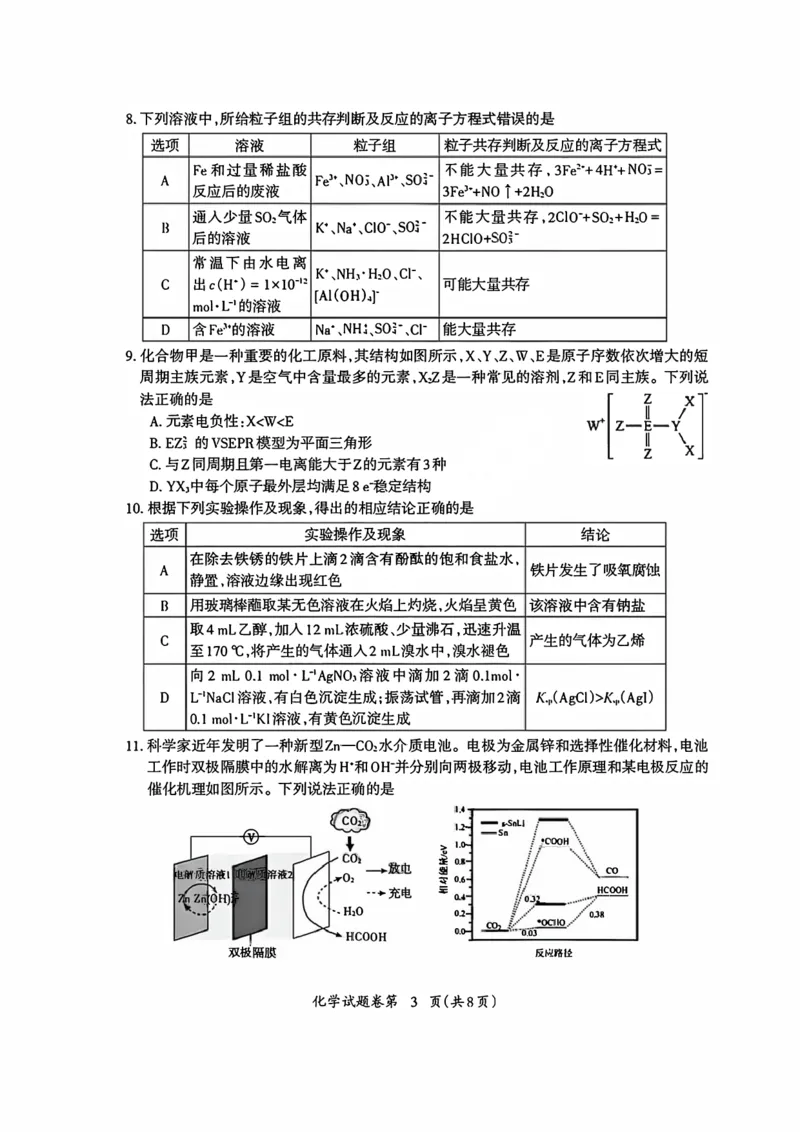
13.异山梨醇是一种由生物质制备的高附加值化学品,150℃时其制备过程及相关物质浓度随
时间变化如图所示,15h后异山梨醇浓度不再变化。 下列说法正确的是
0.10
0.08
浓
(度
0.06
· 山梨醇
m -- 1,4-失水山梨醇
o
l
k - ——异山梨醇
0.04 (3,0.042)
g ……副产物
,
)
0.02
0 5 10 15
时间/h
A.该温度下的平衡常数:反应①<反应②
B.O~3h平均速率v(异山梨醇)=0.014 mol·L-¹·h-¹
C.3h时,反应②正、逆反应速率相等,达到平衡状态
D.加入反应①的催化剂,表示1,4-失水山梨醇的曲线最高点将向左上移动
化学试题卷第 4 页(共8页)14.常温下,向某二元弱酸(H₂A)的难溶盐CaA的悬浊液中通入
HCl气体(无气体生成),平衡时部分组分的1gc(M)随pH变化如
图所示(M表示Ca*、A²、HA^或H₂A)。
下列说法不正确的是
A . Q点:8(A²)=8(H A)
₂
B.Q点对应的pH=2.77
c.
K,( C
a
A)=10*
pH
D . pH=4.27时,2c d(Ca²)+c(H)=c d(OH)+3c( A²)
二、非选择题:本题共4小题,共58分。
15.(14分)碲(Te)及其化合物是重要的半导体材料,碲兼具金属和非金属性质,常用于半导
体、合金、化工、橡胶、玻璃等工业。 电解法精炼铜的阳极泥是碲的主要来源,经预处理后的
阳极泥中含TeO₂及铁、铅、铜的化合物。 可通过如图所示流程制备高纯碲:
NaOH NaS
NH,NO,
HCI so:
预处理后的
破没 过滤
滤液!
沉碲
过滤 TnO
酸溶 还原 粗碲
电解
高纯碲
阳极泥 ₃ (99.5%) 99 .999%)
滤渣1 滤渣2
已知:①TeO:是两性氧化物,微溶于水,可溶于强酸或强碱;
②部分难溶物的K,如表:(溶液中离子浓度小于10°mol·L*时,视为沉淀完全)
化合物 Fe(OH): Pb(OH): Cu(OH) FeS PbS CuS
K 8×10 - ~6 1 . 2×10-¹5 1.3×10 ~ 4×10- ¹ 1×10 ~ * 6×10 ~~
回答下列问题:
(1)碲是第五周期第VIA族元素。基态碲原子价电子排布式为_
。
(2)滤液中加入NaS的目的是 ,为达到该目的滤液1中c(S~)应不低于 _ mol - L”。
(3)“沉碲”时发生反应的离子方程式为
_。
(4)电解法提纯粗碲时,以Na₂TeO,溶液为电解质溶液,电解过程中阴极的电极反应式为
。
(5)常温下,向0.1 mol·L* Na:TeO₃溶液中滴加盐酸,当溶液中c(TeO}):c(H₃TeO₂)=1:5
e
时,溶液pH=_ 。(已知:H T O 的K=1.0×10°、K =2.0×10*)
₂ ₃ ₁ ₂
(6)“酸溶”后,将SO₂通入溶液中进行“还原”得到粗碲。 若阳极泥中含TeO₂的质量分数为8%,
提取过程中碲元素无损失,则处理1kg阳极泥最少需要通入SO₂ _L(标准状况下)。
化学试题卷第 5 页(共8页)16.(15分)配合物乙二胺四乙酸铁钠晶体(NaFeY·3H₃O)可溶于水,是常见的铁营养强化剂。
某实验小组模拟工业生产原理制取乙二胺四乙酸铁钠并测定所制取样品的纯度。
1.产品的制备
步骤1:准确称取m gFeCl₂·6H₃O于烧杯中,加水充分溶解后,再分批加入适量浓氨水。
步骤2;将Fe(OH),、乙二胺四乙酸(H₁Y)、H₂O加入三颈烧瓶中(如图所示),搅拌,80℃水浴
反应1h,用Na₂CO₃溶液调节pH,经过一系列操作,过滤洗涤,晾干得到产品。
(1)“步骤1”利用FeCl₃和氨水的反应制备Fe(OH),,写出反 Na CO
溶₂液₃
应的离子方程式
。 搅拌器
(2)仪器a的名称为_ 。“步骤2”中的“一系列操作”为
温度计
a
o
(3)方案的缺点:氢氧化铁沉淀成胶体状态,难以过滤和洗
涤。 为使沉淀颗粒增大,实验中往往可以采取
(填实验条件)。
Ⅱ.测定所制取样品中铁的含量
取20.00g样品溶于水,然后将其中的铁元素用萃取剂从配合物中“反萃取”出来并配
成250mL溶液,取出25.00mL加入过量的30.00mL0.1500mol·L*H.Y标准溶液并加热煮
沸,充分反应后,再用0.2000 mol·L”的Zn²标准溶液滴定过量的H.Y至终点,消耗Zn²标准
溶液体积为5.00 mLo
已知:Fe”、Zn²*与H₁Y反应的化学计量比均为1:1。
(4)则样品中铁元素的质量分数为_ 。
Ⅲ.在步骤1中FeCl溶解环节,同学们观察到溶液呈黄色,并探究呈黄色的原因。
【查阅资料】[Fe(H₃O)aP”为淡紫色,[Fe(OH)广为黄色。
【实验操作】观察0.01 mol-L FeCl₂溶液、0.005mol·L*Fe:(SO₄),溶液,颜色均为黄色。
【提出猜想】
(5)①Fe”发生了水解反应生成的[Fe(OH)广显黄色,写出该水解反应的离子方程式
。
【实验验证】
取3支洁净的试管,分别加入2mL0.01mol·L*FeCl₃溶液,然后按下表开展实验。
序号 操作 现象
1 滴人10滴6mol-L”的H₂SO,溶液
2 滴入10滴6mol·L~的Na₂SO,溶液 溶液黄色略变浅
3 滴入10滴12 mol·L-'的盐酸 溶液黄色变亮变深
②分析讨论:同学认为根据实验1和实验2的现象可知猜想成立,请补充实验1的实验
现象 。
③进一步探究:根据实验3中的异常现象,进一步查阅资料,FeCl,溶液中还存在反应:
Fe*+4CI [FeClʃ(黄色),请设计实验进一步验证该反应的存在(写出操作和现
象)_
。
化学试题卷第 6 页(共8页)17.(14分)绿氮作为“零碳”燃料,是未来重要的清洁能源。 回答下列问题:
1.氨燃料的应用
工业上用氨气和二氧化碳在一定条件下合成化工产品:
o
①2NH (g)+CO (g)=CO(NH ) (s)+H O(g)△H =-87.0 kJ·m l ' ¹
₃ ₃ ₃ ₂ ₃ ₁
②2NH (g)+CO (g)=H NCOONH (s)△H =-159.5kJ·molr¹
₃ ₃ ₂ ₂ ₂
(1)反应H NCOONH (s)=CO(NH ) (s)+H O(g) △H= kJ·mol²。
₂ ₂ ₂ ₂ ₂
(2)一定温度下,向恒容密闭容器中通入2mol NH₃(g)和1mol CO₂(g),仅发生反应②,下列
说法中能表明该反应达到平衡状态的是 (填标号)。
a.气体密度不变 b.混合气体的平均摩尔质量不变
c . n(NH ):n(CO )=2:1 d.容器内压强不变
₃ ₂
ll.氨气的合成
(3)在不同压强下,以两种不同组成进料,N:(g)+3H₃(g)→2NH₃(g)反应达平衡时氮的物质
的量分数与温度的关系如图所示(物质;的物质的量分数 其中一种进料组
成为xn₂=0.75,xx₂=0.25,另一种为xn₂=0.675、xx₂=0.225kxu=0.10。
0.40 0.40
P P
0.30 A ₃ 0.30 ₃
|
e ; - 2 0 M P a P =2 0M
020 是020
₂ ₈
p 1
P
₁
0.10 0.10
0 ol
500 600 700 800 900 1000 500 600 700 800 900 1000
T/K T/K
图1 图2
①图中压强由大到小的顺序为_ ;进料组成中含有惰性气体Ar的图是
。
②图1中A点所在温度和压强下,xm,=0.25,反应N₃(g)+3H₂(g)→2NH₃(g)的平衡常数
K = _ (MPa)*(列出计算式即可,K,是用分压代替浓度计算的平衡常数,分压=
₁
总压x物质的量分数)。
(4)合成氨工厂以“水煤气”和N:为原料,采用两段间接换热式绝热反应器,由进气口充入
一定量含CO、H₂、H₃O、N₂的混合气体,在反应器A中进行合成氨,其催化剂III(铁触媒)
在500℃时活性最大,反应器B中主要发生的反应为:CO(g)+H₂0(g)→ CO₂(g)+H₃(g)
△H<0,装置如图。
化学试题卷第 7 页(共8页)①温度比较:气流b
_
_气流a(填“>”“<”或“=”)。
②气体流速一定,经由催化剂1到催化剂11,原料转化率有提升,其可能原因之一是:
_(答出一点即可)。
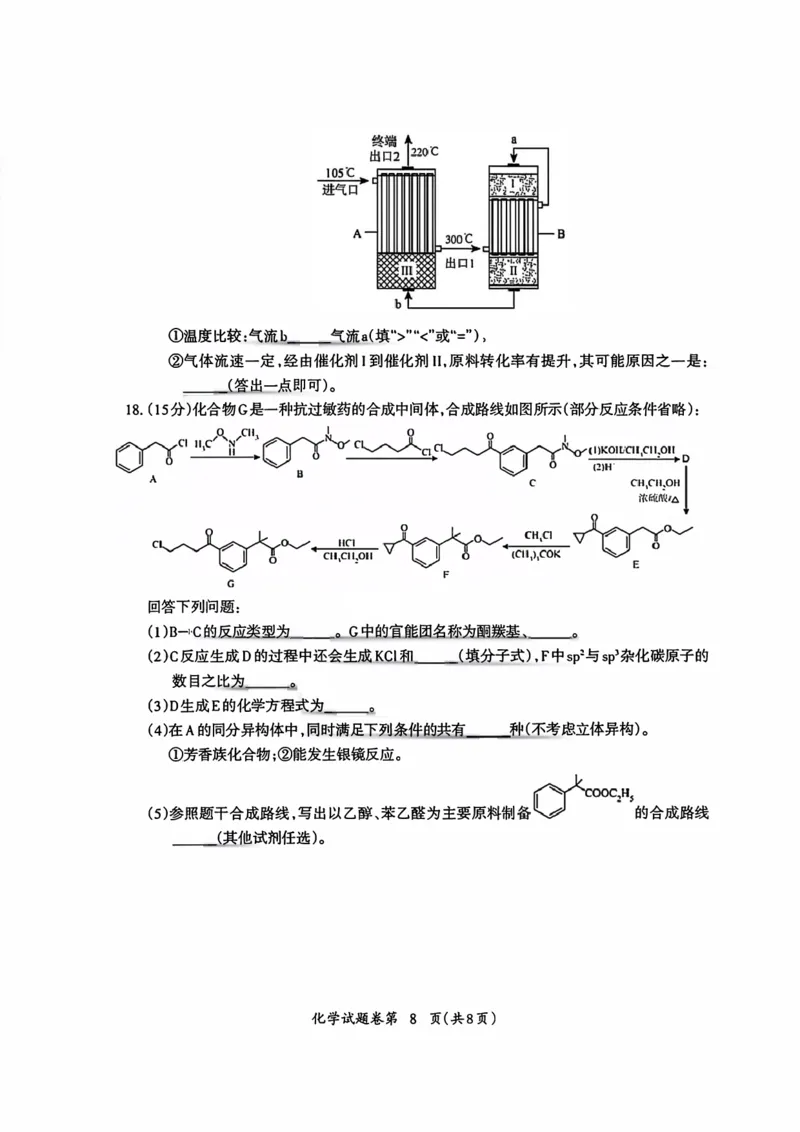
18.(15分)化合物G是一种抗过敏药的合成中间体,合成路线如图所示(部分反应条件省略):
回答下列问题:
(1)B→C的反应类型为 。 G中的官能团名称为酮羰基、
。
(2)C反应生成D的过程中还会生成KC1和 _(填分子式),F中sp²与sp杂化碳原子的
数目之比为
。
(3)D生成E的化学方程式为
。
(4)在A的同分异构体中,同时满足下列条件的共有_ _种(不考虑立体异构)。
①芳香族化合物;②能发生银镜反应。
(5)参照题干合成路线,写出以乙醇、苯乙醛为主要原料制 的合成路线
_(其他试剂任选)。
化学试题卷第 8 页(共8页)