文档内容
秘密 启用前
★
运城市 — 学年第一学期期末调研测试
2025 2026
高三化学参考答案详解及评分说明
评分说明:
考生如按其他方法或步骤解答,正确的,同样给分;有错的,根据错误的性质,参照评分参考中相应的规定评分。
一、选择题:本题共 小题,每小题 分,共 分。
14 3 42
1.B 【解析】钨合金为金属材料;蓝宝石主要成分为氧化铝,属于无机非金属材料;碳化硅增强铝基复合材料属于
复合材料;聚酰亚胺属于合成高分子材料。故选B。
F H •• ••
2.C 【解析】反 , 二氟乙烯的结构式为 , 错误;用电子式表示 的形成过程为 • • •¾¾¾® • • • •,
-1 2- C C A HCl H·+ C••l H C••l
H F
3d
错误;基态 价层电子的轨道表示式为 , 错误。故选 。
3+
B Fe D C
O
3.A 【解析】铱合金制造发动机的火花塞利用了其熔点高、稳定性强的性质,A错误。故选A。
*
4.B 【解析】化合物G属于脂环烃的衍生物,A错误。1molG含有1mol酯基和1mol酰胺基,最 O
* * *
多消耗2molNaOH,C错误。1个G分子中含有如图所示的4个手性碳原子(标*的碳原子),D
N
错误。故选B。
O
G
5.D 【解析】由于HClO的酸性介于HCO 与HCO-之间,故HCO-不能与NaClO发生反应,向NaClO溶液中通入少
2 3
3 3
量CO 只能发生反应:CO +HO+ClO-====HClO+HCO-,D错误。故选D。
2 2 2
3
6.C 【解析】X原子的核外电子只有一种运动状态,故X的原子核外只有1个电子,X为H。Z是人体合成甲状腺激
素的重要微量元素,故Z为I;Z的价电子数与Y的核外电子总数相同,故Y的核外电子总数为7,Y为N;W和Y是
位于第二周期的相邻元素,结合图中W形成4个共价键,可知W为C。电负性:O>N>C,A错误。石墨具有良好
的导电性,B错误。NH 与CuO、NO等物质反应转化为N,N 与O 在放电或高温条件下反应转化为NO,NO易被O
3 2 2 2 2
氧化为NO,NO 与HO反应转化为HNO,C正确。I-的中心原子为I,价层电子对数=2+1×(7+1-2×1)=5,D错
2 2 2 3
3
2
误。故选C。
7.B 【解析】A项,2NO(g) (), 为红棕色气体, 为无色气体,混合气体颜色先变深是因为体积缩
2 N2O4 g NO2 N2O4
小, 浓度增加,由又逐渐变浅可推得平衡向正反应方向移动,即向气体体积缩小的方向移动, 正确。B项,
NO2 A
甲苯可以使酸性KMnO 溶液褪色,是因为苯环上的甲基可以被酸性KMnO 溶液氧化为羧基,说明苯环可以活化
4 4
甲基,B错误。C项,过量,充分反应后仍有 剩余,故 与 发生的反应为可逆反应, 正确。D项,裸露的
- 3+ - 3+
I Fe I Fe C
铁钉附近溶液变红,说明O 在裸露的铁钉表面发生还原反应生成OH-;装置中未产生蓝色沉淀,说明未生成Fe2+,
2
而Zn作负极失去电子被腐蚀,证明了牺牲锌可以保护铁不被腐蚀,D正确。故选B。
8.C 【解析】CHOH中的碳原子采取sp3杂化,A错误。配离子与硝酸根离子之间存在离子键,B错误。配离子带1
3
个单位的正电荷,而中心的Fe3+带3个单位的正电荷,结合题图中Fe3+上下结构相同,可知配体数目为2,为带1个单
位负电荷的阴离子,C正确。由C项分析可知,配合物中配体数目为2,每个配体中均有2个N和1个O作为配位原
子,与中心的Fe3+形成配位键,配位数为6,D错误。故选C。
9.D 【解析】制备乙酸乙酯的传统方案是向反应体系中加入浓硫酸,而浓硫酸可能会使有机物炭化,进一步反应
产生SO,A正确。反应液由蓝色变为紫色,变色硅胶由蓝色变为粉红色,反应充分,停止加热,B正确。由变色硅
2
胶吸水变色可得,在反应进程中,变色硅胶不断吸收生成的水,促进乙酸乙酯的合成反应正向进行,提高乙酸乙酯
的产率,C正确。冷却后,为除去乙酸乙酯粗品中的乙酸,应向烧瓶中缓慢加入饱和NaCO 溶液,D错误。故选D。
2 3
化学试题答案 第 页(共 页)
1 410.D 【解析】六方金刚石的晶体中,碳原子间形成共价键,故六方金刚石属于共价晶体,共价键的强度较大,决定
了六方金刚石硬度大、熔点高的性质特征,A正确。六方金刚石的晶胞中每个碳原子参与形成4个C—C键,每
个C—C键存在于2个碳原子间,故N(C)∶N(C—C键)= 1∶2;2.4 g六方金刚石中所含碳原子的数目为0.2N,
A
C—C键的数目为0.4N,B正确。1个六方金刚石的晶胞含有碳原子的数目为4× 1 + 4×1 + 2×1 + 2×1+
A
12 6 6 3
2× =4,晶胞的体积为 3 a 2 cpm3,故晶体密度为 4 × 12 g/pm3,即32 3×1030g/cm3,C正确。由于1号原
1 a cN
2
2 3 a 2 cN A
A
2
子与2号、3号原子间的距离不同,故每个碳原子与相邻的4个碳原子形成四面体结构,D错误。故选D。
11.D 【解析】由题图可知,步骤 断裂了C—H键,形成了O—H键、C—M键,B正确。步骤 中H元素直接参与化
Ⅰ Ⅰ
学键变化,D比H更重,故MO+与CD 反应时,步骤 的反应速率更慢,活化能更高,对应曲线c,C正确。MO+与
4 Ⅰ
CHD 反应时会断裂C—H键或C—D键,相应的会形成O—H键或O—D键,故会生成CDOH和CHDOD两种氘
3 3 2
代甲醇;断裂C—D键,形成O—D键会导致反应速率变慢,故CHDOD的产量更小,D错误。故选D。
2
12.D 【解析】电极b表面发生氧化反应,故电极b为阳极,应连接外加电源的正极,A错误。电极a表面发生的电
极反应式为O +4e-+2HO====4OH-,B错误。根据电解池中带电粒子移动方向的规律,结合“海水淡化”的需
2 2
求, 室中的阳离子通过阳离子交换膜 移向阴极室 ,阴离子通过阴离子交换膜 移向 室;结合回收锂元
② Ⅰ ① Ⅱ ③
素的需求, 室中的Li+通过阳离子交换膜 移向 室,C错误。 室溶液的质量每减少5.85g,有0.1molNa+与
④ Ⅲ ③ ②
0.1molCl-移出 室, 室电解液中增加0.1molCl-,故理论上有0.1molLi+移向 室,D正确。故选D。
② ③ ③
13.C 【解析】酸浸时,将含锶废渣粉碎研磨,可增大反应物间的接触面积,提高酸浸效率,A正确。K(BaSO)<
sp 4
K(SrSO),用一定浓度的BaCl 溶液浸泡SrSO,可将其转化为BaSO,Sr2+进入溶液,B正确。Sr的金属性强于
sp 4 2 4 4
Ca,SrCl 为强酸强碱盐,不发生水解,C错误。Y与K+形成的超分子能从浸出液中捕获Sr2+,说明Sr2+与Y之间的
2
作用力更强,D正确。故选C。
14.B 【解析】c(Ag+)·c(Cl-)=K (AgCl),则pc(Ag+)=-pc(Cl-)+pK(AgCl),故曲线N表示AgCl的沉淀溶解平衡
sp sp
曲线,A错误。a点时,c(Ag+)>c(Cl-),AgCl的溶解度为c(Cl-);c(Ag+)> 2c(CrO2-),AgCrO 的溶解度为
2 4
4
c(CrO2-),B正确。由图中M、N线上两点(1.7,5)和(4.8,5)可得,K(AgCl)=10-9.8,K(AgCrO)=10-11.7;到达理
sp sp 2 4
4
论滴定终点时,c(Ag+)=c(Cl-)= 10-4.9mol/L,若恰好生成砖红色沉淀AgCrO 指示终点,CrO2-的临界浓度
2 4
4
K 2(AgCl)
c(CrO2-)= 10-1.9 mol/L;故理论上混合液中指示剂的浓度不宜超过10-1.9mol/L,C错误。K= sp =
4 K (Ag CrO )
sp 2 4
10-7.9,D错误。故选B。
二、非选择题:本题共 小题,共 分。
4 58
( 分,除标注外,每空 分)
15. 14 2
()三颈烧瓶( 分)
1 1
() ======
2 12FeCl2·4H2O + 3O2 8FeCl3 + 4Fe(OH)3 + 42H2O
()( 分)
3 b 1
() ====== 生成 等酸性气体抑制
2+
水解
4 FeCl2·4H2O + 4SOCl2 FeCl2 + 4SO2 + 8HCl HCl Fe
()冷凝回流未反应的 ,提高原料利用率
5 SOCl₂
() 中的固体变为灰白色
6 d
m m
()100( 1 - 2)
7 cV
9
【解析】()空气中的氧气将 氧化,根据得失电子守恒和原子守恒即可配平,注意 与 中 原子总
2 FeCl2 FeCl2 FeCl3 Cl
数相等。
()先加热装置 ,使 充满装置,既吸收 脱水产生的水,又生成 等酸性气体抑制 水解。
2+
3 b SOCl2 FeCl₂·4H₂O HCl Fe
()为球形冷凝管, 沸点为 ,未反应的 经过 会冷凝回流进入 ,继续参加反应,提高原料利用率。
5 e SOCl2 76℃ SOCl2 e b
()根据题干中晶体的颜色,当 中固体由蓝绿色变为灰白色时,晶体中的水全部反应。
6 d
化学试题答案 第 页(共 页)
2 4()实验 中酸性 溶液氧化 ,根据关系式 ,m 样品中,n( ) cV ,
-3
7 Ⅰ KMnO4 Fe²⁺ 5Fe²⁺ ~ KMnO4 1 g FeCl₂ = 5 × 10 mol
n( ) ncV ;实验 中同样取m 样品,与足量 反应后,固体质量为m ,但m 不只是
-3
H₂O = 5 × 10 mol Ⅱ ₁ g SOCl₂ ₂ g ₂ g
m m
的质量,还有少量杂质的质量,所以m( ) (m m),n( ) 1 - 2 ,根据两个实验中水的物
FeCl₂ H2O = 1- 2 g H2O = mol
18
m m m m
质的量相等,可得 ncV -3 1 - 2,解得n 100( 1 - 2)。
5 ×10 = = cV
18 9
( 分,除标注外,每空 分)
16. 15 2
()陶瓷中含有 ,在高温下会与 反应,腐蚀容器
1 SiO₂ K₂CO₃
()∶
2 2 7 N>O>Fe>K
() ( 分)
3 Fe₂O₃ 1
()
-33
4 10
()减少产品的损失,快速干燥产品
5
() ====
2- - + 3+
6 Cr2O7 +6I +14H 2Cr +3I2+7H2O
()
7 81.7
高温
【解析】()焙烧在强碱性熔融环境中进行, ======== ,故不可用陶瓷容器。
1 SiO₂+K₂CO₃ K2SiO₃+CO₂↑
() 被氧化为 和 共失去 , 得到 ,依据得失电子数相等,还
- -
2 1molFeO·Cr2O3 K2CrO4 Fe2O3 7mole 1molKNO3 2mole
原剂和氧化剂的物质的量之比为 ∶。第一电离能一般非金属大于金属,基态 原子的最高能级为 ,半充满
3
2 7 N 2p
状态较稳定,第一电离能大于 , 很活泼,易失电子,第一电离能最小,所以第一电离能: 。
O K N>O>Fe>K
()焙烧时, 和 、 反应生成可溶性的 、 和不溶性的 ,同时 、 分别和
3 FeO·Cr2O3 K₂CO₃ KNO3 K2CrO4 KNO2 Fe2O3 SiO2 Al2O3
反应生成可溶性的 、 ,所以滤渣 中的主要成分为 。
K₂CO₃ K₂SiO3 KAlO2 1 Fe2O3
K
()调节 可使 完全沉淀为 ( ),溶液中c( ) -5 -1 ,c( - ) W -9.3
4 pH = 4.7 Al³⁺ Al OH ₃ Al³⁺ ≤ 1 × 10 mol·L OH = c = 10 mol·
+
(H )
,K[ ( )] c( )·c( ),代入数据计算可得K[ ( )] ,所以数量级为 。
-1 3 - -32.9 -33
L sp Al OH 3 = Al³⁺ OH sp Al OH 3 =1×10 10
()产品不溶于乙醇,可以减少产品损失;同时乙醇易挥发,带走水分,快速干燥产品。
5
()根据三种物质之间的反应关系,可利用关系式法计算: ,n( )( )
-3
7 K2Cr2O7~3I2~6Na2S2O3 Na2S2O3 = 0.1×20×10 mol=
1 -3
× 10 × 294 × 10
-3 ,n( ) 1 -3 ,重铬酸钾样品的纯度为 3 。
2×10 mol K2Cr2O7 = ×10 mol ×100%≈81.7%
3 1.20
( 分,除标注外,每空 分)
17. 14 2
() a b c(或c a b)
1 -2 -3 + -2 -3
() ( 分)
2 ①0.4 1
( 分) 压强相同时,升高温度,平衡转化率减小,平衡逆向移动
②< 1
()
3 = 12
()
4 Ⅰ Ⅳ
【解析】()根据已知条件可以写出如下热化学方程式:
1
1 ==== H a -1
①CO(g) + O2(g) CO2(g) Δ 1 = - kJ·mol
2
1 ==== H b -1
②H2(g) + O2(g) H2O(l) Δ 2 = - kJ·mol
2
5 ==== H c -1
③HOCH2CH2OH(g) + O2(g) 2CO2(g) + 3H2O(l) Δ 3 = - kJ·mol
2
根据盖斯定律, 即可得到目标方程式,故目标方程式的 H (c a b) 。
-1
① × 2 + ② × 3 - ③ Δ = -2 -3 kJ·mol
() H,该反应为气体体积减小的反应,温度相同时,增大压强,
2 ①2CO(g) + 3H2(g) HOCH2CH2OH(g) Δ
平衡正向移动,平衡转化率增大,p p p ,故 、 、 对应α分别为 、 、 。
(L1) > (L2) > (L3) L1 L2 L3 0.6 0.5 0.4
由题图 可知,压强相同时,温度升高,平衡转化率减小,说明升高温度平衡逆向移动,则正反应为放热反应,H 。
② 1 Δ <0
化学试题答案 第 页(共 页)
3 4() 、 的进料相同,平衡转化率相等,平衡时各组分物质的量分数分别相等,则K ( ) K ( ); 点对应的平
3 M N x M = x N D
衡转化率为 ,根据题中信息,该反应按化学计量比进料,设起始加入 和 ,列三段式:
0.5 2molCO 3molH2
( ) ( ) ( )
2CO g + 3H2 g HOCH2CH2OH g
起始
(mol) 2 3 0
转化
(mol) 1 1.5 0.5
平衡
(mol) 1 1.5 0.5
1
平衡时, CO 、 H2 、 HOCH2CH2OH 的物质的量分数分别为1、1、1,K x = ( )
3
6 ( )
2
= 12 。
3 2 6 1 × 1
2 3
() 、乙二醇、乙醇的选择性之和为 ,曲线 表示乙二醇的选择性,根据曲线的变化,曲线 、 表示乙醇
4 MG 100 Ⅱ Ⅲ Ⅳ
和 的选择性,所以曲线 表示 的实际转化率。 转化为乙二醇为可逆反应,则二者始终存在于反应
MG Ⅰ DMO MG
体系中,所以曲线 为 的选择性曲线。
Ⅳ MG
( 分,除标注外,每空 分)
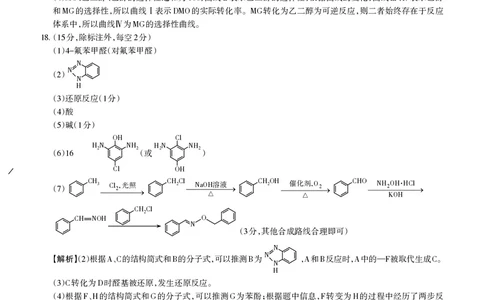
18. 15 2
() 氟苯甲醛(对氟苯甲醛)
1 4-
N
()N
2
N
H
()还原反应( 分)
3 1
()酸
4
()碱( 分)
5 1
OH Cl
() H2N NH2(或H2N NH2)
6 16
Cl OH
(
7
) CH3 ¾¾¾C¾l2¾,¾ 光 ¾ 照 ¾¾® CH2Cl¾¾¾Na¾¾OH¾¾ 溶 ¾ 液 ¾® CH2OH ¾¾¾ 催 ¾ 化 ¾ 剂 ¾¾,O¾¾2® CHO ¾¾¾NH¾¾2O¾¾H¾·¾H¾C¾l®
KOH
CH2Cl
CH NOH O
N ( 分,其他合成路线合理即可)
3
N
【解析】()根据 、的结构简式和 的分子式,可以推测 为N ,和 反应时,中的— 被取代生成 。
2 A C B B A B A F C
N
H
() 转化为 时醛基被还原,发生还原反应。
3 C D
()根据 、 的结构简式和 的分子式,可以推测 为苯酚;根据题中信息,转变为 的过程中经历了两步反
4 F H G G F H
应,再根据第一步的条件中的 ,可以推测第一步是苯酚和 反应生成苯酚钠,所以体现苯酚的酸性。
NaOH NaOH
()根据 、、的结构简式,可以推测 和 发生取代反应生成 ,另一种产物是 ,所以需要在碱性溶液中进行。
5 E J K E J K HCl
()根据信息可以推测该同分异构体的基本结构为苯环上连有 个— 、个— 和 个— ;当 个—
6 1 OH 1 Cl 2 NH2 2 NH2
在苯环上处于邻位时,有 种结构;当 个— 在苯环上处于间位时,有 种结构;当 个— 在苯环上处
6 2 NH2 7 2 NH2
于对位时,有 种结构;所有同分异构体总数为 。当不同化学环境氢原子个数比为 ∶∶ 时,结构对称且
3 16 4 2 1 2
个— 处于对称位,即在苯环上处于间位,且— 和— 在苯环上处于对位,该同分异构体的结构简式为
NH2 Cl OH
OH Cl
H2N NH2或H2N NH2。
Cl OH
化学试题答案 第 页(共 页)
4 4