文档内容
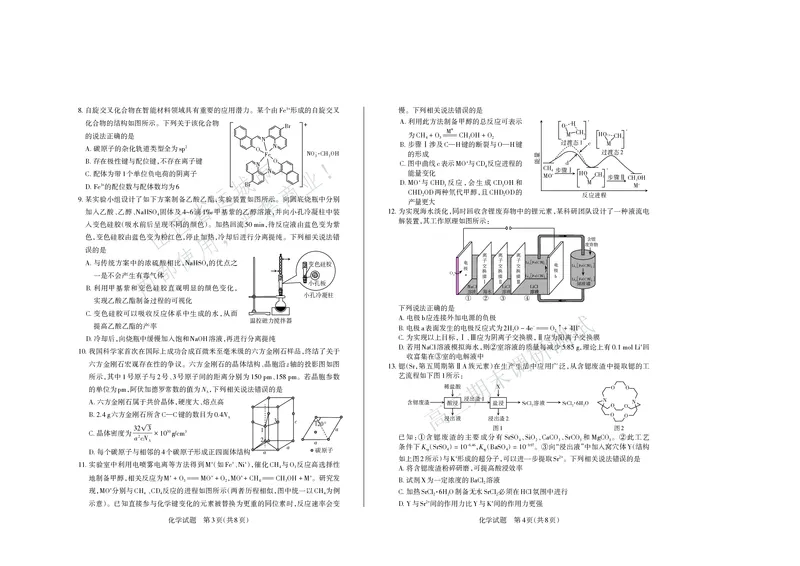
化合物 是某中药的活性成分,其结构如图所示。下列关于化合物 的说法正确
秘密 启用前 4. G G
★ 的是
运城市2025—2026学年第一学期期末调研测试 O
属于芳香烃的衍生物
A.
化 学 高三化学试题 分子式为 O
B. C12H17O3N
与足量 溶液反应,最多可消耗 N
C.1molG NaOH 1molNaOH
2026.02 O
个 分子中含有 个手性碳原子 G
D.1 G 3
本试题满分100分,考试时间75分钟。答案一律写在答题卡上。
下列有关反应的离子方程式错误的是
5.
用适量硫代硫酸钠溶液脱氯: ======
2- 2- - +
注意事项: A. S2O3 +4Cl2+5H2O 2SO4 +8Cl +10H
向 溶液中滴加几滴 溶液,溶液橙色加深:
2-
2- +
答题前考生务必先将自己的姓名、准考证号填写在答题卡上,认真核对条形码上 B. K2Cr2O7 H2SO4 Cr2O7 +H2O 2CrO4 +2H
1. ,
的姓名、准考证号,并将条形码粘贴在答题卡的指定位置上。
向
2+
溶液中加入 固体以除去其中的
2+
: ()
2+
( ) ()
2
(
+
)
C. Mn MnS Cu MnSs +Cu aq CuSs +Mn aq
答题时使用 毫米的黑色中性(签字)笔或碳素笔书写,字体工整、笔迹清楚。 已知K( ) K( ) K( ),向 溶液中通入少量的 :
2. 0.5 D. a1 H2CO3 > a HClO > a2 H2CO3 NaClO CO2
请按照题号在各题的答题区域(黑色线框)内作答,超出答题区域书写的答案无效。 ======
- 2-
3. CO2+H2O+2ClO 2HClO+CO3
保持卡面清洁,不折叠,不破损。 化合物 是一种具有优良双折射性能的材料,其中 的结构如
4. 6. W3X8Y6Z6·3H2O W3X8Y6Z6
可能用到的相对原子质量:H1 C12 O16 Na23 Cl35.5 K39 Cr52 Fe56
图所示。已知 原子的核外电子只有一种运动状态, 和 是位于 下一周期的相
X W Y X
邻元素。 的价电子数与 的核外电子总数相同,且 是人体合成甲状腺激素的重要
一、选择题:本题共 小题,每小题 分,共 分。在每小题给出的四个选项中,只有一
Z Y Z
14 3 42
项是符合题目要求的。 微量元素。下列说法正确的是 YX
2
年中国科技成就举世瞩目。下列科技成果所涉及的材料中属于无机非金属材
的电负性大于同周期相邻元素 X + W + X
1.2025
料的是 A.Y Y Y · -
的同素异形体均无导电性 2Z3
中国“人造太阳”( )中直接与高温等离子体接触的材料为钨合金 B.W W W
A. EAST 由 形成的物质存在转化关系: X 2 Y Y YX 2
超导量子计算原型机“祖冲之三号”中采用蓝宝石作为超导电路的基底材料
B.
C. Y YX3→Y2→YO→YO2→XYO3
“嫦娥六号”使用碳化硅增强铝基复合材料钻取采样,助力月球背面演化历史研究 的中心原子价层电子对数为
-
C. D.Z3 3
侵入式脑机接口神经电极以聚酰亚胺为基底材料 根据下列实验操作及现象,推理得出的结论错误的是
D. 7.
下列化学用语或图示表达正确的是
2. 选项 实验操作及现象 结论
F F
用 注射器吸入 和 的混合气体,用橡胶 其他条件不变,增大压强
A. 反 -1 , 2- 二氟乙烯的结构式: C C 塞封 50 闭 m 细 L 管端,将注射 20 器 m 的 L 活 NO 塞 2 往里 N2O 推 4 ,混合气体的颜色先 会使化学平衡向气体体
A
H H •• •• 变深又逐渐变浅 积缩小的方向移动
B. 用电子式表示 HCl 的形成过程: H·+ • C••l • •¾¾¾® H + [ • • C••l • • ] -
C. 以钙离子撞击锎(2 9 4 8 9 Cf )靶产生超重元素 (2 1 9 1 4 8Og ):2 9 4 8 9 Cf+ 4 2 8 0Ca ¾¾¾®2 1 9 1 4 8Og+3 1 0n B 向盛有 溶 2m 液 L 不 苯 褪 的 色 试 ; 管 将 中 苯替 滴 换 入 为 2~ 甲 3 滴 苯 酸 重 性 复实 KM 验 nO ,溶 4 溶 液 液 褪 , 色 振荡, 甲基可以活化苯环
3d
KMnO4
化 基态 3+ 价层电子的轨道表示式:
D. Fe 将 溶液与 溶液混合, 与 发生的反应为可
- 3+
下列有关物质性质与用途对应关系错误的是 5mL0.1mol/LKI 1mL0.1mol/LFeCl3 I Fe
C 充分反应,再滴加 溶液,溶液变为红色 逆反应
3.
KSCN
铱合金具有生物相容性,用于制造发动机的火花塞
A.
叶绿素铜钠盐为墨绿色粉末,着色力强、安全稳定,可作食品中的着色剂 向培养皿中加入含 的琼脂,滴入 滴酚酞溶液和铁氰
NaCl 5~6 证明了牺牲锌可以保护
B.
化钾溶液;将中段裹有锌皮的铁钉放入培养皿中,一段时间
超临界二氧化碳粘度低、密度高,用于“超碳一号”发电机组中推动涡轮高速旋转发电 D 铁不被腐蚀
C. 后,裸露的铁钉附近溶液变红,装置中未产生蓝色沉淀
放射性同位素 (镱)可以释放伽马射线,可用于金属探伤
169
D. Yb
化学试题 第 页(共 页) 化学试题 第 页(共 页)
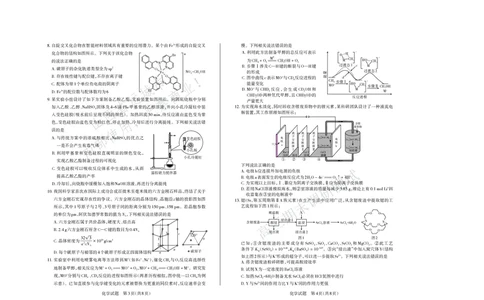
1 8 2 8自旋交叉化合物在智能材料领域具有重要的应用潜力。某个由 形成的自旋交叉 慢。下列相关说法错误的是
3+
8. Fe
化合物的结构如图所示。下列关于该化合物 利用此方法制备甲醇的总反应可表示
A.
Br + 的说法正确的是 为 =M===+==
N 步骤 CH4 涉 +O 及 3 — C 键 H3 的 OH 断 + 裂 O 与 2 — 键 过渡态1
A. 碳原子的杂化轨道类型全为 sp 2 O N - B. 的形成 Ⅰ C H O H 过渡态2
存在极性键与配位键,不存在离子键
Fe NO3·CH3OH
图中曲线 表示 与 反应进程的
B. O + N C. c MO CD4 步骤 C. 配体为带 1 个单位负电荷的阴离子 N 能量变化 Ⅰ 步骤
与 反应,会生成 和 Ⅱ
3+ 的配位数与配体数均为 Br D.MO + CHD3 CD3OH
D.Fe 6 两种氘代甲醇,且 的
反应进程
某实验小组设计了如下方案制备乙酸乙酯,实验装置如图所示。向圆底烧瓶中分别 CHD2OD CHD2OD
产量更大
9.
加入乙酸、乙醇、 固体及 滴 甲基紫的乙醇溶液,并向小孔冷凝柱中装 为实现海水淡化,同时回收含锂废弃物中的锂元素,某科研团队设计了一种液流电
NaHSO4 4~6 1‰ 12.
解装置,其工作原理如图所示:
入变色硅胶(吸水前后呈现不同的颜色)。加热回流 ,待反应液由蓝色变为紫
50min
色,变色硅胶由蓝色变为粉红色,停止加热,冷却后进行分离提纯。下列相关说法错
含锂
废弃物
误的是
离 离 离
A. 与传统方案中的浓硫酸相比, NaHSO4 的优点之 变色硅胶 电 极 子 交 换 子 交 换 子 交 换 Li [ 3F ( eCN ) 6 ] 电 极 Li [ 3 Fe ( CN ) 6 ]
一是不会产生有毒气体 O2 a 膜 膜 膜 Li [ 4 F ( eCN ) 6 ] b [( )]
利用甲基紫和变色硅胶直观明显的颜色变化,
小孔板
Ⅰ Ⅱ Ⅲ
Li4储Fe液C罐N6
B. N溶a液Cl 海水 L溶iC液l L溶L溶iiCC液液ll
小孔冷凝柱
实现乙酸乙酯制备过程的可视化
① ② ③ ④
下列说法正确的是
变色硅胶可以吸收反应体系中生成的水,从而
C. 电极 应连接外加电源的负极
温控磁力搅拌器 A. b
提高乙酸乙酯的产率 电极 表面发生的电极反应式为 ======
- +
B. a 2H2O-4e O2↑+4H
冷却后,向烧瓶中缓慢加入饱和 溶液,再进行分离提纯 为实现以上目标, 、 应为阴离子交换膜, 应为阳离子交换膜
D. NaOH C. Ⅰ Ⅲ Ⅱ
若用 溶液模拟海水,则 室溶液的质量每减少 ,理论上有 回
+
我国科学家首次在国际上成功合成百微米至毫米级的六方金刚石样品,终结了关于 D. NaCl ② 5.85g 0.1molLi
10. 收富集在 室的电解液中
③
六方金刚石宏观存在性的争议。六方金刚石的晶体结构、晶胞沿z轴的投影图如图 锶( ,第五周期第 族元素)在生产生活中应用广泛,从含锶废渣中提取锶的工
13. Sr ⅡA
所示,其中 号原子与 号、号原子间的距离分别为 、 。若晶胞参数 艺流程如下图 所示:
1 2 3 150 pm 158 pm 1
的单位为 ,阿伏加德罗常数的值为N ,下列相关说法错误的是 稀盐酸 X O O
pm A
六方金刚石属于共价晶体,硬度大、熔点高 含锶废渣 酸浸 浸出渣1 盐浸 SrCl溶液 SrCl·6HO N N
A. 2 2 2 O O
六方金刚石所含 — 键的数目为 N O O
B.2.4g C C 0.4 A 3 c 浸出液 浸出渣2
120°
1 a 图 图
晶体密度为32 3 1 2
C. a 2 cN ×10 30 g/cm 3 2 已知: 含锶废渣的主要成分有 、 、 、 和 。 此工艺
A a ① SrSO4 SiO2 CaCO3 SrCO3 MgCO3 ②
每个碳原子与相邻的 个碳原子形成正四面体结构 a a 碳原子 条件下K s ( p SrSO4 ) =10 -6.46 ,K s ( p BaSO4 ) =10 -9.97 。 ③ 向“浸出液”中加入窝穴体 Y (结构
D. 4 如上图 所示)与 形成的超分子,可以进一步提取 。下列相关说法错误的是
+ 2+
实验室中利用电喷雾电离等方法得到 (如 、 ),催化 与 反应高选择性 2 K Sr
11. M + Fe + Ni + CH4 O3 将含锶废渣粉碎研磨,可提高酸浸效率
A.
地制备甲醇,相关反应为 + ====== + , + ====== + 。研究发 试剂 为一定浓度的 溶液
M +O3 MO +O2 MO +CH4 CH3OH+M B. X BaCl2
现, + 分别与 、 反应的进程如图所示(两者历程相似,图中统一以 为例 加热 制备无水 必须在 氛围中进行
MO CH4 CD4 CH4 C. SrCl2·6H2O SrCl2 HCl
示意)。已知直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变 与 间的作用力比 与 间的作用力更强
2+ +
D.Y Sr Y K
化学试题 第 页(共 页) 化学试题 第 页(共 页)
3 8 4 8
量能
H +
O
M CH 3 HO CH +
3 c M
d
C M H O 4 + HO CH + 3 CHOH
M 3
M+一定温度下, (白色沉淀)和 (砖红色沉淀)的沉淀溶解平衡曲线如图所 ()装置 的作用是 。
14. AgCl Ag2CrO4 5 e ▲
示, [c( )( )], [c( )( )]( 代表 或 )。下列 ()制备 反应结束的现象是 。
+ - 2-
pAg = -lg Ag / mol/L pX= -lg X / mol/L X Cl CrO4 6 FeCl2 ▲
说法正确的是 8 ()现有含少量杂质的 n ,为测定n值进行如下实验:
7 7 FeCl₂· H₂O
曲线 表示 的沉淀溶解平衡曲线 N 实验 :称取m 样品,用足量稀硫酸溶解后,用c 酸性 溶液滴定 ,
A. M AgCl 6 (1.7,5) (4.8,5) Ⅰ 1g mol·L⁻¹ KMnO4 Fe 2+
点时c( ) c( ), 和 5 达终点时消耗 溶液V 。
- 2-
B.a Cl = CrO4 AgCl Ag2CrO4 pAg 4 M KMnO4 mL
的溶解度( )相等 实验 :另取m 样品,利用上述装置与足量 充分反应后,剩余固体质量为
mol/L 3 a Ⅱ 1 g SOCl₂
若以 为指示剂,用 标准溶 2 m 。则n的值为 (用含c、V、m、m 的式子表达)。
C. K2CrO4 AgNO3 1 2g ▲ 1 2
液滴定含 Cl - 的水样,理论上混合液中指 0 (注:杂质与 Cl - 在实验过程中均无变化)
示剂的浓度不宜超过 0 1 2 3 4 5 6 7 8 9 10 1112 ( 分)
10 -7.9 mol/L pX 16. 15
D.
反应
2AgC
(
l s
)
+CrO 2 4
(
- aq
)
Ag2CrO
(
4 s
)
+2Cl
(
- aq
)的平衡常数K
=10 7.9
重铬酸钾(
K2Cr2O7
)是一种重要的化工原料和强氧化剂,广泛应用于染料、电镀等领
二、非选择题:本题共 小题,共 分。 域。工业上通常以铬铁矿(主要成分为 ,还含有 、 等杂质)为原料制备重
4 58 FeO·Cr2O3 SiO2 Al2O3
( 分) 铬酸钾。
15. 14
在工业上发挥重要作用,可用作分析试剂、媒染剂、絮凝剂等。实验室可利用 重铬酸钾的制备
FeCl2 Ⅰ.
和亚硫酰氯( )制备。某化学兴趣小组用下图所示装置(加热及夹持装 某兴趣小组模拟制备的工艺流程如下:
FeCl2·4H2O SOCl2
置略)制备无水 。已知 是透明的蓝绿色晶体, 是灰白色的晶体;
FeCl2 FeCl2·4H2O FeCl2
K2CO3
调
沸点为 ,遇水极易反应生成两种酸性气体。 KNO3 H2O pH=4.7 H2SO4
SOCl2 76℃
铬铁矿 焙烧 浸取 滤液 滤液 一系列操作 粗品
1 2 K2Cr2O7
e 滤渣 滤渣
g 溶液 1 2
FeCl2·4H2O f NaOH
重铬酸钾含量的测定
Ⅱ.
准确称取 已干燥的重铬酸钾样品于烧杯中,加 水完全溶解,再加入
d 1.20g 50mL 2g
N c 固体、 稀硫酸,待完全反应后全部转移到 容量瓶中,定容,从中取出
2 KI 20mL 250mL 25mL
溶液于锥形瓶中,加入淀粉指示剂,用 标准液滴定至终点,平行
-1
0.100 0 mol·L Na2S2O3
滴定 次,平均消耗 标准液 。
3 Na2S2O3 20.00mL
浓H 2 S O4 a b S OCl2 已知: ① 焙烧时主反应: FeO·Cr2O3+K2CO3+KNO3 ¾¾¾® K2CrO4+Fe2O3+CO2↑+KNO2
检查装置的气密性完好后,在装置中加入相应的试剂; 2- ==== 2- -
Ⅰ. ②2S2O3 +I2 S4O6 +2I
实验开始时先通 ,排尽装置中的空气,一段时间后,加热装置 、; 回答下列问题:
Ⅱ. N2 b d
反应结束,继续通 至装置冷却; ()焙烧时,不能使用陶瓷容器的原因是 。
Ⅲ. N2 1 ▲
称量产品质量。 ()焙烧时,主反应中还原剂和氧化剂的物质的量之比为 。该反应中所涉及
Ⅳ. 2 ▲
回答下列问题: 的 、、、 四种元素的第一电离能从大到小的顺序为 (用元素符号表示)。
Fe K O N ▲
()装置 的名称是 。 ()滤渣 中的主要成分为 (写化学式)。
1 b ▲ 3 1 ▲
()若实验开始前未通一段时间 ,加热时 会被氧化。写出 ()室温下,调节 时, 完全沉淀,( )的K 的数量级为 (若
3+
2 N2 FeCl2·4H2O FeCl2·4H2O 4 pH = 4.7 Al Al OH 3 sp ▲
加热时反应生成 和 ( )的化学方程式 。 某离子浓度小于等于 时,可认为该离子沉淀完全)。
-5 -1
FeCl3 Fe OH 3 ▲ 1×10 mol·L
()加热装置 、时,应先加热装置 (填“ ”或“ ”)。 ()在一系列操作时,用乙醇洗涤的优点是 。
3 b d ▲ b d 5 ▲
()装置 中 和 反应的化学方程式为 。 的作用:一是 () 和 反应的离子方程式为 。
4 d FeCl2·4H2O SOCl2 ▲ SOCl2 6 K2Cr2O7 KI ▲
吸收 脱水产生的水,另一个作用是 。 ()重铬酸钾样品的纯度为 (保留三位有效数字)。
FeCl₂·4H₂O ▲ 7 ▲ %
化学试题 第 页(共 页) 化学试题 第 页(共 页)
5 8 6 8( 分)
17. 14
乙二醇常用作汽车防冻液,是一种应用广泛的化工原料。煤化工工艺有两种合成
路线。
直接合成法,反应如下:
Ⅰ.
H
2CO(g) + 3H2(g) HOCH2CH2OH(g) Δ
()已知 ()、()、 ()的燃烧热分别为 a 、b 、
-1 -1
1 CO g H2 g HOCH2CH2OH g - kJ·mol - kJ·mol
c ,则上述制备反应的 H (用含a、b、c的式子表示)。
-1 -1
- kJ·mol Δ = ▲ kJ·mol
()按照化学计量比进料,在平衡转化率α分别为 、 、 时,探究反应温度与
2 0.4 0.5 0.6
压强的关系,结果如图 所示:
1
25
20
15
10
5 T 480 490 500 510 520 /K
图
1
p
aPM/
( , )
483 99
100
L1 80
L2 60 N
L3
M D 40
20
0
443 463 483 503 523 温度 /K
性择选或率化转
%/
( 分)
18. 15
苯并三氮唑(化合物 )在植物保护和医疗保健等方面有着广阔的应用,合成路线
K
如下(部分试剂、反应条件省略)。
N N
( ) K2CO3 OHC N LiAlH4
① OHC F +B C6H5N3
DMF THF
A C
N N
N N
HOH2C N
SOCl2
ClH2C N
D E
Ⅰ OH
H3C CHO ( 1 ) G ( C6H6O ) H3C CHO N
Ⅱ NaOH , C2H5OH NH2OH·HCl H3C
( 450 , 50 ) ② N N Cl ( 2 ) DMSO N N O KOH
N
Ⅲ O CH3 CH3 N
CH3
( 483 , 2 ) Ⅳ F H J
N
N
N
图
2 H3C
由图 可得,曲线 代表α ; ③ E+J O
① 1 L3 = ▲ N
H (填“ “” ”或“ ”),原因是 。 N
②Δ ▲ 0 > < = ▲ N
xy xz O
()已知:反应a b y z ,K (Y) (Z),x为组分的物 CH3
3 A(g) + B(g) Y(g) + Z(g) x = xa xb
K
(A) (B)
回答下列问题:
质的量分数。 、 两点对应的体系,K K (填“ ”“ ”或“ ”), 点对应体
M N x(M) ▲ x(N) > < = D
() 的名称是 。
系的K 的值为 。 1 A ▲
x ▲
() 的结构简式为 。
间接合成法,先合成 ,后 发生如下 个放热的连续反应,其中 生成 2 B ▲
Ⅱ. DMO DMO 3 MG
()由 转变为 的反应类型是 。
乙二醇的反应为可逆反应: 3 C D ▲
()由 转变为 的过程中经历了两步反应,第一步反应体现了 的 性。
COOCH +2H CHOH +2H CHOH +H CH 4 F H G ▲
3 2 2 2 2 2 3
() 和 生成 的反应需要在 性(填“酸”“碱”或“中”)溶液中进行。
COOCH 3 -CH 3 OH COOCH 3 -CH 3 OH CH 2 OH -H 2 O CH 2 OH 5 E J K ▲
DMO(g) MG(g) 乙二醇(g) 乙醇(g) ()同时满足下列条件的 的同分异构体有 种(不考虑立体异构)。
6 F ▲
()在 、 催化、固定流速条件下发生上述反应,初始氢酯比固定,出口处 含有两个氨基; 与 3+ 反应显紫色。
4 2MPa Cu/SiO2 ① ② Fe 化
检测到 的实际转化率及 、乙二醇、乙醇的选择性随温度的变化曲线如图 所示 其不同化学环境氢原子个数比为∶∶的同分异构体的结构简式为 (写出一种)。
DMO MG 2 4 2 1 ▲
n 该物质 ()参考上述路线,以甲苯和 (无机试剂任选)为原料,设计
[某物质的选择性 生成( ) ]。 7 NH2OH·HCl
= n × 100%
消耗(DMO)
已知曲线 表示乙二醇的选择性,则曲线 (填图中标号,下同)表示 的 O
Ⅱ ▲ DMO N 的合成路线: 。
转化率,曲线 表示 的选择性。 ▲
▲ MG
化学试题 第 页(共 页) 化学试题 第 页(共 页)
7 8 8 8