文档内容
山东省威海市 2014 年中考化学试卷
参考答案与试题解析
一、单项选择题(共10小题,每小题2分,满分20分)
1.(2分)(2014•威海)从化学的视角看,下列关于化学物质的说法中,错误的是( )
A.绿茵场上的足球运动员、青草和足球都是物质
B.任何化学物质都是由微小粒子构成的
C.你的身体就是你摄入的化学物质做成的
D.看不见的东西都不属于化学物质
考点:化学的研究领域.
专题:课本知识同类信息.
分析:A、世界是由物质组成的;
B、物质是由分子、原子、离子等微粒构成的;
C、世界上所有的物质都是化学物质;
D、世界上的物质包括看的见和看不见的都是化学物质;
解答:解:A、世界是由物质组成的,绿茵场上的足球运动员、青草和足球都是物质,正确;
B、物质是由分子、原子、离子等微粒构成的,任何化学物质都是由微小粒子构成的,正
确;
C、世界上所有的物质都是化学物质,我们摄入的物质也不例外,正确;
D、世界上的物质包括看的见和看不见的都是化学物质,错误;
故选D
点评:化学是研究物质的,世界是物质的,物质是由看不见的微粒构成的.
2.(2分)(2014•威海)某混合物其组成特点是“各成分彼此完全混合,处处相同”,这种混
合物不可能是( )
A.食盐水 B.黄泥水 C.空气 D.不锈钢
考点:纯净物和混合物的判别.
.
专题:物质的分类.
分析:根据“各成分彼此完全混合,处处相同”,来分析回答本题,黄泥水属于悬浊液不均
一、不稳定.
解答:解:A、食盐水属于溶液是均一、稳定的混合物,故A错;
B、黄泥水属于悬浊液不均一、不稳定,故B正确;
C、由于分在不断运动,空气中各成分也是均一混合在一块的,故C错;
D、不锈钢是均一混合在一块的混合物,各成分彼此完全混合,处处相同,故D错.
故选B.
点评:解答本题关键是要知道悬
浊液、乳浊液都是不均
一、不稳定的混合物.
3.(2分)(2014•威海)C﹣12和C﹣14是碳元素的两种不同的原子,二者的不同点有( )
①原子中的电子数;②原子核内的中子数;③原子核内的质子数;④原子的质量.
A.①② B.③④ C.①③ D.②④
考点:原子的定义与构成.
.
专题:物质的微观构成与物质的宏观组成.分析:C﹣12和C﹣14是碳元素的两种不同的原子,属于同位素,其区别是中子数量不同,造
成原子的质量有差别.
解答:解:C﹣12和C﹣14是碳元素的两种不同的原子,其区别是C﹣12的中子数是6,C﹣
14的中子数是8,从而使原子的质量出现差别.
故选D.
点评:本题考查同位素及原子结构的知识,要掌握其区别和联系.
4.(2分)(2014•威海)两种化合物都有甜味,下列推测正确的是( )
A.组成元素一定相同
B.构成分子的原子个数一定相同
C.分子中某些原子的结合方式可能是相似的
D.性质、组成和结构完全相同
考点:物质的元素组成;分子和原子的区别和联系.
.
专题:物质的微观构成与物质的宏观组成.
分析:两种化合物都有甜味说明
构成分子的原子可能
含有相似的结合方式,不能说明组成元素、原子个数、性质、组成、结构一定相同.
解答:解:A、两种化合物都有甜味,组成元素不一定相同,故A错;
B、两种化合物都有甜味,构成分子的原子个数不一定相同,例如葡萄糖和蔗糖都有甜
味,但原子个数不同,故B错;
C、两种化合物都有甜味说明构成分子的原子可能含有相似的结合方式,才具有相似
的性质,故C正确;
D、两种化合物都有甜味,物质的性质、组成和结构不一定相同,例如葡萄糖和蔗糖都
有甜味,性质、组成和结构不同,故D错.
故选C.
点评:解答本题关键是要从题目中提取有用信息,并能灵活运用解决实际问题.
5.(2分)(2014•威海)在化学变化中,下列说法正确的是( )
A.原子既不能被创造也不能被消灭 B.原子可以被创造,但不能被消灭
C.原子可以被消灭,但不能被创造 D.原子总是不断地被创造和被消灭
考点:化学反应的实质.
.
专题:物质的变化与性质.
分析:根据在化学变化中原子既不能被创造也不能被消灭,只是分子分裂为原子,原子的重
新组成新的分子的过程进行解答.
解答:解:A、在化学变化中原子既不能被创造也不能被消灭,只是分子分裂为原子,原子的
重新组成新的分子的过程,故A正确;
B、在化学变化中原子既不能被创造也不能被消灭,故B错误;
C、在化学变化中原子既不能被创造也不能被消灭,故C错误;
D、在化学变化中原子既不能被创造也不能被消灭,故D错误;
故选:A.
点评:本题主要从不同的角度对化学变化的实质中原子的进行了分析,难度不大.
6.(2分)(2014•威海)氧循环和碳循环密不可分,其中属于二氧化碳转化为氧气的变化是(
)
A.海水吸收二氧化碳 B.动植物的呼吸作用
C.绿色植物的光合作用 D.化石燃料的燃烧
考点:自然界中的碳循环.
.专题:碳单质与含碳化合物的性质与用途.
分析:结合光合作用、呼吸作用、燃烧的常识等进行分析解答,自然界中由二氧化碳转化为氧
气唯一的方法是光合作用,据此进行分析判断.
解答:解:A、海水能吸收部分二氧化碳,但不能放出氧气,故选项错误;
B、动植物的呼吸,是将
氧气在体内发生缓慢
氧化释放出二氧化碳,是将氧气转化为二氧化碳,故选项错误;
C、绿色植物的光合作用是吸收植物吸收二氧化碳释放氧气的过程,能将二氧化碳转
化为氧气,故选项正确;
D、化石燃料的燃烧,是燃料与氧气反应生成二氧化碳,是将氧气转化为二氧化碳,故
选项错误.
故选:C.
点评:本题难度不大,了解光合作用、呼吸作用、燃烧的原理等是正确解答本题的关键.
7.(2分)(2014•威海)下列现象或事实,可用金属活动性作出解释的是( )
①黄铜(铜锌合金)外观与黄金相似,但可将两者放入稀盐酸中加以区别
②金属铝比金属锌更耐腐蚀,说明锌比铝活动性强
③用硫酸铜、石灰水配置农药波尔多液时,不能用铁制容器.
A.② B.①③ C.②③ D.①②③
考点:金属活动性顺序及其应用.
.
专题:金属与金属材料.
分析:根据金属活动性顺序表的应用分析解答.在金属活
动性顺序表中,排在氢
前面的金属可置换出酸中的氢元素,排在前面的金属能把排在后面的金属从它们的化
合物溶液中置换出来;铝与氧气反应能生成致密的氧化物薄膜.
解答:解:①在金属活动性顺序表中,金位于氢的后面,不能与稀盐酸反应,锌位于氢的前
面,能与稀盐酸反应,所以,黄铜与黄金,可将两者放入稀盐酸中加以区别.故①正确.
②金属铝更耐腐蚀是由于其化学性质活泼,在常温下就可以和氧气反应而形成致密的
氧化铝薄膜,从而阻止进一步氧化,而不是说明锌的活动性比铝强,故②错误.
③铁的活动性比铜强,所以可以铁能将硫酸铜中的铜置换出来,故不能用铁桶来配制
波尔多液,故③正确.
由以上分析可知,B正确
,A、C、D错误.
故选B.
点评:熟记金属活动性顺序,理解其应用原则,学会处理实际问题.
8.(2分)(2014•威海)人体就像一个复杂的“化学工厂”,在下列食物中,不能给这个“化
学工厂”提供能源的是( )
A.汉堡 B.花生油 C.矿泉水 D.馒头
考点:生命活动与六大营养素.
.
专题:化学与生活.
分析:人体需要的营养素包括糖类、油脂、蛋白质、维生素、水和无机盐,其中糖类、油脂和蛋
白质能够为人体提供能量.
解答:解:A、汉堡中含有淀粉,能够为人体提供能量;
B、花生油中含有油脂,能够为人体提供能量;
C、矿泉水中不含有糖类、油脂和蛋白质,不能为人体提供能量;D、馒头中含有淀粉,能够为人体提供能量.
故选 :C.
点评:要了解各种食物的成分,只有这样才能合理搭配膳食,促进身体健康.
9.(2分)(2014•威海)常温下,某气体无色、无味、无毒、能溶于水,密度比空气大,如果在实
验室里采用如下装置且不需要加热制备该气体,则应选择的发生装置和收集装置是( )
A.①和③ B.②和③ C.②和④ D.②和⑤
考点:常用气体的发生装置和收集装置与选取方法.
.
专题:常见气体的实验室制法、检验、干燥与净化.
分析:根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置.
解答:解:反应不需要加热,应该用②装置作为发生装置;
气体能够溶于水,不能用排水法收集,密度比空气大,可以用向上排空气法收集,即用
⑤装置收集.
故选:D.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会
设计实验 、进行实验、
分析实验,为学好化学知识奠定基础.
10.(2分)(2014•威海)甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中错
误的是( )
A.t ℃时,50g甲的饱和溶液中溶解了10g的甲
1
B.将t ℃时的甲、乙两种物质的变化溶液升温至t ℃(溶剂的量不变),两种溶液中溶质的
2 3
质量分数相等
C.t ℃时,要使接近饱和的乙溶液达到饱和状态,可以用蒸发溶剂的方法
2
D.甲物质的饱和溶液中含有少量乙,可采用降温结晶的方法分离提纯甲
[来源:
学科网]
考点:固体溶解度曲线及其作用;结晶的原理、方法及其应用;饱和溶液和不饱和溶液相互转
变的方法;溶质的质量分数、溶解性和溶解度的关系.
.
专题:溶液、浊液与溶解度.分析:A、据t ℃时甲的溶解度分析解答;
1
B、据t ℃时的甲、乙两种物质的溶解度随温度的变化情况分析解答;
2
C、据t ℃时乙的溶解度随温度的变化情况分析解答;
2
D、据甲的溶解度随温度的变化情况分析得到其晶体的方法;
解答:解:
A、t ℃时,甲的溶解度是20g,即120g饱和溶液中含有溶质甲的质量为20g,所以60g
1
甲的饱和溶液中含有溶质10g,故错;
B、t ℃时的甲、乙两种物质的溶解度相等,所以其饱和溶
2
液中溶质的质量分数
也相等甲、乙两种物质的溶解度随温度的升高而增大,无晶体析出,饱和溶液中溶质的
质量分数的计算式 ×100%,将甲、乙两种物质的饱和溶液升温到t ℃
3
后,甲、乙中溶质、溶剂的质量不变,溶质的质量分数不变,故对;
C、t ℃时乙的溶解度随温度随温度的升高而增大,要使接近饱和的乙溶液达到饱和状
2
态,可以用蒸发溶剂的方法,故对;
D、由图可知:甲的溶解度受温度影响较大,乙的溶解度受温度影响变化不大,所以除
去甲中含有少量的乙,可采用降温结晶的方法分离提纯甲,故对;
答案:A
点评:了解溶解度的概念,明确饱和溶液中溶质的质量分数的计算方法,溶解度曲线的意义,
并能将所学知识灵活应用来分析和解答相关问题,是解答此题的关键因素.
二、解答题(共5小题,满分43分)
11.(7分)(2014•威海)宏观与微观的桥梁﹣﹣粒子结构模型
微观粒子看不见、摸不着,化学之用通过模型来说明他们心目中粒子的“模样”,揭示物质
的微观结构特点,解释微观结构与宏观现象之间的因果关系.模型化的方法是化学科学重要
的思想工具,试回答下列问题:
(1)原子的结构
一百多年来,化学有借助构建原子结构模型,逐渐揭开了原子构成的神秘面纱,并通过不断
提出新的原子结构模型,逐步形成了今天的原子结构理论.
①如图1两种模型是汤姆森和卢瑟福分别于1897年和1911年提出的,其中(填代号,下同)
A 是由汤姆森提出的.
②下列关于原子结构理论的学说中,汤姆森的观点是(填代号,下同) ACDG ,卢瑟福的
观点是 BEFH .
A、原子是不可分的
B、原子是可分的
C、原子呈球形
D、在球体内充斥着正电荷,电子镶嵌其中
E、带正电荷的原子核居于原子的中心F、带正电荷的原子核很小,但集中了原子的大部
分质量
G、电子带负电
H、电子在原子核外很大的空间内高速运动
(2)离子的结构
在初中化学中,离子的结构可以用离子结构示意图来表示.在如图2中:
属于阳离子的是(填代号,下同) B ,属于阴离子的是 AD .
(3)分子的结构
如图3中(Ⅰ)和(Ⅱ)分别是两个分子的微观结构模型,你认为它们所代表的物质的化学式
是否相同? 相同 .二者是不是同一种物质? 不是 .
[来源:学§科§网Z§X§X§K]
考点:原子的定义与构成;原子结构示意图与离子结构示意图.
.
专题:物质的微观构成与物质的宏观组成;化学用语和质量守恒定律.
分析:(1)汤姆森发现电子并提出类似“西瓜”的
原子模型,认为电子就
像“西瓜子”一样镶嵌在带正电荷的“西瓜瓤”中;卢瑟福的原子核式结构模型:在
原子的中心有一个很小的核,叫原子核,原子的全部正电荷和几乎全部质量都集中在
原子核里,带负电的电子在核外空间里绕着核旋转.
(2)阳离子的核内质子数小于核外电子数;阴离子的核内质子数大于核外电子数;
(3)比例模型可以直观地表示分子的形状,其碳原子的成键情况是确定分子结构的关
键,碳原子的成键情况主要根据与碳原子形成共价键的原子的数目确定,原子半径的
关系为C>O>H.
解答:解:(1)①汤姆森发现电子并提出类似“西瓜”的
原子模型,认为电子就
像“西瓜子”一样镶嵌在带正电荷的“西瓜瓤”中;卢瑟福的原子核式结构模型:在
原子的中心有一 个很
小的核,叫原子核,原子的全部正电荷和几乎全部质量都集中在原子核里,带负电的电
子 在核外空间里绕着
核旋转.故答案为:A;②由分析可知,ACDG代表汤姆森的观点;BEFH代表卢瑟福的观点,故答案为:
ACDG;BEFH;
(2)阳离子的核内质子数小于核外电子数;阴离子的核内质子数大于核外电子数;故
答案为:B;AD;
(3)CH ﹣CH ﹣OH和CH ﹣O﹣CH 分子式相同,但结构不同,互为同分异构体;故
3 2 3 3
答案为:相同;不是.
点评:本题考查原子、离子、分子的结构知识,基础性强.
12.(11分)(2014•威海)探秘海滩上的物质
在海滩上,你能看到各种各样的物质,除海洋生物外,最常见的有海沙,贝壳和海水,虽然他
们性质与用途各异,但从元素组成的角度看,这些物质都是由氧、硅、氟、钾、钙等有限的几种
元素组成的.
原子是构成物质的“基石”,一种原子,可以构成
最常见的单质,但更多的是
和其他原子结合成各种化合物,请回答:
(1)从化学的视角认识物质
①海沙是由石英和贝壳的碎片组成,石英的主要成分是(用化学符号表示,下同) SiO ,
2
贝壳的主要成分是 CaCO ;
3
②请写出一种同时符合下列两个条件的化合物的名称或
化学式 氢氧化钙或 C a
( OH )
2
(Ⅰ)由氧、硅、氟、钾、钙五种元素中的三种组成;
(Ⅱ)根据分类,与①中两种物质的主要成分类别不同
③海水中含有多种无机盐,各离子的含量如图1所示,其中由硫酸根离子和镁离子构成的化
学式是 MgSO ,假设海水中无机盐的含量为3.8%,钾离子全部以氯化钾的形式存在,则
4
W 海水中含有氯化钾质量的计算公式为 .
g
④各地海水中盐的含量并不完全相同,在接近入海口处,海水中盐的含量较低,原因是 河
水中的淡水将海水中的盐分稀释 .
⑤食用微钠盐可预防高血压,低碘盐是在氯化钠中加了氯化钾,氯化钾除了有咸味外,还带
有苦味,从物质构成的角度看,氯化钾有苦味可能是 钾离子 造成的.
(2)用化学的方法改造物质海水中含有丰富的镁元素,目前工业上绝大多数的金属镁是从海水中提取的,其生产流程如
图2:
①步骤一中发生反应的化学方程式为 CaO+H O=Ca ( OH ) , C a( OH ) +MgCl =Mg
2 2 2 2
( OH ) ↓+CaCl .
2 2
②上述生产流程中发生的反应,没有涉及到的基本反应类型是 置换反应 .
③在步骤一中,分离出沉淀A的方法是 过滤 .
考点:化学式的书写及意义;生石灰的性质与用途;盐
的化学性质;化合物中
某元素的质量计算;反应类型的判定;书写化学方程式、文字表达式、电离方程式;对
海洋资源的合理开发与利
用.
.
专题:化学式的计算;化学用语和质量守恒定律;常见的盐 化学肥料.
分析:(1)①熟记常见物质的主要成分;②根据提供的元素和物质的类别来确定物质的化学
式;③根据溶质的质量=溶液的质量×溶液中溶质的质量分数来计算;④从入海的河水
含盐量较低来分析;⑤从氯化钠和氯化钾的构成异同点来分析;
(2)①当将生石灰放入海水中,氧化钙先与水反应生成氢氧化钙,然后氢氧化钙再与
氯化镁反应;
②明确每一步中发生的化学反应及其类型就能顺利解答;
③将固体与液体分离开的方法是过滤.
解答:解:(1)①石英砂的主要成分是二氧化硅,贝壳的主要成分是碳酸钙;故填:SiO
2
;CaCO ;
3
②上述两种物质分属于氧化物和盐,根据提供的元素可以组成的符合两个条件的是氢
氧化 钙.故填:氢氧化
钙或Ca(OH) ;
2
③镁离子带2个单位的正电荷,硫酸根离子带2个单位的负电荷,故硫酸镁的化学式
为:MgSO ,Wg海水中含有钾离子的质量为:Wg×3.8%×1.10%,那么氯化钾的质量为
4
.故填:MgSO ; ;
4
④在河流的入海口处,有大量的河水注入海洋,相对于海水来讲,注入海洋的河流属于
淡水.所以注入海洋的河水,等于是增加了入海口处海水中的水(溶剂),造成该处海
水盐的浓度降低;故填:河水中的淡水将海水中的盐分稀释;
⑤氯化钠是由钠离子和氯离子构成的,没有苦味,氯化钾是由钾离子和氯离子构成的,
有苦味,据此分析可能是钾离子导致氯化钾具有苦味的;故填:钾离子;
(2)①在步骤一中:氧化钙与水反应生成氢氧化钙,然后氢氧化钙与氯化镁反应生成
氯化钙和氢氧化镁白色沉淀;故填:CaO+H O=Ca(OH);Ca(OH)+MgCl =Mg(OH)
2 2 2 2
↓+CaCl ;
2 2
② 上述过程中氧化钙
和水反应生成氢氧化钙,属于化合反应;,氢氧化钙与氯化镁反应生成氯化钙和氢氧化
镁沉淀属于复分解反应,盐酸和氢氧化镁反应能生成氯化镁和水,属于复分解反应;电
解熔融的氯化镁生成氯气和镁,属于分解反应;没有涉及到置换反应.故填:置换反
应;
③通过过滤可以把沉淀从溶液中分离出来.故填:过滤.
点评:化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,
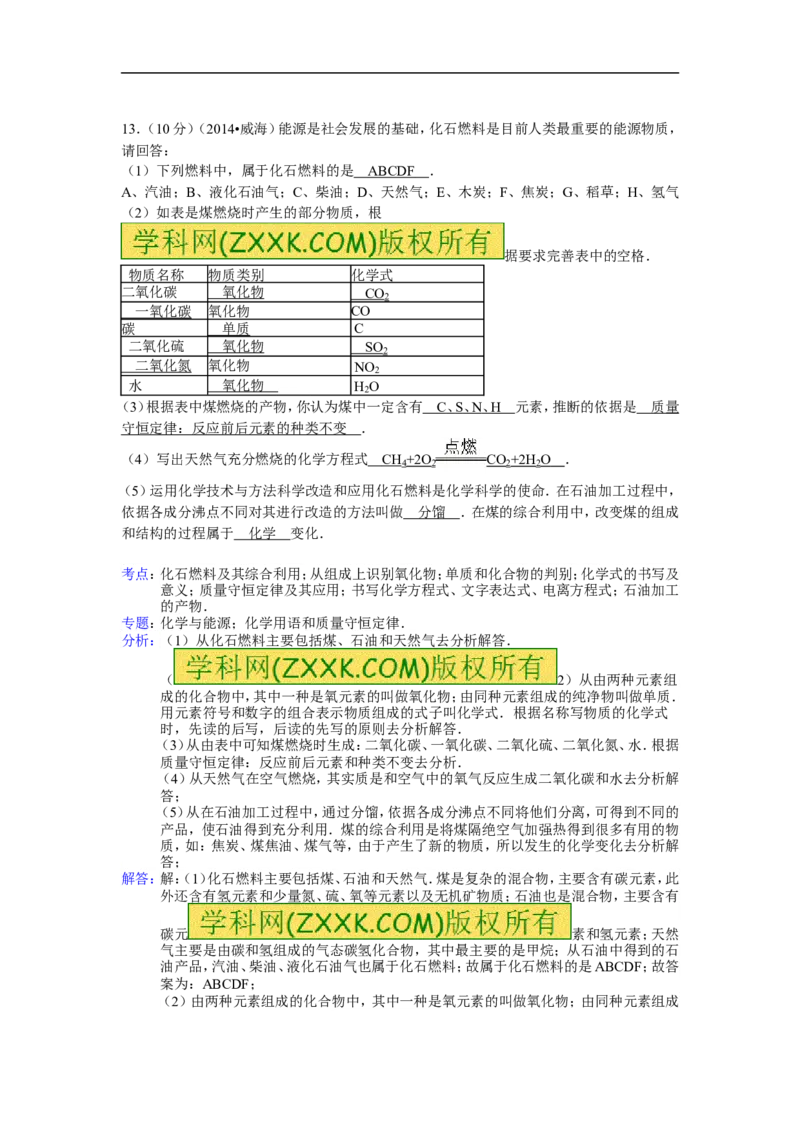
掌握物质的性质和相互之间的反应关系,有助于提高观察实验、进行实验的能力.13.(10分)(2014•威海)能源是社会发展的基础,化石燃料是目前人类最重要的能源物质,
请回答:
(1)下列燃料中,属于化石燃料的是 ABCDF .
A、汽油;B、液化石油气;C、柴油;D、天然气;E、木炭;F、焦炭;G、稻草;H、氢气
(2)如表是煤燃烧时产生的部分物质,根
据要求完善表中的空格.
物质名称 物质类别 化学式
二氧化碳 氧化物 CO
2
一氧化碳 氧化物 CO
碳 单质 C
二氧化硫 氧化物 SO
2
二氧化氮 氧化物 NO
2
水 氧化物 H O
[来源:学+科+网 Z+X+X+K] 2
(3)根据表中煤燃烧的产物,你认为煤中一定含有 C 、 S 、 N 、 H 元素,推断的依据是 质量
守恒定律:反应前后元素的种类不变 .
(4)写出天然气充分燃烧的化学方程式 CH +2O CO +2H O .
4 2 2 2
(5)运用化学技术与方法科学改造和应用化石燃料是化学科学的使命.在石油加工过程中,
依据各成分沸点不同对其进行改造的方法叫做 分馏 .在煤的综合利用中,改变煤的组成
和结构的过程属于 化学 变化.
考点:化石燃料及其综合利用;从组成上识别氧化物;单质和化合物的判别;化学式的书写及
意义;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式;石油加工
的产物.
.
专题:化学与能源;化学用语和质量守恒定律.
分析:(1)从化石燃料主要包括煤、石油和天然气去分析解答.
( 2)从由两种元素组
成的化合物中,其中一种是氧元素的叫做氧化物;由同种元素组成的纯净物叫做单质.
用元素符号和数字的组合表示物质组成的式子叫化学式.根据名称写物质的化学式
时,先读的后写,后读的先写的原则去分析解答.
(3)从由表中可知煤燃烧时生成:二氧化碳、一氧化碳、二氧化硫、二氧化氮、水.根据
质量守恒定律:反应前后元素和种类不变去分析.
(4)从天然气在空气燃烧,其实质是和空气中的氧气反应生成二氧化碳和水去分析解
答;
(5)从在石油加工过程中,通过分馏,依据各成分沸点不同将他们分离,可得到不同的
产品,使石油得到充分利用.煤的综合利用是将煤隔绝空气加强热得到很多有用的物
质,如:焦炭、煤焦油、煤气等,由于产生了新的物质,所以发生的化学变化去分析解
答;
解答:解:(1)化石燃料主要包括煤、石油和天然气.煤是复杂的混合物,主要含有碳元素,此
外还含有氢元素和少量氮、硫、氧等元素以及无机矿物质;石油也是混合物,主要含有
碳元 素和氢元素;天然
气主要是由碳和氢组成的气态碳氢化合物,其中最主要的是甲烷;从石油中得到的石
油产品,汽油、柴油、液化石油气也属于化石燃料;故属于化石燃料的是ABCDF;故答
案为:ABCDF;
(2)由两种元素组成的化合物中,其中一种是氧元素的叫做氧化物;由同种元素组成的纯净物 叫做单质.用
元素符号和数字的组合表示物质组成的式子叫化学式.根据名称写物质的化学式时,
先读的后写,后读的先写的原则.
①二氧化碳由碳、氧两种元素组成,其中一种是氧元素,属于氧化物,根据其名称可知
其化学式为:CO ;故答案为:氧化物 CO ;
2 2
②一氧化碳由碳、氧两种元素组成,其中一种是氧元素,属于氧化物,根据其名称可知
其化学式为:CO;故答案为:一氧化碳 单质;
③碳是由碳元素组成纯净物,属于单质,其化学式用元素符号表示;故答案为:单质;
④二氧化硫由硫、氧两种元素组成,其中一种是氧元素,属于氧化物,根据其名称可知
其化学式为:SO ;故答案为:氧化物 SO ;
2 2
⑤二氧化氮由氮、氧两种元素组成,其中一种是氧元素,属于氧化物,根据其名称可知
其化学式为:NO ;故答案为:氧化物 NO ;
2 2
⑥水由氢、氧两种元素组成,其中一种是氧元素,属于氧化物;故答案为:氧化物;
(3)由表中可知煤燃烧时生成:二氧化碳、一氧化碳、二氧化硫、二氧化氮、水.根据质
量守恒定律:反应前后元素和种类不变.
由反应后的生成 物可
知:生成物中的元素为:C、N、S、H、O,则反应物中也应该由这几种元素组成;由于氧
气是由氧元素组成的,则煤中一定有C、N、S、H四种元素,可能含有氧元素;故答案
为:C、N、S、H 质量守恒定律:反应前后元素的种类不变;
(4)天然气在空气燃烧,其实质是和空气中的氧气反应生成二氧化碳和水,其反应的
化学方程式为:CH +2O CO +2H O;
4 2 2 2
(5)在石油加工过程中,通过分馏,依据各成分沸点不同将他们分离,可得到不同的产
品,使石油得到充分利用.煤的综合利用是将煤隔绝空气加强热得到很多有用的物质,
如:焦炭、煤焦油、煤气等,由于产生了新的物质,所以发生的化学变化;故答案为:分
馏;化学.
点评:石油的分馏属于物理变化,煤的综合利用则是化学变化.
14.(5分)(2014•威海)用科学方法去思考
形成科学认识需要运用一定的科学方法,请回答:
(1)观察、猜想、假设、实验等收集证据的方法是获得感性认识的重要方法.
观察是用感官或借助仪器去获得信息的过程.
猜想是没有事实根据、不知真假的主观猜测,可能会出错,可不去证明,也可能无法证明.
假设是对客观事实的假定性说明.假设必须建立在观察和已有知识经验基础上,能够被检验,
不是对的,就是错的.
下面的5个陈述,来自一位食品与营养化学工作者的笔记.其中,哪个陈述是观察?
(填代号,下同) D ;哪个陈述是猜想? A ;哪个陈述是假设? C .
A、包装良好的食物可以长期储存,不会滋长霉菌
B、在对34名志愿者跟踪和检测后发现,持续一周的饮食为全麦、新鲜蔬菜和水果,可以让每
个人的体重平均减轻1.9Kg
C、如果食物遇到碘水变蓝,那么食物中含有淀粉
D、早餐时,看到一袋胀包的牛奶,打开后,嗅到酸臭味
F、实验表明,橘子、柠檬、草莓中富含维生素C
(2)抽象、归纳、演绎等是理性思维的重要方法.
抽象 是从众多事物中抽取它们共同的本质特征的过程.例如,微观粒子Na+、Mg2+、K+、
NH +共同的本质特征是都带正电荷,这类微观粒子称为阳离子.
4
归纳是根据一系列具体事实概括出一般原理或结论的过程,如你在买樱桃时,先拿几个樱桃
尝一尝,如果都很甜,就能归纳出这份樱桃是甜的.下面的4个陈述,来自某同学的化学笔记.其中,哪个陈述是抽象的? C ;哪个陈述是归
纳? B .
A、重金属盐能使蛋 白质变
性,所以摄入铅对人体有害
B、实验证明,盐酸能跟NaOH反应,也能跟Ca(OH) 反应,所以盐酸能和碱反应
2
C、NaOH、KOH、Ca(OH)都能使酚酞试液变红的本质原因,是它们的溶液中都存在OH﹣,
2
我们把溶于水离解出的阴离子全部是OH﹣的一类化合物称为碱
D、石蕊试液遇到盐酸变红,因为盐酸中有氢离子
考点:生命活动与六大营养素;酸的化学性质;碱的化学性质;中和反应及其应用;常见中毒
途径及预防方法;鉴别淀粉、葡萄糖的方法与蛋白质的性质.
.
专题:物质的微观构成与物质的宏观组成;化学与生活.
分析:根据观察、猜想、假设、实验、抽象、归纳、演绎等说明可以进行相关方面的判断.
解答:解:(1)A、包装良好的食物可以长期储存,不会滋长霉菌,该选项属于猜想;
B、在对34名志愿者跟踪和检测后发现,持续一周的饮食为全麦、新鲜蔬菜和水果,可
以让每个人的体重平均减轻1.9Kg,该选项属于实验;
C、如果食物遇到碘水变蓝,那么食物中含有淀粉,该选项属于假设;
D、早餐时,看到一袋胀包的牛奶,打开后,嗅到酸臭味,该选项属于观察;
F、实验表明,橘子、柠檬、草莓中富含维生素C,该选项属于实验.
故填:D;A;C.
(2)A、重金属盐能使蛋白质变性,所以摄入铅对人体有害,该选项不属于抽象、归纳;
B、实验证明,盐酸能跟NaOH反应,也能跟Ca(OH)反应,所以盐酸能和碱反应,该
2
选项属于归纳;
C、NaOH、KOH、Ca(OH)都能使酚酞试液变红的本质原因,是它们的溶液中都存在
2
OH﹣,我们把溶于水离解出的阴离子全部是OH﹣的一类化合物称为碱,该选项属于抽
象;
D、石蕊试液遇到盐酸变红,因为盐酸中有氢离子,该选项不属于抽象、归纳.
故填:C;B.
点评:本题主要考查对各项叙述的判断能力,要根据提示逐项分析,从而得出正确的结论.
15.(10分)(2014•威海)像科学家一样做科学
﹣﹣探究胡萝卜汁对过氧化氢分解的催化作用
体育课上,小华不慎擦伤了皮肤,她和过氧化氢溶液对皮肤进行消毒时,惊奇地发现有嘶嘶
的响声,并产生大量气泡.
[来源:学科网]
小华通过查阅文献获得以下
信息:
信息Ⅰ:人体皮肤细胞中存在一种叫做过氧化氢酶的物质,能加快过氧化氢分解反应的速率.
信息Ⅱ:胡萝卜汁等植物细胞中也含有过氧化氢酶.
信息Ⅲ:酶是动植物体内活细胞产生的具有催化作用的生物大分子,其催化作用受温度影响.
信息Ⅳ:在没有催化剂时,60℃以下,温度对过氧化氢的分解基本没有影响.
请你在小华的探究的基础上,完成以下探究活动.
(1)胡萝卜汁对过氧化氢的分解是否有催化作用?
[来源:学科网]
请完成下表中的实验报告(实验步骤中应包括使用的仪器、药品和实验过程)
实验步骤 实验现象 实验结论
胡萝卜汁对过氧化氢的分解有催化作用,反应的化学方程
式 2H O 2H O+O ↑
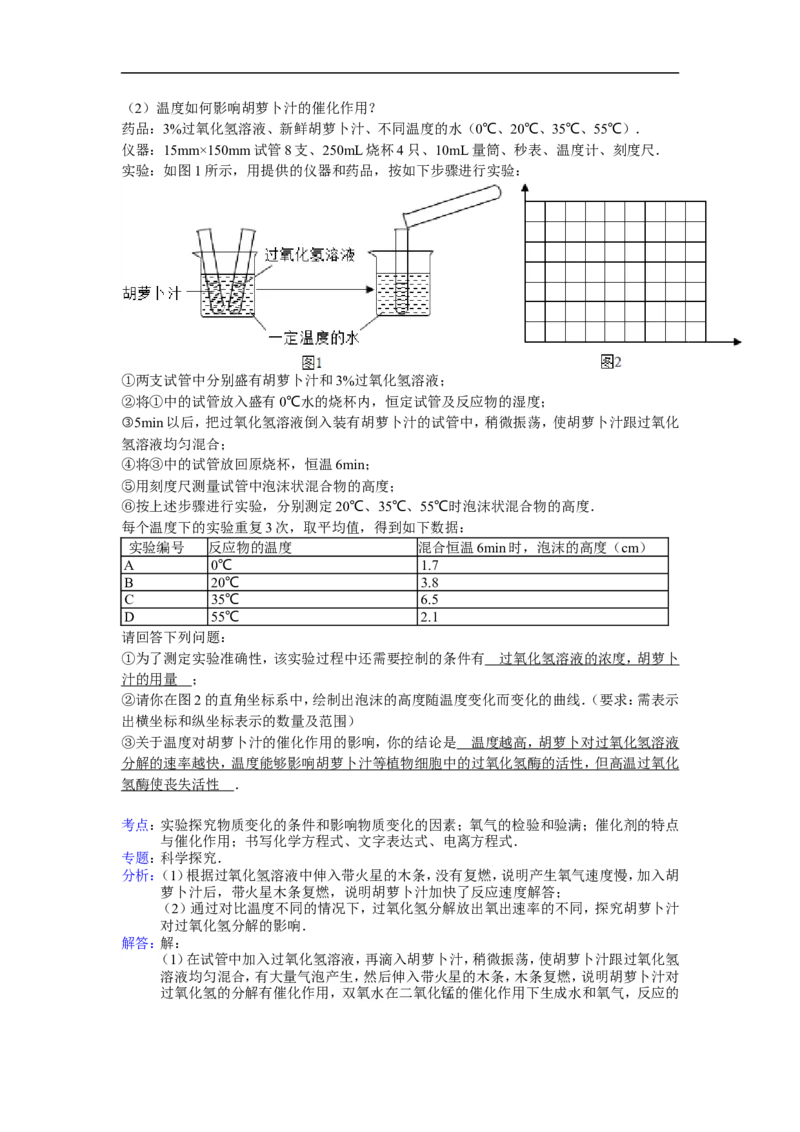
2 2 2 2(2)温度如何影响胡萝卜汁的催化作用?
药品:3%过氧化氢溶液、新鲜胡萝卜汁、不同温度的水(0℃、20℃、35℃、55℃).
[来源:学*科*网Z*X*X*K]
仪器:15mm×150mm试管8支、250mL烧杯4只、10mL量筒、秒表、温度计、刻度尺.
实验:如图1所示,用提供的仪器和药品,按如下步骤进行实验:
①两支试管中分别盛有胡萝卜汁和3%过氧化氢溶液;
②将①中的试管放入盛有0℃水的烧杯内,恒定试管及反应物的湿度;
③5min以后,把过氧化氢溶液倒入装有胡萝卜汁的试管中,稍微振荡,使胡萝卜汁跟过氧化
氢溶液均匀混合;
④将③中的试管放回原烧杯,恒温6min;
⑤用刻度尺测量试管中泡沫状混合物的高度;
⑥按上述步骤进行实验,分别测定20℃、35℃、55℃时泡沫状混合物的高度.
每个温度下的实验重复3次,取平均值,得到如下数据:
实验编号 反应物的温度 混合恒温6min时,泡沫的高度(cm)
A 0℃ 1.7
B 20℃ 3.8
C 35℃ 6.5
D 55℃ 2.1
[来源:学#科#网]
请回答下列问题:
①为了测定实验准确性,该实验过程中还需要控制的条件有 过氧化氢溶液的浓度,胡萝卜
汁的用量 ;
②请你在图2的直角坐标系中,绘制出泡沫的高度随温度变化而变化的曲线.(要求:需表示
出横坐标和纵坐标表示的数量及范围)
③关于温度对胡萝卜汁的催化作用的影响,你的结论是 温度越高,胡萝卜对过氧化氢溶液
分解的速率越快,温度能够影响胡萝卜汁等植物细胞中的过氧化氢酶的活性,但高温过氧化
氢酶使丧失活性 .
考点:实验探究物质变化的条件和影响物质变化的因素;氧气的检验和验满;催化剂的特点
与催化作用;书写化学方程式、文字表达式、电离方程式.
.
专题:科学探究.
分析:(1)根据过氧化氢溶液中伸入带火星的木条,没有复燃,说明产生氧气速度慢,加入胡
萝卜汁后,带火星木条复燃,说明胡萝卜汁加快了反应速度解答;
(2)通过对比温度不同的情况下,过氧化氢分解放出氧出速率的不同,探究胡萝卜汁
对过氧化氢分解的影响.
解答:解:
(1)在试管中加入过氧化氢溶液,再滴入胡萝卜汁,稍微振荡,使胡萝卜汁跟过氧化氢
溶液均匀混合,有大量气泡产生,然后伸入带火星的木条,木条复燃,说明胡萝卜汁对
过氧化氢的分解有催化作用,双氧水在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H O 2H O+O ↑;
2 2 2 2
(2)
①为了测定实验准确性,该实验过程中还需要控制的条件有过氧化氢溶液的浓度,胡
萝卜汁的用量;
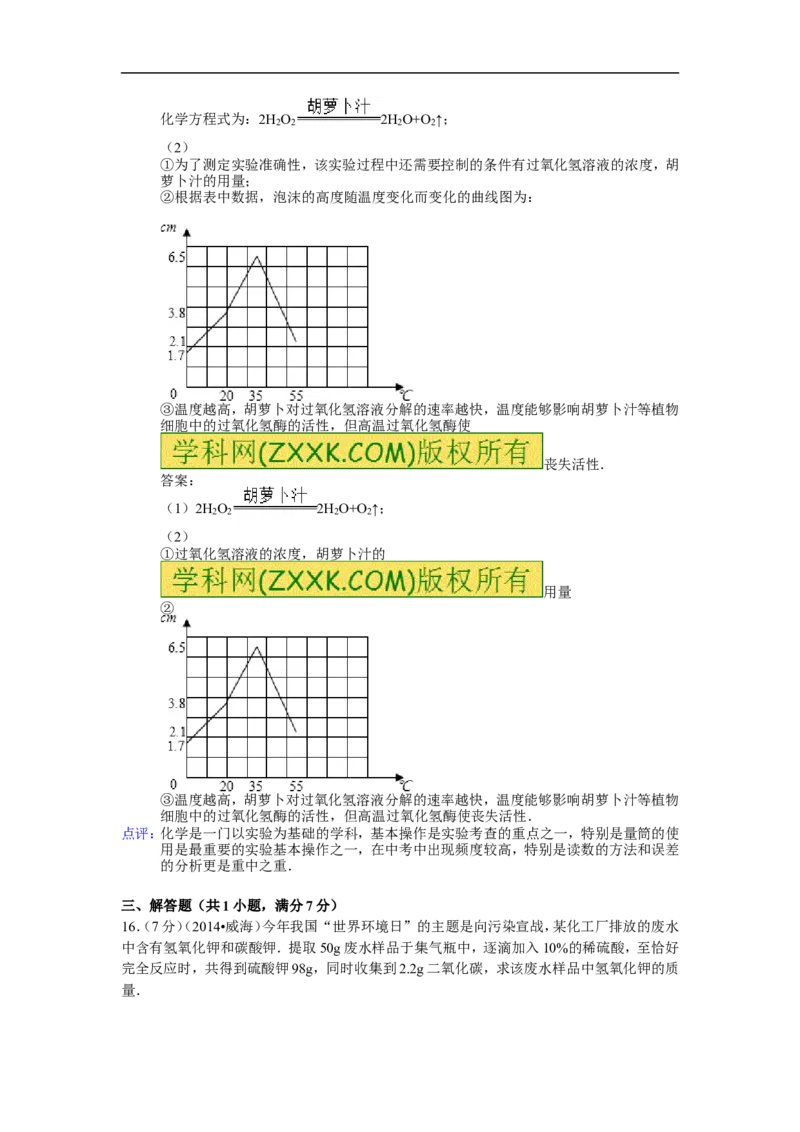
②根据表中数据,泡沫的高度随温度变化而变化的曲线图为:
③温度越高,胡萝卜对过氧化氢溶液分解的速率越快,温度能够影响胡萝卜汁等植物
细胞中的过氧化氢酶的活性,但高温过氧化氢酶使
丧失活性.
答案:
(1)2H O 2H O+O ↑;
2 2 2 2
(2)
①过氧化氢溶液的浓度,胡萝卜汁的
用量
②
③温度越高,胡萝卜对过氧化氢溶液分解的速率越快,温度能够影响胡萝卜汁等植物
细胞中的过氧化氢酶的活性,但高温过氧化氢酶使丧失活性.
点评:化学是一门以实验为基础的学科,基本操作是实验考查的重点之一,特别是量筒的使
用是最重要的实验基本操作之一,在中考中出现频度较高,特别是读数的方法和误差
的分析更是重中之重.
三、解答题(共1小题,满分7分)
16.(7分)(2014•威海)今年我国“世界环境日”的主题是向污染宣战,某化工厂排放的废水
中含有氢氧化钾和碳酸钾.提取50g废水样品于集气瓶中,逐滴加入10%的稀硫酸,至恰好
完全反应时,共得到硫酸钾98g,同时收集到2.2g二氧化碳,求该废水样品中氢氧化钾的质
量.考点:根据化学反应方程式的计算.
.
专题:有关化学方程式的计算.
分析:先利用质量守恒定律计算出反应消耗的稀硫酸的质量,再根据二氧化碳的质量结合化
学方程式计算出废水中碳酸钾消耗的硫酸溶液的质量,利用质量差即可计算出氢氧化
钾消耗的硫酸质量,根据硫酸与氢氧化钾反应的化学方程式即可解答.
解答:解:反应消耗的硫酸质量为:98g+2.2g﹣50g=50.2g
设,碳酸钾消耗的硫酸溶液质量为x,
K CO +H SO =K SO +H O+CO ↑;
2 3 2 4 2 4 2 2
98 44
x•10% 2.2g
x=49g
故氢氧化钾消耗的硫酸溶液质量为:50.2g﹣49g=3.2g
设,废水样品中氢氧化钾的质量为y,
2KOH+H SO =K SO +
2 4 2 4
2H O
2
112 98
y 3.2g×10%
y=0.366g
答:废水样品中氢氧化钾的质量是0.366g;
点评:解答本题的关键是利用质量守恒定律计算出消耗硫酸溶液质量,在利用化学方程式计
算即可.