文档内容
2022年东营市初中学业水平考试
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Cl 35.5 K
39 Ca 40 Se 79
第Ⅰ卷(选择题 共40分)
一、选择题(本题包括12小题,共40分。1至8题每小题3分,9至12题每小题4
分。每小题只有一个选项符合题意)
1.(2022东营,1,3分)生态保护,从我做起。下列做法不合理的是 ( )
A.大力推广使用太阳能
B.出行多骑共享单车
C.少用或不用一次性餐具
D.节日期间大量燃放烟花爆竹
2.(2022东营,2,3分)生活中的下列做法不正确的是 ( )
A.电动车应利用充电桩充电,以免引发火灾
B.不因好奇点燃杨絮柳絮,以免发生危险
C.高层楼房发生火灾时,立即乘电梯逃生
D.避免将燃着的烟头等物品扔进下水道,以免引起爆炸
3.(2022东营,3,3分)正确规范的操作是实验成功和人身安全的重要保证。下列
实验操作正确的是 ( )
A. B.C. D.
4.(2022东营,4,3分)下列所用材料属于有机合成材料的是 ( )
A.陶瓷冰墩墩 B.橡胶冰球
C.碳纤维钢架雪车 D.冬奥奖牌
5.(2022东营,5,3分)广饶花官被誉为“富硒大蒜之乡”,富硒大蒜中的有机硒
主要由硒代蛋氨酸(C H NO Se)合成。关于硒代蛋氨酸,下列说法正确的是 (
5 11 2
)
A.硒是人体必需的微量元素
B.结构中含有NO 分子
2
C.氢元素的质量分数最大
D.硒代蛋氨酸中碳、氢两种元素的质量比为 5∶11
6.(2022东营,6,3分)下列观点不正确的是 ( )
A.自然界中金属多以化合物形式存在,说明多数金属比较活泼
B.不同种元素最本质的区别是质子数不同
C.氧化物中含有氧元素,则氧化物属于含氧化合物
D.催化剂在化学反应前后质量和化学性质不变,因此反应前后质量和化学性质不
变的物质一定是催化剂
7.(2022东营,7,3分)已知过氧化钠(Na O )与水反应生成氢氧化钠和氧气。此反
2 2
应涉及的化学用语表示方法正确的是 ( )A.两个氧分子:2O
B.Na O 中氧的化合价Na -1
2 2 2O
2
C.氢氧化钠由钠离子(Na1+)和氢氧根离子(OH1-)构成
D.此反应的化学方程式:2Na O +2H O 4Na(OH)+O
2 2 2 2
8.(2022东营,8,3分)唐朝炼丹家马和在《平龙认》中指出:阴气(氧气)还存在
于青石、火硝中,用火加热它们,阴气就会放出。火硝的主要成分是KNO ,下列
3
有关KNO 的叙述不正确的是 ( )
3
A.类别:化合物
B.物理性质:难溶于水
C.化学性质:可能发生分解反应
D.用途:可作复合肥料
9.(2022东营,9,4分)为了防止燃气泄漏,常在燃气中加入少量有特殊气味的乙
硫醇(C H SH),一旦燃气泄漏即可闻到气味。乙硫醇在充足的氧气中燃烧时会
2 5
生成一种空气污染物,该气体可能为( )
A.CO B.CO C.SO D.NO
2 2 2
10.(2022东营,10,4分)神舟十三号载人飞船使用的是目前世界上最先进的砷化
镓太阳能电池。砷(As)、镓的原子结构示意图和镓元素在元素周期表中的信息
如下图所示,下列说法不正确的是 ( )
A.砷和镓元素位于同一周期
B.砷化镓的化学式为Ga As
3 5C.镓的相对原子质量为69.72
D.铝原子的最外层电子数为3,铝能与盐酸反应,故镓也可能与盐酸反应
11.(2022东营,11,4分)东营某化工厂产生的污水pH=2,主要污染物是硫酸。现
要将污水调节至接近中性,达标后再排放,下列说法不正确的是 ( )
A.检测:用pH试纸或pH计检测污水的酸碱度
B.原理:处理酸性污水的实质是消耗污水中的氢离子
C.验证:取水样,加入少量氯化钡溶液后出现白色沉淀,证明处理未达标
D.应用:可与造纸厂排放的碱性污水混合,达标后再排放
12.(2022东营,12,4分)中国芯片蚀刻技术国际领先。NF 进行硅芯片蚀刻时的
3
产物均为气体,在蚀刻物表面不留任何残留物。该反应微观示意图如下,下列说
法正确的是( )
A.上述四种物质均由分子构成
B.反应前后各元素的化合价均不变
C.空气中物质丁的质量分数为78%
D.反应生成的丙和丁微粒数之比为3∶2
第Ⅱ卷(非选择题 共60分)
二、填空简答题(本题包括5小题,共36分)
13.(2022东营,13,7分)节假日双休日,买一顶帐篷去野营成为时尚。小东同学
野营中遇到以下问题,该如何处理?(1)若被蚊虫叮咬(蚊虫能分泌出蚁酸),可选用下列 (填序号,下同)物质
涂抹以减轻痒痛。
A.肥皂水 B.食醋
C.食盐水 D.纯碱水
(2)野营食谱如下:面包、羊肉串、豆腐皮、酱牛肉,从均衡饮食角度来看,你认
为食谱还应添加 。
A.炒鸡蛋 B.牛奶
C.水果 D.新鲜蔬菜
(3)野营结束后,为防止引发火灾,小东同学用沙土将所有火源全部盖灭,他利用
的原理是 。
(4)垃圾分类投放已成为生活常态。小东同学捡拾到如下垃圾:废纸、铝制易拉
罐、废电池、矿泉水瓶、骨头,其中废电池应投入的垃圾箱上所印标识是 。
他通过网络发出倡议:“如果没有设置垃圾箱,请大家收拾好垃圾后打包带走,让
我们共建一个美丽、文明的东营!”
A B
C D
14.(2022东营,14,8分)(1)黄河水经沉降、 、吸附、杀菌消毒等净化
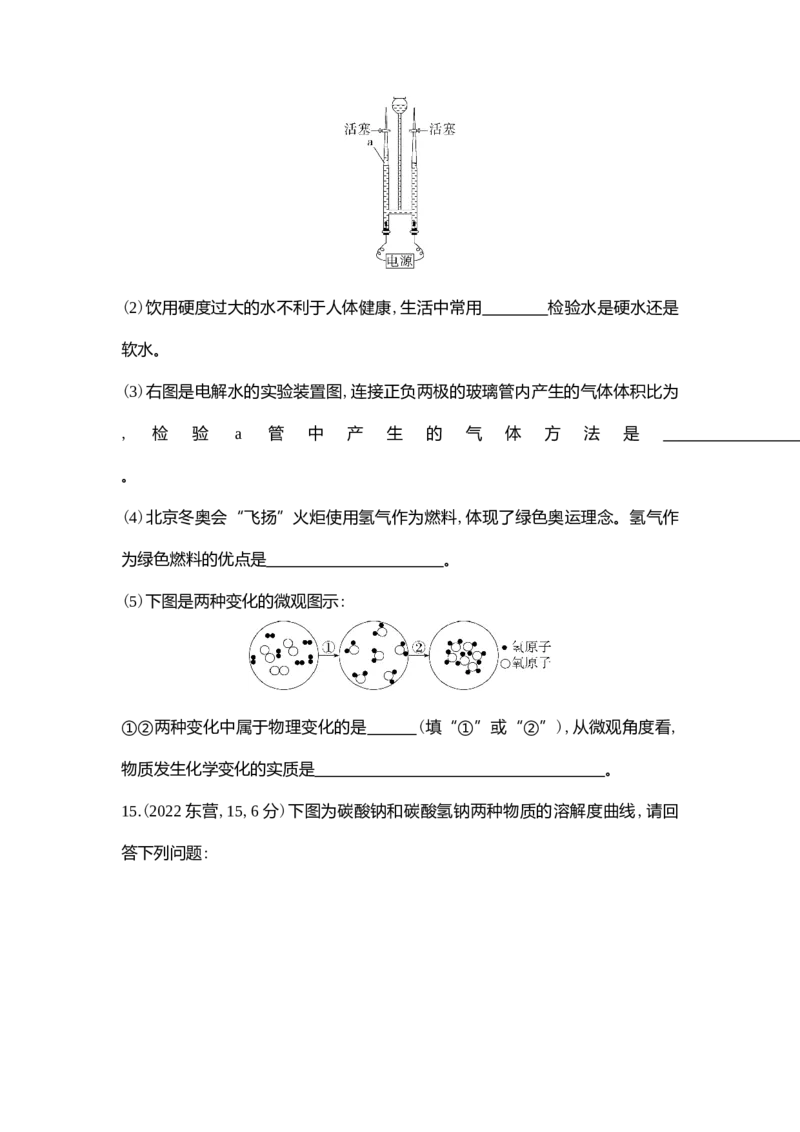
过程可得到自来水。自来水属于 (填“混合物”或“纯净物”)。(2)饮用硬度过大的水不利于人体健康,生活中常用 检验水是硬水还是
软水。
(3)右图是电解水的实验装置图,连接正负两极的玻璃管内产生的气体体积比为
, 检 验 a 管 中 产 生 的 气 体 方 法 是
。
(4)北京冬奥会“飞扬”火炬使用氢气作为燃料,体现了绿色奥运理念。氢气作
为绿色燃料的优点是 。
(5)下图是两种变化的微观图示:
①②两种变化中属于物理变化的是 (填“①”或“②”),从微观角度看,
物质发生化学变化的实质是 。
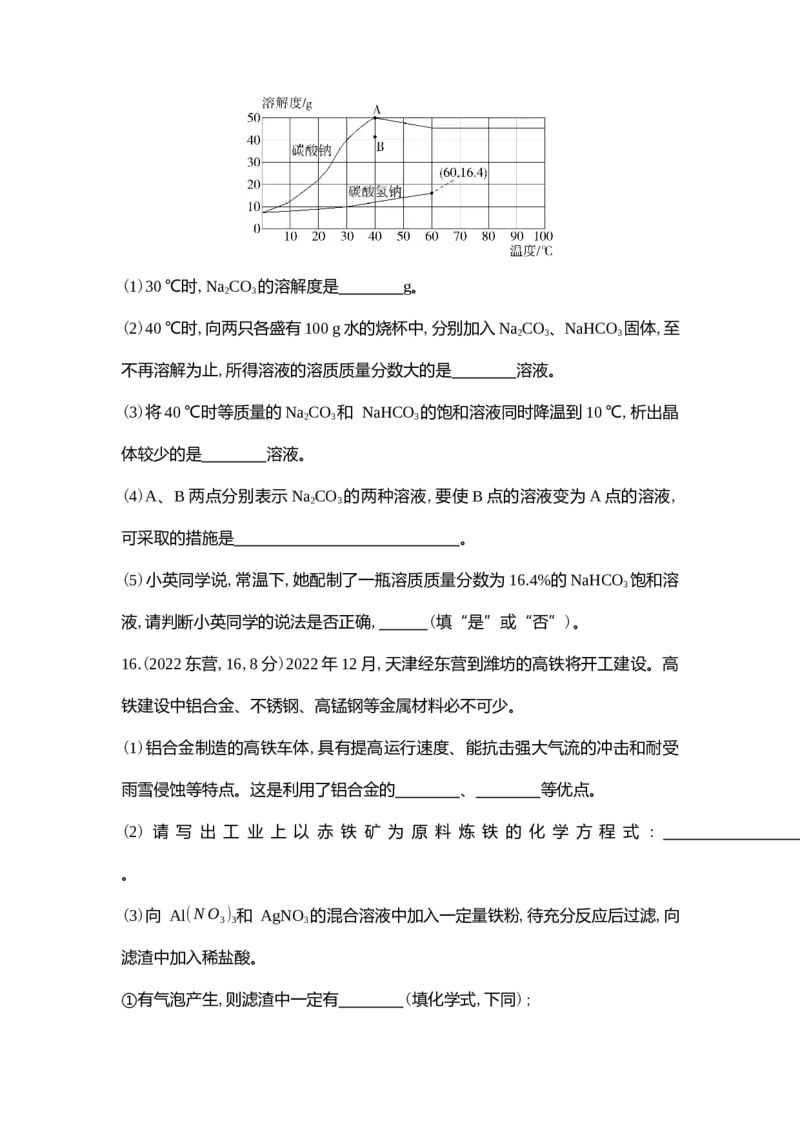
15.(2022东营,15,6分)下图为碳酸钠和碳酸氢钠两种物质的溶解度曲线,请回
答下列问题:(1)30 ℃时,Na CO 的溶解度是 g。
2 3
(2)40 ℃时,向两只各盛有100 g水的烧杯中,分别加入Na CO 、NaHCO 固体,至
2 3 3
不再溶解为止,所得溶液的溶质质量分数大的是 溶液。
(3)将40 ℃时等质量的Na CO 和 NaHCO 的饱和溶液同时降温到10 ℃,析出晶
2 3 3
体较少的是 溶液。
(4)A、B两点分别表示Na CO 的两种溶液,要使B点的溶液变为A点的溶液,
2 3
可采取的措施是 。
(5)小英同学说,常温下,她配制了一瓶溶质质量分数为 16.4%的NaHCO 饱和溶
3
液,请判断小英同学的说法是否正确, (填“是”或“否”)。
16.(2022东营,16,8分)2022年12月,天津经东营到潍坊的高铁将开工建设。高
铁建设中铝合金、不锈钢、高锰钢等金属材料必不可少。
(1)铝合金制造的高铁车体,具有提高运行速度、能抗击强大气流的冲击和耐受
雨雪侵蚀等特点。这是利用了铝合金的 、 等优点。
(2) 请 写 出 工 业 上 以 赤 铁 矿 为 原 料 炼 铁 的 化 学 方 程 式 :
。
(3)向 Al(NO ) 和 AgNO 的混合溶液中加入一定量铁粉,待充分反应后过滤,向
3 3 3
滤渣中加入稀盐酸。
①有气泡产生,则滤渣中一定有 (填化学式,下同);②若没有气泡产生,滤液中一定有的溶质是 。
17.(2022东营,17,7分)海洋是人类巨大的资源宝库,下图为某课题小组模拟从
海水中提取金属镁的简易流程图。
【信息】
某品牌不同碱的价格
试剂 NaOH Ca(OH) KOH
2
价格
(元/吨 3 100 670 7 000
)
请分析:
(1)海水和母液都可以作为制取氯化镁的原料,小真同学提出选择母液更好,小组
同学一致同意他的观点,理由是 。
(2)在工业生产中为了降低成本,步骤Ⅰ中的试剂①最好选择表格中的
。
(3) 步 骤 Ⅱ 由 氢 氧 化 镁 制 得 氯 化 镁 反 应 的 化 学 方 程 式 为
,该反应属于 反应(填基本反应类型)。
(4)在步骤Ⅳ的反应中 能转变成了 能。
三、实验题(本题包括1小题,共15分)
18.(2022 东营,18,15 分)2021 年 12 月 9 日,由航天员王亚平主讲的“天宫课
堂”压轴实验圆满成功。实验中往飘浮在空中的蓝色水球中放入半片泡腾片[主
要成分是柠檬酸(H C H O )和碳酸氢钠],泡腾片与水作用,不断产生小气泡,水
3 6 5 7
球逐渐变大。产生的气泡是什么呢?为什么泡腾片遇到水才产生气泡?【猜想与假设】
小亮同学结合已有知识,判断产生的气泡是 CO ,他的判断依据是
2
。
【设计并进行实验】
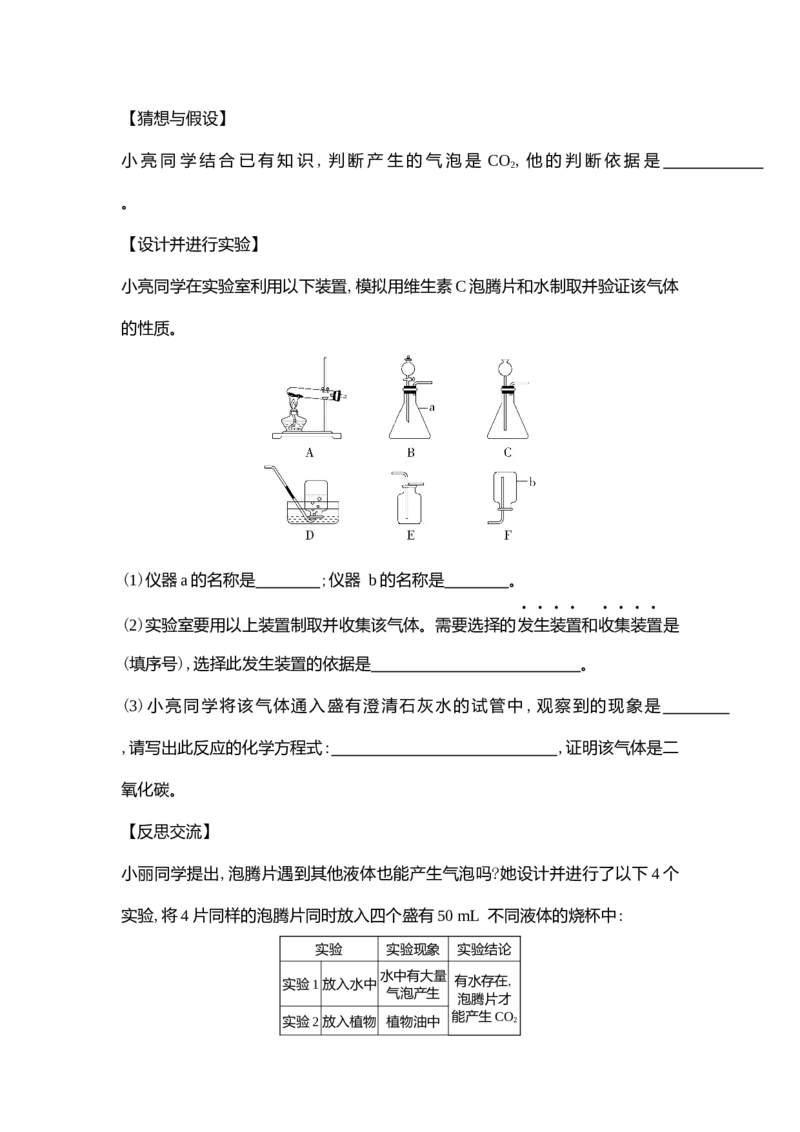
小亮同学在实验室利用以下装置,模拟用维生素C泡腾片和水制取并验证该气体
的性质。
(1)仪器a的名称是 ;仪器 b的名称是 。
(2)实验室要用以上装置制取并收集该气体。需要选择的发生装置和收集装置是
(填序号),选择此发生装置的依据是 。
(3)小亮同学将该气体通入盛有澄清石灰水的试管中,观察到的现象是
,请写出此反应的化学方程式: ,证明该气体是二
氧化碳。
【反思交流】
小丽同学提出,泡腾片遇到其他液体也能产生气泡吗?她设计并进行了以下4个
实验,将4片同样的泡腾片同时放入四个盛有50 mL 不同液体的烧杯中:
实验 实验现象 实验结论
实验1放入水中
水中有大量 有水存在,
气泡产生
泡腾片才
能产生CO
实验2放入植物 植物油中 2油中
放入酒精 酒精中无
实验3
中 明显现象
放入白醋 白醋中
实验4
中
设置实验 1 的目的是 ;通过以上实验你还能得出的结论是
。
【实验启示】
维生素C泡腾片最好 保存。
四、计算题(本题包括1小题,共9分)
19.(2022东营,19,9分)长久使用的花洒、热水壶底部和热水锅炉有一层水垢,
主要成分是碳酸钙和氢氧化镁,用酸溶液可以清除水垢。某兴趣小组的同学为测
定水垢中碳酸钙的含量,向盛有不同质量水垢粉末的烧杯中均加入250 g等浓度
的稀盐酸,充分反应后测得的实验数据如下:
第二
实验组数 第一组 第三组 第四组
组
水垢的质量/g 10 20 30 40
烧杯中剩余物质总质量/g 256.7 263.4 272.3 282.3
(1)第一组实验中所得二氧化碳的质量为 g。
(2)水垢中CaCO 的质量分数(要求写出计算过程)。
3
(3)第三组实验所得溶液的溶质有 。
2022年东营市初中学业水平考试
1.考点:化学与环境、环境污染与防治。
D 大力推广使用太阳能,能减少使用化石能源对环境造成的污染,故A合理。出行多骑共享单
车,能减少化石能源的使用,从而减少环境污染,故B合理。少用或不用一次性餐具,有利于保护环境,故C合理。节日期间大量燃放烟花爆竹,会产生大量的二氧化硫气体,造成环境污染,不利
于生态保护,故D不合理。
2.考点:燃烧与灭火。
C 电动车充电过程中会导致充电器或电瓶温度升高,不合理的充电方式易引起火灾,应利用充
电桩充电,故A正确。杨絮柳絮易燃烧,随意点燃易引发火灾,故B正确。发生火灾时,电梯可能
会断电或因热的作用变形而使人被困在电梯内,故C不正确。下水道中容易产生沼气,将燃着的
烟头等物品扔进下水道,可能会引起沼气燃烧而发生爆炸,故D正确。
3.考点:实验基本技能。
C 给试管中的液体加热时,液体体积不能超过试管容积的三分之一,故A错误。蒸发时,应用玻
璃棒不断搅拌,以防止局部温度过高,造成液滴飞溅,故B错误。闻气体的气味时,应用手在瓶口
轻轻扇动,使极少量的气体飘进鼻子中,不能将鼻子凑到瓶口去闻气体的气味,故C正确。稀释
浓硫酸时,切不可把水注入浓硫酸中,因为浓硫酸的密度比水大,水会浮在浓硫酸上,又由于浓硫
酸溶于水放出大量的热,能使水沸腾,容易造成酸液飞溅;要把浓硫酸缓缓地沿器壁注入水中,同
时用玻璃棒不断搅拌,以使热量及时地扩散,故D错误。
4.考点:有机合成材料。
B 陶瓷不属于有机合成材料,故A错误。橡胶属于有机合成材料,故B正确。碳纤维钢架雪车
所用材料属于复合材料,故C错误。制作冬奥奖牌的金、银、铜属于金属材料,故D错误。
5.考点:化学与生活、化学式及计算。
A 铁、锌、碘、硒等元素属于人体必需的微量元素,故A正确。硒代蛋氨酸是由硒代蛋氨酸分
子构成的,硒代蛋氨酸分子是由碳原子、氢原子、氧原子、氮原子和硒原子构成的,不含有二氧
化氮分子,故 B 错误。硒代蛋氨酸中碳、氢、氮、氧、硒五种元素的质量比为
(12×5)∶(1×11)∶(14×1)∶(16×2)∶(79×1)=60∶11∶14∶32∶79,则硒代蛋氨酸中硒元素的质量分数最大,
故C错误。硒代蛋氨酸中碳、氢元素的质量比为(12×5)∶(1×11)=60∶11,故D错误。
6.考点:物质的分类、元素与元素周期表。
D 自然界中的金属除金、银、铂等外,大多以化合物的形式存在,故A正确。决定元素种类的
是质子数或核电荷数,不同种元素的本质区别是质子数或核电荷数不同,故B正确。氧化物一定
是含氧化合物,含氧化合物不一定是氧化物,如碳酸钠、硫酸铜中含有氧元素,但不是氧化物,故
C正确。反应前后质量和化学性质不变的物质不一定是催化剂,也可能是没有参加反应的杂质,
故D不正确。
7.考点:化学符号周围数字的意义、化学方程式。
B 2O表示2个氧原子,2个氧分子表示为2O,故A错误。在NaO 中,钠元素的化合价为+1价,
2 2 2
根据化合物中各元素正负化合价的代数和为零,可计算出氧元素的化合价为-1价,化合价标在元
素符号的上方,正负号在前、数字在后,表示为Na -1 ,故B正确。氢氧化钠是由钠离子(Na+)和
2O
2
氢氧根离子(OH-)构成的,故C错误。化学式中原子团的个数为1时不需要加括号;化学方程式
中生成物中有气体且反应物中无气体时,气体的后面要标注“↑”,则过氧化钠和水反应的化学方
程式为2NaO+2HO 4NaOH+O↑,故D错误。
2 2 2 2
8.考点:化学肥料、物质的性质与用途。
B 硝酸钾是由钾元素、氮元素和氧元素组成的纯净物,属于化合物,故A正确。硝酸钾易溶于
水,故B不正确。加热火硝会产生氧气,故C正确。硝酸钾中含有氮元素和钾元素,属于复合肥
料,故D正确。
9.考点:质量守恒定律。C 乙硫醇中含有碳元素、氢元素和硫元素,氧气充足时,乙硫醇会完全燃烧,产生二氧化碳、水
和二氧化硫,不会产生一氧化碳,故A错误。二氧化碳不是空气污染物,故B错误。二氧化硫属
于空气污染物,故C正确。乙硫醇中不含有氮元素,燃烧不会产生二氧化氮气体,故D错误。
10.考点:元素周期表。
B 砷元素和镓元素都位于元素周期表第四周期,故A正确。砷原子和镓原子的最外层电子数分
别为5和3,在化学反应中分别易得到3个电子和失去3个电子,可得砷化镓的化学式为GaAs,故
B不正确。元素周期表单元格中,汉字下面的数字表示相对原子质量,则镓的相对原子质量为
69.72,故C正确。最外层电子数相同,化学性质相似,铝原子和镓原子的最外层电子数都是3,则
镓也可能和盐酸反应,故D正确。
11.考点:酸碱度(pH)、中和反应。
C 一般用pH试纸或pH计测定液体的酸碱度,故A正确。酸性溶液中含有氢离子,处理酸性污
水的实质是消耗污水中的氢离子,故B正确。硫酸根离子能和钡离子结合生成硫酸钡白色沉淀,
因此加入氯化钡溶液产生白色沉淀不能证明污水处理未达标,故C不正确。酸、碱能发生中和
反应,因此可将酸性污水和碱性污水混合,达中性后再排放,故D正确。
12.题型:图表分析题。
D 通过反应的微观示意图,可得出该反应的化学方程式为4NF+3Si 3SiF↑+2N↑。乙
3 4 2
物质(Si)是由硅原子构成的,其他三种物质是由分子构成的,故A错误。该反应属于置换反应,反
应前后一定有元素化合价发生改变,故B错误。丁物质为氮气,空气中氮气的体积分数为78%,
故C错误。由反应的化学方程式可知,反应生成的丙和丁的微粒数之比为3∶2,故D正确。
13.考点:中和反应、燃烧与灭火、化学与生活。
答案 (1)AD (2)CD (3)隔绝氧气 (4)B
解析 (1)蚁酸呈酸性,应用碱性物质中和以减轻痒痛。肥皂水和纯碱水显碱性,食醋显酸性,食
盐水显中性,故选A、D。(2)面包中富含淀粉,淀粉属于糖类;豆腐皮和酱牛肉中富含蛋白质;羊
肉串中富含蛋白质和油脂,因此食谱中缺少的营养物质是维生素。炒鸡蛋中富含蛋白质和油脂,
牛奶中富含蛋白质,水果和新鲜蔬菜中富含维生素,故选C、D。(3)灭火原理:①清除或隔离可
燃物;②隔绝氧气或空气;③使温度降到可燃物的着火点以下。用沙土覆盖火源,可使火源与氧
气隔绝,从而达到灭火的目的。(4)废旧电池中含有重金属离子,属于有害垃圾。
14.考点:自然界的水、化学与能源、物质的变化和性质。
答案 (1)过滤 混合物 (2)肥皂水 (3)1∶2 将带火星的木条放在a管口,观察到带火星的木
条复燃,证明该气体是氧气 (4)燃烧只生成水,无污染 (5)② 分子分成原子,原子重新结合成
新的分子
解析 (1)黄河水通过沉降(除去大颗粒杂质)、过滤(除去不溶性杂质)、吸附(除去颜色和异味)、
杀菌消毒(除去微生物)等净化过程可得到自来水;自来水中还含有可溶性杂质,属于混合物。(2)
检验硬水和软水用肥皂水,加入肥皂水,振荡,产生泡沫多、浮渣少的为软水,产生泡沫少、浮渣
多的为硬水。 (3)电解水实验中正极产生氧气,负极产生氢气,氧气和氢气的体积比为1∶2;a管中
产生的是氧气,氧气具有助燃性,检验方法是将带火星的木条放在a管口,观察到带火星的木条复
燃,证明该气体是氧气。(4)氢气燃烧只生成水,无污染,因此可作为绿色燃料。(5)①变化中分
子发生了改变,属于化学变化;②变化中分子不变,只是分子之间的间隔和排列方式发生了改变,
属于物理变化;从微观角度看,物质发生化学变化的实质是分子分成原子,原子重新结合成新的分
子。
15.考点:溶解度及溶解度曲线。
答案 (1)40 (2)碳酸钠 (3)碳酸氢钠 (4)加入碳酸钠(合理即可) (5)否解析 (1)观察碳酸钠的溶解度曲线可知,30 ℃时碳酸钠的溶解度是40 g。(2)饱和溶液中溶质质
溶解度
量分数= ×100%,40 ℃时碳酸钠的溶解度大于碳酸氢钠的溶解度,则所得溶液
100 g+溶解度
的溶质质量分数大的是碳酸钠溶液。(3)40 ℃时,分别将相同质量的碳酸钠、碳酸氢钠的饱和溶
液降温到10 ℃,碳酸氢钠的溶解度受温度的影响变化小,故析出晶体较少的是碳酸氢钠溶液。
(4)B点表示40 ℃时碳酸钠的不饱和溶液,A点表示40 ℃时碳酸钠的饱和溶液,则B溶液变为A
溶液的方法可以是加入碳酸钠。(5)常温下,碳酸氢钠的溶解度小于10 g,其溶液的溶质质量分数
10 g
小于 ×100%≈9.1%,则小英不可能配制出16.4%的碳酸氢钠溶液。
100 g+10 g
16.考点:金属材料、金属资源的冶炼和利用、金属的化学性质。
答案 (1)密度小 耐腐蚀(合理即可) (2)3CO+FeO 2Fe+3CO (3)①Fe、Ag
2 3 2
②Al(NO)、Fe(NO)
3 3 3 2
解析 (1)根据题干信息“提高运行速度”“能抗击强大气流的冲击”和“耐受雨雪侵蚀”可知,
这是利用了铝合金的密度小、强度大、耐腐蚀等优点。(2)赤铁矿的主要成分为氧化铁,用赤铁
矿炼铁的化学方程式为3CO+FeO 2Fe+3CO。(3)①铁不能和硝酸铝反应,但能置换出硝酸
2 3 2
银中的银,银不能和稀盐酸反应;向滤渣中滴加稀盐酸时有气泡产生,是因为铁和稀盐酸反应生成
了氢气,即铁过量,则滤渣中一定含有Fe、Ag。②若滤渣中加入稀盐酸后无气泡产生,说明没有
铁剩余,滤渣中只有银;因为硝酸铝与铁不反应,所以反应后的溶液中一定含有硝酸铝;铁能与硝
酸银发生置换反应生成硝酸亚铁和银,则滤液中一定含有硝酸亚铁;硝酸银是否完全反应不能确
定,则滤液中一定含有的溶质是Al(NO)、Fe(NO),可能含有AgNO。
3 3 3 2 3
17.题型四:工艺流程题。
答案 (1)母液中氯化镁的浓度大,生产效率高 (2)Ca(OH) (3)Mg(OH)+2HCl
2 2
MgCl+2HO 复分解 (4)电 化学
2 2
解析 (1)海水晒盐后所得的母液中氯化镁的浓度比海水高,用母液制取氯化镁时生产效率更高。
(2)氢氧化钙的价格最便宜,所以最好选择氢氧化钙。(3)由氢氧化镁制氯化镁,加入的试剂是稀
盐酸,反应的化学方程式为Mg(OH)+2HCl MgCl+ 2HO,该反应是两种化合物相互交换成
2 2 2
分生成两种新的化合物的反应,属于复分解反应。(4)步骤Ⅳ是氯化镁在通电的条件下生成氯气
和金属镁,反应中电能转变成了化学能。
18.考点:常见气体的制备、实验方案的设计与评价。
答案 【猜想与假设】碳酸氢钠能和酸反应产生二氧化碳气体
【设计并进行实验】(1)锥形瓶 集气瓶 (2)BE或CE 所用试剂是固体和液体,反应不需要
加热
(3)石灰水变浑浊 CO+Ca(OH) CaCO↓+HO
2 2 3 2
【反思交流】无明显现象 有大量气泡产生 对照 维生素C泡腾片不溶于植物油和酒精
【实验启示】密封
解析 【猜想与假设】碳酸氢钠能和酸反应产生二氧化碳气体,柠檬酸属于酸,则可判断产生的
气体是二氧化碳。
【设计并进行实验】(2)维生素C泡腾片为固体,水为液体,且反应不需要加热,则发生装置选B
或C;二氧化碳密度比空气大且能溶于水,则收集装置选E。(3)检验二氧化碳的方法是将气体通入澄清石灰水中,石灰水变浑浊,则气体为二氧化碳,反应的化学方程式为CO+Ca(OH)
2 2
CaCO↓+HO。
3 2
【反思交流】实验结论是有水存在才能产生二氧化碳,植物油和酒精中无水存在,则泡腾片放入
植物油和酒精中都无明显现象;白醋中含有水,且醋酸也能和碳酸氢钠反应产生二氧化碳,则泡腾
片放入白醋中会产生大量气泡。设置实验1的目的是起对照作用;通过实验还可以得出维生素C
泡腾片不溶于植物油和酒精。
【实验启示】维生素C泡腾片接触水会发生化学反应,所以最好密封保存。
19.题型 5:化学计算题。
答案 (1)3.3
(2)解:设第一组水垢中碳酸钙的质量为x。
CaCO+2HCl CaCl+HO+CO↑
3 2 2 2
100 44
x 3.3 g
100∶44=x∶3.3 g
x=7.5 g
7.5 g
水垢中碳酸钙的质量分数为 ×100%=75%
10 g
答:水垢中碳酸钙的质量分数为75%。
(3)CaCl、MgCl
2 2
解析 (1)第一组实验中,产生二氧化碳的质量为10 g+250 g-256.7 g=3.3 g。(2)根据题表数据可
知,第一组和第二组实验中,稀盐酸过量,碳酸钙完全反应,根据反应生成CO 的质量即可求出
2
CaCO 的质量,进而求出碳酸钙的质量分数。(3)第三组实验中30 g水垢参加反应,但只产生了
3
7.7 g二氧化碳气体,说明水垢过量,稀盐酸完全反应,则溶液中的溶质有氯化钙和氯化镁。