文档内容
绝密★启用前
2024 年中考押题预测卷 02【南京卷】
C. 加入稀硫酸 D. 收集氢气
化 学
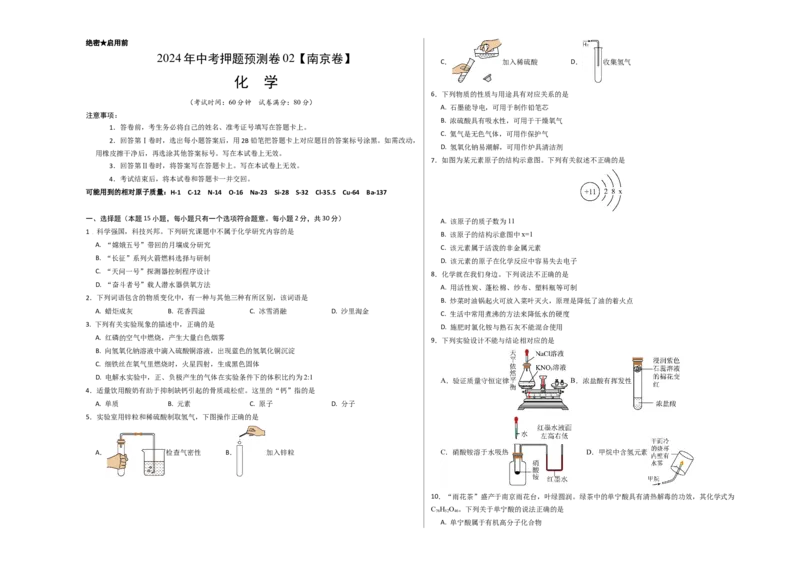
6.下列物质的性质与用途具有对应关系的是
(考试时间:60分钟 试卷满分:80分)
A. 石墨能导电,可用于制作铅笔芯
注意事项:
B. 浓硫酸具有吸水性,可用于干燥氧气
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
C. 氦气是无色气体,可用作保护气
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
D. 氢氧化钠易潮解,可用作炉具清洁剂
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
7.如图为某元素原子的结构示意图。下列有关叙述不正确的是
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Si-28 S-32 Cl-35.5 Cu-64 Ba-137
一、选择题(本题15小题,每小题只有一个选项符合题意。每小题2分,共30分)
A. 该原子的质子数为11
1.科学强国,科技兴邦。下列研究课题中不属于化学研究内容的是
B. 该原子的结构示意图中x=1
A. “嫦娥五号”带回的月壤成分研究
C. 该元素属于活泼的非金属元素
B. “长征”系列火箭燃料选择与研制
D. 该元素的原子在化学反应中容易失去电子
C. “天问一号”探测器控制程序设计
8.化学就在我们身边。下列说法不正确的是
D. “奋斗者号”载人潜水器供氧方法
A. 用活性炭、蓬松棉、纱布、塑料瓶等可制
2.下列词语包含的物质变化中,有一种与其他三种有所区别,该词语是
B. 炒菜时油锅起火可放入菜叶灭火,原理是降低了油的着火点
A. 蜡炬成灰 B. 花香四溢 C. 冰雪消融 D. 沙里淘金
C. 生活中常用煮沸的方法来降低水的硬度
3. 下列有关实验现象的描述中,正确的是
D. 施肥时氯化铵与熟石灰不能混合使用
A. 红磷的空气中燃烧,产生大量白色烟雾
9.下列实验设计不能与结论相对应的是
B. 向氢氧化钠溶液中滴入硫酸铜溶液,出现蓝色的氢氧化铜沉淀
C. 细铁丝在氧气里燃烧时,火星四射,生成黑色固体
D. 电解水实验中,正、负极产生的气体在实验条件下的体积比约为2:1
A.验证质量守恒定律 B.浓盐酸有挥发性
4.适量饮用酸奶有助于抑制缺钙引起的骨质疏松症。这里的“钙”指的是
A. 单质 B. 元素 C. 原子 D. 分子
5.实验室用锌粒和稀硫酸制取氢气,下图操作正确的是
A. 检查气密性 B. 加入锌粒 C.硝酸铵溶于水吸热 D.甲烷中含氢元素
10.“雨花茶”盛产于南京雨花台,叶绿圆润。绿茶中的单宁酸具有清热解毒的功效,其化学式为
C H O 。下列关于单宁酸的说法正确的是
76 52 46
A. 单宁酸属于有机高分子化合物………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
B. 单宁酸中氧元素的质量分数大于碳元素的质量分数 15.Cu O能与硫酸反应生成CuSO 和Cu。用下图装置研究高温下木炭与CuO的反应产物。下列说法不正
2 4
C. 单宁酸中碳、氢、氧三种元素质量比为76∶52∶46 确的是
D. 一个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成
此
11.分析和推理是化学学习中常用的思维方法。下列因果关系完全正确的一组是
A. 中和反应生成盐和水,则有盐和水生成的反应一定是中和反应
卷
B. 催化剂能改变化学反应速率,则能改变化学反应速率的物质一定是催化剂
只
C. 碱能使酚酞溶液变红,碳酸钾能使酚酞溶液变红,则碳酸钾一定属于碱
D. 化合物由不同种元素组成,则不同种元素组成的纯净物一定是化合物
装
A. 装置②用于检验是否有CO 生成
2
12.下列实验设计不能达到实验目的的是
B. 装置③、④的作用是除去CO 和水蒸气
2 订 A. 用pH试纸检验溶液的酸碱性
C. 装置⑤中黑色固体变红,装置⑥中石灰水变浑浊,说明产物中有CO
B. 闻气味鉴别浓硫酸和稀硫酸
不
D. 一段时间后,取少量装置①中固体加入稀硫酸,振荡后溶液变蓝,说明产物中有Cu O
2
C. 冷却热饱和溶液自制白糖晶体
二、(本题包括2小题,除标注外,每空1分,共17分)
密
D. 加熟石灰研磨鉴别氯化钾和氯化铵
16. (9分)研究气体的制备及相关气体的性质。
13.我国科学家实现了从二氧化碳到葡萄糖和油脂的人工合成,合成过程中的一个反应的微观示意图如下。
封
(1)请根据所提供的试剂和仪器(铁架台、陶土网等已省略),按要求填空。
下列有关说法正确的是
试剂:稀盐酸、稀硫酸、过氧化氢溶液,块状大理石、二氧化锰
A. 甲和丙属于有机物
B. 乙和丁中氧元素的化合价均为-2价
①实验室制取氧气时,为了便于获得平稳的气流,发生装置可选用图中的______(填字母),反应的化
C. 参加反应的甲与生成的丙的质量之比为14∶15
学方程式为______。
D. 参加反应的乙和生成丁的分子个数之比为1∶1
②用提供的试剂还可以制取另一种气体,反应的化学方程式为_______。
14.下列实验操作不能达到实验目的的是
(2)下图为木炭燃烧的实验。
选 目
物质 主要实验操作
项 的
鉴 取少量样品于燃烧匙中,在酒精灯火焰上加
A 蔗糖和食盐
别 热,观察现象
除
B FeSO 溶液中混有CuSO 加入过量的铁粉,充分反应后过滤
4 4
杂
①对比Ⅰ和Ⅱ的现象,得出可燃物燃烧的条件之一是______。
分 加入过量NaCO 溶液,过滤、洗涤,向所得
2 3
C NaCl和CaCl 混合溶液 ②对比Ⅱ和Ⅲ的现象,得出可燃物燃烧的剧烈程度与______有关。
2 离 固体中加适量稀盐酸
③请设计实验验证Ⅲ中燃烧产物含CO 并完成实验报告。
2
检 取样,先加入过量稀盐酸,再滴入BaCl 溶
2
D NaCO 溶液是否含有NaSO 实验操 实验现
2 3 2 4
验 液,观察现象 实验结论
作 象
A. A B. B C. C D. D
______ ______ 木炭在氧气中燃烧产物含
试题 第27页(共48页) 试题 第28页(共48页)(3)某工厂化验室用10%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液40
CO
2
g,洗涤后的溶液呈中性。这一定量石油产品中含硫酸的质量是多少?(在答题卡上写出计算过程)
17.(8分)宏微相结合是认识物质结构与性质的重要方法。 19.(7分)像科学家一样“做科学”——探秘金属的活动性顺序:
(1)下图为部分元素的原子结构示意图。 某研究小组为验证铁、铜、锌、银的金属活动性顺序,设计如图甲所示三个实验(三种金属均已用砂纸打
磨过,其形状和大小相同,稀盐酸的浓度和用量也相同)。
①氦元素与镁元素化学性质 (填“相似”或“不相似”)。
②钠原子在形成化合物时,易失去最外层的电子,形成的阳离子是 (填粒子符号)。 (1)实验前用砂纸打磨金属的目的是______。
③写出二氧化硅中硅元素的化合价 。 (2)一段时间后,观察到B试管中的实验现象为______,该反应的化学方程式为:______。
(2)从陶瓷、玻璃到电子芯片,硅元素用途非常广泛。工业制取高纯硅的部分反应原理示意图如图所示。 (3)甲同学认为通过实验A和C可比较锌和铁的金属活动性,他依据的实验现象是______。
(4)乙同学认为仅仅通过上述实验不足以得出四种金属的活动性顺序,因此在上述实验的基础上,乙同
学又补做了一个实验,装置如图乙所示,且实现了探究目的。乙同学的实验:X、Y物质分别为:
______。
①该化学反应中,没有发生变化的是 (填“分子”或“原子”),反应生成的副产品丁的溶液有很
多用途,下列不属于丁溶液用途的是 (填字母)。
A.除铁锈 B.制药物 C.干燥剂
②写出该反应的化学方程式 ;反应中,甲、乙物质的分子个数比为 。
【拓展与延伸】
三、(本题包括2小题,共16分)
(5)好奇地小华在老师的指导下,把一定量的锌粒加入硫酸铜和硝酸银的混合溶液中,充分反应一段时
18.(9分)溶液在生产生活中有重要的用途。
间后,过滤,发现滤液呈无色,此时,滤渣中一定含有______。
(1)稀盐酸可用于除铁锈。稀盐酸中的溶质是___________(填名称)。 四、(本题包括1小题,化学方程式2分,共7分)
(2)甲、乙是两种不含结晶水的固体物质,请结合图1、图2,回答下列问题。
20. (7分)图中A~I表示初中化学常见的物质。A是单质;G是氧化物,呈黑色,其中氧元素的质量分数为
20%;D俗称纯碱;E是生物体中含量最多的物质;H常用于改良酸性土壤。图中“—”表示两端的物质
间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物或生成物已略去。
①t ℃时,乙饱和溶液中溶质和溶液的质量比为___________(填最简整数比)。
1
②将t ℃时甲、乙两种物质的饱和溶液分别升温至t ℃,所得两种溶液的溶质质量分数的关系为
2 3
___________(填字母)。
A.甲 > 乙 B.甲 = 乙 C.甲 < 乙 D.无法比较
③某同学按图2所示步骤进行实验。下列说法正确的是___________(填字母)。
A.I中溶液是t ℃时甲的不饱和溶液 B.I中甲的质量分数为15% (1)写出化学式:B______,D______。
2
C.Ⅱ中溶液是t ℃时甲的不饱和溶液 D.Ⅲ中有10 g甲的晶体析出 (2)写出A与G反应的化学方程式______。
3
(3)写出I→D反应的化学方程式______。………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
(4)E→H的基本反应类型是______。 实验验证:小组的同学利用数字化传感器探究样品的成分。取少量样品于试管中,加入一定量的稀盐酸,
五、实验探究题(本大题共1小题,每空1分,共10分。) 测得体系中溶解氧、pH及CO 体积分数的数据如图。
2
21.(10分)牙膏是人们生活中不可缺少的必需品,某化学小组对牙膏展开探究。
此
某品牌牙膏主要成分:水、水合硅石、碳酸氢钠、香精、焦磷酸四钠、珍珠粉(含蛋白质、碳酸钙、多
种微量元素)等。
卷
【摩擦剂】牙膏中摩擦剂的作用是通过摩擦去除食物残渣、牙渍、牙菌斑等。常用摩擦剂有水合硅石、
(8)小凌同学分析实验数据后认为样品固体中一定有CaO、Ca(OH) 、CaCO 。小静同学认为该结论不
碳酸钙等。 2 2 3 只
正确,请结合图中数据分析,结论不正确的原因是________。
(1)根据以上信息推测水合硅石可能的物理性质有________(写1条)。
(9)由于CaO 易变质影响牙膏的保质期,不慎吞服后,会对口腔黏膜、食道等造成伤害,因此现在牙 装
【酸碱度调节剂】研究表明,口腔中pH在6.6~7.1有利于维持口腔生态平衡,若pH过低易导致牙齿持 2
膏中常加入二氧化钛、焦磷酸盐等其他美白成分。分析本题中介绍的牙膏成分,其中具有美白作用的物
续脱矿引发龋齿等疾病,在牙膏中添加NaHCO 3 等物质可调节口腔酸碱度。 订
质可能是________。
不
密
封
(2)某小组同学用如图装置测定某品牌牙膏中NaHCO 的质量分数。结合图中数据,计算牙膏样品中 3
NaHCO 的质量分数(写出计算过程)________。
3
(3)用该方法测得的NaHCO 质量分数偏大的原因可能是_______。(填一点)
3
【美白剂】牙膏中添加过氧化钙(CaO)可除去吸附在牙齿微孔中的有色物质,美白牙齿。
2
资料:①氨气极易溶于水;②2CaO+2H O=2Ca(OH) +O↑
2 2 2 2
I.CaO 的制备:实验室可用如图装置制备CaO。
2 2
向CaCl 溶液中加入30%的HO 溶液,通入氨气,反应生成CaO·8H O晶体,脱水后得到CaO 固体。反
2 2 2 2 2 2
应原理:CaCl +HO+2NH ·HO=CaO·8H O+2NH Cl
2 2 2 3 2 2 2 4
(4)a的仪器名称为________,长颈漏斗的作用________。
(5)甲中发生反应的化学方程式为________。
(6)乙中反应时常用冰水浴控制温度在0℃左右,目的可能是________。
(7)反应结束后,经过滤、洗涤、低温烘干可获得CaO·8H O。检验CaO·8H O是否洗涤干净的方法是:
2 2 2 2
取最后一次洗涤滤液,________。
II.CaO 的变质:
2
提出猜想:久置CaO样品的成分可能为CaO、Ca(OH) 、CaCO 中的一种或多种。
2 2 3
试题 第47页(共48页) 试题 第48页(共48页)