文档内容
人教版九年级上册化学期末考试推断题专项训练Ⅱ
参考答案及解析
一、推断题。
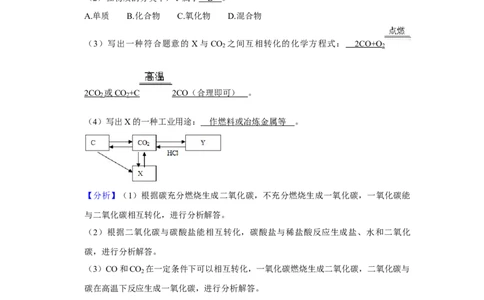
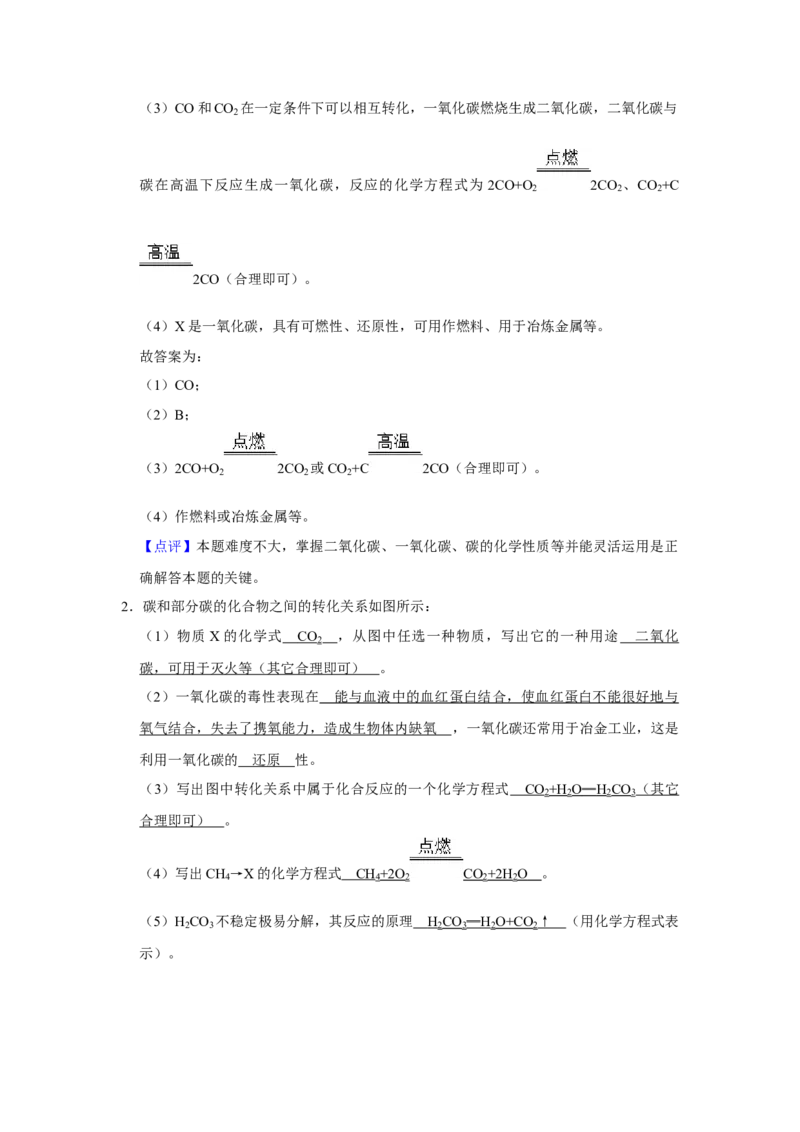
1.碳和部分碳的化合物间转化关系如图所示:
(1)物质X的化学式为 CO 。
(2)在物质的分类中,Y属于 B 。
A.单质 B.化合物 C.氧化物 D.混合物
(3)写出一种符合题意的 X与CO 之间互相转化的化学方程式: 2CO+O
2 2
2CO 或 CO +C 2CO (合理即可) 。
2 2
(4)写出X的一种工业用途: 作燃料或冶炼金属等 。
【分析】(1)根据碳充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳,一氧化碳能
与二氧化碳相互转化,进行分析解答。
(2)根据二氧化碳与碳酸盐能相互转化,碳酸盐与稀盐酸反应生成盐、水和二氧化
碳,进行分析解答。
(3)CO和CO 在一定条件下可以相互转化,一氧化碳燃烧生成二氧化碳,二氧化碳与
2
碳在高温下反应生成一氧化碳,进行分析解答。
(4)X是一氧化碳,具有可燃性、还原性,进行分析解答。
【解答】解:(1)碳充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳,一氧化碳能
与二氧化碳相互转化,X是碳,其化学式为CO。
(2)二氧化碳与碳酸盐能相互转化,如碳酸钙,二氧化碳与碳酸钙能相互转化,碳酸
钙与稀盐酸反应生成氯化钙、水和二氧化碳,Y是碳酸钙等碳酸盐,在物质的分类中,
碳酸钙等碳酸盐是由不同种元素组成的纯净物,属于化合物,含有三种元素,不属于氧
化物。(3)CO和CO 在一定条件下可以相互转化,一氧化碳燃烧生成二氧化碳,二氧化碳与
2
碳在高温下反应生成一氧化碳,反应的化学方程式为 2CO+O 2CO 、CO +C
2 2 2
2CO(合理即可)。
(4)X是一氧化碳,具有可燃性、还原性,可用作燃料、用于冶炼金属等。
故答案为:
(1)CO;
(2)B;
(3)2CO+O 2CO 或CO +C 2CO(合理即可)。
2 2 2
(4)作燃料或冶炼金属等。
【点评】本题难度不大,掌握二氧化碳、一氧化碳、碳的化学性质等并能灵活运用是正
确解答本题的关键。
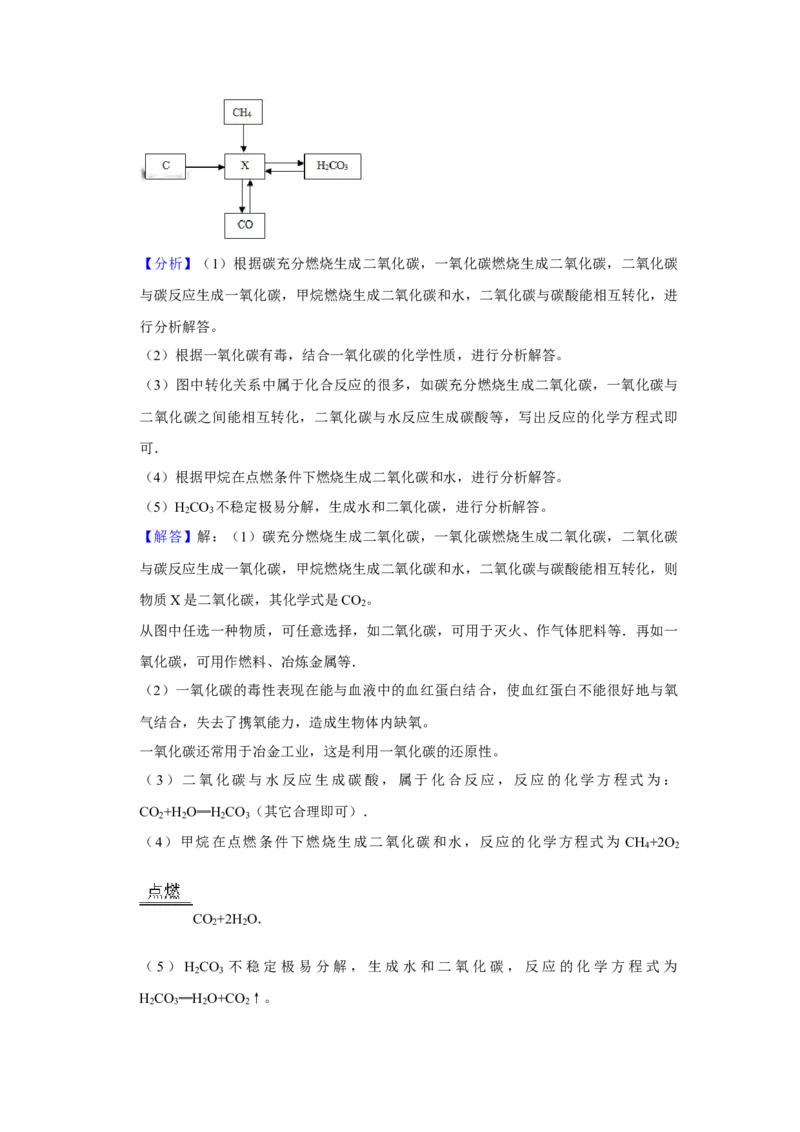
2.碳和部分碳的化合物之间的转化关系如图所示:
(1)物质X的化学式 CO ,从图中任选一种物质,写出它的一种用途 二氧化
2
碳,可用于灭火等(其它合理即可) 。
(2)一氧化碳的毒性表现在 能与血液中的血红蛋白结合,使血红蛋白不能很好地与
氧气结合,失去了携氧能力,造成生物体内缺氧 ,一氧化碳还常用于冶金工业,这是
利用一氧化碳的 还原 性。
(3)写出图中转化关系中属于化合反应的一个化学方程式 CO +H O ═ H CO (其它
2 2 2 3
合理即可) 。
(4)写出CH →X的化学方程式 CH +2O CO +2H O 。
4 4 2 2 2
(5)H CO 不稳定极易分解,其反应的原理 H CO ═ H O+CO ↑ (用化学方程式表
2 3 2 3 2 2
示)。【分析】(1)根据碳充分燃烧生成二氧化碳,一氧化碳燃烧生成二氧化碳,二氧化碳
与碳反应生成一氧化碳,甲烷燃烧生成二氧化碳和水,二氧化碳与碳酸能相互转化,进
行分析解答。
(2)根据一氧化碳有毒,结合一氧化碳的化学性质,进行分析解答。
(3)图中转化关系中属于化合反应的很多,如碳充分燃烧生成二氧化碳,一氧化碳与
二氧化碳之间能相互转化,二氧化碳与水反应生成碳酸等,写出反应的化学方程式即
可.
(4)根据甲烷在点燃条件下燃烧生成二氧化碳和水,进行分析解答。
(5)H CO 不稳定极易分解,生成水和二氧化碳,进行分析解答。
2 3
【解答】解:(1)碳充分燃烧生成二氧化碳,一氧化碳燃烧生成二氧化碳,二氧化碳
与碳反应生成一氧化碳,甲烷燃烧生成二氧化碳和水,二氧化碳与碳酸能相互转化,则
物质X是二氧化碳,其化学式是CO 。
2
从图中任选一种物质,可任意选择,如二氧化碳,可用于灭火、作气体肥料等.再如一
氧化碳,可用作燃料、冶炼金属等.
(2)一氧化碳的毒性表现在能与血液中的血红蛋白结合,使血红蛋白不能很好地与氧
气结合,失去了携氧能力,造成生物体内缺氧。
一氧化碳还常用于冶金工业,这是利用一氧化碳的还原性。
(3)二氧化碳与水反应生成碳酸,属于化合反应,反应的化学方程式为:
CO +H O═H CO (其它合理即可).
2 2 2 3
(4)甲烷在点燃条件下燃烧生成二氧化碳和水,反应的化学方程式为 CH +2O
4 2
CO +2H O.
2 2
(5)H CO 不稳定极易分解,生成水和二氧化碳,反应的化学方程式为
2 3
H CO ═H O+CO ↑。
2 3 2 2故答案为:
(1)CO ;二氧化碳,可用于灭火等(其它合理即可);
2
(2)能与血液中的血红蛋白结合,使血红蛋白不能很好地与氧气结合,失去了携氧能
力,造成生物体内缺氧;还原;
(3)CO +H O═H CO (其它合理即可).
2 2 2 3
(4)CH +2O CO +2H O;
4 2 2 2
(5)H CO ═H O+CO ↑。
2 3 2 2
【点评】本题难度不大,掌握二氧化碳与一氧化碳的化学性质、碳的化学性质、化学方
程式的书写方法等并能灵活运用是正确解答本题的关键.
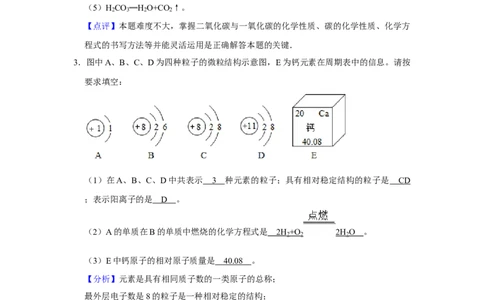
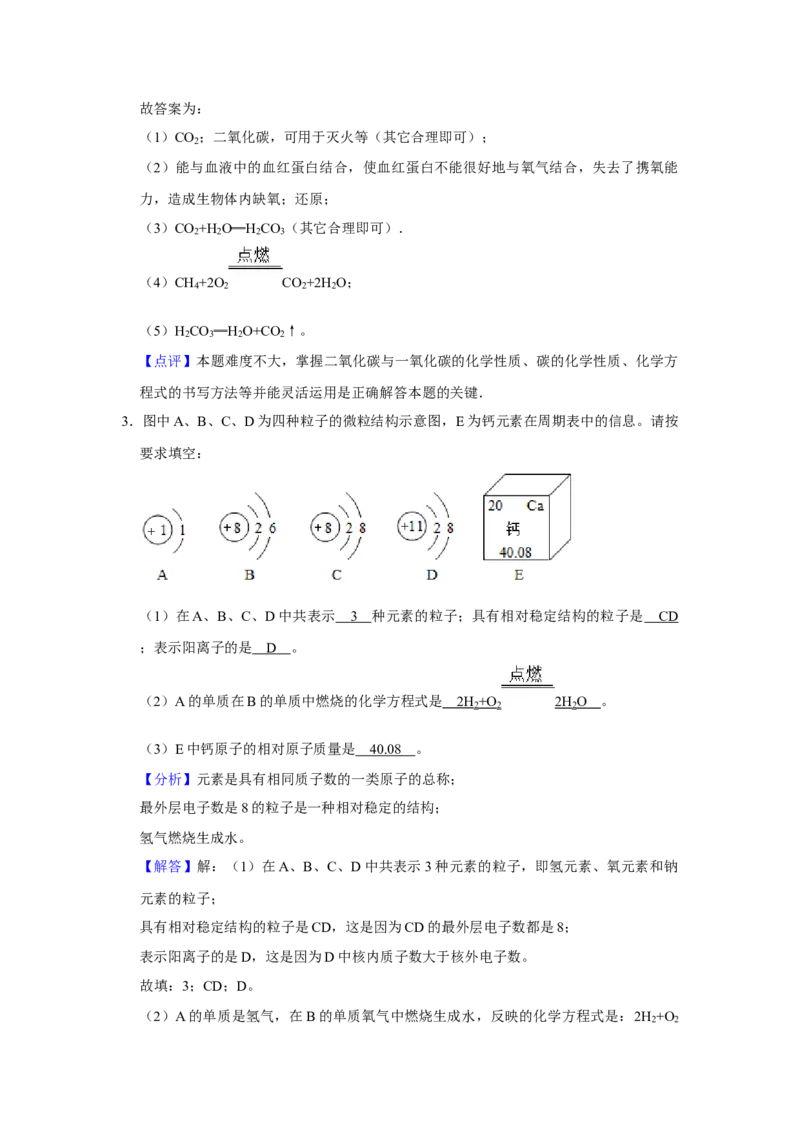
3.图中A、B、C、D为四种粒子的微粒结构示意图,E为钙元素在周期表中的信息。请按
要求填空:
(1)在A、B、C、D中共表示 3 种元素的粒子;具有相对稳定结构的粒子是 CD
;表示阳离子的是 D 。
(2)A的单质在B的单质中燃烧的化学方程式是 2H +O 2H O 。
2 2 2
(3)E中钙原子的相对原子质量是 40.0 8 。
【分析】元素是具有相同质子数的一类原子的总称;
最外层电子数是8的粒子是一种相对稳定的结构;
氢气燃烧生成水。
【解答】解:(1)在A、B、C、D中共表示3种元素的粒子,即氢元素、氧元素和钠
元素的粒子;
具有相对稳定结构的粒子是CD,这是因为CD的最外层电子数都是8;
表示阳离子的是D,这是因为D中核内质子数大于核外电子数。
故填:3;CD;D。
(2)A的单质是氢气,在B的单质氧气中燃烧生成水,反映的化学方程式是:2H +O
2 22H O。
2
故填:2H +O 2H O。
2 2 2
(3)E中钙原子的相对原子质量是40.08。
故填:40.08。
【点评】元素周期表反映了元素之间的内在联系,要注意理解和应用。
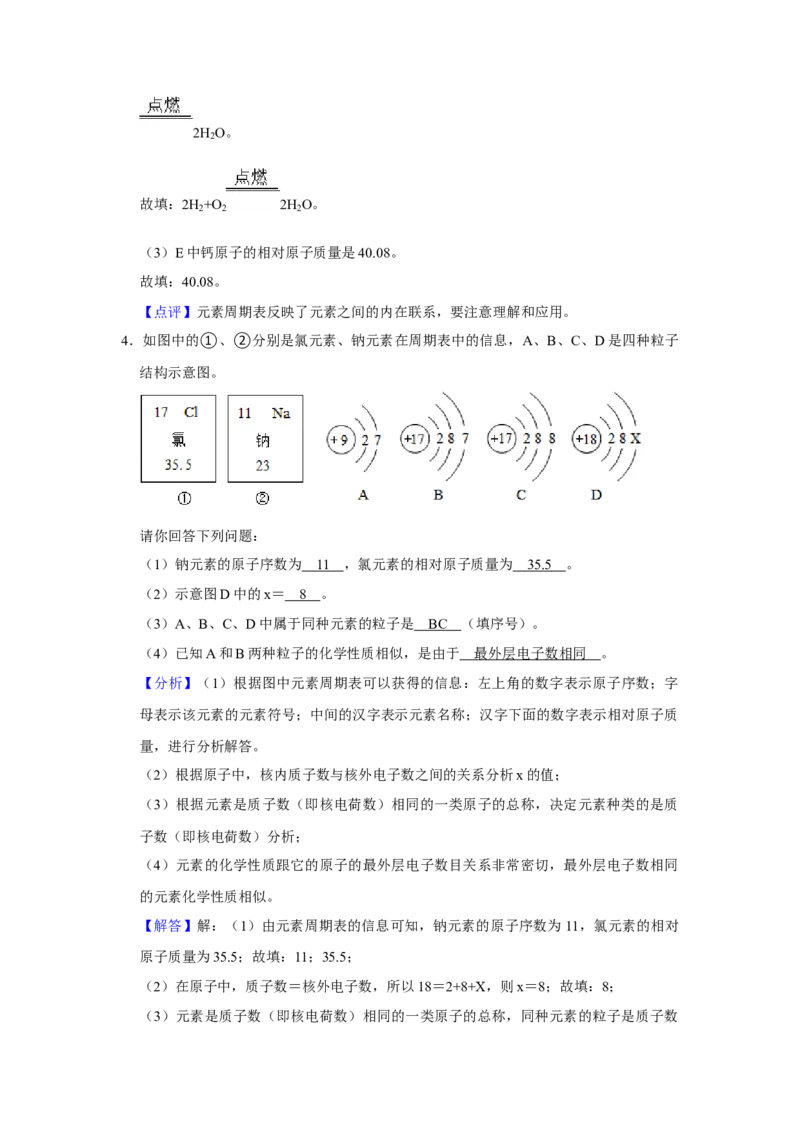
4.如图中的①、②分别是氯元素、钠元素在周期表中的信息,A、B、C、D是四种粒子
结构示意图。
请你回答下列问题:
(1)钠元素的原子序数为 1 1 ,氯元素的相对原子质量为 35. 5 。
(2)示意图D中的x= 8 。
(3)A、B、C、D中属于同种元素的粒子是 BC (填序号)。
(4)已知A和B两种粒子的化学性质相似,是由于 最外层电子数相同 。
【分析】(1)根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字
母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质
量,进行分析解答。
(2)根据原子中,核内质子数与核外电子数之间的关系分析x的值;
(3)根据元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质
子数(即核电荷数)分析;
(4)元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同
的元素化学性质相似。
【解答】解:(1)由元素周期表的信息可知,钠元素的原子序数为11,氯元素的相对
原子质量为35.5;故填:11;35.5;
(2)在原子中,质子数=核外电子数,所以18=2+8+X,则x=8;故填:8;
(3)元素是质子数(即核电荷数)相同的一类原子的总称,同种元素的粒子是质子数相同,BC的核内质子数相同,属于同种元素。故填:BC;
(4)决定元素化学性质的是最外层电子数,原子的最外层电子数相同,具有相似的化
学性质,由于A\B的最外层电子数均为7,故具有相似的化学性质。故填:最外层电子
数相同。
【点评】本题考查学生对在原子中,原子序数,质子数,核外电子数,核电荷数之间的
关系及元素的最外层电子数决定元素的化学性质的理解与掌握。
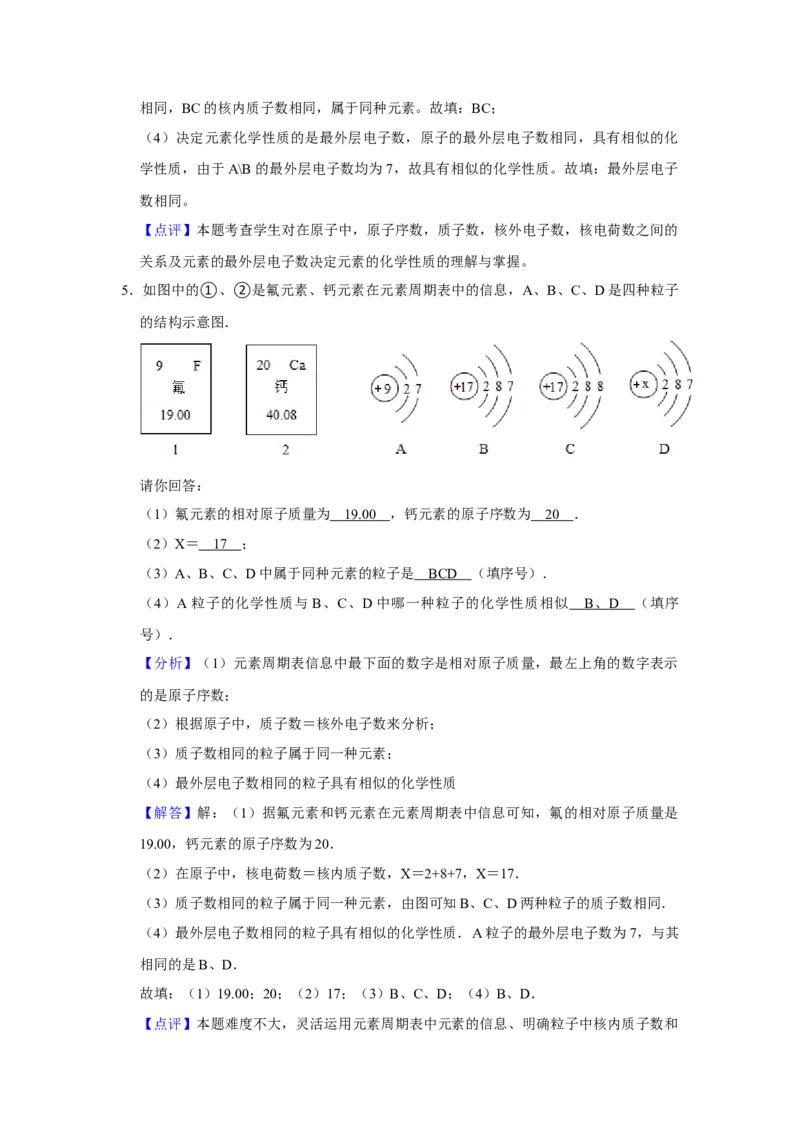
5.如图中的①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子
的结构示意图.
请你回答:
(1)氟元素的相对原子质量为 19.0 0 ,钙元素的原子序数为 2 0 .
(2)X= 1 7 ;
(3)A、B、C、D中属于同种元素的粒子是 BCD (填序号).
(4)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似 B 、 D (填序
号).
【分析】(1)元素周期表信息中最下面的数字是相对原子质量,最左上角的数字表示
的是原子序数;
(2)根据原子中,质子数=核外电子数来分析;
(3)质子数相同的粒子属于同一种元素;
(4)最外层电子数相同的粒子具有相似的化学性质
【解答】解:(1)据氟元素和钙元素在元素周期表中信息可知,氟的相对原子质量是
19.00,钙元素的原子序数为20.
(2)在原子中,核电荷数=核内质子数,X=2+8+7,X=17.
(3)质子数相同的粒子属于同一种元素,由图可知B、C、D两种粒子的质子数相同.
(4)最外层电子数相同的粒子具有相似的化学性质.A粒子的最外层电子数为7,与其
相同的是B、D.
故填:(1)19.00;20;(2)17;(3)B、C、D;(4)B、D.
【点评】本题难度不大,灵活运用元素周期表中元素的信息、明确粒子中核内质子数和核外电子数之间的关系、决定元素化学性质的因素等是即可正确决定本题.
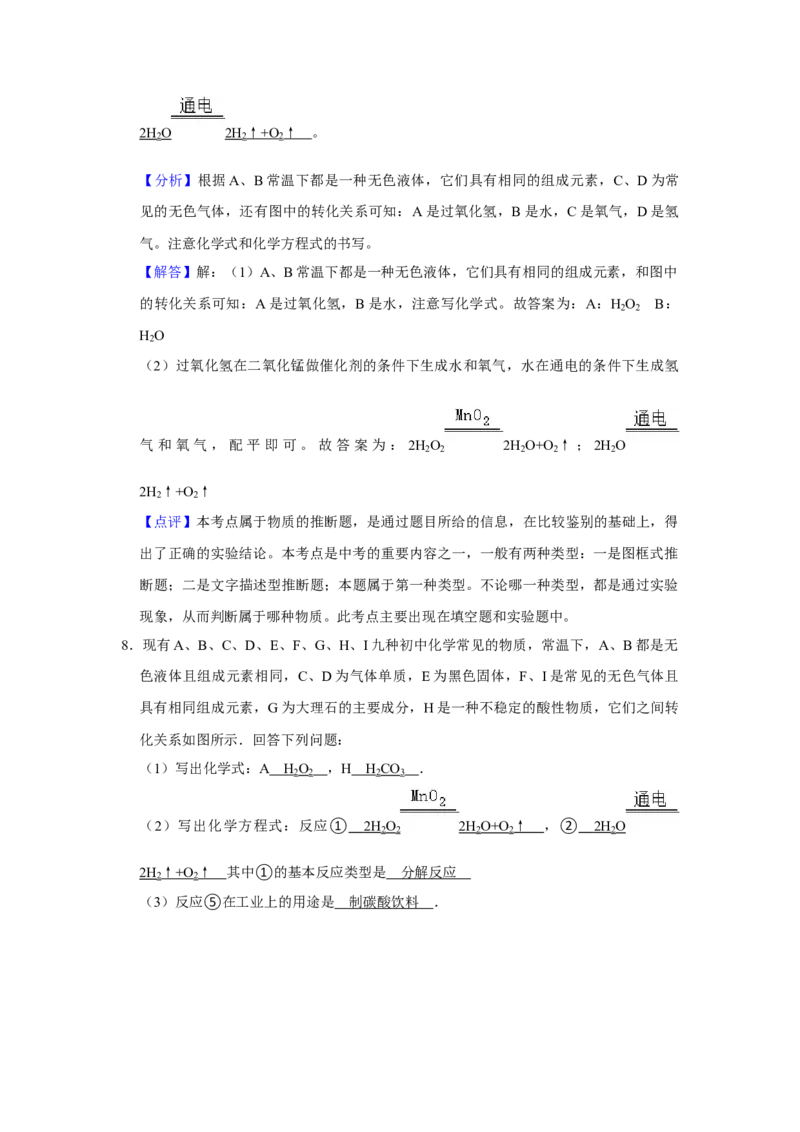
6.如图1是元素周期表中的一部分,图2是硒原子的结构示意图。据图回答问题:
(1)图2中m的值为 3 4 ,n的值为 6 ;
(2)硒元素位于元素周期表中的第 四 周期,硒化钠的化学式为 N a Se 。
2
【分析】(1)根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;原
子序数=核电荷数=质子数,结合当质子数=核外电子数,为原子,进行分析解答。
(2)根据周期数=原子核外电子层数,以及化合物的化学式写法进行分析解答。
【解答】解:(1)根据元素周期表中的一格可知,左上角的数字为34,表示原子序数
为34;根据原子序数=核电荷数=质子数,则图2中m的值为34;当质子数=核外电
子数,为原子,则34=2+8+18+n,n=6.故填:34;6
(2)周期数=原子核外电子层数,硒原子的核外有 4个电子层,则硒元素位于元素周
期表中的第四周期。钠原子最外层有1个电子,在化学反应中易失去1个电子而显+1
价;硒原子最外层有 6个电子,易得到 2个电子而显﹣2价,故硒化钠的化学式为
Na Se;故填:四;Na Se。
2 2
【点评】本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、元
素名称、相对原子质量)、原子结构示意图的含义是正确解答本题的关键。
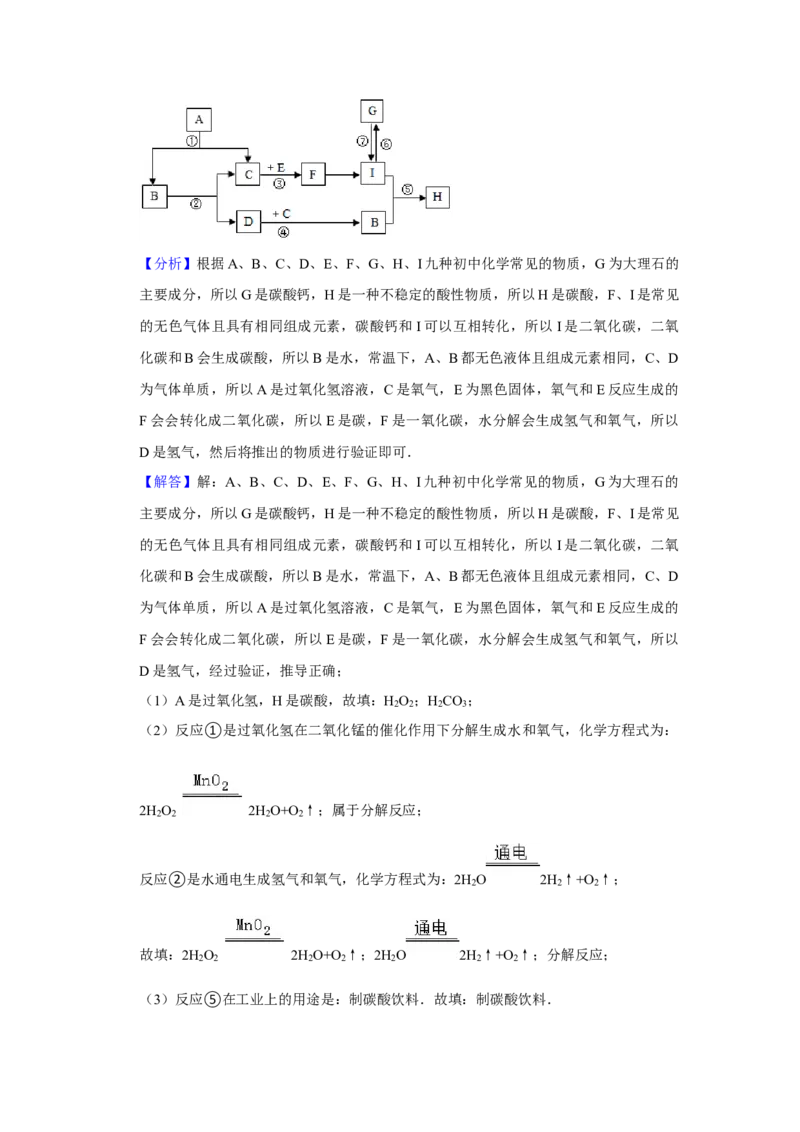
7.现有A、B、C、D四种物质,其中A、B常温下都是一种无色液体,它们具有相同的组
成元素,C、D为常见的无色气体。一定条件下四种物质存在如图所示的转化关系:请
根据以上事实回答下列问题:
(1)写出有关物质的名称或化学式:A H O ,B H O 。
2 2 2
(2)写出下列反应的化学方程式:反应 ① 2H O 2H O+O ↑ ,反应 ②
2 2 2 22H O 2H ↑ +O ↑ 。
2 2 2
【分析】根据A、B常温下都是一种无色液体,它们具有相同的组成元素,C、D为常
见的无色气体,还有图中的转化关系可知:A是过氧化氢,B是水,C是氧气,D是氢
气。注意化学式和化学方程式的书写。
【解答】解:(1)A、B常温下都是一种无色液体,它们具有相同的组成元素,和图中
的转化关系可知:A是过氧化氢,B是水,注意写化学式。故答案为:A:H O B:
2 2
H O
2
(2)过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,水在通电的条件下生成氢
气和氧气,配平即可。故答案为: 2H O 2H O+O ↑;2H O
2 2 2 2 2
2H ↑+O ↑
2 2
【点评】本考点属于物质的推断题,是通过题目所给的信息,在比较鉴别的基础上,得
出了正确的实验结论。本考点是中考的重要内容之一,一般有两种类型:一是图框式推
断题;二是文字描述型推断题;本题属于第一种类型。不论哪一种类型,都是通过实验
现象,从而判断属于哪种物质。此考点主要出现在填空题和实验题中。
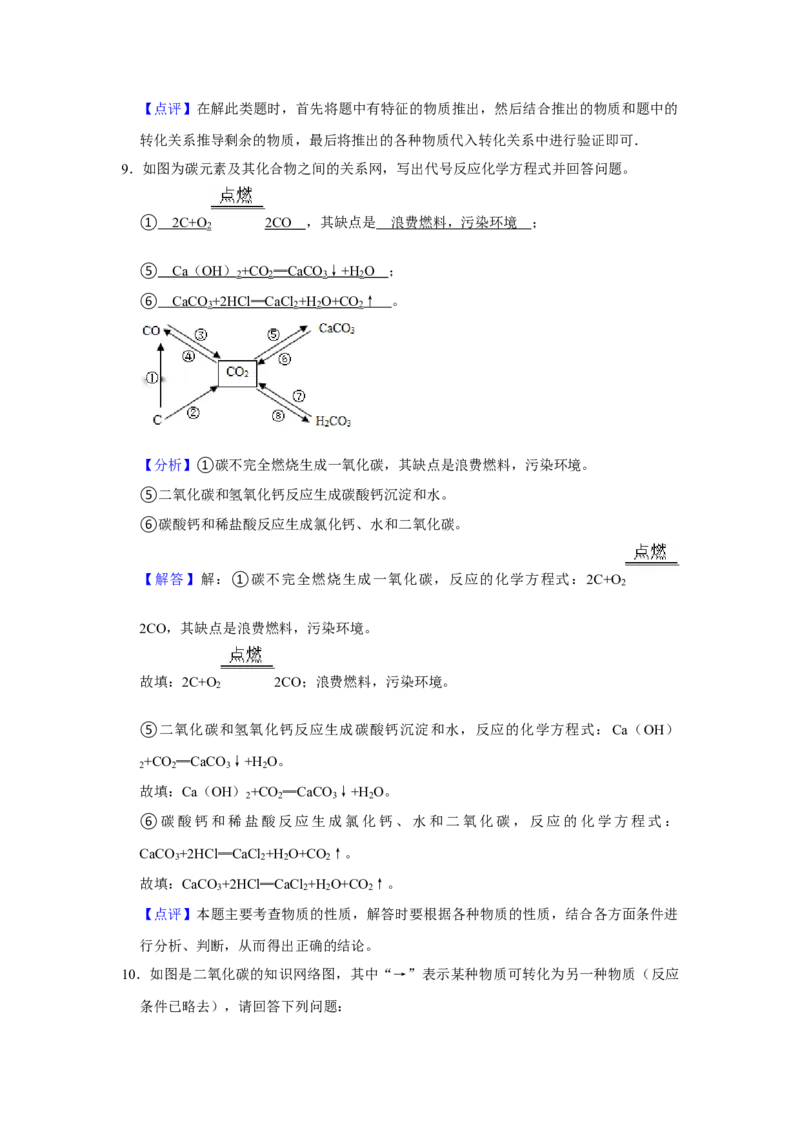
8.现有A、B、C、D、E、F、G、H、I九种初中化学常见的物质,常温下,A、B都是无
色液体且组成元素相同,C、D为气体单质,E为黑色固体,F、I是常见的无色气体且
具有相同组成元素,G为大理石的主要成分,H是一种不稳定的酸性物质,它们之间转
化关系如图所示.回答下列问题:
(1)写出化学式:A H O ,H H CO .
2 2 2 3
(2)写出化学方程式:反应① 2H O 2H O+O ↑ ,② 2H O
2 2 2 2 2
2H ↑ +O ↑ 其中①的基本反应类型是 分解反应
2 2
(3)反应⑤在工业上的用途是 制碳酸饮料 .【分析】根据A、B、C、D、E、F、G、H、I九种初中化学常见的物质,G为大理石的
主要成分,所以G是碳酸钙,H是一种不稳定的酸性物质,所以H是碳酸,F、I是常见
的无色气体且具有相同组成元素,碳酸钙和I可以互相转化,所以I是二氧化碳,二氧
化碳和B会生成碳酸,所以B是水,常温下,A、B都无色液体且组成元素相同,C、D
为气体单质,所以A是过氧化氢溶液,C是氧气,E为黑色固体,氧气和E反应生成的
F会会转化成二氧化碳,所以E是碳,F是一氧化碳,水分解会生成氢气和氧气,所以
D是氢气,然后将推出的物质进行验证即可.
【解答】解:A、B、C、D、E、F、G、H、I九种初中化学常见的物质,G为大理石的
主要成分,所以G是碳酸钙,H是一种不稳定的酸性物质,所以H是碳酸,F、I是常见
的无色气体且具有相同组成元素,碳酸钙和I可以互相转化,所以I是二氧化碳,二氧
化碳和B会生成碳酸,所以B是水,常温下,A、B都无色液体且组成元素相同,C、D
为气体单质,所以A是过氧化氢溶液,C是氧气,E为黑色固体,氧气和E反应生成的
F会会转化成二氧化碳,所以E是碳,F是一氧化碳,水分解会生成氢气和氧气,所以
D是氢气,经过验证,推导正确;
(1)A是过氧化氢,H是碳酸,故填:H O ;H CO ;
2 2 2 3
(2)反应①是过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为:
2H O 2H O+O ↑;属于分解反应;
2 2 2 2
反应②是水通电生成氢气和氧气,化学方程式为:2H O 2H ↑+O ↑;
2 2 2
故填:2H O 2H O+O ↑;2H O 2H ↑+O ↑;分解反应;
2 2 2 2 2 2 2
(3)反应⑤在工业上的用途是:制碳酸饮料.故填:制碳酸饮料.【点评】在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的
转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.
9.如图为碳元素及其化合物之间的关系网,写出代号反应化学方程式并回答问题。
① 2C+O 2CO ,其缺点是 浪费燃料,污染环境 ;
2
⑤ C a ( OH ) +CO ═ CaCO ↓ +H O ;
2 2 3 2
⑥ CaCO +2HCl ═ CaCl +H O+CO ↑ 。
3 2 2 2
【分析】①碳不完全燃烧生成一氧化碳,其缺点是浪费燃料,污染环境。
⑤二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水。
⑥碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳。
【解答】解:①碳不完全燃烧生成一氧化碳,反应的化学方程式:2C+O
2
2CO,其缺点是浪费燃料,污染环境。
故填:2C+O 2CO;浪费燃料,污染环境。
2
⑤二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式:Ca(OH)
+CO ═CaCO ↓+H O。
2 2 3 2
故填:Ca(OH) +CO ═CaCO ↓+H O。
2 2 3 2
⑥碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式:
CaCO +2HCl═CaCl +H O+CO ↑。
3 2 2 2
故填:CaCO +2HCl═CaCl +H O+CO ↑。
3 2 2 2
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进
行分析、判断,从而得出正确的结论。
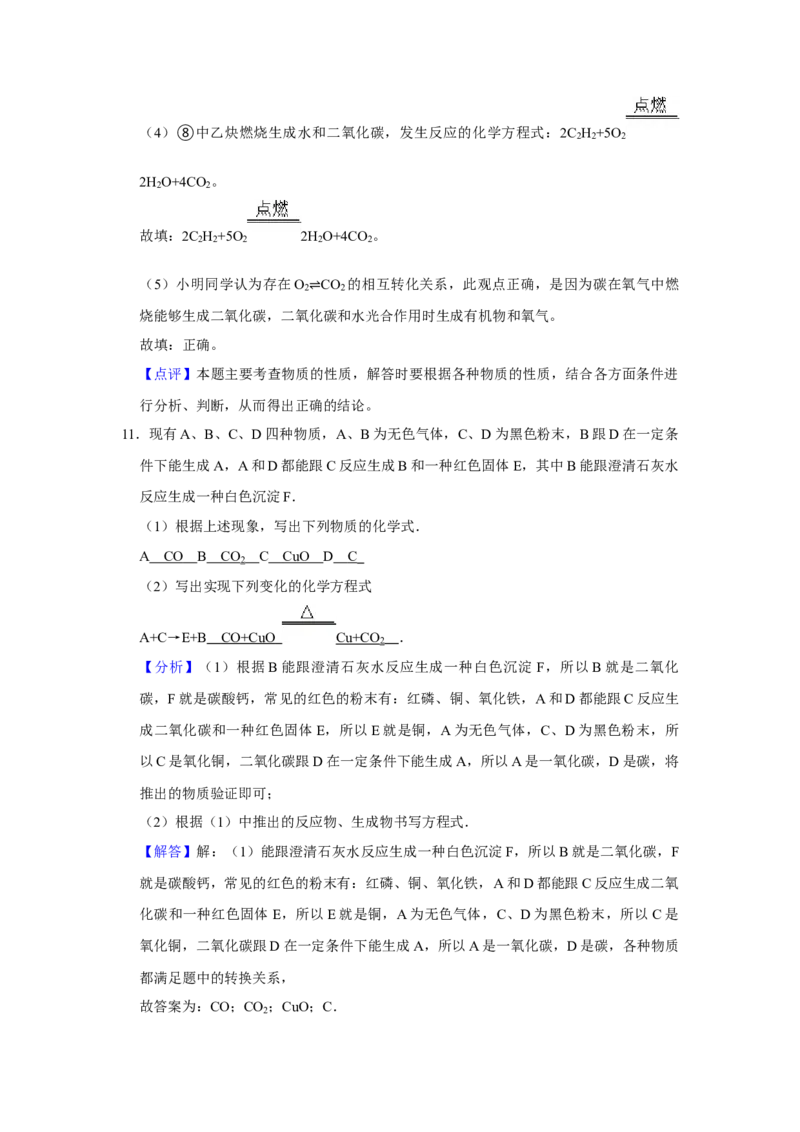
10.如图是二氧化碳的知识网络图,其中“→”表示某种物质可转化为另一种物质(反应
条件已略去),请回答下列问题:(1)完善该网络图:物质a CO (填化学式);
(2)②中CO 向H CO 转换的反应基本类型是 化合 反应;
2 2 3
(3)转化关系⑥可用于检验二氧化碳,写出该反应的化学方程式 Ca ( OH )
+CO ═ CaCO ↓ +H O ;
2 2 3 2
(4)写出转化关系⑧发生反应的化学方程式 2C H +5O 2H O+4CO ;
2 2 2 2 2
(5)小明同学认为存在O CO 的相互转化关系,你认为此观点是 正确 (填“正
2 2
确”或“错误”)。 ⇌
【分析】(1)碳完全燃烧生成二氧化碳,不完全燃烧生成一氧化碳;
(2)二氧化碳和水反应生成碳酸;
(3)氢氧化钙和二氧化碳反应生成白色沉淀碳酸钙和水;
(4)乙炔燃烧生成水和二氧化碳;
(5)碳在氧气中燃烧能够生成二氧化碳,二氧化碳和水光合作用时生成有机物和氧
气。
【解答】解:(1)碳完全燃烧生成二氧化碳,不完全燃烧生成一氧化碳,因此物质a
是CO,
故填:CO。
(2)②中二氧化碳和水反应生成碳酸,是化合反应。
故填:化合。
(3)转化关系⑥可用于检验二氧化碳,是因为氢氧化钙和二氧化碳反应生成白色沉淀
碳酸钙和水,该反应的化学方程式:Ca(OH) +CO ═CaCO ↓+H O。
2 2 3 2
故填:Ca(OH) +CO ═CaCO ↓+H O。
2 2 3 2(4)⑧中乙炔燃烧生成水和二氧化碳,发生反应的化学方程式:2C H +5O
2 2 2
2H O+4CO 。
2 2
故填:2C H +5O 2H O+4CO 。
2 2 2 2 2
(5)小明同学认为存在O CO 的相互转化关系,此观点正确,是因为碳在氧气中燃
2 2
烧能够生成二氧化碳,二氧化⇌碳和水光合作用时生成有机物和氧气。
故填:正确。
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进
行分析、判断,从而得出正确的结论。
11.现有A、B、C、D四种物质,A、B为无色气体,C、D为黑色粉末,B跟D在一定条
件下能生成A,A和D都能跟C反应生成B和一种红色固体E,其中B能跟澄清石灰水
反应生成一种白色沉淀F.
(1)根据上述现象,写出下列物质的化学式.
A CO B CO C CuO D C
2
(2)写出实现下列变化的化学方程式
A+C→E+B CO+CuO Cu+CO .
2
【分析】(1)根据B能跟澄清石灰水反应生成一种白色沉淀 F,所以B就是二氧化
碳,F就是碳酸钙,常见的红色的粉末有:红磷、铜、氧化铁,A和D都能跟C反应生
成二氧化碳和一种红色固体E,所以E就是铜,A为无色气体,C、D为黑色粉末,所
以C是氧化铜,二氧化碳跟D在一定条件下能生成A,所以A是一氧化碳,D是碳,将
推出的物质验证即可;
(2)根据(1)中推出的反应物、生成物书写方程式.
【解答】解:(1)能跟澄清石灰水反应生成一种白色沉淀F,所以B就是二氧化碳,F
就是碳酸钙,常见的红色的粉末有:红磷、铜、氧化铁,A和D都能跟C反应生成二氧
化碳和一种红色固体E,所以E就是铜,A为无色气体,C、D为黑色粉末,所以C是
氧化铜,二氧化碳跟D在一定条件下能生成A,所以A是一氧化碳,D是碳,各种物质
都满足题中的转换关系,
故答案为:CO;CO ;CuO;C.
2(2)一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳,故答案为:CO+CuO
Cu+CO .
2
故答案为:
(1)CO;CO ;CuO;C;(2)CO+CuO Cu+CO .
2 2
【点评】本题的突破口是B能跟澄清石灰水反应生成一种白色沉淀F,可推测B为二氧
化碳,然后利用转化和物质的颜色及体现的化学性质来解答推导出各物质.
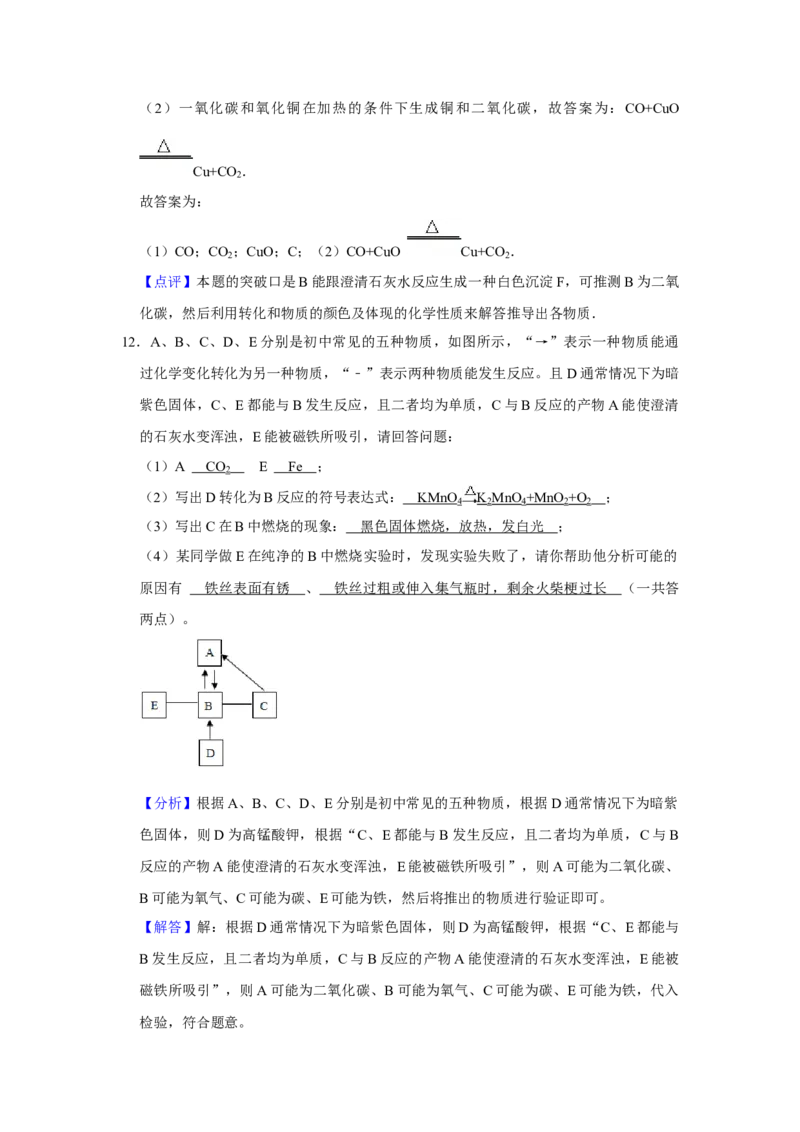
12.A、B、C、D、E分别是初中常见的五种物质,如图所示,“→”表示一种物质能通
过化学变化转化为另一种物质,“﹣”表示两种物质能发生反应。且 D通常情况下为暗
紫色固体,C、E都能与B发生反应,且二者均为单质,C与B反应的产物A能使澄清
的石灰水变浑浊,E能被磁铁所吸引,请回答问题:
(1)A CO E F e ;
2
(2)写出D转化为B反应的符号表达式: KMnO K MnO +MnO +O ;
4 2 4 2 2
(3)写出C在B中燃烧的现象: 黑色固体燃烧,放热,发白光 ;
(4)某同学做E在纯净的B中燃烧实验时,发现实验失败了,请你帮助他分析可能的
原因有 铁丝表面有锈 、 铁丝过粗或伸入集气瓶时,剩余火柴梗过长 (一共答
两点)。
【分析】根据A、B、C、D、E分别是初中常见的五种物质,根据D通常情况下为暗紫
色固体,则D为高锰酸钾,根据“C、E都能与B发生反应,且二者均为单质,C与B
反应的产物A能使澄清的石灰水变浑浊,E能被磁铁所吸引”,则A可能为二氧化碳、
B可能为氧气、C可能为碳、E可能为铁,然后将推出的物质进行验证即可。
【解答】解:根据D通常情况下为暗紫色固体,则D为高锰酸钾,根据“C、E都能与
B发生反应,且二者均为单质,C与B反应的产物A能使澄清的石灰水变浑浊,E能被
磁铁所吸引”,则A可能为二氧化碳、B可能为氧气、C可能为碳、E可能为铁,代入
检验,符合题意。(1)根据分析,A可能为二氧化碳,E可能为铁,则其化学式分别为:CO ;Fe;
2
(2)D 转化为 B ,即高 锰酸钾分解,故反应的符号表 达式: KMnO
4
K MnO +MnO +O ;
2 4 2 2
(3)C在B中燃烧,即碳燃烧,故反应的现象:黑色固体燃烧,放热,发白光;
(4)某同学做E在纯净的B中燃烧实验时,发现实验失败了,可能的原因有:铁丝表
面有锈、铁丝过粗或伸入集气瓶时,剩余火柴梗过长。
故答案为:
(1)CO ;Fe; (2)KMnO K MnO +MnO +O ;
2 4 2 4 2 2
(3)黑色固体燃烧,放热,发白光;
(4)铁丝表面有锈;铁丝过粗或伸入集气瓶时,剩余火柴梗过长。(合理即可)
【点评】在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的
转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。
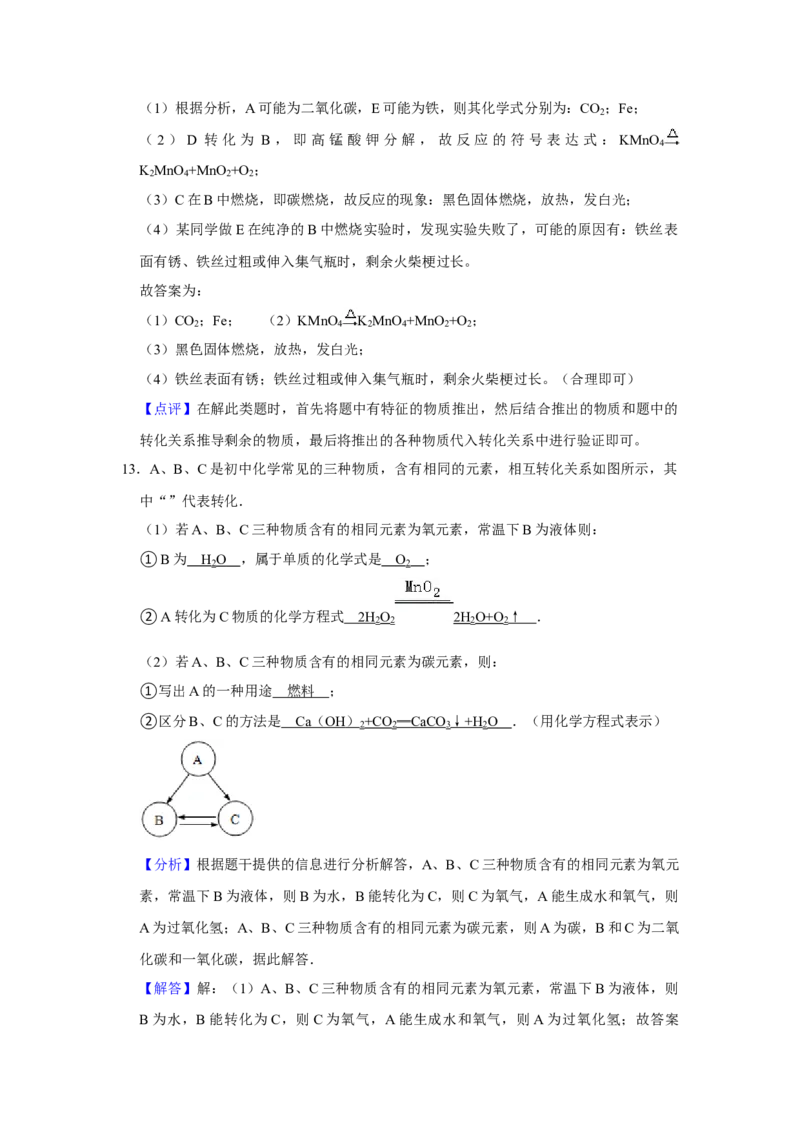
13.A、B、C是初中化学常见的三种物质,含有相同的元素,相互转化关系如图所示,其
中“”代表转化.
(1)若A、B、C三种物质含有的相同元素为氧元素,常温下B为液体则:
①B为 H O ,属于单质的化学式是 O ;
2 2
②A转化为C物质的化学方程式 2H O 2H O+O ↑ .
2 2 2 2
(2)若A、B、C三种物质含有的相同元素为碳元素,则:
①写出A的一种用途 燃料 ;
②区分B、C的方法是 C a ( OH ) +CO ═ CaCO ↓ +H O .(用化学方程式表示)
2 2 3 2
【分析】根据题干提供的信息进行分析解答,A、B、C三种物质含有的相同元素为氧元
素,常温下B为液体,则B为水,B能转化为C,则C为氧气,A能生成水和氧气,则
A为过氧化氢;A、B、C三种物质含有的相同元素为碳元素,则A为碳,B和C为二氧
化碳和一氧化碳,据此解答.
【解答】解:(1)A、B、C三种物质含有的相同元素为氧元素,常温下B为液体,则
B为水,B能转化为C,则C为氧气,A能生成水和氧气,则A为过氧化氢;故答案为:H O;O ;2H O 2H O+O ↑;
2 2 2 2 2 2
(2)A、B、C三种物质含有的相同元素为碳元素,则A为碳,B和C为二氧化碳和一
氧化碳,碳具有可燃性,可以用作燃料;区分二氧化碳和一氧化碳使用的是澄清的石灰
水,二氧化碳你能与氢氧化钙反应生成碳酸钙沉淀和水,故填:燃料;Ca(OH)
+CO ═CaCO ↓+H O.
2 2 3 2
【点评】本题考查的是常见的物质间的转化,完成此题,可以依据已有的物质的性质进
行.
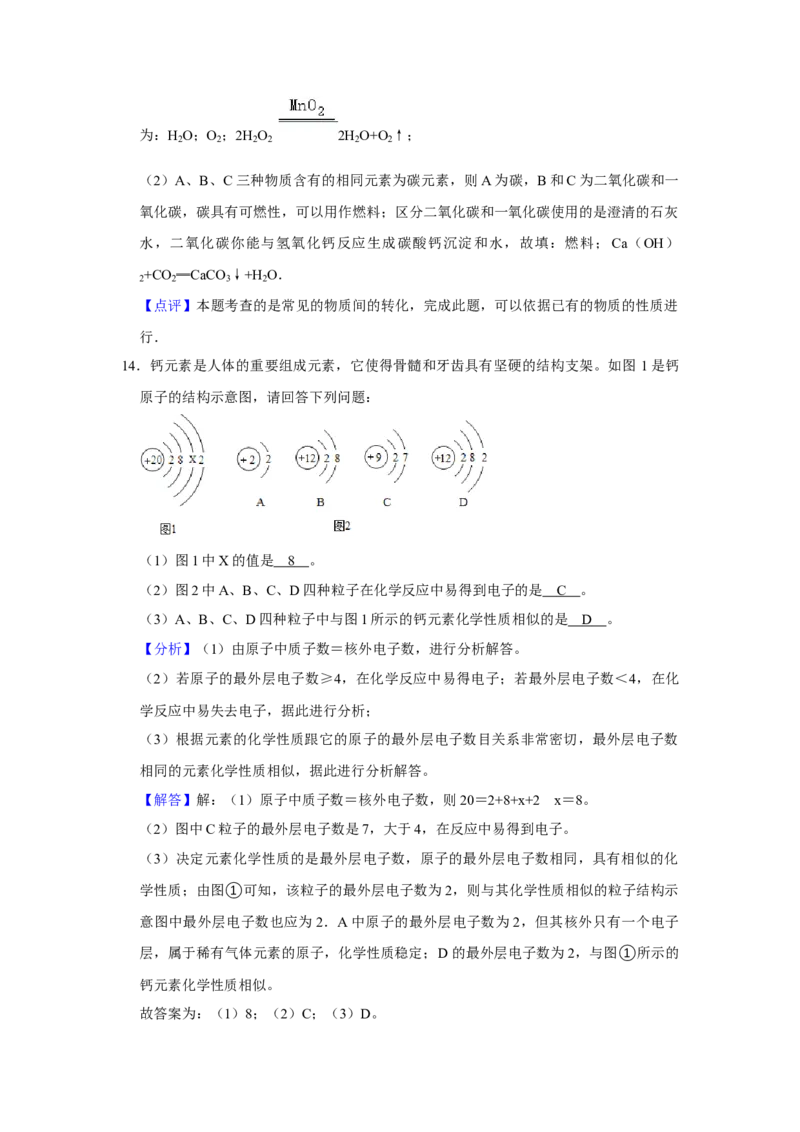
14.钙元素是人体的重要组成元素,它使得骨髓和牙齿具有坚硬的结构支架。如图 1是钙
原子的结构示意图,请回答下列问题:
(1)图1中X的值是 8 。
(2)图2中A、B、C、D四种粒子在化学反应中易得到电子的是 C 。
(3)A、B、C、D四种粒子中与图1所示的钙元素化学性质相似的是 D 。
【分析】(1)由原子中质子数=核外电子数,进行分析解答。
(2)若原子的最外层电子数≥4,在化学反应中易得电子;若最外层电子数<4,在化
学反应中易失去电子,据此进行分析;
(3)根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数
相同的元素化学性质相似,据此进行分析解答。
【解答】解:(1)原子中质子数=核外电子数,则20=2+8+x+2 x=8。
(2)图中C粒子的最外层电子数是7,大于4,在反应中易得到电子。
(3)决定元素化学性质的是最外层电子数,原子的最外层电子数相同,具有相似的化
学性质;由图①可知,该粒子的最外层电子数为2,则与其化学性质相似的粒子结构示
意图中最外层电子数也应为2.A中原子的最外层电子数为2,但其核外只有一个电子
层,属于稀有气体元素的原子,化学性质稳定;D的最外层电子数为2,与图①所示的
钙元素化学性质相似。
故答案为:(1)8;(2)C;(3)D。【点评】本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内
质子数和核外电子数之间的关系是解题的关键。
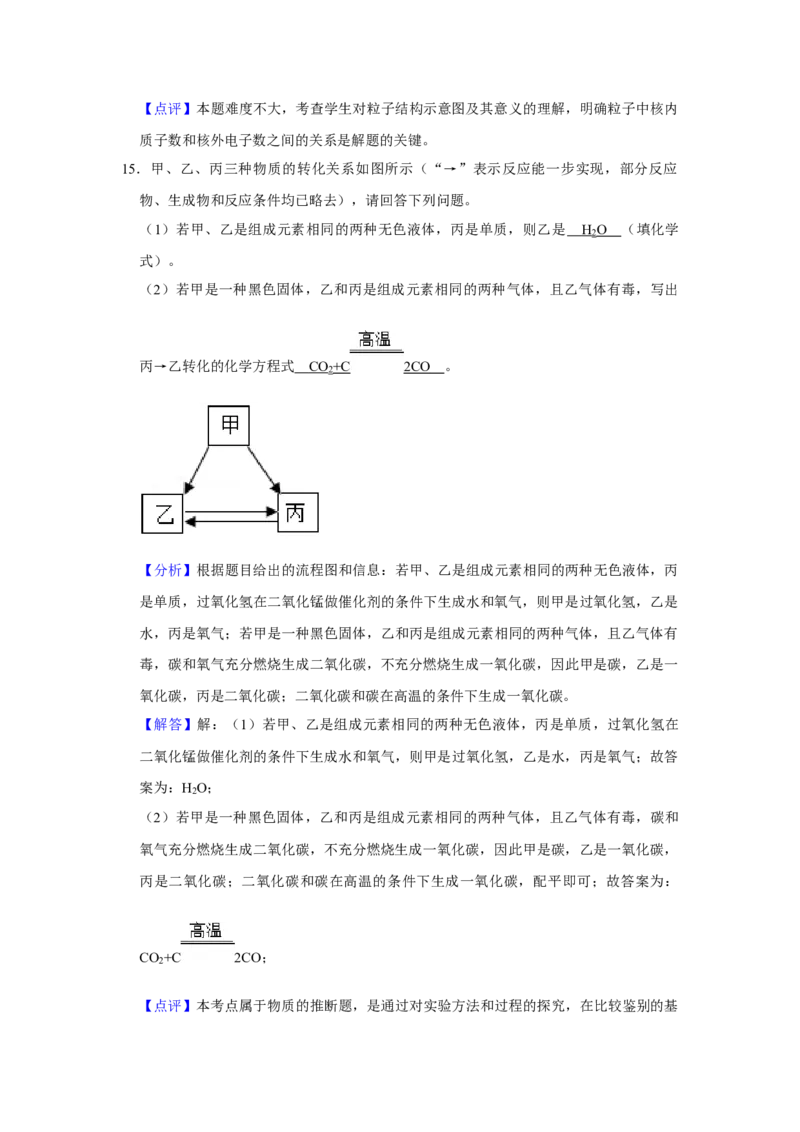
15.甲、乙、丙三种物质的转化关系如图所示(“→”表示反应能一步实现,部分反应
物、生成物和反应条件均已略去),请回答下列问题。
(1)若甲、乙是组成元素相同的两种无色液体,丙是单质,则乙是 H O (填化学
2
式)。
(2)若甲是一种黑色固体,乙和丙是组成元素相同的两种气体,且乙气体有毒,写出
丙→乙转化的化学方程式 CO +C 2CO 。
2
【分析】根据题目给出的流程图和信息:若甲、乙是组成元素相同的两种无色液体,丙
是单质,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,则甲是过氧化氢,乙是
水,丙是氧气;若甲是一种黑色固体,乙和丙是组成元素相同的两种气体,且乙气体有
毒,碳和氧气充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳,因此甲是碳,乙是一
氧化碳,丙是二氧化碳;二氧化碳和碳在高温的条件下生成一氧化碳。
【解答】解:(1)若甲、乙是组成元素相同的两种无色液体,丙是单质,过氧化氢在
二氧化锰做催化剂的条件下生成水和氧气,则甲是过氧化氢,乙是水,丙是氧气;故答
案为:H O;
2
(2)若甲是一种黑色固体,乙和丙是组成元素相同的两种气体,且乙气体有毒,碳和
氧气充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳,因此甲是碳,乙是一氧化碳,
丙是二氧化碳;二氧化碳和碳在高温的条件下生成一氧化碳,配平即可;故答案为:
CO +C 2CO;
2
【点评】本考点属于物质的推断题,是通过对实验方法和过程的探究,在比较鉴别的基础上,得出了正确的实验结论。本考点是中考的重要内容之一,一般有两种类型:一是
图框式推断题;二是文字描述型推断题;本题属于第一种类型。不论哪一种类型,都是
通过实验现象,从而得出物质的组成。此考点主要出现在填空题和实验题中。
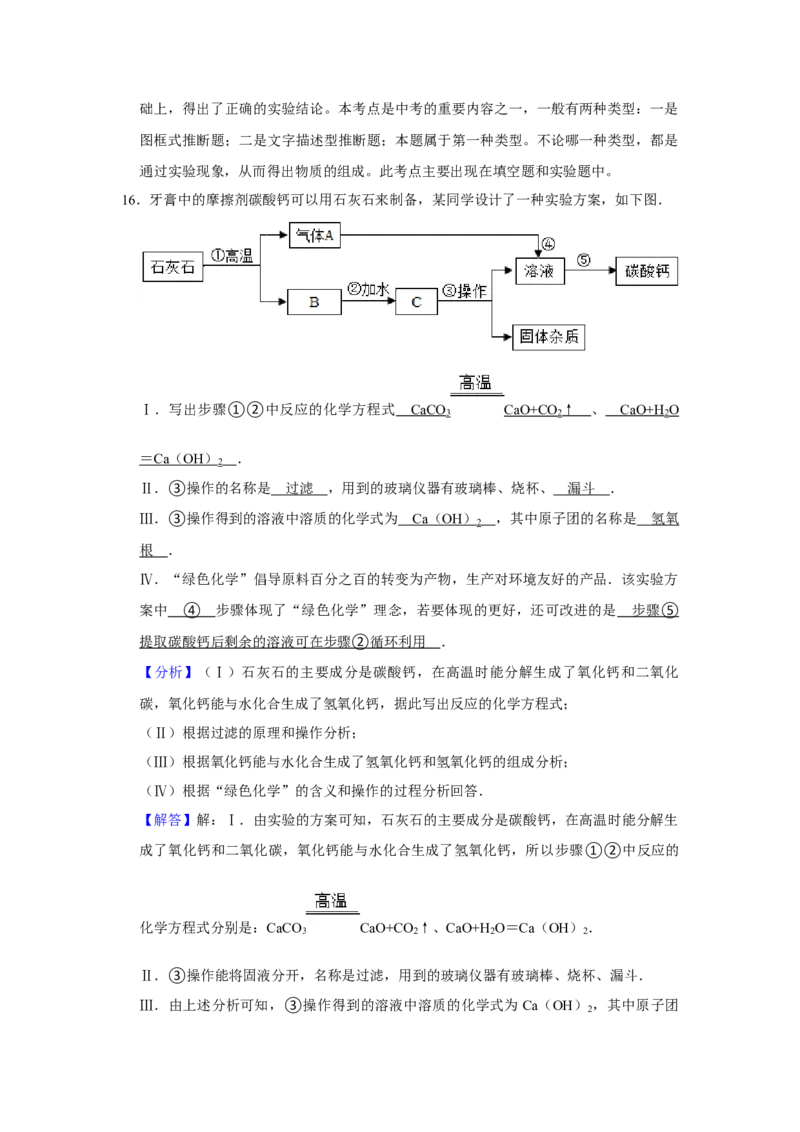
16.牙膏中的摩擦剂碳酸钙可以用石灰石来制备,某同学设计了一种实验方案,如下图.
Ⅰ.写出步骤①②中反应的化学方程式 CaCO CaO+CO ↑ 、 CaO+H O
3 2 2
= C a ( OH ) .
2
Ⅱ.③操作的名称是 过滤 ,用到的玻璃仪器有玻璃棒、烧杯、 漏斗 .
Ⅲ.③操作得到的溶液中溶质的化学式为 C a ( OH ) ,其中原子团的名称是 氢氧
2
根 .
Ⅳ.“绿色化学”倡导原料百分之百的转变为产物,生产对环境友好的产品.该实验方
案中 ④ 步骤体现了“绿色化学”理念,若要体现的更好,还可改进的是 步骤 ⑤
提取碳酸钙后剩余的溶液可在步骤 ② 循环利用 .
【分析】(Ⅰ)石灰石的主要成分是碳酸钙,在高温时能分解生成了氧化钙和二氧化
碳,氧化钙能与水化合生成了氢氧化钙,据此写出反应的化学方程式;
(Ⅱ)根据过滤的原理和操作分析;
(Ⅲ)根据氧化钙能与水化合生成了氢氧化钙和氢氧化钙的组成分析;
(Ⅳ)根据“绿色化学”的含义和操作的过程分析回答.
【解答】解:Ⅰ.由实验的方案可知,石灰石的主要成分是碳酸钙,在高温时能分解生
成了氧化钙和二氧化碳,氧化钙能与水化合生成了氢氧化钙,所以步骤①②中反应的
化学方程式分别是:CaCO CaO+CO ↑、CaO+H O=Ca(OH) .
3 2 2 2
Ⅱ.③操作能将固液分开,名称是过滤,用到的玻璃仪器有玻璃棒、烧杯、漏斗.
Ⅲ.由上述分析可知,③操作得到的溶液中溶质的化学式为 Ca(OH) ,其中原子团
2的名称是氢氧根.
Ⅳ.“绿色化学”倡导原料百分之百的转变为产物,生产对环境友好的产品.该实验方
案中④步骤中反应的原子完全被利用且全部转入氢氧化钙中,原子的利用率100%,体
现了“绿色化学”理念,若要体现的更好,还可改进的是:步骤⑤提取碳酸钙后剩余
的溶液可在步骤②循环利用.
故答为:Ⅰ CaCO CaO+CO ↑,CaO+H O=Ca(OH) ;Ⅱ过滤,漏斗;
3 2 2 2
ⅢCa(OH) ,氢氧根;Ⅳ.④步骤⑤,提取碳酸钙后剩余的溶液可在步骤②循环利
2
用.
【点评】本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也
是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学
性质结合实验目的进行分析解答.