文档内容
人教版九年级上册化学期末考试计算题专项训练Ⅰ
参考答案及解析
可能用到的相对原子质量:C:12 H:1 O:16 N:14 Ca:40
一、计算题。
1.某实验小组同学利用氯酸钾和二氧化锰加热制氧气,在 100mL的集气瓶中装满的水,
不小心造成集气瓶的水洒出一部分。然后用排水集气法将集气瓶内的水全部排出,收集
一瓶气体,将带火星的木条伸入集气瓶中,小木条复燃。请回答:
(1)通过上述实验可以看出,使用带火星的木条检验氧气集满的方法 不可靠 。
(填“可靠”或“不可靠”)
(2)计算收集100mL氧气体积分数为60%气体时,集气瓶中的应注入水的体积是多
少?(空气中氧气体积分数按20%计,写出计算过程)
【分析】(1)根据实验的现象分析回答;
(2)根据集气瓶内氧气的体积和空气的体积以及空气中氧气的体积分数分析计算。
【解答】解:(1)通过题意实验可以看出,使用带火星的木条检验氧气集满的方法不
可靠;故答案为:不可靠;
(2)设水的体积约为x,则x+20%×(100ml﹣x)=100ml×60%,解得x=50mL;
答:集气瓶中的应注入水的体积是50mL。
2.一般情况下,正常成年人每次吸入的空气体积约为0.6L,每分钟呼吸15次,则一个成
年人每天吸入的氧气大约是多少升?
【分析】气中各成分的体积分数分别是:氮气大约占空气体积的78%、氧气大约占空气
体积的21%、稀有气体大约占空气体积的0.94%、二氧化碳大约占空气体积的0.03%、
水蒸气和其它气体和杂质大约占0.03%。
【解答】解:一个成年人每天吸入的氧气大约是:24×60×15×0.6L×21%=2721.6L。
3.乙醇俗称酒精,它是一种重要的化工原料,还常用作酒精灯和内燃机的燃料。乙醇的化
学式是C H OH,计算:
2 5
(1)乙醇中C、H、O三种元素的质量比是多少?
(2)乙醇中氢元素的质量分数是多少?
(3)230kg乙醇中含有氢元素的质量是多少千克?
【分析】(1)根据乙醇化学式的含义、化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答;
(2)化合物中元素的质量分数的计算公式,进行分析解答;
(3)根据元素的质量=化合物的质量×化合物中该元素的质量分数,进行分析解答。
【解答】解:(1)乙醇的化学式为 C H OH,乙醇中碳、氢、氧元素的质量比为
2 5
(12×2):(1×6):(16×1)=12:3:8;
答:乙醇中C、H、O三种元素的质量比是12:3:8;
(2)乙醇中氢元素的质量分数为 ×100%≈13.0%;
答:乙醇中氢元素的质量分数是13.0%;
(3)230kg乙醇中含有氢元素的质量是230kg× ×100%=30kg。
答:230kg乙醇中含有氢元素的质量是30kg。
4.葡萄酒中含有白藜芦醇(C H O ),现代科技证明,白藜芦醇具有美容美颜之功效,
x 12 3
其相对分子质量为228。试计算:
(1)x= 1 4 。
(2)22.8g白藜芦醇中氧元素的质量 4. 8 g。
【分析】(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分
析;
(2)根据元素的质量=化合物的质量×化合物中该元素的质量分数来分析。
【解答】解:(1)白藜芦醇的相对分子质量为12×x+1×12+16×3=228,x=14;
(2)22.8g白藜芦醇中氧元素的质量为:22.8g× =4.8g。
故答案为:(1)14;(2)4.8。
5.2020 新春以来全球各国先后出现了罕见的新型冠状病毒肺炎疫情,过氧乙酸
(CH COOOH)是杀灭病毒的主要消毒剂之一,请计算:
3
(1)过氧乙酸的相对分子质量为 7 6 ;
(2)过氧乙酸中碳、氧的元素质量比为 1 : 2 ;
(3)列式计算152g的过氧乙酸中碳元素的质量为多少?
【分析】(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分
析;
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析;
(3)根据元素的质量=化合物的质量×化合物中该元素的质量分数来分析。【解答】解:(1)过氧乙酸的相对分子质量为12×2+1×4+16×3=76;故答案为:76;
(2)过氧乙酸中碳、氧的元素质量比为(12×2):(16×3)=1:2;故答案为:1:
2;
(3)152g的过氧乙酸中碳元素的质量为152g× =48g
答:152g的过氧乙酸中碳元素的质量为48g。
6.在一次作业批改中,王老师发现4位同学在同一题中出现了不同的错误,为帮大家理清
思路,老师将错误的解题过程写在黑板上,请同学们仔细观察,发现问题,纠正错误。
某工厂需要96kg氧气作原料,若用电解水的方法制取氧气,消耗水的质量是多少?
设:消耗水的质量为x
2H O H ↑+O ↑
2 2 2
20 32
x 96kg
=
x=60kg
(1)仔细观察:你发现解题过程中的错误有 5 处。
(2)纠正错误:老师点拨后,请将正确的解题过程写出来。
【分析】根据化学方程式得出各物质之间的质量比,列出比例式,通过计算得出所需物
质的质量。
【解答】解:设消耗水的质量为x。
2H O 2H ↑+O ↑
2 2 2
36 32
x 96kg
x=108kg
答:消耗水的质量是108kg。
可知,解题过程中的错误有方程式没有配平、关系式错误、比例式错误、结果错误、没有答,共5处错误。
故答案为:(1)5;
(2)解:设消耗水的质量为x。
2H O 2H ↑+O ↑
2 2 2
36 32
x 96kg
x=108kg
答:消耗水的质量是108kg。
7.(1)已知某粒子符号为Rm+,其核外电子数为n,则其质子数为 m+ n ;
(2)一个OH﹣中所含质子数为 9 ,电子数为 1 0 ,原子核个数为 2 ;
(3)已知一个氧原子的质量为akg,一个碳﹣12原子的质量为bkg,求氧原子的相对原
子质量。(写出计算过程)
【分析】(1)根据离子的形成过程来分析;
(2)根据离子结构、质子数、电子数来分析;
(3)根据相对原子质量的计算方法来分析。
【解答】解:(1)Rm+是由R失去m个电子后形成的,所以R的电子数为m+n,在原
子中,质子数=核外电子数,则质子数也为m+n;故填:m+n;
(2)一个OH﹣中含有1个氢原子和1个氧原子,则质子数为1+8=9,电子数为9+1=
10,一个OH﹣中含有两个原子,则原子核个数为2;故填:9;10;2;
(3)已知一个氧原子的质量为akg,一个碳﹣12原子的质量为bkg,则氧原子的相对原
子质量为: = ;
答:氧原子的相对原子质量为 。
8.在农业生产中有一种重要的化肥叫尿素[CO(NH ) ],极大的保障了水稻等粮食作物
2 2
的产量。试求:
(1)尿素的相对分子质量= 6 0 ;尿素中碳元素和氧元素的质量比= 3 : 4 。(2)尿素中氮元素的质量分数。(精确到0.1%,写出计算过程)
(3)原计划用90kg尿素,现因缺货改用硝酸铵(NH NO ),计算需要用多少千克的
4 3
硝酸铵才能与90kg尿素的含氮量相等?(写出计算过程)
【分析】(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,化合物中
各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答。
(2)根据化合物中元素的质量分数= ×100%,进行分析
解答。
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解
答。
【解答】解:(1)尿素的相对分子质量为12+16+(14+1×2)×2=60。
尿素中碳元素和氧元素的质量比为12:16=3:4。
(2)尿素中氮元素的质量分数为 ×100%≈46.7%。
(3)设需要硝酸铵的质量为x,
90kg× ×100%=x× ×100% x=120kg。
答:(2)尿素中氮元素的质量分数为46.7%;
(3)需要硝酸铵的质量为120kg。
故答案为:
(1)60;3:4;
(2)46.7%;
(3)120kg。
9.N(NO ) 是科学家2011年发现的一种新型火箭燃料。试计算:
2 3
(1)N(NO ) 中氮原子和氧原子的原子个数比是 2 : 3 。
2 3
(2)N(NO ) 中氮元素和氧元素的元素质量比是(求最简比) 7 : 1 2 。
2 3
(3)N(NO ) 的相对分子质量。(写出计算过程)
2 3
(4)求152克N(NO ) 中氮元素的质量。(写出计算过程)
2 3
【分析】(1)根据1个N(NO ) 分子的构成,进行分析解答。
2 3
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解
答。(3)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答。
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解
答。
【解答】解:(1)1个N(NO ) 分子中含有4个氮原子、6个氧原子,则N(NO )
2 3 2 3
中氮原子和氧原子的原子个数比是4:6=2:3。
(2)N(NO ) 中氮元素和氧元素的元素质量比是(14×4):(16×6)=7:12。
2 3
(3)N(NO ) 的相对分子质量为14×4+16×6=152。
2 3
(4)152克N(NO ) 中氮元素的质量为152g× ×100%=56g。
2 3
答:(3)N(NO ) 的相对分子质量为152;
2 3
(4)152克N(NO ) 中氮元素的质量为56g。
2 3
故答案为:
(1)2:3;
(2)7:12;
(3)152;
(4)56g。
10.豆腐中含有多种人体所需的氨基酸,其中含量最多的是亮氨酸(化学式C H NO )。
6 13 2
请计算:(要求写出计算过程,只有答案不给分)
(1)亮氨酸的相对分子质量是多少?
(2)亮氨酸中碳元素的质量分数是多少?(精确到0.1%)
(3)若262g亮氨酸所含的碳元素完全转化为CO ,则产生的CO 的质量为多少?
2 2
【分析】(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析
解答。
(2)根据化合物中元素的质量分数= ×100%,进行分析
解答。
(3)根据质量守恒定律,反应前后碳元素的质量不变,进行分析解答。
【解答】解:(1)亮氨酸的相对分子质量为12×6+1×13+14+16×2=131。
(2)亮氨酸中若262g亮氨酸所含的碳元素完全转化为CO ,则产生的CO 的质量为碳
2 2
元素的质量分数是 ×100%≈55.0%。(3)若 262g亮氨酸所含的碳元素完全转化为 CO ,则产生的 CO 的质量为 262g×
2 2
×100%÷( ×100%)=528g。
答:(1)亮氨酸的相对分子质量是131;
(2)亮氨酸中碳元素的质量分数是55.0%;
(3)产生的CO 的质量为528g。
2
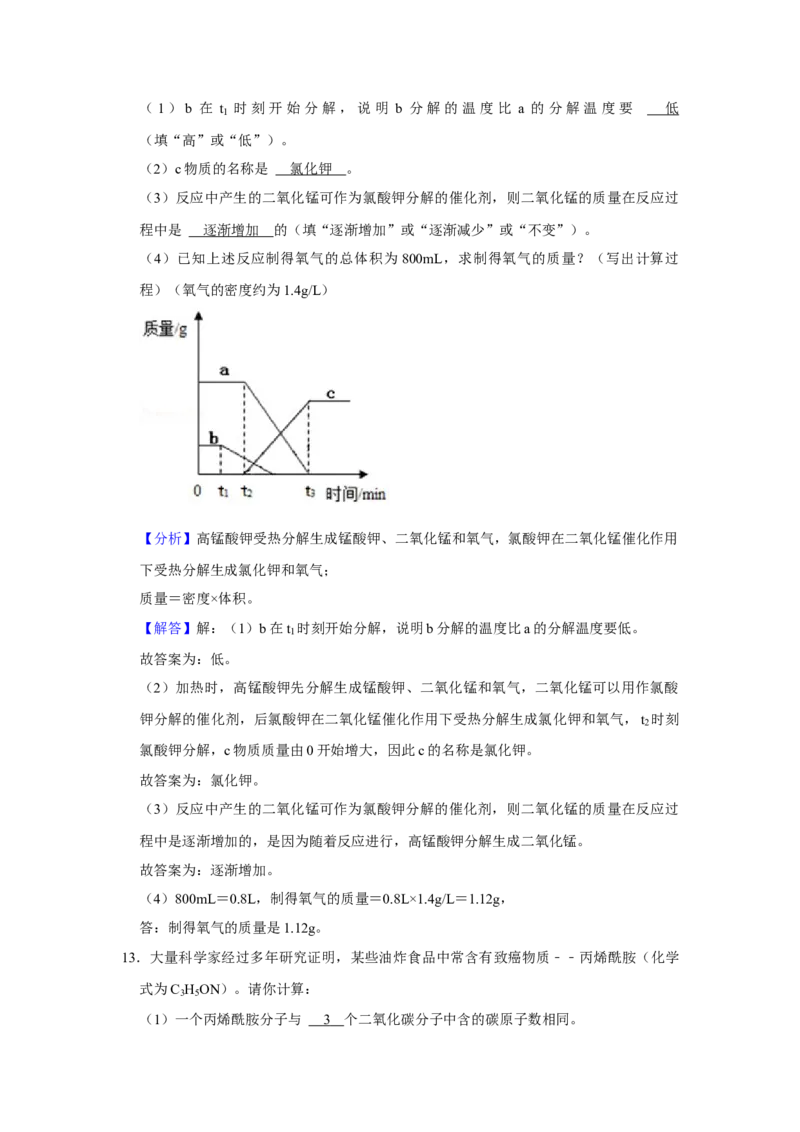
11.在探究铁丝在氧气中燃烧的实验时,小明进行了如下的实验:图 1的集气瓶中装有
80%的水,用排水法收集氧气后,集气瓶中仍留有15%的水,如图2所示。
(1)铁丝在氧气中燃烧的实验时,集气瓶中仍留有少量水的原因是 防止铁燃烧形成
的高温熔融物溅落炸裂集气瓶 。
(2)铁丝在氧气中燃烧的文字表达式是: 铁 + 氧气 四氧化三铁 。
(3)图2集气瓶气体中氧气的体积分数是多少?(写出计算过程)
【分析】铁燃烧生成四氧化三铁;
氧气约占空气总体积的五分之一。
【解答】解:(1)铁丝在氧气中燃烧的实验时,集气瓶中仍留有少量水的原因是防止
铁燃烧形成的高温熔融物溅落炸裂集气瓶。
故答案为:防止铁燃烧形成的高温熔融物溅落炸裂集气瓶。
(2)铁丝在氧气中燃烧生成四氧化三铁,反应的文字表达式是:铁+氧气 四氧化三
铁。
故答案为:铁+氧气 四氧化三铁。
(3)图2集气瓶气体中氧气的体积分数是:80%﹣15%+20%×20%=69%,
答:图2集气瓶气体中氧气的体积分数是69%。
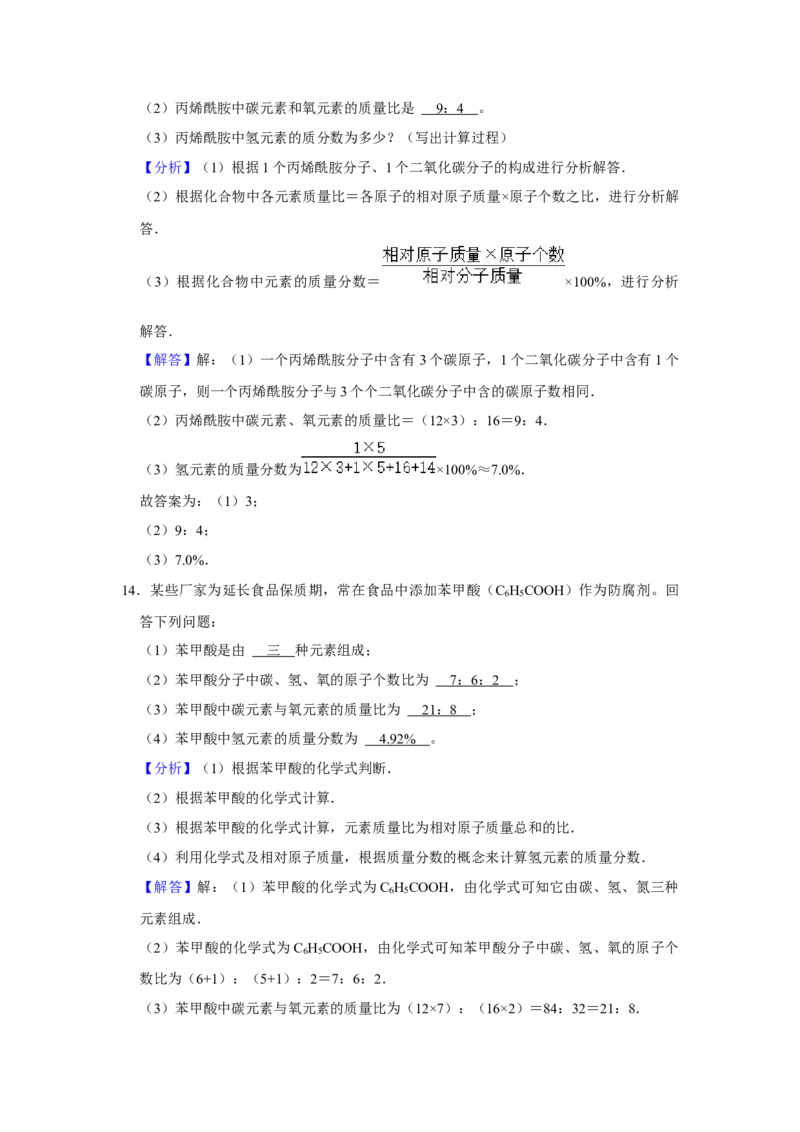
12.某同学误将少量高锰酸钾当成二氧化锰加入氯酸钾中进行加热制取氧气,部分物质的
质量随时间变化如图所示。a、b、c曲线代表不同固体的质量。(1)b 在 t 时刻开始分解,说明 b 分解的温度比 a 的分解温度要 低
1
(填“高”或“低”)。
(2)c物质的名称是 氯化钾 。
(3)反应中产生的二氧化锰可作为氯酸钾分解的催化剂,则二氧化锰的质量在反应过
程中是 逐渐增加 的(填“逐渐增加”或“逐渐减少”或“不变”)。
(4)已知上述反应制得氧气的总体积为800mL,求制得氧气的质量?(写出计算过
程)(氧气的密度约为1.4g/L)
【分析】高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,氯酸钾在二氧化锰催化作用
下受热分解生成氯化钾和氧气;
质量=密度×体积。
【解答】解:(1)b在t 时刻开始分解,说明b分解的温度比a的分解温度要低。
1
故答案为:低。
(2)加热时,高锰酸钾先分解生成锰酸钾、二氧化锰和氧气,二氧化锰可以用作氯酸
钾分解的催化剂,后氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,t 时刻
2
氯酸钾分解,c物质质量由0开始增大,因此c的名称是氯化钾。
故答案为:氯化钾。
(3)反应中产生的二氧化锰可作为氯酸钾分解的催化剂,则二氧化锰的质量在反应过
程中是逐渐增加的,是因为随着反应进行,高锰酸钾分解生成二氧化锰。
故答案为:逐渐增加。
(4)800mL=0.8L,制得氧气的质量=0.8L×1.4g/L=1.12g,
答:制得氧气的质量是1.12g。
13.大量科学家经过多年研究证明,某些油炸食品中常含有致癌物质﹣﹣丙烯酰胺(化学
式为C H ON)。请你计算:
3 5
(1)一个丙烯酰胺分子与 3 个二氧化碳分子中含的碳原子数相同。(2)丙烯酰胺中碳元素和氧元素的质量比是 9 : 4 。
(3)丙烯酰胺中氢元素的质分数为多少?(写出计算过程)
【分析】(1)根据1个丙烯酰胺分子、1个二氧化碳分子的构成进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解
答.
(3)根据化合物中元素的质量分数= ×100%,进行分析
解答.
【解答】解:(1)一个丙烯酰胺分子中含有3个碳原子,1个二氧化碳分子中含有1个
碳原子,则一个丙烯酰胺分子与3个个二氧化碳分子中含的碳原子数相同.
(2)丙烯酰胺中碳元素、氧元素的质量比=(12×3):16=9:4.
(3)氢元素的质量分数为 ×100%≈7.0%.
故答案为:(1)3;
(2)9:4;
(3)7.0%.
14.某些厂家为延长食品保质期,常在食品中添加苯甲酸(C H COOH)作为防腐剂。回
6 5
答下列问题:
(1)苯甲酸是由 三 种元素组成;
(2)苯甲酸分子中碳、氢、氧的原子个数比为 7 : 6 : 2 ;
(3)苯甲酸中碳元素与氧元素的质量比为 2 1 : 8 ;
(4)苯甲酸中氢元素的质量分数为 4.92% 。
【分析】(1)根据苯甲酸的化学式判断.
(2)根据苯甲酸的化学式计算.
(3)根据苯甲酸的化学式计算,元素质量比为相对原子质量总和的比.
(4)利用化学式及相对原子质量,根据质量分数的概念来计算氢元素的质量分数.
【解答】解:(1)苯甲酸的化学式为C H COOH,由化学式可知它由碳、氢、氮三种
6 5
元素组成.
(2)苯甲酸的化学式为C H COOH,由化学式可知苯甲酸分子中碳、氢、氧的原子个
6 5
数比为(6+1):(5+1):2=7:6:2.
(3)苯甲酸中碳元素与氧元素的质量比为(12×7):(16×2)=84:32=21:8.(4)苯甲酸中,氢元素的质量分数为: ≈4.92%.
故答案为:(1)三;
(2)7:6:2;
(3)21:8;
(4)4.92%。
15.葡萄糖酸钙(化学式C H O Ca,相对分子质量为430)主要用作食品的钙強化剂与
12 22 14
营养剂。工业上常以葡萄糖、碳酸钙和蒸馏水为原料,将它们混匀后控温于37℃,在葡
萄糖氧化酶和过氧化氢酶作用下,得到葡萄糖酸钙。反应的化学方程式为
2C H O +O +CaCO C H O Ca+H O+CO 。
6 12 6 2 3 12 22 14 2 2
(1)葡萄糖酸钙中碳元素与氧元素的质量比为 9 : 1 4 (填最简整数比)。
(2)若生产86kg葡萄糖酸钙,理论上所需碳酸钙的质量是多少?
【分析】(1)根据化合物中各元素的质量比=各元素的相对原子质量与原子个数乘积
之比分析;
(2)根据葡萄糖酸钙的质量,结合化学方程式进行计算。
【解答】解:(1)葡萄糖酸钙中碳元素与氧元素的质量比为:(12×12):(16×14)
=9:14;故答案为:9:14;
(2)解设所求CaCO 的质量为x。
3
2C H O +O +CaCO C H O Ca+H O+CO
6 12 6 2 3 12 22 14 2 2
100
430
x
86kg
=
x=20kg
答:生产86kg葡糖酸钙需要20kg碳酸钙。
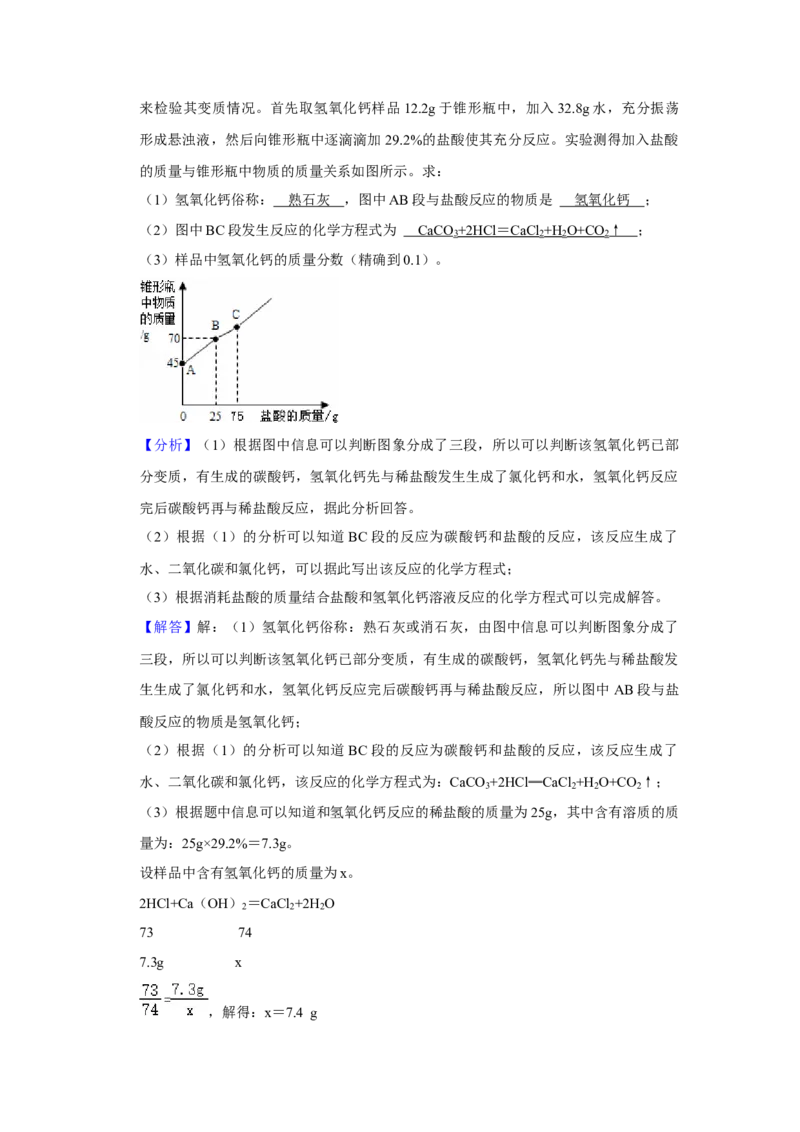
16.氢氧化钙长期存放容易变质。某科学探究小组在实验时取了一瓶存放多年的氢氧化钙来检验其变质情况。首先取氢氧化钙样品12.2g于锥形瓶中,加入32.8g水,充分振荡
形成悬浊液,然后向锥形瓶中逐滴滴加29.2%的盐酸使其充分反应。实验测得加入盐酸
的质量与锥形瓶中物质的质量关系如图所示。求:
(1)氢氧化钙俗称: 熟石灰 ,图中AB段与盐酸反应的物质是 氢氧化钙 ;
(2)图中BC段发生反应的化学方程式为 CaCO +2HCl = CaCl +H O+CO ↑ ;
3 2 2 2
(3)样品中氢氧化钙的质量分数(精确到0.1)。
【分析】(1)根据图中信息可以判断图象分成了三段,所以可以判断该氢氧化钙已部
分变质,有生成的碳酸钙,氢氧化钙先与稀盐酸发生生成了氯化钙和水,氢氧化钙反应
完后碳酸钙再与稀盐酸反应,据此分析回答。
(2)根据(1)的分析可以知道BC段的反应为碳酸钙和盐酸的反应,该反应生成了
水、二氧化碳和氯化钙,可以据此写出该反应的化学方程式;
(3)根据消耗盐酸的质量结合盐酸和氢氧化钙溶液反应的化学方程式可以完成解答。
【解答】解:(1)氢氧化钙俗称:熟石灰或消石灰,由图中信息可以判断图象分成了
三段,所以可以判断该氢氧化钙已部分变质,有生成的碳酸钙,氢氧化钙先与稀盐酸发
生生成了氯化钙和水,氢氧化钙反应完后碳酸钙再与稀盐酸反应,所以图中 AB段与盐
酸反应的物质是氢氧化钙;
(2)根据(1)的分析可以知道BC段的反应为碳酸钙和盐酸的反应,该反应生成了
水、二氧化碳和氯化钙,该反应的化学方程式为:CaCO +2HCl═CaCl +H O+CO ↑;
3 2 2 2
(3)根据题中信息可以知道和氢氧化钙反应的稀盐酸的质量为25g,其中含有溶质的质
量为:25g×29.2%=7.3g。
设样品中含有氢氧化钙的质量为x。
2HCl+Ca(OH) =CaCl +2H O
2 2 2
73 74
7.3g x
,解得:x=7.4 g样品中氢氧化钙的质量分数= ×100%=60.7%
答:样品中氢氧化钙的质量分数为60.7%.
故答案为:(1)熟石灰或消石灰;氢氧化钙;
(2)CaCO +2HCl═CaCl +H O+CO ↑;
3 2 2 2
(3)60.7%。
17.实验室用碳酸钙与盐酸反应制取二氧化碳,如果制取8.8g 二氧化碳,至少需要多少克
碳酸钙?
【分析】根据二氧化碳的质量和对应的化学方程式求算碳酸钙的质量。
【解答】解:设该石灰石样品中碳酸钙的质量为x,
CaCO +2HCl═CaCl +H O+CO ↑
3 2 2 2
100 44
x 8.8g
=
x=20g
答:需要的碳酸钙的质量为20g。