文档内容
2024 年中考第三次模拟考试(南通卷)
化 学
(考试时间:60分钟 试卷满分:60分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Ca-40
第I卷 选择题(共 20 分)
(共10小题,每小题只有一个选项符合题意。每小题2分,共20分。)
1.海安东临黄海,南望长江,河道纵横交错,莲是多年生水生草木,莲藕富含维生素C、铁、淀粉和膳食
纤维,莲子中钙、磷、钾含量很高,下列说法错误的是
A.莲藕富含糖类、无机盐等营养素
B.淀粉在人体内与水发生反应最终转化为氨基酸
C.膳食纤维是天然有机高分子物质
D.维生素C是对生命活动有重要意义的有机物
2.下列有关物质的组成或分类说法正确的是
A.甲烷和乙醇的组成元素相同
B.生理盐水和石蕊溶液都是混合物
C.纯碱和烧碱都含有氢氧根离子
D.钙和铁都是人体必需的微量元素
3.下列有关物质的性质与用途对应关系正确的是
A.石墨质软,可用作电池电极 B.氮气难溶于水,可用作保护气
C.醋酸具有酸性,可用于去除水垢 D.铁粉能与氧气反应,可用作干燥剂
4.如图所示的实验操作或说法不正确的是
A.可用于分离泥水 B.说明该装置气密性良好C.滴管用毕即插回 D.可用于反应容器
阅读下列材料,完成下面小题。
南海是中国四大海中最大、最深的海区,矿产、水产、可燃冰等自然资源最为丰富,海洋为人类提供了食
物、能源和交通,也是应对气候变化的忠实“朋友”。
5.下列说法正确的是
A.自然资源是可以再生的 B.自然资源需要抓紧大量开采,促进经济的发展
C.可燃冰主要含有甲烷水合物,是未来新能源 D.海洋“消化二氧化碳”时没有发生化学变化
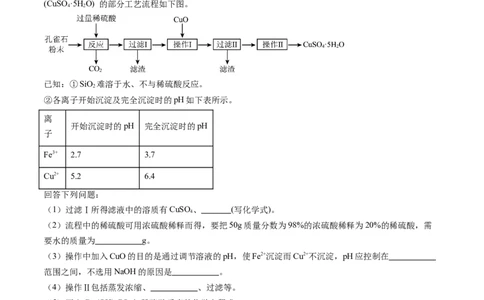
6.海水淡化系统(如图)工作时,蒸发腔中的水在光热作用下变为水蒸气,太阳能风扇将水蒸气吹到冷
凝腔冷凝,实现海水淡化,下列说法错误的是
A.光热作用下,水分子运动速率加快
B.海水淡化有着广阔的开发前景
C.海水变为淡水,水分子化学性质不变
D.冰变为水和水变为水蒸气,水分子间的间隔都变大
7.“证据推理与模型认知”是化学学科核心素养的重要组成部分。下列推断合理的是
A.合金的硬度一般比组成他们的纯金属更高,因此黄铜的硬度高于铜和锌
B.活泼金属与酸反应生成氢气是置换反应,所以有单质气体生成的反应都是置换反应
C.NaO、CaO均能与水反应生成碱,因此所有金属氧化物都能与水反应生成碱
2
D.化学变化常常伴随能量的变化,所以有能量变化的一定属于化学变化
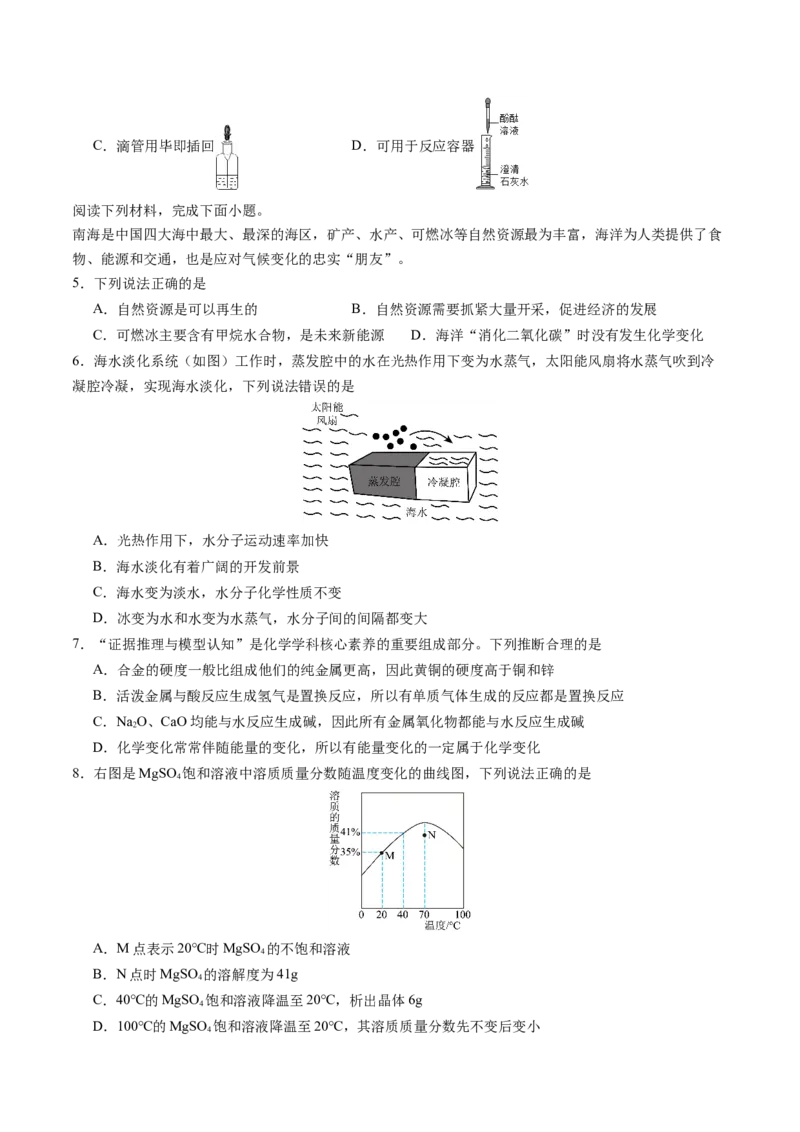
8.右图是MgSO 饱和溶液中溶质质量分数随温度变化的曲线图,下列说法正确的是
4
A.M点表示20℃时MgSO 的不饱和溶液
4
B.N点时MgSO 的溶解度为41g
4
C.40℃的MgSO 饱和溶液降温至20℃,析出晶体6g
4
D.100℃的MgSO 饱和溶液降温至20℃,其溶质质量分数先不变后变小
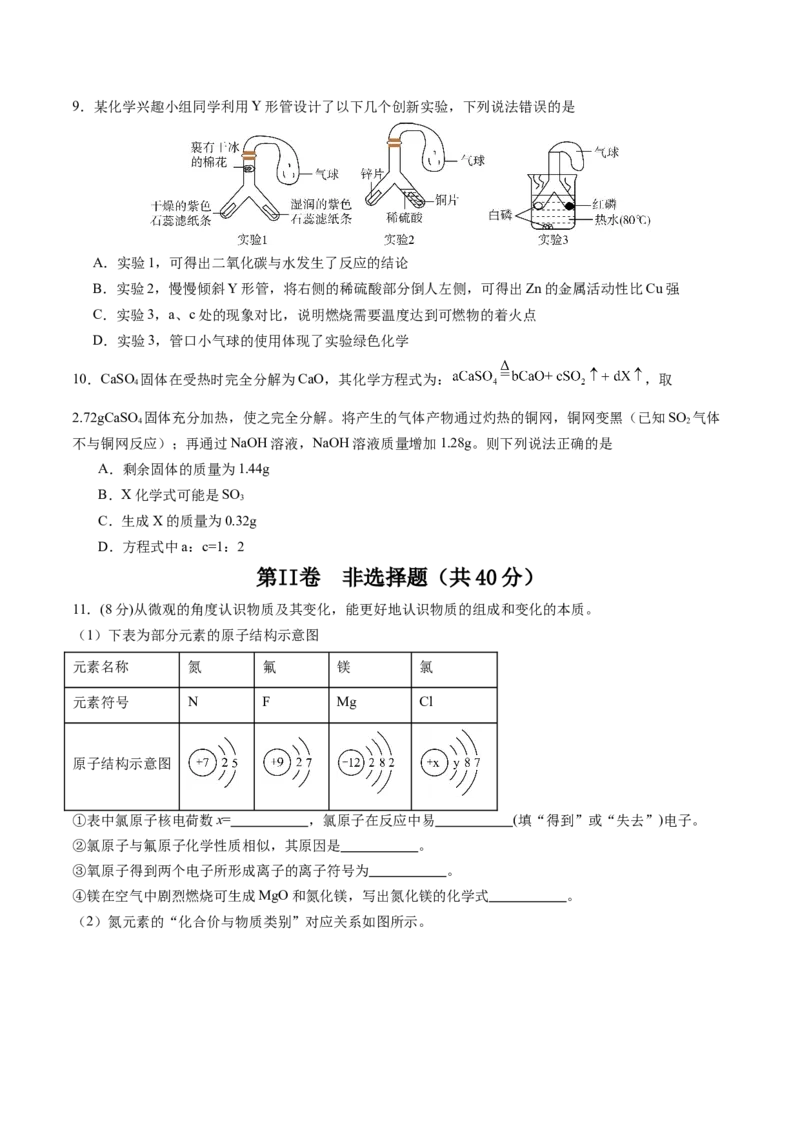
49.某化学兴趣小组同学利用Y形管设计了以下几个创新实验,下列说法错误的是
A.实验1,可得出二氧化碳与水发生了反应的结论
B.实验2,慢慢倾斜Y形管,将右侧的稀硫酸部分倒人左侧,可得出Zn的金属活动性比Cu强
C.实验3,a、c处的现象对比,说明燃烧需要温度达到可燃物的着火点
D.实验3,管口小气球的使用体现了实验绿色化学
10.CaSO 固体在受热时完全分解为CaO,其化学方程式为: ,取
4
2.72gCaSO 固体充分加热,使之完全分解。将产生的气体产物通过灼热的铜网,铜网变黑(已知SO 气体
4 2
不与铜网反应);再通过NaOH溶液,NaOH溶液质量增加1.28g。则下列说法正确的是
A.剩余固体的质量为1.44g
B.X化学式可能是SO
3
C.生成X的质量为0.32g
D.方程式中a:c=1:2
第II卷 非选择题(共 40 分)
11.(8分)从微观的角度认识物质及其变化,能更好地认识物质的组成和变化的本质。
(1)下表为部分元素的原子结构示意图
元素名称 氮 氟 镁 氯
元素符号 N F Mg Cl
原子结构示意图
①表中氯原子核电荷数x= ,氯原子在反应中易 (填“得到”或“失去”)电子。
②氯原子与氟原子化学性质相似,其原因是 。
③氧原子得到两个电子所形成离子的离子符号为 。
④镁在空气中剧烈燃烧可生成MgO和氮化镁,写出氮化镁的化学式 。
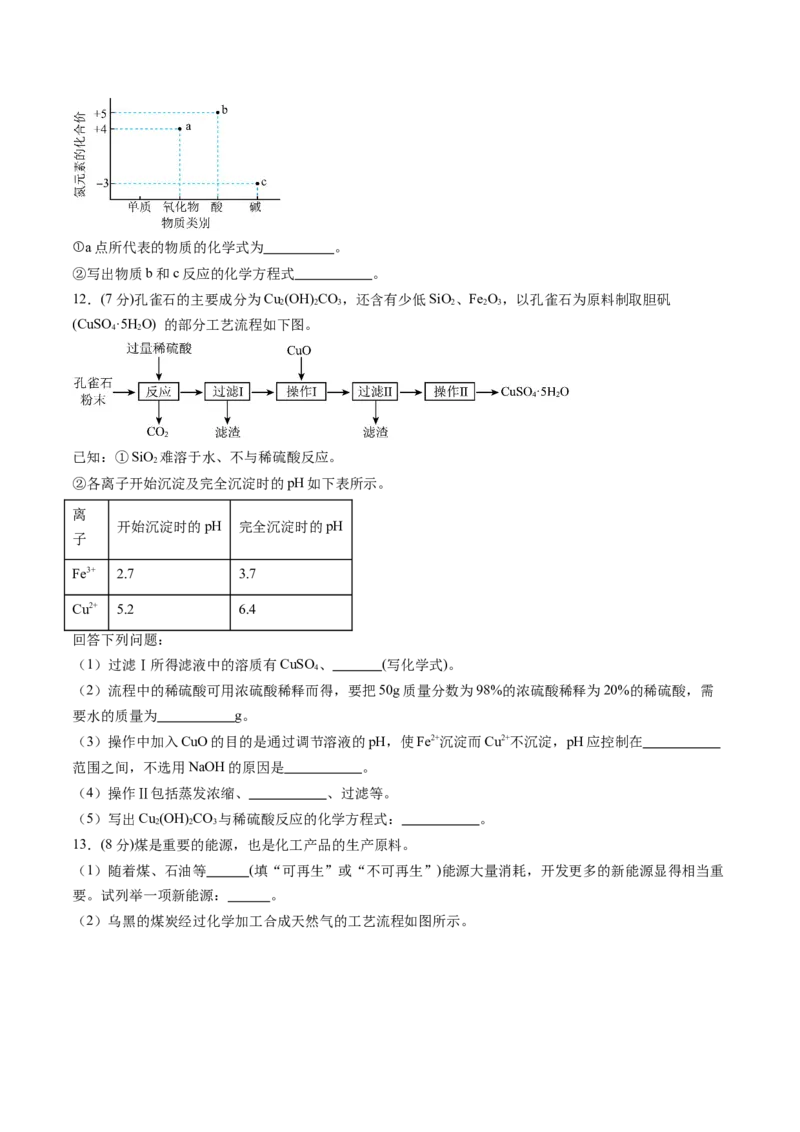
(2)氮元素的“化合价与物质类别”对应关系如图所示。①a点所代表的物质的化学式为 。
②写出物质b和c反应的化学方程式 。
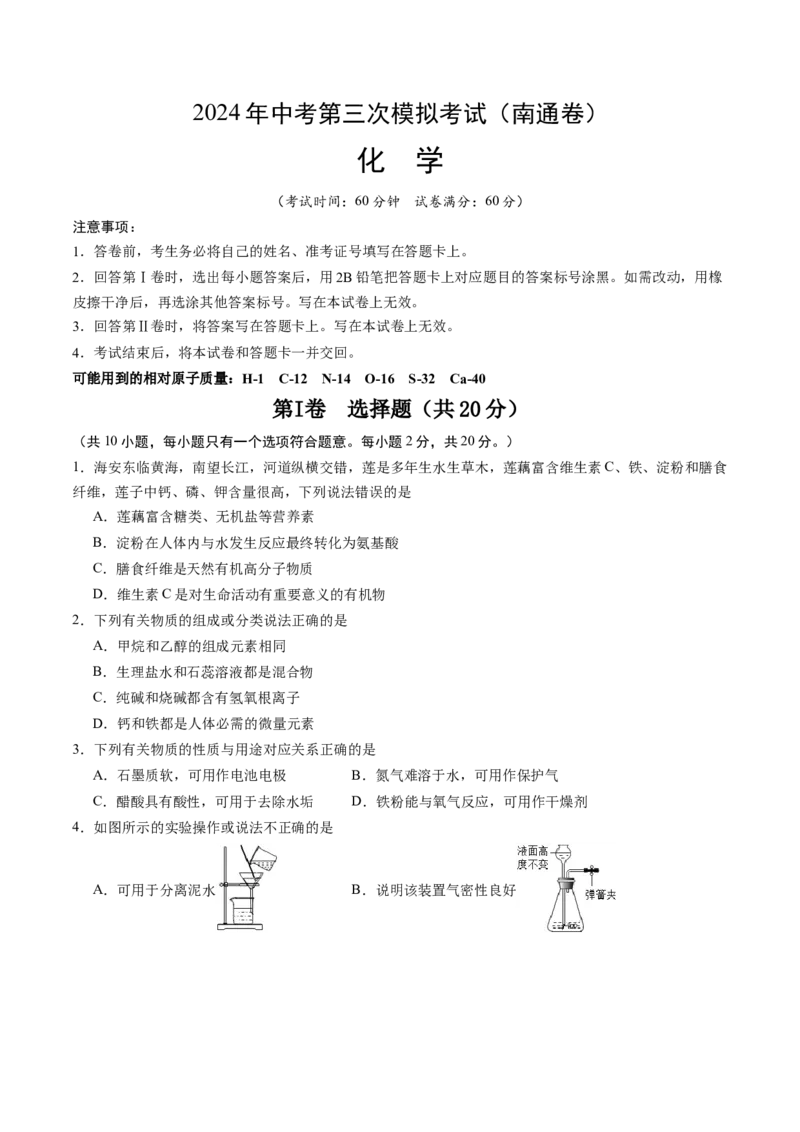
12.(7分)孔雀石的主要成分为Cu (OH) CO,还含有少低SiO、Fe O,以孔雀石为原料制取胆矾
2 2 3 2 2 3
(CuSO ·5H O) 的部分工艺流程如下图。
4 2
已知:①SiO 难溶于水、不与稀硫酸反应。
2
②各离子开始沉淀及完全沉淀时的pH如下表所示。
离
开始沉淀时的pH 完全沉淀时的pH
子
Fe3+ 2.7 3.7
Cu2+ 5.2 6.4
回答下列问题:
(1)过滤Ⅰ所得滤液中的溶质有CuSO 、 (写化学式)。
4
(2)流程中的稀硫酸可用浓硫酸稀释而得,要把50g质量分数为98%的浓硫酸稀释为20%的稀硫酸,需
要水的质量为 g。
(3)操作中加入CuO的目的是通过调节溶液的pH,使Fe2+沉淀而Cu2+不沉淀,pH应控制在
范围之间,不选用NaOH的原因是 。
(4)操作Ⅱ包括蒸发浓缩、 、过滤等。
(5)写出Cu (OH) CO 与稀硫酸反应的化学方程式: 。
2 2 3
13.(8分)煤是重要的能源,也是化工产品的生产原料。
(1)随着煤、石油等 (填“可再生”或“不可再生”)能源大量消耗,开发更多的新能源显得相当重
要。试列举一项新能源: 。
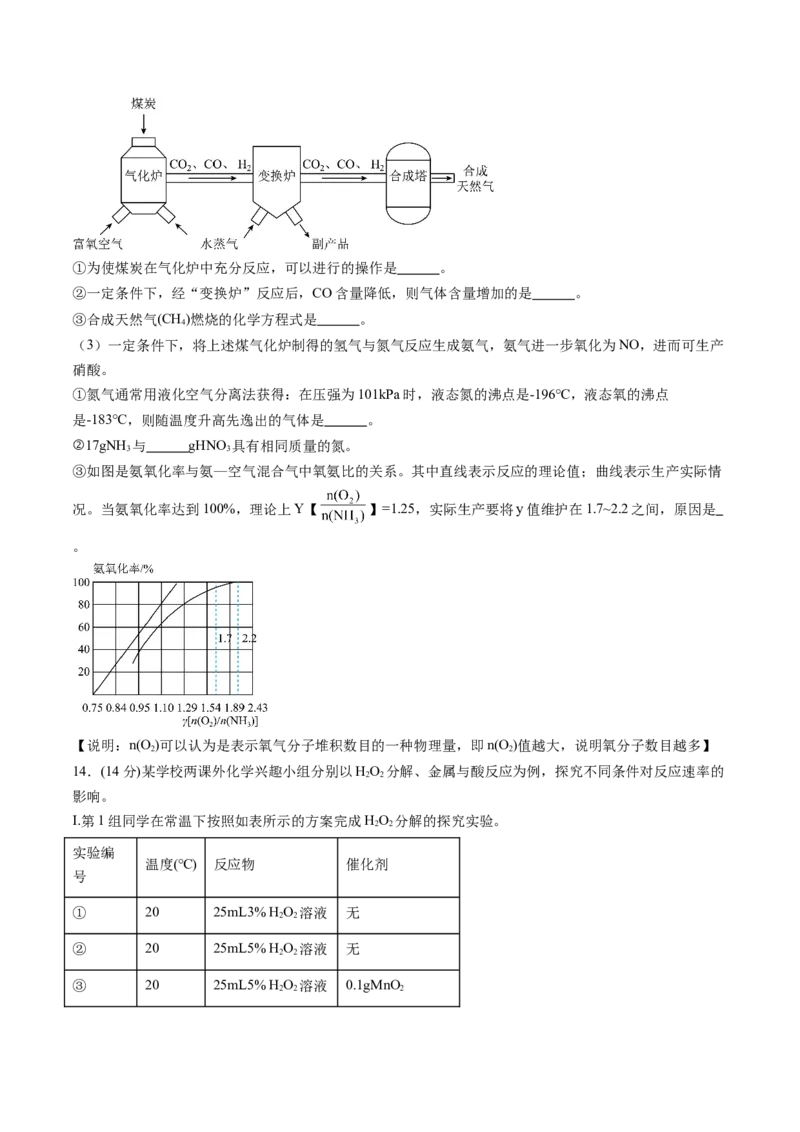
(2)乌黑的煤炭经过化学加工合成天然气的工艺流程如图所示。①为使煤炭在气化炉中充分反应,可以进行的操作是 。
②一定条件下,经“变换炉”反应后,CO含量降低,则气体含量增加的是 。
③合成天然气(CH)燃烧的化学方程式是 。
4
(3)一定条件下,将上述煤气化炉制得的氢气与氮气反应生成氨气,氨气进一步氧化为NO,进而可生产
硝酸。
①氮气通常用液化空气分离法获得:在压强为101kPa时,液态氮的沸点是-196℃,液态氧的沸点
是-183℃,则随温度升高先逸出的气体是 。
②17gNH 与 gHNO 具有相同质量的氮。
3 3
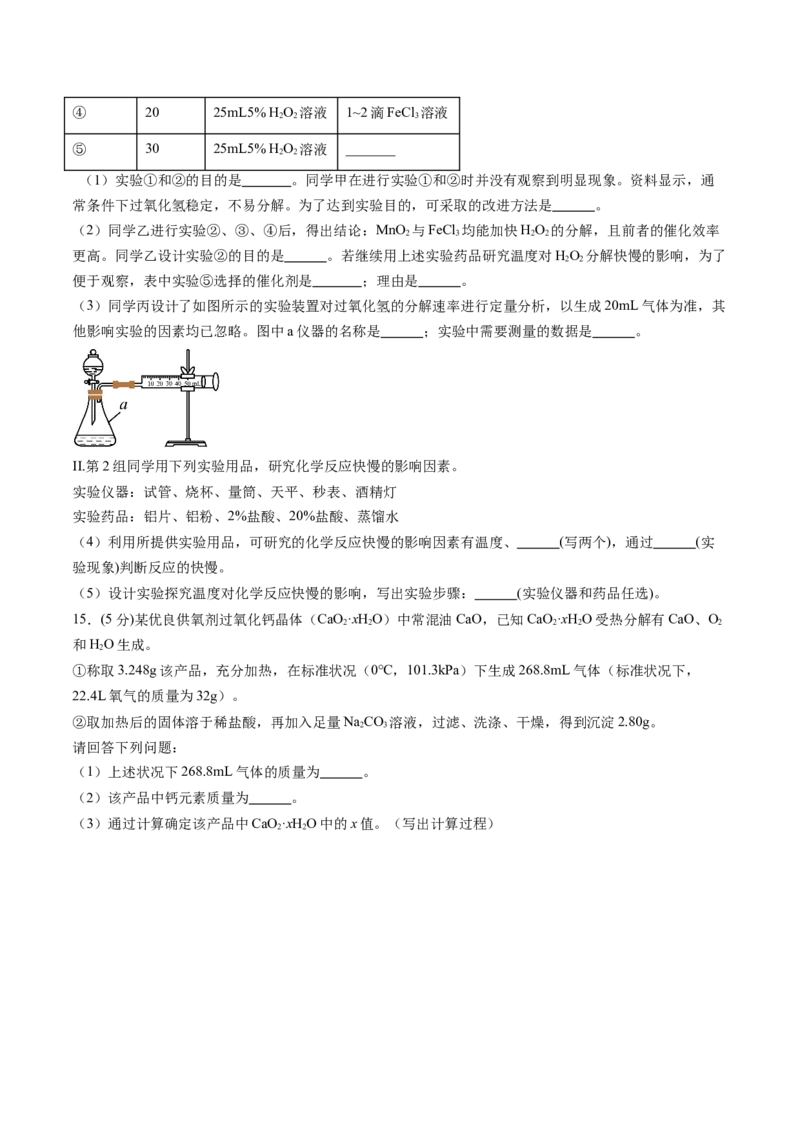
③如图是氨氧化率与氨—空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情
况。当氨氧化率达到100%,理论上Y【 】=1.25,实际生产要将y值维护在1.7~2.2之间,原因是
。
【说明:n(O )可以认为是表示氧气分子堆积数目的一种物理量,即n(O )值越大,说明氧分子数目越多】
2 2
14.(14分)某学校两课外化学兴趣小组分别以HO 分解、金属与酸反应为例,探究不同条件对反应速率的
2 2
影响。
I.第1组同学在常温下按照如表所示的方案完成HO 分解的探究实验。
2 2
实验编
温度(℃) 反应物 催化剂
号
① 20 25mL3% HO 溶液 无
2 2
② 20 25mL5% HO 溶液 无
2 2
③ 20 25mL5% HO 溶液 0.1gMnO
2 2 2④ 20 25mL5% HO 溶液 1~2滴FeCl 溶液
2 2 3
⑤ 30 25mL5% HO 溶液 _______
2 2
(1)实验①和②的目的是 。同学甲在进行实验①和②时并没有观察到明显现象。资料显示,通
常条件下过氧化氢稳定,不易分解。为了达到实验目的,可采取的改进方法是 。
(2)同学乙进行实验②、③、④后,得出结论:MnO 与FeCl 均能加快HO 的分解,且前者的催化效率
2 3 2 2
更高。同学乙设计实验②的目的是 。若继续用上述实验药品研究温度对HO 分解快慢的影响,为了
2 2
便于观察,表中实验⑤选择的催化剂是 ;理由是 。
(3)同学丙设计了如图所示的实验装置对过氧化氢的分解速率进行定量分析,以生成20mL气体为准,其
他影响实验的因素均已忽略。图中a仪器的名称是 ;实验中需要测量的数据是 。
II.第2组同学用下列实验用品,研究化学反应快慢的影响因素。
实验仪器:试管、烧杯、量筒、天平、秒表、酒精灯
实验药品:铝片、铝粉、2%盐酸、20%盐酸、蒸馏水
(4)利用所提供实验用品,可研究的化学反应快慢的影响因素有温度、 (写两个),通过 (实
验现象)判断反应的快慢。
(5)设计实验探究温度对化学反应快慢的影响,写出实验步骤: (实验仪器和药品任选)。
15.(5分)某优良供氧剂过氧化钙晶体(CaO·xHO)中常混油CaO,已知CaO·xHO受热分解有CaO、O
2 2 2 2 2
和HO生成。
2
①称取3.248g该产品,充分加热,在标准状况(0℃,101.3kPa)下生成268.8mL气体(标准状况下,
22.4L氧气的质量为32g)。
②取加热后的固体溶于稀盐酸,再加入足量NaCO 溶液,过滤、洗涤、干燥,得到沉淀2.80g。
2 3
请回答下列问题:
(1)上述状况下268.8mL气体的质量为 。
(2)该产品中钙元素质量为 。
(3)通过计算确定该产品中CaO·xHO中的x值。(写出计算过程)
2 2