文档内容
2024 年中考第二次模拟考试(新疆卷)
化 学
(考试时间:50分钟 试卷满分:60分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cu-64 S-32
一、选择题(本大题共10小题,每小题2分,共20分。每小题给出的四个选项中,只有一个选项最符合
题目的要求)
1.下列同学们在周末进行的劳动实践活动中,一定发生了化学变化的是( )
A.采摘苹果 B.整理书本
C.生火做饭 D.缝补衣服
【答案】C
【详解】A、采摘苹果没有新物质生成,是物理变化;
B、整理书本没有新物质生成,是物理变化;
C、生火做饭有燃烧发生,有新物质生成,是化学变化;
D、缝补衣服没有新物质生成,是物理变化;
故选C。
2.氮气和氧气都是空气中的主要成分,下列比较错误的是( )
A.空气中氮气比氧气多 B.氧气比氮气化学性质活泼
C.氮气、氧气都不易溶解于水 D.氧气能够在空气中燃烧而氮气不能
【答案】D
【详解】A、空气的成分主要以氮气和氧气为主,氧气约占五分之一,氮气约占五分之四,因此空气中氮
气比氧气多,说法正确,不符合题意;
B、氧气比氮气化学性质活泼,说法正确,不符合题意;
C、氮气、氧气都不易溶解于水,说法正确,不符合题意;
D、氧气不具有可燃性,不能在空气中燃烧,氧气具有助燃性,可燃物可以在氧气中燃烧;氮气不能燃烧也不支持燃烧,说法错误,符合题意。
故选:D。
3.化肥和农药对农业增产有重要作用。下列说法正确的是( )
A.磷酸二氢铵属于磷肥
B.碳酸氢铵需密封保存于阴凉处
C.改善植物叶片发黄,应施用钾肥
D.用熟石灰区分氯化钾和尿素[ ]
【答案】B
【详解】A、磷酸二氢铵中含有磷元素和氮元素,属于复合肥,不符合题意;
B、磷酸二氢铵受热易分解,需密封保存于阴凉处,符合题意;
C、改善植物叶片发黄,应施用氮肥,不符合题意;
D、氯化钾和尿素都不能与熟石灰反应,故不能用熟石灰区分氯化钾和尿素,不符合题意。
故选:B。
4.下列实验操作或叙述中,正确的是( )
A.手持试管给试管里的物质加热
B.将鼻孔凑到集气瓶口闻气体的气味
C.酒精灯的火焰可以用嘴吹灭
D.一般用药匙或镊子取用固体药品
【答案】D
【详解】A、给试管内的物质加热,应用试管夹夹持试管进行加热,不符合题意;
B、闻药品气味通常采用扇闻的方法,即用手在瓶口轻轻扇动,使少量气体飘入鼻孔,不符合题意;
C、用完酒精灯后,必须用灯帽盖灭酒精灯,不符合题意;
D、取用块状固体药品用镊子或药匙,取用粉末状固体药品用药匙,符合题意。
故选:D。
5.溴元素广泛用于医药、农业、印染工业。有关元素信息如图所示,下列说法不正确的是( )
A.溴元素是金属元素
B.溴原子的质子数为35C.溴元素与氯元素化学性质相似
D.溴元素的相对原子质量为79.90
【答案】A
【详解】A、溴带有“氵”字旁,属于非金属元素,故选项说法错误;
B、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为35;根据原子中原
子序数=核电荷数=质子数=核外电子数,则溴原子的质子数为35,故选项说法正确;
C、最外层电子数相同,化学性质相似。溴元素与氯元素的最外层电子数相同,所以化学性质相似,故选
项说法正确;
D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,溴元素的相对原子质量为79.90,
故选项说法正确。
故选A。
6.2024年1月11日发布的《中共中央、国务院关于全面推进美丽中国建设的意见》提出要“培育弘扬生
态文化,践行绿色低碳生活方式”。下列做法中不符合该要求的是( )
A.推行无纸化办公 B.掩埋废旧电池
C.回收塑料,再生利用 D.坐公共交通工具出行
【答案】B
【详解】A、推行无纸化办公会减少环境污染,故选项做法合理;
B、掩埋废旧电池会造成土壤污染,故选项做法不合理;
C、回收塑料,再生利用会减少白色污染,故选项做法合理;
D、坐公共交通工具出行,能减少尾气排放,有利于保护环境,故选项做法合理。
故选:B。
7.逻辑推理是化学常用的思维方法,下列推理正确的是( )
A.单质由同种元素组成,所以由同种元素组成的纯净物一定是单质
B.阳离子是带正电荷的粒子,所以带正电荷的粒子一定是阳离子
C.溶液具有均一性和稳定性,所以均一、稳定的液体一定是溶液
D.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
【答案】A
【详解】A、单质是由同种元素组成的纯净物,单质由同种元素组成,由同种元素组成的纯净物一定是单
质,正确;
B、阳离子是带正电的粒子,但是带正电的粒子不一定是阳离子,如质子带正电,错误;
C、溶液是均一、稳定的混合物,但是均一、稳定的液体不一定是溶液,如水是均一、稳定的液体,却不是溶液,错误;
D、中和反应生成盐和水,但是生成盐和水的反应不一定是中和反应,如氢氧化钠和二氧化碳反应生成碳
酸钠和水,错误。
故选A。
8.下列有关化学用语的说法正确的是( )
A.O 表示3个氧原子
3
B.NaCl是由Na+和Cl-构成的
C.S-2表示单质硫中硫元素的化合价为-2
D.3Mg2+中的“2”表示3个镁离子带2个单位的正电荷
【答案】B
【详解】A、O 表示一个臭氧分子,3个氧原子用3O表示,选项错误;
3
B、氯化钠是由钠离子和氯离子构成的,钠离子带一个单位的正电荷,氯离子带一个单位负电荷,根据离
子符号的书写,将数字和正负号标在元素符号的右上角,先写数字,后标正负号,数值为1,省略不写。
故钠离子和氯离子分别表示为:Na+和Cl-,选项正确;
C、标注元素的化合价标在元素符号的正上方,先写正负号,后写数字,1不省略,且硫单质中硫元素化合
价为0,表示为 ,选项错误;
D、3Mg2+中的“2”表示1个镁离子带2个单位的正电荷,选项错误;
故选B。
9.甲、乙、丙三种物质的溶解度曲线如图所示,下列说法正确的是( )
A.用搅拌或加热的方法能增大乙在水中的溶解度
B.将甲溶液由t℃降温至t℃,不一定有晶体析出
3 1
C.气体溶解度随温度的变化趋势与甲相似
D.将t℃等质量的甲、乙、丙饱和溶液分别降温到t℃,所得溶液的质量:丙=甲>乙
3 1
【答案】B
【详解】A、乙的溶解度随温度的升高而升高,故加热能增大乙在水中的溶解度,但是搅拌方法不能增大乙在水中的溶解度,故A错误;
B、将甲溶液由t℃降温至t℃,未说明溶液是否饱和,不一定有晶体析出,故B正确;
3 1
C、气体的溶解度随温度升高而降低,变化的趋势与丙相似,故 C错误;
D、将t℃时等质量的甲、乙、丙三种物质的饱和溶液同时降温至t℃,丙的溶解度变大,变为不饱和溶液,
3 1
没有固体析出;降温时,甲的溶解度减少的数值大于乙,即甲析出的固体质量大于乙,所以所得溶液质量
由大到小的顺序为丙>乙>甲;故D错误。
故选B。
10.下列实验方案不能达到实验目的的是( )
选
实验目的 实验方案
项
A 除去粗盐中混有的泥沙 溶解、过滤、蒸发
B 检验碳酸钠溶液中是否含有氯化钠 加入过量的稀盐酸后,再滴加硝酸银溶液
从MgCl 和NaCl的混合溶液中提纯 加入过量的NaOH溶液,过滤,洗涤,向滤渣中加适量稀盐
C 2
MgCl 酸,蒸发
2
D 分离二氧化锰和氯化钾固体 加入足量水溶解,过滤,洗涤滤渣、干燥;滤液蒸发结晶
A.A B.B C.C D.D
【答案】B
【详解】A、氯化钠易溶于水,泥沙难溶于水,可以采用溶解、过滤的方法除去不溶性泥沙,再通过蒸发
结晶得到氯化钠,该实验能达到实验目的,不符合题意;
B、向溶液中加入过量的稀盐酸,盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,再加入硝酸银溶液,无
论原溶液中是否含有氯化钠,都会产生氯化银沉淀,该实验不能达到实验目的,符合题意;
C、加入过量的NaOH溶液,氯化镁与氢氧化钠反应生成氢氧化镁沉淀和氯化钠,经过过滤、洗涤,向滤
渣中加适量稀盐酸,氢氧化镁与盐酸反应生成氯化镁和水,再通过蒸发结晶得到纯净的氯化镁,该实验能
达到实验目的,不符合题意;
D、氯化钾易溶于水,二氧化锰难溶于水,可以用加水溶解、过滤、洗涤滤渣、干燥的方法得到二氧化锰;
再对滤液进行蒸发结晶得到氯化钾,该实验能达到实验目的,不符合题意。
故选:B。
二、填空与简答题(本大题共3小题,每空1分,共20分)
11.(6分)“一稻济天下”说的就是我国著名企业家袁隆平,在不断培育高产水稻的同时,还成功培育
出了适合碱性土地的“海水稻”,解决了全世界的粮食危机是中国和世界之所幸。
(1)人体健康:“海水稻”富含淀粉和硒元素,淀粉属于六大营养素中的 ,硒属于 元素(选填“金属”或“非金属”),可以有效预防疾病。
(2)粮食高产:“庄稼好不好全靠施肥巧不巧”,常见的化肥有 等,其中
中碳的化合价为 ,属于复合肥的是 。
(3)绿色环保:稻草是一种宝贵的资源,其主要成分纤维素在催化剂和水的作用下会产生葡萄糖,葡萄
糖再与酒化酶作用转化成乙醇,其中反应为 请写出X的化学式 。因
此从能源分类来看属于 资源(选填“可再生”或“不可再生”)。
【答案】(1) 糖类 非金属
(2) +4 KNO /硝酸钾
3
(3) CO 可再生
2
【详解】(1)淀粉属于六大营养素中的糖类;硒元素名称带“石”字旁,属于非金属元素,故填:糖类;
非金属;
(2) 中钾元素化合价为+1价,氧元素化合价为-2价,设碳元素化合价为x,根据化合物中正负化
合价代数为0,则有(+1)×2+ x+(-2)×3=0,得x=+4价;
中含有N、P、K中的钾元素,属于钾肥,Ca(HPO ) 中含有N、P、K中的磷元素,属于磷肥,
2 4 2
KNO 中含有N、P、K中的钾元素和氮元素,属于复合肥;
3
故填:+4或+4价;KNO 或硝酸钾;
3
(3)根据质量守恒定律,反应前后原子的种类、数目不变,反应前C、H、O的原子个数分别为6、12、
6,反应后C、H、O的原子个数分别为4、12、2,则2X中含有2个碳原子和4个氧原子,X的化学式为
CO;
2
稻草通过一系列反应能转化为乙醇,说明乙醇属于可再生能源;
故填:CO;可再生。
2
12.(7分)随着我国科技的进步,航天工业蓬勃发展。
(1)空间站中利用如图所示原理为航天员提供氧气,产生氧气的一端连接的应是太阳能电池的
(填“正”或“负”)极。在水中加入适量的 可增强水的导电性。该化学反应说明了水由
组成。(2)航天员在空间站中呼吸的人造空气成分与我们周围的空气成分相似。为保障空间站中航天员的正常
呼吸,人造空气中的氧气应占人造空气总体积的约__________(填标号)。
A.78% B.21% C.0.94%
(3)SO 、NO 、O、CO均会造成空气污染,下雨时还会进一步形成酸雨的是 (填化学式)。
2 2 3
请写出一条保护空气的合理措施: 。
(4)实验兴趣小组的同学记录了某地区四天的空气质量指数,其中空气质量最好的是第 天。
第一天 第二天 第三天 第四天
空气质量指
35 65 23 108
数
【答案】(1) 正 氢氧化钠或硫酸钠 氢元素和氧元素
(2)B
(3) SO 、NO 植树造林、加强大气质量监测、绿色出行等(合理即可)
2 2
(4)三
【详解】(1)电解水实验中,正极产生氧气,故产生氧气的一端连接的应是太阳能电池的正极;在水中
加入适量的氢氧化钠或硫酸钠可增强水的导电性;水通电生成氢气和氧气,氧气是由氧元素组成,氢气是
由氢元素组成,依据反应前后元素种类不变,说明水是由氢、氧元素组成的;
(2)空气中氧气含量为21%,“人造空气”与我们身边的空气成分含量基本相同,故“人造空气”中氧
气含量也约为21%,观察选项,20%与21%最接近;故选:B;
(3)会导致酸雨形成的是 SO 、NO ;为了保护空气,可以多植树造林、加强大气质量监测、绿色出行等;
2 2
(4)空气质量指数越小,说明空气质量越好,故空气质量最好的是第三天。
13.(7分)酸、碱、盐是几类重要的化合物,它们与人类的日常生活和工农业生产密切相关。
(1)请从下列物质中选择适当物质的序号填空。
A.浓硫酸 B.氯化钠 C.氢氧化钙
①可用作气体干燥剂的是 。
②可用于改良酸性土壤的是 。
③可作调味品的是 。
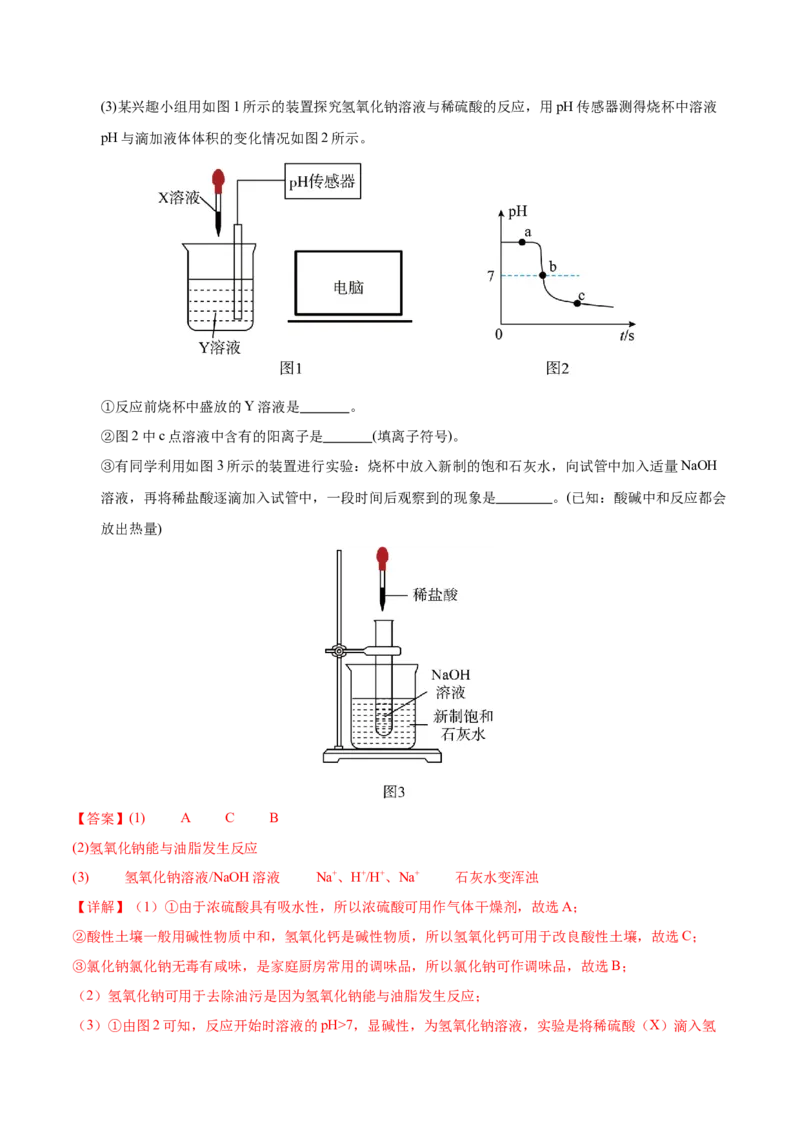
(2)氢氧化钠可用于去除油污,这是因为 。(3)某兴趣小组用如图1所示的装置探究氢氧化钠溶液与稀硫酸的反应,用pH传感器测得烧杯中溶液
pH与滴加液体体积的变化情况如图2所示。
①反应前烧杯中盛放的Y溶液是 。
②图2中c点溶液中含有的阳离子是 (填离子符号)。
③有同学利用如图3所示的装置进行实验:烧杯中放入新制的饱和石灰水,向试管中加入适量NaOH
溶液,再将稀盐酸逐滴加入试管中,一段时间后观察到的现象是 。(已知:酸碱中和反应都会
放出热量)
【答案】(1) A C B
(2)氢氧化钠能与油脂发生反应
(3) 氢氧化钠溶液/NaOH溶液 Na+、H+/H+、Na+ 石灰水变浑浊
【详解】(1)①由于浓硫酸具有吸水性,所以浓硫酸可用作气体干燥剂,故选A;
②酸性土壤一般用碱性物质中和,氢氧化钙是碱性物质,所以氢氧化钙可用于改良酸性土壤,故选C;
③氯化钠氯化钠无毒有咸味,是家庭厨房常用的调味品,所以氯化钠可作调味品,故选B;
(2)氢氧化钠可用于去除油污是因为氢氧化钠能与油脂发生反应;
(3)①由图2可知,反应开始时溶液的pH>7,显碱性,为氢氧化钠溶液,实验是将稀硫酸(X)滴入氢氧化钠溶液(Y)中;
②图中c点溶液的pH<7,显酸性,说明加入的硫酸过量,此时溶液中的阳离子有:Na+、H+;
③氢氧化钠和硫酸反应放出热量,饱和石灰水的温度上升,氢氧化钙的溶解度随温度的升高而减小,氢氧
化钙固体析出,所以石灰水变浑浊。
三、实验探究题(本大题共2个小题,每空1分,共13分)
14.(7分)根据如图所示装置,结合所学知识回答下列问题。
(1)实验室用A装置制取氧气,写出反应的化学方程式 。
(2)实验室用B、E、C装置制取并收集干燥的氧气,则E中应盛放的试剂是 。
(3)实验室用D装置收集氧气, 时开始收集;E装置中充满水时,也可以作为氧气的收集装置,
则氧气应从 端通入(填“a”或“b”)。
(4)实验室要制取二氧化碳气体,选择的发生装置是 (填代号),反应的化学方程式为 。
(5)B装置还可用来制取生活中一种常见气体,写出实验室制取该气体的化学方程式 。
【答案】(1)
(2)浓硫酸/浓HSO
2 4
(3) 待导管口气泡连续均匀冒出 b
(4) B
(5)
【详解】(1)A装置适用于固体加热反应制取气体,且试管口有一团棉花,适用于加热高锰酸钾制取氧气,
高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,该反应的化学方程式为:
;
(2)实验室用B、E、C装置制取并收集干燥的氧气,则E中应盛放的试剂是浓硫酸,浓硫酸具有吸水性,
且与氧气不反应,可用浓硫酸干燥氧气;
(3)实验室用D装置,即排水法收集氧气,应待导管口气泡连续均匀冒出时,开始收集,因为一开始排出的是空气;
E装置中充满水时,也可以作为氧气的收集装置,氧气的密度比水小,则氧气应从b端通入;
(4)实验室通常用石灰石(或大理石)与稀盐酸反应制取二氧化碳,该反应属于固液不加热反应,发生
装置可选B;
石灰石的主要成分碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,该反应的化学方程式为:
;
(5)B装置也适用于实验室制取氢气,实验室通常用锌粒与稀硫酸反应制取氢气,锌和稀硫酸反应生成硫
酸锌和氢气,该反应的化学方程式为: 。
15.(6分)某化学兴趣小组的同学发现,不同物质的变化常伴随着相同的实验现象。但从化学的角度去
研究,会发现其本质的区别。
实验Ⅰ:
【实验操作】如图所示,分别向盛有一定量氢氧化钠固体、氧化钙固体的试管里加入一定量的水,U
形管内装有红墨水。
【实验现象]
(1)甲、乙两组实验均观察到U形管的a、b液面变化情况是 。
【本质归纳】
(2)相同的实验现象,可以由不同的变化引起。请从变化的本质分析,甲、乙实验的区别是 。
实验Ⅱ:
【实验操作】实验室中有一瓶变质的氢氧化钠溶液和一瓶新制的氢氧化钠溶液。由于标签污染,同学
取两种适量液体于试管中,滴人酚酞溶液后,发现溶液均变红。同学们将两瓶溶液标注为A、B,分
别取适量A、B溶液于两支试管中,并设计了以下三组实验进行鉴别:
分组 现象 结论
第一组:将足量稀盐酸分别滴 A中液体中无明显现象,B A液体为新制的氢化钠溶液,B
入A、B液体中 中液体______ 液体为变质的氢氧化钠溶液第二组:将适量氯化钡溶液
A中液体中无明显现象,B
(呈中性)分别滴入A、B液
中液体有白色沉淀产生
体中
第三组:将适量X溶液分别滴 A中液体中无明显现象,B
入A、B液体中 中液体有白色沉淀产生
【实验分析】
(3)根据实验结论推断,第一组实验的现象为A中液体中无明显现象,B中液体 。
(4)请写出第二组实验中产生白色沉淀的化学方程式: 。
(5)已知三组同学选取的实验药品的种类不同,请写出符合第三组实验选取的药品X的化学式:
(写出一个即可)。
【拓展反思】
(6)为证明变质的氢氧化钠溶液中含有氢氧化钠,同学们取第二组滴入了适量氯化钡溶液的B液体,测
其pH (选填“>”“<”或“=”)7,再向其中加入碳酸钠溶液,产生白色沉淀,能说明B中液体
含有氢氧化钠。
【答案】(1)a端液面下降,b端液面上升
(2)甲实验为物理变化没有新物质产生,乙实验为化学变化有新物质产生
(3)有气泡产生
(4)Na CO+ BaCl =BaCO ↓+2NaCl
2 3 2 3
(5)Ca(OH) 或Ba(OH)(合理即可)
2 2
(6)>
【详解】(1)甲组氢氧化钠固体溶于水放热,乙组氧化钙和水反应生成氢氧化钙,该反应放热,均会导
致温度升高,装置内压强增大,则a端液面下降,b端液面上升;
(2)甲实验为氢氧化钠固体的溶解,没有新物质生成,属于物理变化,乙实验为氧化钙和水反应生成氢
氧化钙,有新物质生成,属于化学变化;
(3)氢氧化钠的变质是氢氧化钠和二氧化碳反应生成碳酸钠和水,根据实验结论A液体为新制的氢化钠
溶液,B液体为变质的氢氧化钠溶液,则B中含有碳酸钠,所以第一组实验中,加入足量的稀盐酸,稀盐
酸和碳酸钠反应生成氯化钠、二氧化碳和水,则可观察到B中液体有气泡产生;
(4)根据实验结论A液体为新制的氢化钠溶液,B液体为变质的氢氧化钠溶液,则B中含有碳酸钠,加
入适量的氯化钡溶液,氯化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠,化学方程式为:
;
(5)已知三组同学选取的实验药品的种类不同,第一组实验中用的稀盐酸(属于酸),第二组实验中用的氯化钡(属于盐),则第三组实验选取的实验药品种类可以为碱,根据碳酸钠和氢氧化钙或氢氧化钡反
应会生成白色沉淀,则可选取Ca(OH) 或Ba(OH)(合理即可);
2 2
(6)为证明变质的氢氧化钠溶液中含有氢氧化钠,同学们取第二组滴入了适量氯化钡溶液的B液体,氯
化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠,根据结论B液体中含有氢氧化钠,氢氧化钠溶液显碱性,则
测其pH>7,再向其中加入碳酸钠溶液,产生白色沉淀,说明B液体中含有氯化钡,即第二组实验中,氯
化钡过量,则液体B中不可能含有碳酸钠,所以B液体中溶液的pH>7,能说明B中液体含有氢氧化钠。
四、计算题(本题共1小题,共7分)
16.计算题某废液100克,含有硫酸和硫酸铜,向废液中慢慢滴入16%的NaOH溶液,溶液pH的变化如
图所示。
(1)与CuSO 反应的NaOH溶液的质量是 g。
4
(2)反应结束后,原废液中硫酸铜的质量分数为多少 ?(写出计算过程)
【答案】(1)150
(2)解:设原废液中硫酸铜的质量为x
原废液中硫酸铜的质量分数为
答:原废液中硫酸铜的质量分数为48%。
【分析】将氢氧化钠加到硫酸和硫酸铜的混合溶液中,氢氧化钠与硫酸优先反应,消耗氢氧化钠溶液
50g,然后氢氧化钠再与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,消耗氢氧化钠溶液200g-50g=150g。
【详解】(1) 根据分析,与CuSO 反应的NaOH溶液的质量是150g,故填:150;
4
(2)见答案