文档内容
2024 年中考第一次模拟考试(盐城卷)
化 学
一、单项选择题(本大题包括15小题,每小题有四个选项,其中只有一个选项符合题意,请将符合题意的
选项代号填在相应位置上。每小题2分,共30分)
1.化学是人类进步的阶梯。下列说法正确的是
A.化学与家居:含有食品添加剂的食品对人体都有害
B.化学与出行:为减少公交压力,提倡多开私家车出行
C.化学与环境:为防止工厂废气污染空气,可将工厂烟囱加高
D.化学与社会发展:新材料的使用为我国空间站的建设提供了保障
【答案】D
【解析】A、合理使用食品添加剂,对丰富食品生产和促进人体健康有好处,可以食用,但不能过量,故
A说法错误;
B、多开私家车会增加化石燃料的消耗,增大有害气体与烟尘的排放而造成环境污染,故B说法错误;
C、将工厂烟囱加高只会将有害气体排放到高空,但不能从根本上减少污染物的排放,不能解决空气污染
问题,故C说法错误;
D、化学可以研制新材料,新材料的使用为我国空间站的建设提供了保障,故D说法正确;
故选:D。
2.“千里海岸,广袤滩涂,一片胜景”。盐城坚持把“生态优先、绿色低碳”作为高质量发展的“命
脉”,以下选项不符合这一理念的是
A.发展公共交通,提倡绿色出行 B.开发新能源,减少化石燃料使用
C.大量使用化肥,提高粮食产量 D.建立自然保护区,保护生物多样性
【答案】C
【解析】A、发展公共交通,提倡绿色出行,有利于环保,符合“生态优先、绿色低碳”的理念,不符合
题意;
B、开发新能源,减少化石燃料使用,有利于改善生态环境,符合“生态优先、绿色低碳”的理念,不符
合题意;
C、大量使用化肥,提高粮食产量,会造成水体和土壤污染,不符合“生态优先、绿色低碳”的理念,符
合题意;
D、建立自然保护区,保护生物多样性,可以有效的保护生物,符合“生态优先、绿色低碳”的理念,不
符合题意;
故选:C。
3.2022年元月8日,盐城非遗体验馆正式对外开放,下列非遗项目中涉及化学变化的是
A.陈皮酒酿造 B.麦秆剪贴 C.海盐晒制 D.老虎鞋绣制
【答案】A
【解析】A、陈皮酒酿造过程中有新物质酒精生成,涉及化学变化,故A正确;B、麦秆剪贴没有新物质生成,属于物理变化,故B错误;
C、海盐晒制属于蒸发结晶,没有新物质生成,故C错误;
D、老虎鞋绣制没有新物质生成,属于物理变化,故D错误。
故选A。
4.二氧化钒的“冷热双吸”材料,可助力我国实现“双碳”目标。钒元素在周期表中的信息如图所示,
下列说法不正确的是
A.钒属于金属元素 B.钒原子中子数为23
C.钒的相对原子质量为50.94 D.二氧化钒的化学式为VO
2
【答案】B
【解析】A、由元素名称的偏旁“金”字可知,钒属于金属元素,故说法正确;
B、根据钒元素在周期表中的信息可知,原子序数=核外电子数=质子数=核电荷数=23,不能得出钒原子中
子数为23,故说法错误;
C、根据钒元素在周期表中的信息可知,钒的相对原子质量为50.94,故说法正确;
D、根据氧化物的书写原则,氧化物中,氧在后,并在氧元素右下角标出氧原子的个数,则二氧化钒的化
学式为VO ,故说法正确。
2
故选B。
5.规范操作是实验成功的前提。下列实验操作正确的是
A.倾倒液体 B.稀 释浓硫酸 C.过滤 D.测溶液pH
【答案】C
【解析】A、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨试管口;图中瓶塞没有
倒放,故A错误;
B、稀释浓硫酸时,要把浓硫酸慢慢地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时的扩散;
一定不能把水注入浓硫酸中,以防止酸液飞溅;且不能在量筒内稀释浓硫酸,故B错误;
C、过滤时,要“一贴、二低、三靠”,故C正确;
D、用pH试纸测定溶液的pH时,正确的操作方法为在白瓷板或玻璃片上放一小片pH试纸,用玻璃棒蘸
取待测液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,读出pH;不能将pH试纸伸入待测液中,
以免污染待测液,故D错误。
故选:C。6.下列有关化学用语的叙述,正确的是
A.He:表示氖气 B.C :表示60个碳原子
60
C.2N:表示2个氮原子 D.Fe2+:表示铁离子
【答案】C
【解析】A、 由原子构成的物质,物质符号直接用元素符号表示(金属、稀有气体、金刚石等都是由原子
直接构成的物质);Ne表示氖气,错误;
B、 表示一个分子中原子或原子团的个数数字要加在右下方,C 可以表示1个C 分子中含有60个碳原子,
60 60
错误;
C、 原子的表示方法用元素符号表示,表示微粒的个数在微粒前面加对应数字;2N:表示2个氮原子,正
确;
D、由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正
负符号在后,带1个电荷时,1要省略;表示多个该离子,在其符号前加上相应的数字;Fe2+可以表示亚铁
离子,错误。
故选C。
7.某海水淡化系统(如下图)工作时,蒸发腔中的水在光热作用下变为水蒸气,太阳能风扇将水蒸气吹到冷
凝腔冷凝,实现海水淡化。下列说法错误的是
A.光热作用下,水分子运动速率加快
B.液态水变为水蒸气,水分子间的间隔变大
C.水蒸气冷凝为水,水分子本身变小
D.海水变为淡水,水分子化学性质不变
【答案】C
【解析】A、温度越高分子运动速度越快,故光热作用下,水分子运动速率加快,选项正确;
B、液态水变为水蒸气,水分子本身没有改变而是水分子间的间隔变大,选项正确;
C、水蒸气冷凝为水,水分子本身没有改变而是水分子间的间隔变小 ,选项错误;
D、海水变为淡水,水分子本身没有改变,分子是保持物质化学性质的最小粒子,故水的化学性质不变,
选项正确;
答案为:C。
8.今年央视“3·15”特别节目曝光,某品牌肉制品中含有毒物质瘦肉精。某种瘦肉精的化学式为
C H ClNO,下列有关该瘦肉精的说法中正确的是
12 19 3 2
A.该瘦肉精由12个碳原子,19个氢原子、3个氯原子、2个氮原子和1个氧原子构成
B.该瘦肉精由碳、氢、氯、氮、氧五种元素组成
C.该瘦肉精分子中含有氮分子
D.该瘦肉精分子中含有氧气
【答案】B
【分析】化学式中元素符号右下角的数字表示该微粒的个数。
【解析】A、由化学式可知,一个瘦肉精分子由12个碳原子,19个氢原子、3个氯原子、2个氮原子和1
个氧原子构成,不符合题意;B、由化学式可知,该瘦肉精由碳、氢、氯、氮、氧五种元素组成,符合题意;
C、由化学式可知,一个瘦肉精分子中含有两个氮原子,不符合题意;
D、由化学式可知,一个瘦肉精分子中含有1个氧原子,不符合题意;
故选B。
9.科学思维是从化学视角研究物质及其变化规律的思路与方法,下列说法正确的是
A.变化与守恒:依据质量守恒定律,64gCu和16gO 充分反应可得到80gCuO
2
B.模型与推理:化学反应伴随能量的变化,有能量变化的一定是化学反应
C.宏观与微观:氧气和液氧物理性质差异较大,因为两者的分子构成不同
D.探究与创新:探究氧化铜是否为过氧化氢分解的催化剂,只需设计实验证明氧化铜能否改变化学反应
速率即可
【答案】A
【解析】A、根据化学方程式, ,128份质量的铜与32份质量的氧气反应生成
160份质量的氧化铜,所以64gCu和16gO 充分反应可得到80gCuO,故选项符合题意;
2
B、化学反应伴随着能量的变化,但有能量变化的不一定是化学反应,如电灯通电发光放热,有能量变化,
但不是化学反应,故选项不符合题意;
C、氧气和液氧都是由氧气分子构成,分子构成相同,两者物理性质差异较大是因为分子间的间隔与分子
的运动情况不同,故选项不符合题意;
D、催化剂能改变化学反应速率,且反应前后质量和化学性质不变,所以需要验证氧化铜可以做过氧化氢
分解的催化剂,除了验证氧化铜能改变化学反应速率外,还需要验证其反应前后质量和化学性质不变,故
选项不符合题意。
故选:A。
10.下列物质的转化在给定条件下均能实现的是
A.
B.
C.
D.
【答案】C
【解析】A、碱式碳酸铜受热分解为氧化铜、水和二氧化碳,但氧化铜不与水反应,无法转化为氢氧化铜,
故A错误;
B、铁和氧气在点燃条件下反应生成四氧化三铁,故B错误;
C、氯化钠和氨气、水及二氧化碳反应生成碳酸氢钠和氯化铵,碳酸氢钠与稀硫酸反应生成硫酸钠、水和
二氧化碳,故C正确;
D、氢氧化钙和稀盐酸反应生成氯化钙和水,但氯化钙与二氧化碳不反应,氯化钙应与碳酸钠反应转为碳酸钙,故D错误。
故选C。
11.如图为硫的价类图,纵坐标表示硫的化合价,横坐标表示含硫物质的类别,例如:C点可表示+4价硫元
素的氧化物(SO )。下列说法错误的是
2
A.A 点表示的物质的化学式可以是 NaS
2
B.B点表示的物质类别属于单质
C.C点表示的物质有毒,可以用 HO或者 NaOH 溶液吸收
2
D.若 F点表示的物质含铜元素,E转化为 F只能加 Cu(OH) 实现
2
【答案】D
【解析】A、据图可知,A 点表示的物质是盐,硫元素的化合价是-2价, NaS属于盐,在 NaS中,钠
2 2
的化合价是+1,硫的化合价是-2。A正确;
B、据图可知,B点表示的物质中硫元素的化合价为0,单质硫中硫元素的化合价为0,所以B点表示的物
质类别属于单质。B正确;
C、据图可知,C点表示的物质是氧化物,硫元素的化合价为+4价,即C点表示的物质是二氧化硫,二氧
化硫有毒;二氧化硫与水反应生成亚硫酸;二氧化硫与氢氧化钠反应生成亚硫酸钠和水。C正确;
D、据图可知,F点表示的物质含铜元素,F是盐,则F是硫酸铜;E是酸,硫元素的化合价是+6,即是硫
酸,硫酸转化为硫酸铜,可以加CuO或Cu(OH) 实现。D错误。
2
综上所述:选择D。
12.通过下列实验操作和现象能得出相应结论的是
实验操作 现象 结论
向收集满CO 的软塑料瓶中加入约三分之一体积滴有石蕊 塑料瓶变瘪,溶
2
A CO 能与石蕊反应
2
试液的水,旋紧瓶盖,振荡 液变红
B 往久置于空气中的氢氧化钠溶液滴加稀硫酸 有气泡产生 氢氧化钠溶液已变质
无色溶液中一定含有
C 在某无色溶液中滴加氯化钡溶液和稀硝酸 有白色沉淀
离子
把质量相同的镁条与锌粒同时放入相同浓度和体积的盐酸 镁条与盐酸产生 镁的金属活动性比锌
D
中 气体更快 强
【答案】B
【解析】A、根据二氧化碳溶于水,并且能和水反应产生碳酸,使塑料瓶内压强减小,因此该实验产生的
现象为:瓶子变瘪,溶液变红,但不能得出结论:CO 能与石蕊反应,故A错误;
2
B、氢氧化钠变质是与空气中的二氧化碳反应生成碳酸钠和水,氢氧化钠和稀硫酸反应不能产生气泡,而
氢氧化钠变质的产物碳酸钠能够和稀硫酸反应产生二氧化碳,因此观察到气泡产生,说明氢氧化钠已经变
质,故B正确;
C、氯化钡能够和硫酸根离子或银离子结合产生沉淀,因此不能说明无色溶液中一定含有硫酸根离子,故C错误;
D、把质量相同的镁条与锌粒同时放入相同浓度和体积的盐酸中,不能比较两种金属的活动性顺序,因为
选择的两种金属的形状不同,故D错误;
故选:B。
13.如图是A、B、C三种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是
A.将50℃时A、B的溶液降温至20℃,析出晶体的质量A>B
B.将50℃时A、B、C的溶液降温至30℃,可得溶液的溶质质量分数为
A=B>C
C.将50℃时C的溶液降温至30℃,C溶液的溶质质量分数一定不变
D.M点表示30℃时A、B两种物质的溶液质量相同
【答案】C
【解析】A、由于没有确定50℃时A、B两溶液的质量和溶液是否是饱和溶
液,因此无法比较A、B析出晶体的多少,故选项说法错误;
B、由于没有确定50℃时A、B、C的溶液是否是饱和溶液,因此无法比较A、B、C三种溶液的溶质质量
分数大小,故选项说法错误;
C、由于C物质的溶解度随温度降低而增大,因此将50℃时C的溶液降温至30℃时,C物质的溶解度增
大,此时溶液一定为不饱和溶液(不管50℃时,C的溶液是否饱和),该过程中没有晶体析出,溶液组成
不变,即C溶液的溶质质量分数一定不变,故选项说法正确;
D、M点表示30℃时A、B两种物质的溶解度相同,故选项说法错误。
故选:C。
14.CH 与CO 在催化剂作用下可得到合成气(CO和H),反应过程中催化剂表面还同时存在积碳反应
4 2 2
和消碳反应,原理如图1所示。以下说法错误的是
A.消碳反应的产物“ ”是CO
B.积碳反应为分解反应
C.为减少催化剂表面的积碳,可在原料气中加入适量二氧化碳
D.图2中温度高于600℃,催化剂表面积碳量减少的原因是生成的碳多于消耗的碳
【答案】D
【解析】A、甲烷和二氧化碳反应生成一氧化碳和氢气,一氧化碳分子由两种不同的原子构成,所以
是一氧化碳气体,故A正确;B、从图1可知,积碳反应是甲烷在催化剂的作用下转化为碳和氢气,该反应符合“一变多”,属于分解
反应,故B正确;
C、从图1可以看出,甲烷先转化为碳和氢气,碳和二氧化碳反应生成一氧化碳,所以为减少积碳,可在
原料气中适当增加二氧化碳气体的量,使催化剂表面的碳更快的转化为一氧化碳,故C正确;
D、图2中温度高于600℃,催化剂表面积碳量减少的原因可能是温度升高,消碳反应所消耗的碳的量多于
积碳反应产生的碳,故D错误。
故选D。
15.工业上可利用Fe O 和太阳能分解水制氢,流程如图。下列说法不正确的是
3 4
已知:①反应I:2Fe O 6FeO+O↑ ②反应Ⅱ:3FeO+HO Fe O +H ↑
3 4 2 2 3 4 2
A.上述流程中有三种元素的化合价发生了变化
B.理论上,每产生32gO,消耗水的质量为18g
2
C.相较电解水制氢而言,该方法具有节约能源,产品易分离的优点
D.2.9g可能由Fe、FeO、Fe O、Fe O 中的两种或多种组成的混合物中,铁元素质量为2.1g,则其中一定
2 3 3 4
含Fe O
2 3
【答案】B
【解析】A、过程中,由四氧化三铁转化为氧化亚铁,铁元素的化合价由+2价、+3价转化为+2价,有单
质的氧气和氢气生成故氢氧元素化合价发生了改变,故铁、氢、氧元素的化合价都发生了变化,说法正确;
B、解:设消耗水的质量为x,由反应Ⅰ、Ⅱ化学方程式可知:水与氧气的关系式为
则理论上,每产生32gO,消耗水的质量为36g,说法不正确;
2
C、较电解水制氢而言,该方法不需要通电,利用太阳能,具有节约能源的优点,产品Fe O 为固体,H 为
3 4 2
气体,具有产品易分离的优点,说法正确;
D、2.9g混合物中铁元素质量分数为 ,铁单质中铁元素质量分数为100%,氧化亚铁中
铁元素质量分数为: ,氧化铁中铁元素质量分数为: ,四氧化三铁
中铁元素质量分数为: ,只有氧化铁质量分数小于72.4%,故一定含有氧化铁,说法
正确;
故选B。
二、非选择题(本大题包括5小题,除标注分值外,每空1分,共40分)
16.(8分)“人间烟火,抚慰凡心”。疫情来袭,中国人仍可“医食无忧”,岁月静好,是因为祖国的繁荣富强,国士的负重前行!
(1)疫情期间,外出一定要戴口罩。佩戴活性炭口罩有防毒、除臭、滤菌、阻尘等功效,这是利用活性
炭的 性;
(2)测量体温,从微观角度看,水银体温计的原理是温度改变时 发生改变;
(3)治疗新冠肺炎的药物阿比多尔【其化学式为C H BrNOS】该物质中碳原子与氢原子的个数比为
22 25 2 3
;该药物需遮光,密封保存的可能原因是 ;
(4)84消毒液的有效成分是次氯酸钠(NaClO),电解饱和氯化钠溶液可制得次氯酸钠和一种可燃性气体,
该反应的化学方程式为 ;
(5)过氧乙酸(CHCOOOH)也是有效的消毒剂,某医疗小组用溶质质量分数为0.5%的过氧乙酸溶液200kg
3
对环境进行消毒,需要溶质质量分数为20%的过氧乙酸溶液 kg,在配制过程中量取20%的过氧乙
酸溶液用俯视读数,则最终配得的溶液浓度将 (“偏大”、“不变”或“偏小”)。
【答案】(1)吸附
(2)粒子的间隔(原子的间隔)
(3) 22:25 阿比多尔见光会分解(阿比多尔会发生反应、会与氧气反应等)
(4)
(5)5 偏小
【解析】(1)活性炭具有吸附性,佩戴活性炭口罩有防毒、除臭、滤菌、阻尘等功效,这是利用活性炭
的吸附性,故填:吸附。
(2)测量体温,从微观角度看,水银体温计的原理是温度改变时粒子的间隔(原子的间隔)发生改变;故填:
粒子的间隔(原子的间隔)。
(3)由化学式可知,该物质中碳原子与氢原子的个数比为22:25,该药物需遮光,密封保存的可能原因
是阿比多尔见光会分解(阿比多尔会发生反应、会与氧气反应等),故填:22:25;阿比多尔见光会分解(阿
比多尔会发生反应、会与氧气反应等)。
(4)电解饱和氯化钠溶液可制得次氯酸钠和一种可燃性气体,根据质量守恒元素种类不变,可燃性气体
是氢气,故填: 。
(5)用溶质质量分数为0.5%的过氧乙酸溶液200kg对环境进行消毒,需要溶质质量分数为20%的过氧乙
酸溶液 ,在配制过程中量取20%的过氧乙酸溶液,俯视读数,读数偏大,20%的
过氧乙酸溶液体积偏小,则最终配得的溶液浓度将偏小,故填:5;偏小。
17.(8分)某小组利用如图装置制备CO,并模拟自然界中CO 的循环。回答下列问题。
2 2(1)装置B中仪器①的名称是 。
(2)实验室用稀盐酸和石灰石制取CO,反应的化学方程式为 ,发生装置是
2
(填字母序号),用该装置制取气体的不足之处是 。
(3)为制得CO 的水溶液,CO 应从装置C的 (填“m”或“n”)端通入。
2 2
(4)将CO 的水溶液转移至烧杯,并组装装置如图D所示,置于阳光下一段时间,观察到有气泡产生,
2
检验该气体的方法是 。
(5)若气体M只能选用装置E收集,推测M具有的性质有 。
①能与氢氧化钠反应 ②密度比空气大
③密度比空气小 ④易溶于水或与水反应
【答案】(1)试管
(2)
A 无法控制反应速率或无法控制反应的发生和停止
(3)m
(4)将带火星的木条伸入收集到的气体中,观察木条是否复燃
(5)③④
【解析】(1)由图可知,装置B中仪器①的名称是:试管;
(2)石灰石的主要成分碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,该反应的化学方程式为:
;
该反应属于固液不加热反应,发生装置可选A;
用该装置制取气体的不足之处是不能控制反应速率或不能控制反应的发生和停止;
(3)为制得CO 的水溶液,CO 应从装置C的m端通入,这样反应比较充分;
2 2
(4)将CO 的水溶液转移至烧杯,并组装装置如图D所示,置于阳光下一段时间,观察到有气泡产生,
2
植物进行光合作用,吸收二氧化碳释放氧气,产生的气泡是氧气,氧气具有助燃性,检验氧气的方法:将
带火星的木条伸入收集到的气体中,观察木条是否复燃,木条复燃,说明是氧气;
(5)①M气体可用氢氧化钠干燥,说明M气体不能与氢氧化钠反应,错误;
②用万用瓶收集该气体,从短管通入,说明该气体密度比空气小,错误;
③用万用瓶收集该气体,从短管通入,说明该气体密度比空气小,正确;
④可用水吸收尾气,说明该气体易溶于水或与水反应,正确。
故选③④。
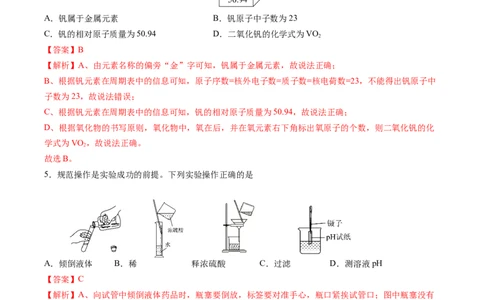
18.(7分)许多化学反应无明显现象,CO 与NaOH溶液的反应就是其中之一。
2
【提出问题】怎样证明CO 与NaOH溶液发生了反应?
2
【实验设计】
(1)同学们根据碱的化学性质,推测CO 与NaOH反应的化学方程式为 ,并从不同
2
的角度分别设计了实验加以验证。【实验验证】
(2)从压强变化的角度探究。
①利用图甲装置进行实验,先挤压胶头滴管,再打开止水夹,观察到烧瓶内形成红色“喷泉”,原因是烧
瓶内压强 (填“大于”或“小于”)外界大气压。
②利用图乙装置进行实验,将氢氧化钠溶液全部推入集气瓶中,过一会观察到气球鼓起,认为二者发生了
反应。同学们经过讨论认为该实验不严谨,理由是 。于是同学们将该装置中NaOH溶液换成
,做了对比实验,证明二者发生了反应。
(3)从新物质生成的角度探究。利用图丙装置进行实验,将氢氧化钠溶液全部推入集气瓶中,过一会打
开止水夹,观察到 ,也证明二者发生了反应。
(4)利用“数字化实验”探究。
实验测得烧杯中溶液的pH随时间的变化关系如图丁所示,由图可推知反应过程中浓度不断减少的离子
是 (填离子符号)。
【答案】(1)
(2)小于 氢氧化钠溶液含有水,而二氧化碳可以溶于水,且可与水反应 蒸馏水
(3)稀盐酸倒吸进入集气瓶,有气泡产生
(4) OH-
【解析】(1)碱可以与非金属氧化物反应,生成盐和水,故答案为: ;
(2)①由于二氧化碳气体可以溶于水同水反应,也能与氢氧化钠反应,生成碳酸钠和水,圆底烧瓶内气
体减少,内部压强减小,外界大气压大于内部压强,将烧杯内带有酚酞的氢氧化钠溶液压入圆底烧瓶内,
故①答案为:小于;
②因为二氧化碳可以溶于水同水反应,不存在氢氧化钠也可能出现相同现象,所以为了排除水的干扰,需要设计对比实验,将氢氧化钠溶液替换成蒸馏水,故②答案为:氢氧化钠溶液含有水,而二氧化碳可以溶
于水,且可与水反应;故③答案为:蒸馏水;
(3)二氧化碳与氢氧化钠反应后生成碳酸钠和水,气体减少,压强降低,外界大气压将烧杯内的稀盐酸
压入集气瓶,同时盐酸与集气瓶内的碳酸钠反应生成氯化钠、二氧化碳、水,所以可以看到集气瓶内有气
泡产生,故答案为:稀盐酸倒吸进入集气瓶,有气泡产生;
(4)根据图像可知,溶液PH值在减小,所以氢氧根离子浓度在不断减小,故答案为:OH-。
【点睛】本题主要考查二氧化碳与碱的反应及实验。
19.(8分)MgSO ·7H O是一种重要的化工原料,某工厂以一种镁矿石(主要成分为SiO 和MgCO ,还含
4 2 2 3
有少量FeCO,其它成分忽略)为原料制备MgSO ·7H O的主要流程如下:
3 4 2
查阅资料:
①SiO 既不溶于水也不溶于稀硫酸。
2
②已知:各离子开始沉淀及完全沉淀时的pH如下表所示:
离子 开始沉淀时的pH 完全沉淀时的pH
Fe3+ 2.7 3.7
Mg2+ 8 10.1
③硫酸镁溶液在不同温度下进行浓缩结晶,可得到不同的晶体:
温度/℃ -3.9~1.8 1.8~48.1 48.1~67.5 67.5~200
析出晶
MgSO ·12H O MgSO ·7H O MgSO ·6H O MgSO ·H O等
4 2 4 2 4 2 4 2
体
请回答下列问题:
(1)“操作a”的名称是 。
(2)为了提高“酸浸”的速率,可采取的措施有:适当升高温度、 。
(3)MgCO 溶于稀硫酸的化学方程式为 。
3
(4)“废渣Y”中含有少量的FeOOH,其中铁元素的化合价为 价。
(5)“溶液A”中反应:HO+2FeSO+H SO =Fe (SO )+2H O,温度不变情况下,随着Fe (SO ) 的生成,
2 2 4 2 4 2 4 3 2 2 4 3
一段时间后观察到溶液中急速产生大量气泡,其可能原因是 。
(6)选用MgO调节pH使Fe3+转化为沉淀,调节时应控制溶液的pH范围是___________(填序号)
A.2.7~10.1 B.2.7~8 C.3.7~8 D.3.7~10.1
(7)“操作b”的具体操作是:蒸发浓缩溶液C至表面有晶膜出现(此时MgSO 溶液已饱和)、 、
4
过滤、95%的乙醇洗涤、低温干燥。
【答案】(1)过滤(2)将煤矿石粉碎(或搅拌、适当提高硫酸浓度等)
(3)
(4)+3
(5)生成的Fe (SO ) 催化过氧化氢的分解,产生较多氧气
2 4 3
(6)C
(7)降温至1.8℃~48.1℃结晶
【解析】(1)操作a为分离滤液和滤渣的操作,即为过滤操作;
(2)增大反应速率的方法有:升高温度或增大反应物的接触面积,故为了提高“酸浸”的速率,可采取
的措施有:适当升高温度、将煤矿石粉碎(或搅拌、适当提高硫酸浓度等);
(3)碳酸镁与稀硫酸反应生成硫酸镁、二氧化碳和水,该反应方程式为
;
(4)FeOOH中氧元素组成-2价,氢元素显示+1价,设其中铁元素的化合价为x,根据在化合物中正负化
合价代数和为0的原则,则有x+(-2)×2+(+1)=0,解得x=+3;
(5)温度不变情况下,随着Fe (SO ) 的生成,一段时间后观察到溶液中急速产生大量气泡,其可能原因
2 4 3
生成的Fe (SO ) 催化过氧化氢的分解,产生较多氧气;
2 4 3
(6)由表格数据可知,铁离子开始沉淀的pH为2.7,完全沉淀的pH为3.7,镁离子开始沉淀的pH为8,
完全沉淀的pH为10.1,选用MgO调节pH使Fe3+转化为沉淀,所以控制pH在3.7~8之间,故选C;
(7)“操作b”后得到MgSO ·7H O,故具体操作是:蒸发浓缩溶液C至表面有晶膜出现(此时MgSO 溶液
4 2 4
已饱和)、降温至1.8℃~48.1℃结晶、过滤、95%的乙醇洗涤、低温干燥。
20.(9分)硫酸铜及硫酸铜晶体(CuSO ·5H O,相对分子质量为250)广泛应用于生产、生活及实验中。
4 2
Ⅰ、硫酸铜制取
方案一:
方案二:将废铜屑倒入稀硫酸中,控温80℃并通入氧气制备硫酸铜。
(1)图1是方案二实验室模拟工业制备硫酸铜的装置。反应的化学方程式为 。
Ⅱ、硫酸铜晶体的性质
(2)将25.0g胆矾放在坩埚内加热,固体质量与成分随温度变化的曲线如图2,加热至1000℃时,CuO开
始分解,生成Cu O与一种能使带火星的木条复燃的气体,则CuO完全分解时产生该气体的质量为 。
2
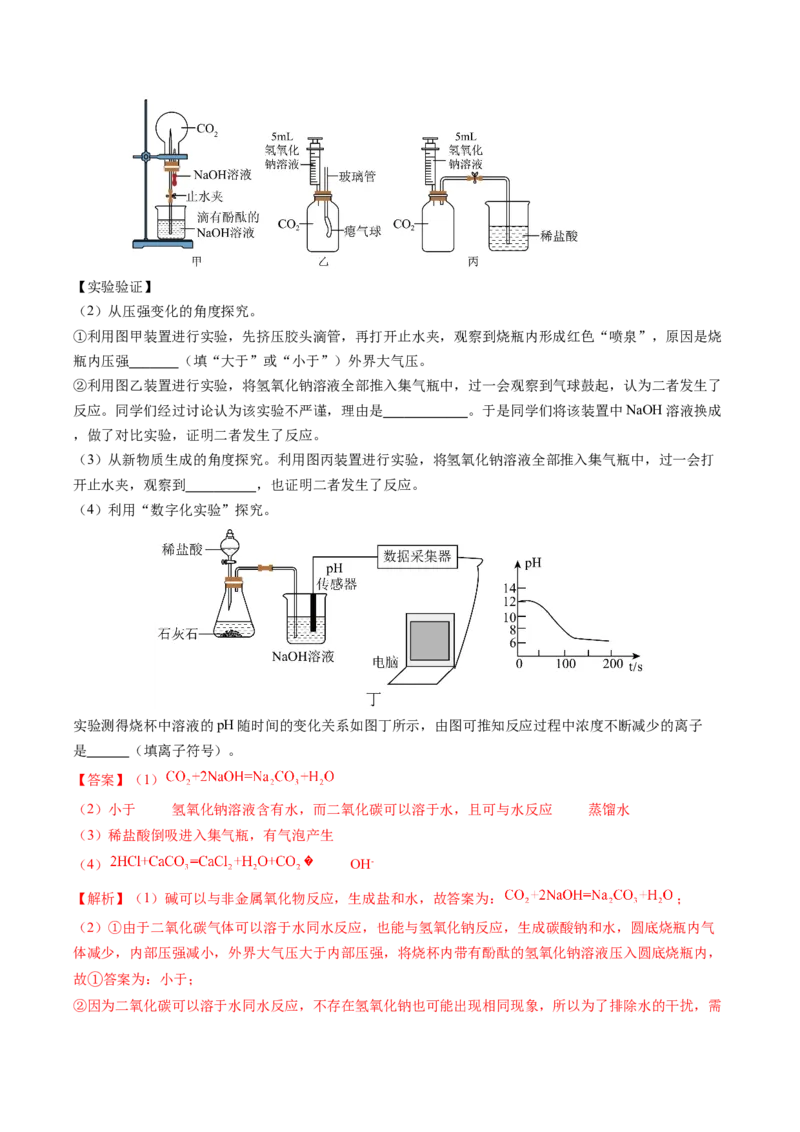
Ⅲ、硫酸铜应用(3)切割钢板时,通常利用硫酸铜溶液在钢板上先画出红线,该反应的化学方程式为
。
(4)工业上用含有硫酸铜的微蚀刻废液(含有一定量Cu2+、H+、 、HO 和微量Fe3+)来制备高纯度碱式
2 2
碳酸铜[Cu (OH) CO],用于生产木材防腐剂等。其制备过程如下:
2 2 3
①第二次“沉淀”时的反应为:2CuSO +2Na CO+H O=Cu (OH) CO↓+2 +CO ↑。
4 2 3 2 2 2 3 2
②烘干时若产品中出现少量黑色物质,可能的原因为 。
③第二次“沉淀”时,若有少量5Cu(OH) ·2CuCO 生成,则产品中铜元素的质量分数 。(填
2 3
“偏大”“不变”或“偏小”)
④加入NaCO 进行反应时,反应液pH对产品中的 含量以及反应液中Cu2+沉淀效率的影响如图所示,
2 3
此时溶液pH最好控制在 。
【答案】(1)
(2)解:能使带火星的木条复燃的气体为氧气,设若CuO完全分解时产生氧气的质量是x
答:若CuO完全分解时产生该气体的质量是0.8g。
(3)Fe+CuSO=FeSO+Cu
4 4
(4)NaSO 烘干温度高,部分碱式碳酸铜受热分解生成氧化铜 偏大 8.5左右
2 4
【解析】(1)80℃时,铜、氧气、稀硫酸反应生成硫酸铜和水,该反应的化学方程式为:2Cu+O2+2H2SO4 2CuSO4+2H2O,故填:2Cu+O2+2H2SO4 2CuSO +2H O;
4 2
(3)铁与硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为Fe+CuSO=Cu+FeSO ,故填:
4 4
Fe+CuSO=Cu+FeSO ;
4 4
(4)①根据质量守恒定律,反应前后原子的种类、数目不变,反应前Cu、S、O、Na、C、H的原子个数
分别为2、2、15、4、2、2,反应后Cu、S、O、Na、C、H原子个数分别为2、0、7、0、2、2,还缺少2
个硫原子、8个氧原子和4个钠原子,则横线上物质的化学式为NaSO ,故填:NaSO ;
2 4 2 4
②烘干时产品中出现少量黑色物质,可能的原因为烘干温度高,部分碱式碳酸铜受热分解生成氧化铜,故
填:烘干温度高,部分碱式碳酸铜受热分解生成氧化铜;
③1个碱式碳酸铜分子中有2个铜原子,而1个3Cu(OH) •2CuCO 分子中有5个铜原子,所以“沉淀”时
2 3
若有少量5Cu(OH) •2CuCO 生成,所以产品中铜元素的质量分数偏大,故填:偏大;
2 3
④由图可知,溶液pH为8.5左右时,硫酸根离子含量最低,溶液中铜离子沉淀效率最高,因此第二次沉淀
时溶液pH最好控制在8.5左右,故填:8.5左右。