文档内容
2024 年中考第一次模拟考试(盐城卷)
化 学
(考试时间:60分钟 试卷满分:70分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Ca-40 Fe-56 Cu-64
一、单项选择题(本大题包括15小题,每小题有四个选项,其中只有一个选项符合题意,请将符合题意的
选项代号填在相应位置上。每小题2分,共30分)
1.化学是人类进步的阶梯。下列说法正确的是
A.化学与家居:含有食品添加剂的食品对人体都有害
B.化学与出行:为减少公交压力,提倡多开私家车出行
C.化学与环境:为防止工厂废气污染空气,可将工厂烟囱加高
D.化学与社会发展:新材料的使用为我国空间站的建设提供了保障
2.“千里海岸,广袤滩涂,一片胜景”。盐城坚持把“生态优先、绿色低碳”作为高质量发展的“命
脉”,以下选项不符合这一理念的是
A.发展公共交通,提倡绿色出行
B.开发新能源,减少化石燃料使用
C.大量使用化肥,提高粮食产量
D.建立自然保护区,保护生物多样性
3.2022年元月8日,盐城非遗体验馆正式对外开放,下列非遗项目中涉及化学变化的是
A.陈皮酒酿造 B.麦秆剪贴 C.海盐晒制 D.老虎鞋绣制
4.二氧化钒的“冷热双吸”材料,可助力我国实现“双碳”目标。钒元素在周期表中的信息如图所示,
下列说法不正确的是
A.钒属于金属元素 B.钒原子中子数为23
C.钒的相对原子质量为50.94 D.二氧化钒的化学式为VO
2
5.规范操作是实验成功的前提。下列实验操作正确的是A.倾倒液体 B.稀释浓硫酸 C.过滤 D.测溶液pH
6.下列有关化学用语的叙述,正确的是
A.He:表示氖气 B.C :表示60个碳原子
60
C.2N:表示2个氮原子 D.Fe2+:表示铁离子
7.某海水淡化系统(如下图)工作时,蒸发腔中的水在光热作用下变为水蒸气,太阳能风扇将水蒸气吹到冷
凝腔冷凝,实现海水淡化。下列说法错误的是
A.光热作用下,水分子运动速率加快
B.液态水变为水蒸气,水分子间的间隔变大
C.水蒸气冷凝为水,水分子本身变小
D.海水变为淡水,水分子化学性质不变
8.今年央视“3·15”特别节目曝光,某品牌肉制品中含有毒物质瘦肉精。某种瘦肉精的化学式为
C H ClNO,下列有关该瘦肉精的说法中正确的是
12 19 3 2
A.该瘦肉精由12个碳原子,19个氢原子、3个氯原子、2个氮原子和1个氧原子构成
B.该瘦肉精由碳、氢、氯、氮、氧五种元素组成
C.该瘦肉精分子中含有氮分子
D.该瘦肉精分子中含有氧气
9.科学思维是从化学视角研究物质及其变化规律的思路与方法,下列说法正确的是
A.变化与守恒:依据质量守恒定律,64gCu和16gO 充分反应可得到80gCuO
2
B.模型与推理:化学反应伴随能量的变化,有能量变化的一定是化学反应
C.宏观与微观:氧气和液氧物理性质差异较大,因为两者的分子构成不同
D.探究与创新:探究氧化铜是否为过氧化氢分解的催化剂,只需设计实验证明氧化铜能否改变化学
反应速率即可
10.下列物质的转化在给定条件下均能实现的是
A.
B.
C.D.
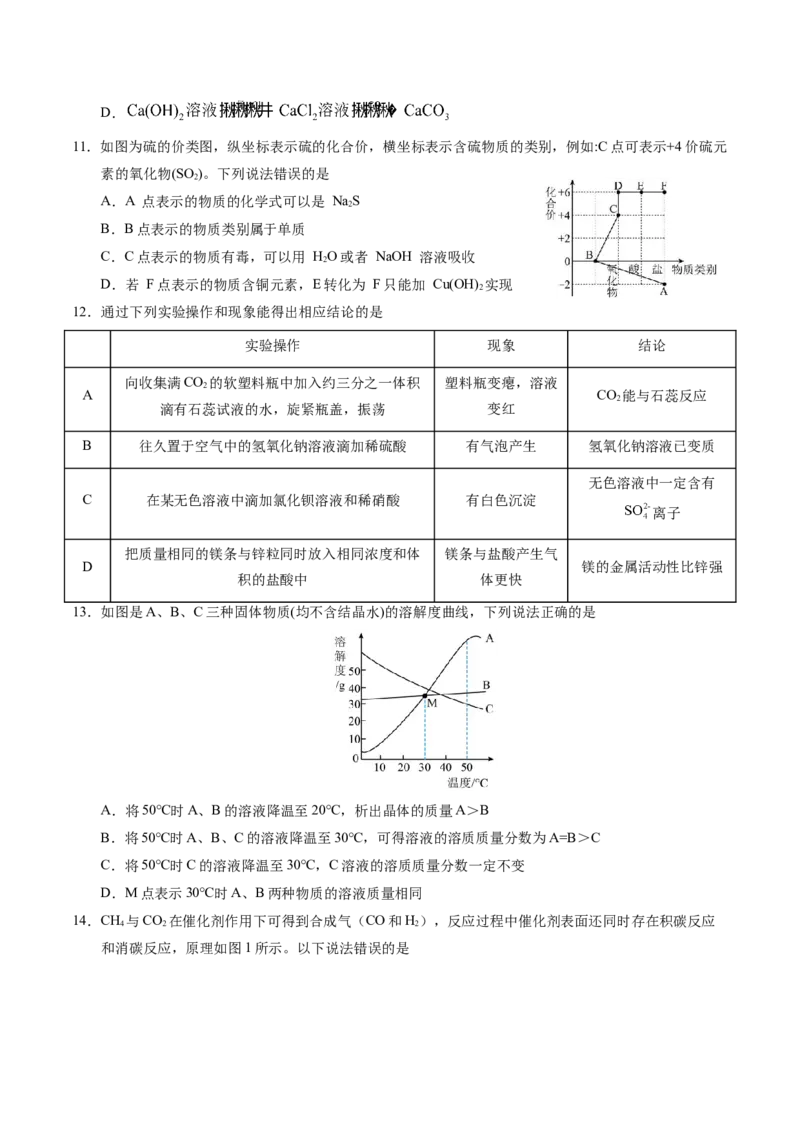
11.如图为硫的价类图,纵坐标表示硫的化合价,横坐标表示含硫物质的类别,例如:C点可表示+4价硫元
素的氧化物(SO )。下列说法错误的是
2
A.A 点表示的物质的化学式可以是 NaS
2
B.B点表示的物质类别属于单质
C.C点表示的物质有毒,可以用 HO或者 NaOH 溶液吸收
2
D.若 F点表示的物质含铜元素,E转化为 F只能加 Cu(OH) 实现
2
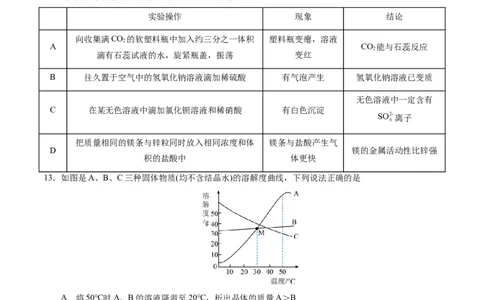
12.通过下列实验操作和现象能得出相应结论的是
实验操作 现象 结论
向收集满CO 的软塑料瓶中加入约三分之一体积 塑料瓶变瘪,溶液
2
A CO 能与石蕊反应
2
滴有石蕊试液的水,旋紧瓶盖,振荡 变红
B 往久置于空气中的氢氧化钠溶液滴加稀硫酸 有气泡产生 氢氧化钠溶液已变质
无色溶液中一定含有
C 在某无色溶液中滴加氯化钡溶液和稀硝酸 有白色沉淀
离子
把质量相同的镁条与锌粒同时放入相同浓度和体 镁条与盐酸产生气
D 镁的金属活动性比锌强
积的盐酸中 体更快
13.如图是A、B、C三种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是
A.将50℃时A、B的溶液降温至20℃,析出晶体的质量A>B
B.将50℃时A、B、C的溶液降温至30℃,可得溶液的溶质质量分数为A=B>C
C.将50℃时C的溶液降温至30℃,C溶液的溶质质量分数一定不变
D.M点表示30℃时A、B两种物质的溶液质量相同
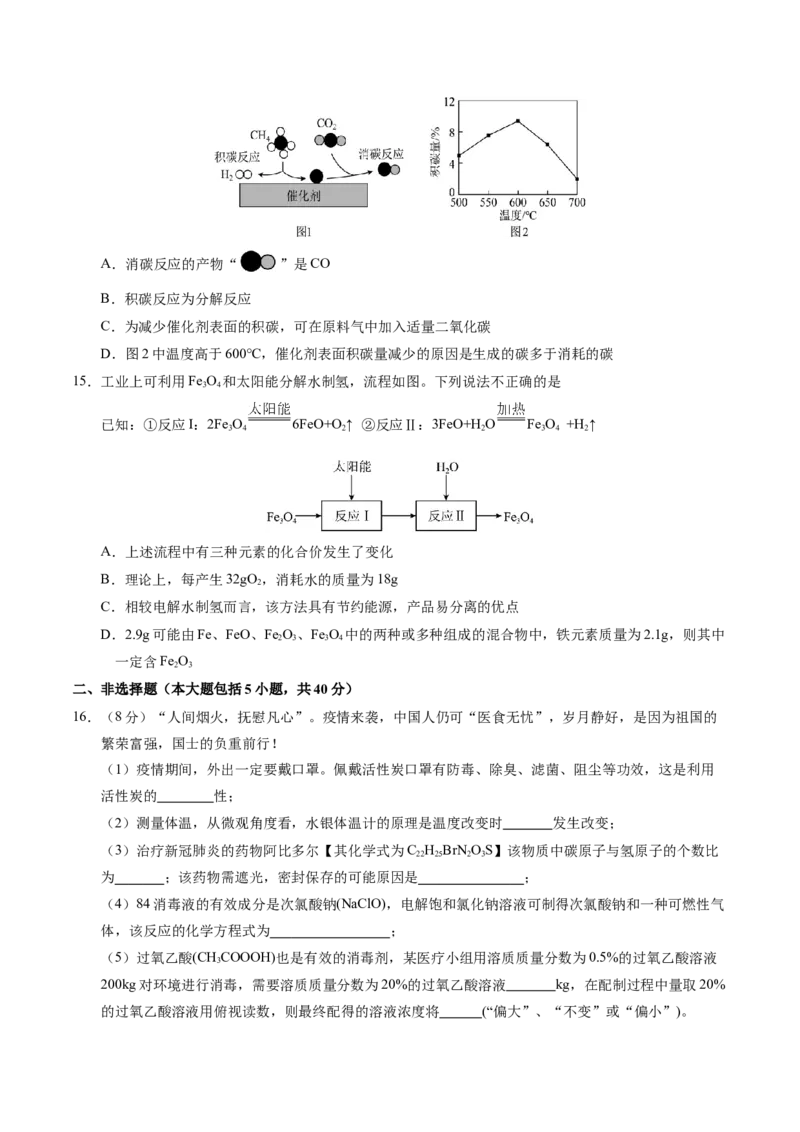
14.CH 与CO 在催化剂作用下可得到合成气(CO和H),反应过程中催化剂表面还同时存在积碳反应
4 2 2
和消碳反应,原理如图1所示。以下说法错误的是A.消碳反应的产物“ ”是CO
B.积碳反应为分解反应
C.为减少催化剂表面的积碳,可在原料气中加入适量二氧化碳
D.图2中温度高于600℃,催化剂表面积碳量减少的原因是生成的碳多于消耗的碳
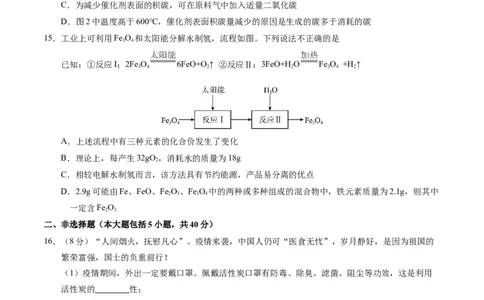
15.工业上可利用Fe O 和太阳能分解水制氢,流程如图。下列说法不正确的是
3 4
已知:①反应I:2Fe O 6FeO+O↑ ②反应Ⅱ:3FeO+HO Fe O +H ↑
3 4 2 2 3 4 2
A.上述流程中有三种元素的化合价发生了变化
B.理论上,每产生32gO,消耗水的质量为18g
2
C.相较电解水制氢而言,该方法具有节约能源,产品易分离的优点
D.2.9g可能由Fe、FeO、Fe O、Fe O 中的两种或多种组成的混合物中,铁元素质量为2.1g,则其中
2 3 3 4
一定含Fe O
2 3
二、非选择题(本大题包括5小题,共40分)
16.(8分)“人间烟火,抚慰凡心”。疫情来袭,中国人仍可“医食无忧”,岁月静好,是因为祖国的
繁荣富强,国士的负重前行!
(1)疫情期间,外出一定要戴口罩。佩戴活性炭口罩有防毒、除臭、滤菌、阻尘等功效,这是利用
活性炭的 性;
(2)测量体温,从微观角度看,水银体温计的原理是温度改变时 发生改变;
(3)治疗新冠肺炎的药物阿比多尔【其化学式为C H BrNOS】该物质中碳原子与氢原子的个数比
22 25 2 3
为 ;该药物需遮光,密封保存的可能原因是 ;
(4)84消毒液的有效成分是次氯酸钠(NaClO),电解饱和氯化钠溶液可制得次氯酸钠和一种可燃性气
体,该反应的化学方程式为 ;
(5)过氧乙酸(CHCOOOH)也是有效的消毒剂,某医疗小组用溶质质量分数为0.5%的过氧乙酸溶液
3
200kg对环境进行消毒,需要溶质质量分数为20%的过氧乙酸溶液 kg,在配制过程中量取20%
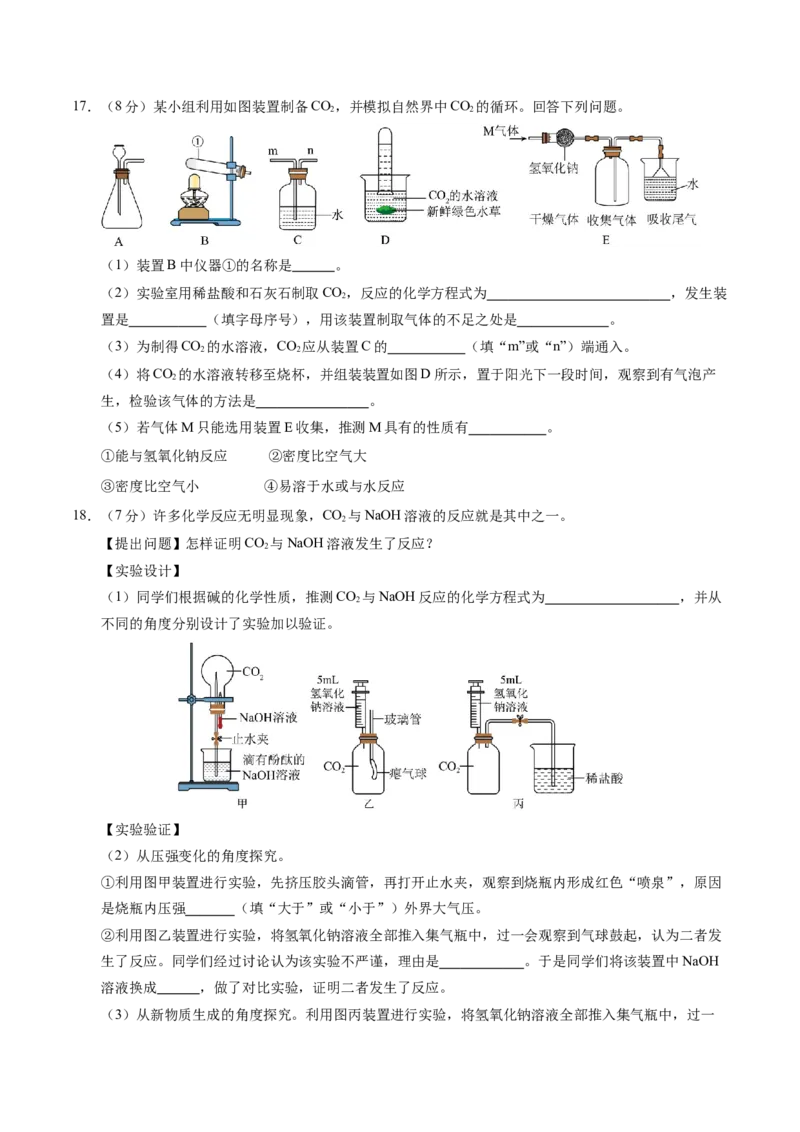
的过氧乙酸溶液用俯视读数,则最终配得的溶液浓度将 (“偏大”、“不变”或“偏小”)。17.(8分)某小组利用如图装置制备CO,并模拟自然界中CO 的循环。回答下列问题。
2 2
(1)装置B中仪器①的名称是 。
(2)实验室用稀盐酸和石灰石制取CO,反应的化学方程式为 ,发生装
2
置是 (填字母序号),用该装置制取气体的不足之处是 。
(3)为制得CO 的水溶液,CO 应从装置C的 (填“m”或“n”)端通入。
2 2
(4)将CO 的水溶液转移至烧杯,并组装装置如图D所示,置于阳光下一段时间,观察到有气泡产
2
生,检验该气体的方法是 。
(5)若气体M只能选用装置E收集,推测M具有的性质有 。
①能与氢氧化钠反应 ②密度比空气大
③密度比空气小 ④易溶于水或与水反应
18.(7分)许多化学反应无明显现象,CO 与NaOH溶液的反应就是其中之一。
2
【提出问题】怎样证明CO 与NaOH溶液发生了反应?
2
【实验设计】
(1)同学们根据碱的化学性质,推测CO 与NaOH反应的化学方程式为 ,并从
2
不同的角度分别设计了实验加以验证。
【实验验证】
(2)从压强变化的角度探究。
①利用图甲装置进行实验,先挤压胶头滴管,再打开止水夹,观察到烧瓶内形成红色“喷泉”,原因
是烧瓶内压强 (填“大于”或“小于”)外界大气压。
②利用图乙装置进行实验,将氢氧化钠溶液全部推入集气瓶中,过一会观察到气球鼓起,认为二者发
生了反应。同学们经过讨论认为该实验不严谨,理由是 。于是同学们将该装置中NaOH
溶液换成 ,做了对比实验,证明二者发生了反应。
(3)从新物质生成的角度探究。利用图丙装置进行实验,将氢氧化钠溶液全部推入集气瓶中,过一会打开止水夹,观察到 ,也证明二者发生了反应。
(4)利用“数字化实验”探究。
实验测得烧杯中溶液的pH随时间的变化关系如图丁所示,由图可推知反应过程中浓度不断减少的离
子
是 (填离子符号)。
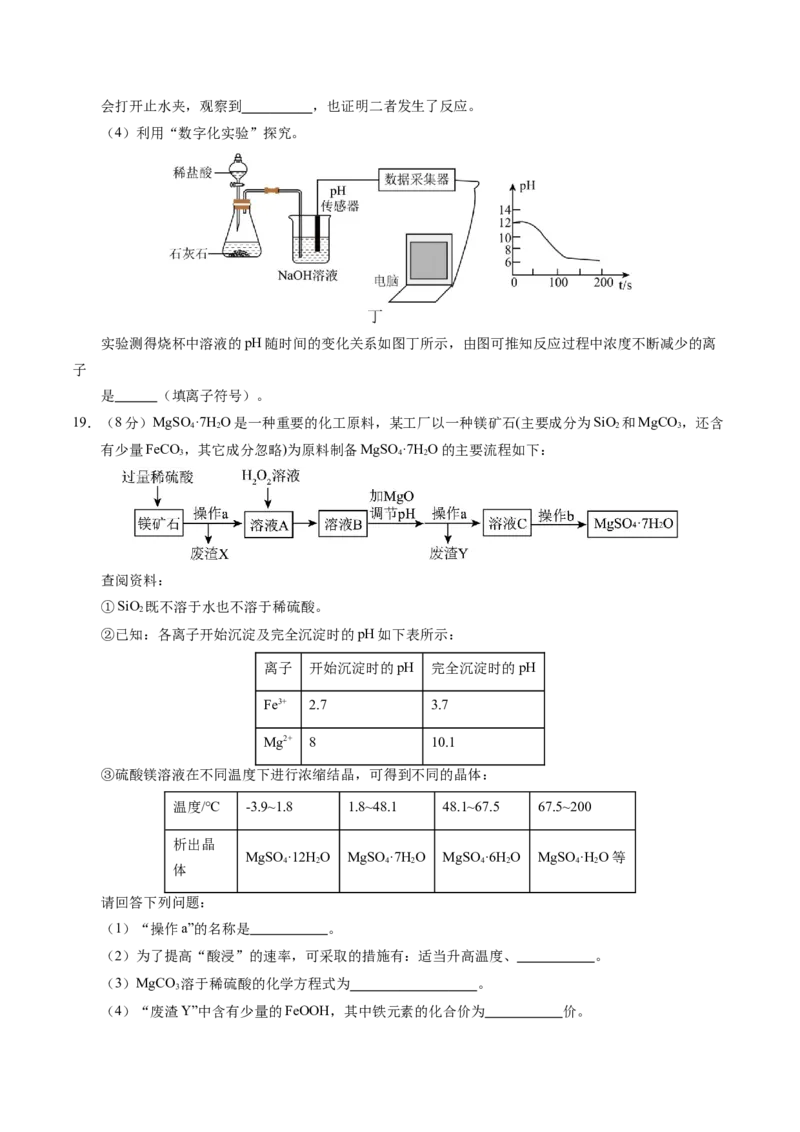
19.(8分)MgSO ·7H O是一种重要的化工原料,某工厂以一种镁矿石(主要成分为SiO 和MgCO ,还含
4 2 2 3
有少量FeCO,其它成分忽略)为原料制备MgSO ·7H O的主要流程如下:
3 4 2
查阅资料:
①SiO 既不溶于水也不溶于稀硫酸。
2
②已知:各离子开始沉淀及完全沉淀时的pH如下表所示:
离子 开始沉淀时的pH 完全沉淀时的pH
Fe3+ 2.7 3.7
Mg2+ 8 10.1
③硫酸镁溶液在不同温度下进行浓缩结晶,可得到不同的晶体:
温度/℃ -3.9~1.8 1.8~48.1 48.1~67.5 67.5~200
析出晶
MgSO ·12H O MgSO ·7H O MgSO ·6H O MgSO ·H O等
4 2 4 2 4 2 4 2
体
请回答下列问题:
(1)“操作a”的名称是 。
(2)为了提高“酸浸”的速率,可采取的措施有:适当升高温度、 。
(3)MgCO 溶于稀硫酸的化学方程式为 。
3
(4)“废渣Y”中含有少量的FeOOH,其中铁元素的化合价为 价。(5)“溶液A”中反应:HO+2FeSO+H SO =Fe (SO )+2H O,温度不变情况下,随着Fe (SO ) 的生
2 2 4 2 4 2 4 3 2 2 4 3
成,一段时间后观察到溶液中急速产生大量气泡,其可能原因是 。
(6)选用MgO调节pH使Fe3+转化为沉淀,调节时应控制溶液的pH范围是___________(填序号)
A.2.7~10.1 B.2.7~8 C.3.7~8 D.3.7~10.1
(7)“操作b”的具体操作是:蒸发浓缩溶液C至表面有晶膜出现(此时MgSO 溶液已饱和)、
4
、过滤、95%的乙醇洗涤、低温干燥。
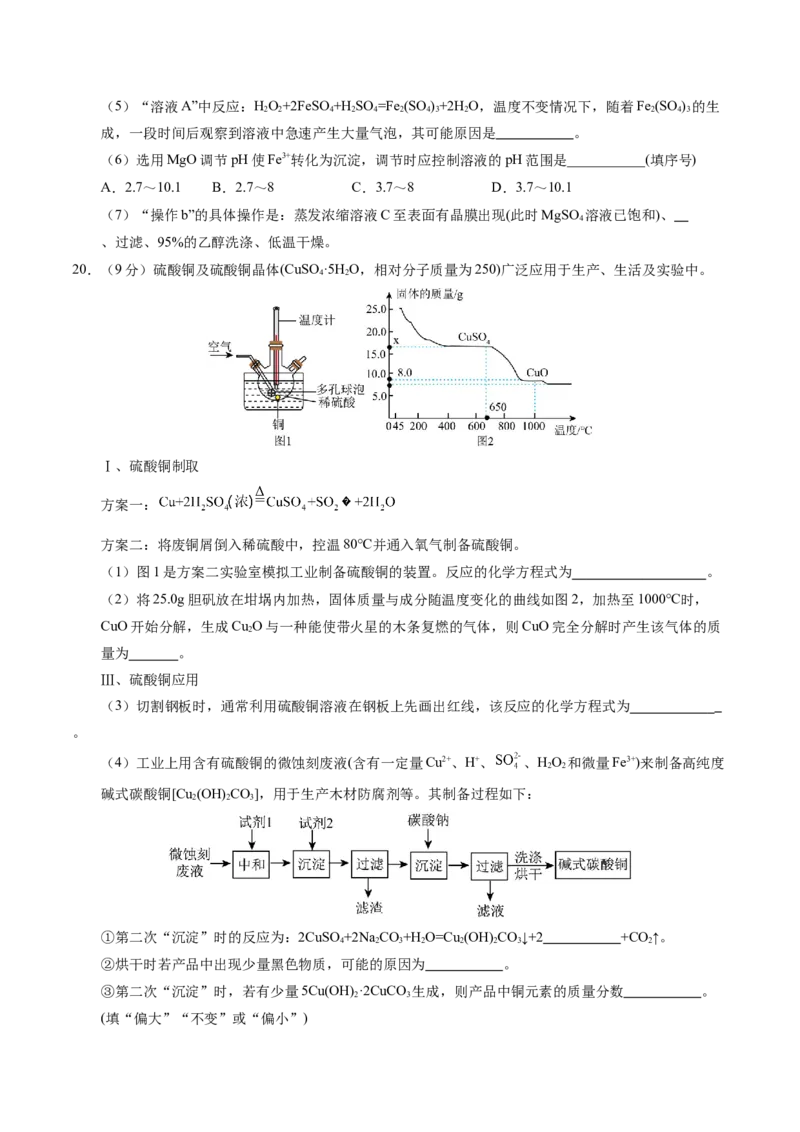
20.(9分)硫酸铜及硫酸铜晶体(CuSO ·5H O,相对分子质量为250)广泛应用于生产、生活及实验中。
4 2
Ⅰ、硫酸铜制取
方案一:
方案二:将废铜屑倒入稀硫酸中,控温80℃并通入氧气制备硫酸铜。
(1)图1是方案二实验室模拟工业制备硫酸铜的装置。反应的化学方程式为 。
(2)将25.0g胆矾放在坩埚内加热,固体质量与成分随温度变化的曲线如图2,加热至1000℃时,
CuO开始分解,生成Cu O与一种能使带火星的木条复燃的气体,则CuO完全分解时产生该气体的质
2
量为 。
Ⅲ、硫酸铜应用
(3)切割钢板时,通常利用硫酸铜溶液在钢板上先画出红线,该反应的化学方程式为
。
(4)工业上用含有硫酸铜的微蚀刻废液(含有一定量Cu2+、H+、 、HO 和微量Fe3+)来制备高纯度
2 2
碱式碳酸铜[Cu (OH) CO],用于生产木材防腐剂等。其制备过程如下:
2 2 3
①第二次“沉淀”时的反应为:2CuSO +2Na CO+H O=Cu (OH) CO↓+2 +CO ↑。
4 2 3 2 2 2 3 2
②烘干时若产品中出现少量黑色物质,可能的原因为 。
③第二次“沉淀”时,若有少量5Cu(OH) ·2CuCO 生成,则产品中铜元素的质量分数 。
2 3
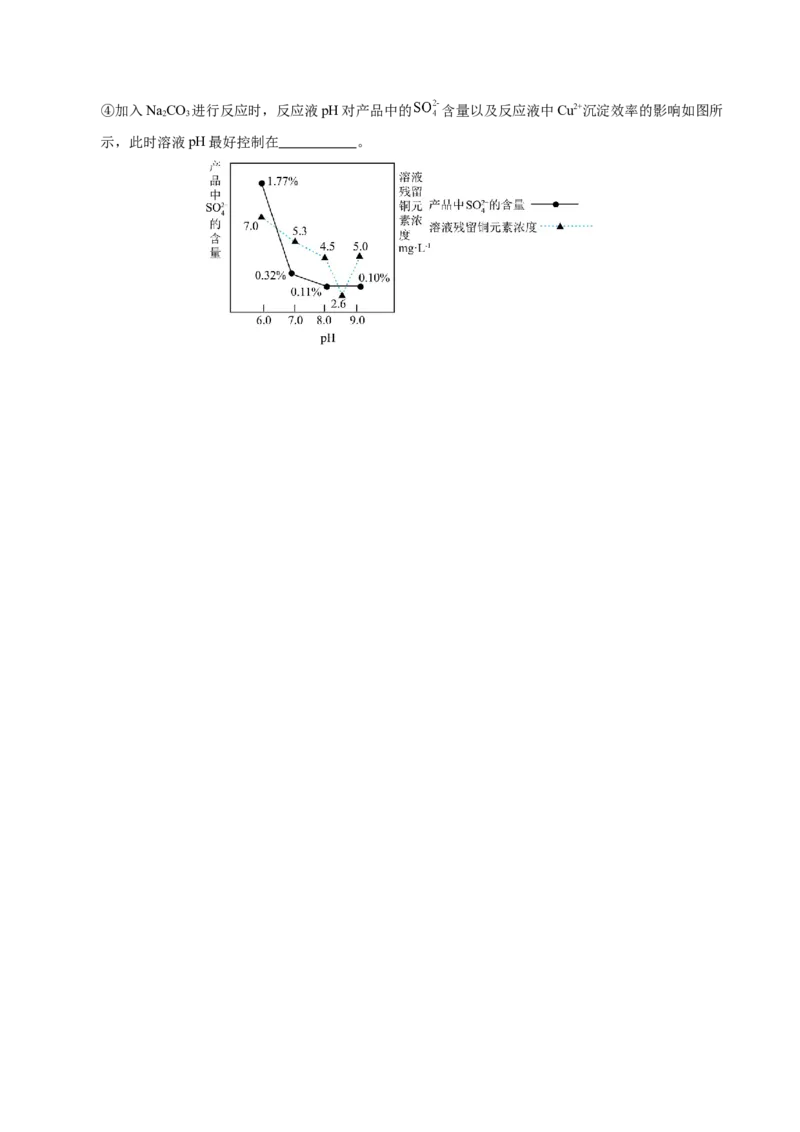
(填“偏大”“不变”或“偏小”)④加入NaCO 进行反应时,反应液pH对产品中的 含量以及反应液中Cu2+沉淀效率的影响如图所
2 3
示,此时溶液pH最好控制在 。