文档内容
2024 年中考第二次模拟考试(盐城卷)
化 学
(考试时间:60分钟 试卷满分:70分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Fe-56 Cu-64
一、选择题(本大题包括15小题,每小题只有一个正确选项,每小题2分,共30分)
1.节约资源、保护环境有利于社会可持续发展。下列做法不符合这一理念的是
A.回收废弃金属,实现资源再生 B.开发燃煤新技术,促进煤的完全燃烧
C.用工业废水灌溉,以节约用水 D.使用无磷洗衣粉,防止水体富营养化
2.下列物质属于纯净物的是
A.医用酒精 B.冰水混合物 C.清新空气 D.加碘食盐
3.下列物质属于氧化物的是
A.MgO B.O C.NaOH D.HCO
2 2 3
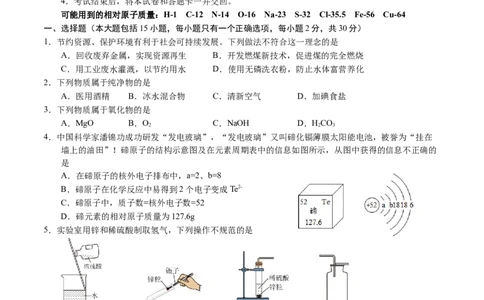
4.中国科学家潘锦功成功研发“发电玻璃”,“发电玻璃”又叫碲化镉薄膜太阳能电池,被誉为“挂在
墙上的油田”!碲原子的结构示意图及在元素周期表中的信息如图所示,从图中获得的信息不正确的
是
A.在碲原子的核外电子排布中,a=2、b=8
B.碲原子在化学反应中易得到2个电子变成Te2-
C.碲原子中,质子数=核外电子数=52
D.碲元素的相对原子质量为127.6g
5.实验室用锌和稀硫酸制取氢气,下列操作不规范的是
A.甲:稀释浓硫酸 B.乙:加入锌粒 C.丙:产生氢气 D.丁:收集氢气
6.化学与生活密切相关。下列生活中常见物质的俗名与化学式不对应的是
A.小苏打—NaHCO B.纯碱—NaOH C.酒精—C HOH D.生石灰—CaO
3 2 5
7.下列有关碳和碳的氧化物的说法,错误的是
A.《清明上河图》至今图案清晰可见,是因为在常温下碳单质的化学性质稳定
B.碳在空气充分燃烧时生成CO,不充分燃烧时生成CO
2
C.CO和CO 组成元素相同,所以它们的化学性质也相同
2
D.CO可用于冶炼金属、做气体燃料; CO 可用于人工降雨、灭火
2
8.某同学在奥运五环中填入了五种物质,图中环的相交部分是两种物质在一定条件下发生化学反应的现象,其中描述错误的是
A.产生淡蓝色火焰,生成无色无味气体
B.剧烈燃烧,火星四射,生成黑色固体
C.有红色固体析出,溶液逐渐由蓝色变成浅绿色
D.产生蓝色沉淀
9.下列指定反应的化学方程式正确的是
A.用氢氧化铝中和过多胃酸:
B.酸雨形成的原因:
C.氧乙炔焰的完全燃烧:
D.石灰石粉掺入煤中,燃烧时吸收SO :
2
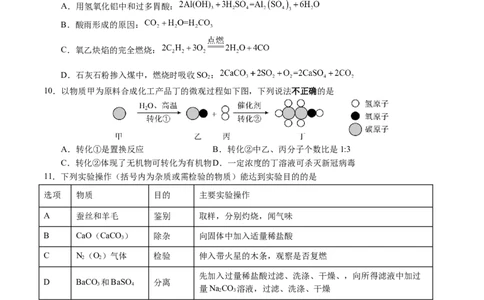
10.以物质甲为原料合成化工产品丁的微观过程如下图,下列说法不正确的是
A.转化①是置换反应 B.转化②中乙、丙分子个数比是1:3
C.转化②体现了无机物可转化为有机物D.一定浓度的丁溶液可杀灭新冠病毒
11.下列实验操作(括号内为杂质或需检验的物质)能达到实验目的的是
选项 物质 目的 主要实验操作
A 蚕丝和羊毛 鉴别 取样,分别灼烧,闻气味
B CaO(CaCO ) 除杂 向固体中加入适量稀盐酸
3
C N(O)气体 检验 伸入带火星的木条,观察是否复燃
2 2
先加入过量稀盐酸过滤、洗涤、干燥、,向所得滤液中加过
D BaCO 和BaSO 分离
3 4
量NaCO 溶液,过滤、洗涤、干燥
2 3
12.下图是 三种物质的溶解度曲线。下列有关说法不正确的是
A. 时,三种物质的溶解度大小关系为B. 时,把 的KCl溶液变成饱和溶液,需至少加入 固体
C. 时,若三种物质的饱和溶液质量相等,则溶液中水的质量最少的是
D. 时,三种物质的饱和溶液中,溶质质量分数最小的是
13.Ca(OH) 与HO 溶液反应可制备CaO。反应过程包括:
2 2 2 2
步骤—: ,其中O代表氧原子;
步骤二:主要发生 ,少量发生 。
下列说法不正确的是
A.为增大反应混合物中Ca(OH) 的含量,应使用石灰乳而非石灰水
2
B.生成CaO 的总反应为
2
C.增加Ca(OH) 的用量,可以消耗更多O,减少O 的生成
2 2
D.制备时反应每生成72gCaO,同时生成32gO
2 2
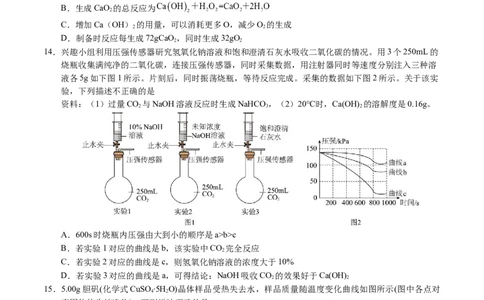
14.兴趣小组利用压强传感器研究氢氧化钠溶液和饱和澄清石灰水吸收二氧化碳的情况。用3个250mL的
烧瓶收集满纯净的二氧化碳,连接压强传感器,同时采集数据,用注射器同时等速度分别注入三种溶
液各5g如下图1所示。片刻后,同时振荡烧瓶,等待反应完成。采集的数据如下图2所示。关于该实
验,下列描述不正确的是
资料:(1)过量CO 与NaOH溶液反应时生成NaHCO ,(2)20℃时,Ca(OH) 的溶解度是0.16g。
2 3 2
A.600s时烧瓶内压强由大到小的顺序是a>b>c
B.若实验1对应的曲线是b,该实验中CO 完全反应
2
C.若实验2对应的曲线是c,则氢氧化钠溶液的浓度大于10%
D.若实验3对应的曲线是a,可得结论:NaOH吸收CO 的效果好于Ca(OH)
2 2
15.5.00g胆矾(化学式CuSO ∙5H O)晶体样品受热失去水,样品质量随温度变化曲线如图所示(图中各点对
4 2
应固体均为纯净物)。下列说法正确的是
A.受热过程中晶体样品颜色由白色逐渐变成蓝色B.受热过程中固体物质里Cu元素的质量分数逐渐减小
C.固体物质在102℃和113℃时失去水的质量比为2:1
D.200℃时固体物质的化学式为CuSO ∙H O
4 2
二、非选择题(本题包含4小题,共40分)
16.(9分)岁月静好,是因为我们祖国的繁荣富强,以及众多国士的负重前行。
(1)屠呦呦研究青蒿素对抗疟疾,获医学诺贝尔奖。
①青蒿素(C H O)中碳元素和氧元素的质量比为 。
15 22 5
②为提高药物在水中的溶解性,需对其进行分子结构修饰,说明物质的 决定物质的性质。
(2)袁隆平院士一生致力于杂交水稻技术。
①水稻为人类提供的营养素是 ,稻米在人体内先转化为葡萄糖,葡萄糖在酶的催化作用下经
缓慢氧化转变成两种氧化物,葡萄糖缓慢氧化过程的化学方程式为 。
②富硒大米中的硒元素是人体中的 (填“微量”或“常量”)元素。
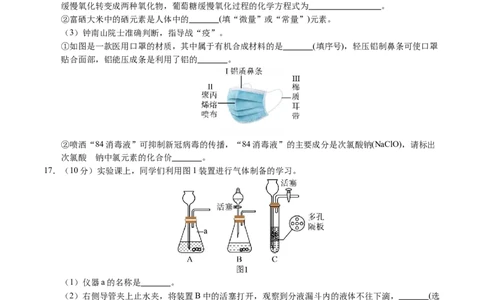
(3)钟南山院士准确判断,指导战“疫”。
①如图是一款医用口罩的材质,其中属于有机合成材料的是 (填序号),轻压铝制鼻条可使口罩
贴合面部,铝能压成条是利用了铝的 。
②喷洒“84消毒液”可抑制新冠病毒的传播,“84消毒液”的主要成分是次氯酸钠(NaClO),请标出
次氯酸 钠中氯元素的化合价 。
17.(10分)实验课上,同学们利用图1装置进行气体制备的学习。
(1)仪器a的名称是 。
(2)右侧导管夹上止水夹,将装置B中的活塞打开,观察到分液漏斗内的液体不往下滴, (选
填“能”或“不能”)说明装置B的气密性良好。
(3)实验室用装置C制取CO,该反应的化学方程式为 。装置C与装置A、
2
B相比较,优点是 ,关闭活塞后,C中多孔隔板处依次观察到的现象如图2所示,
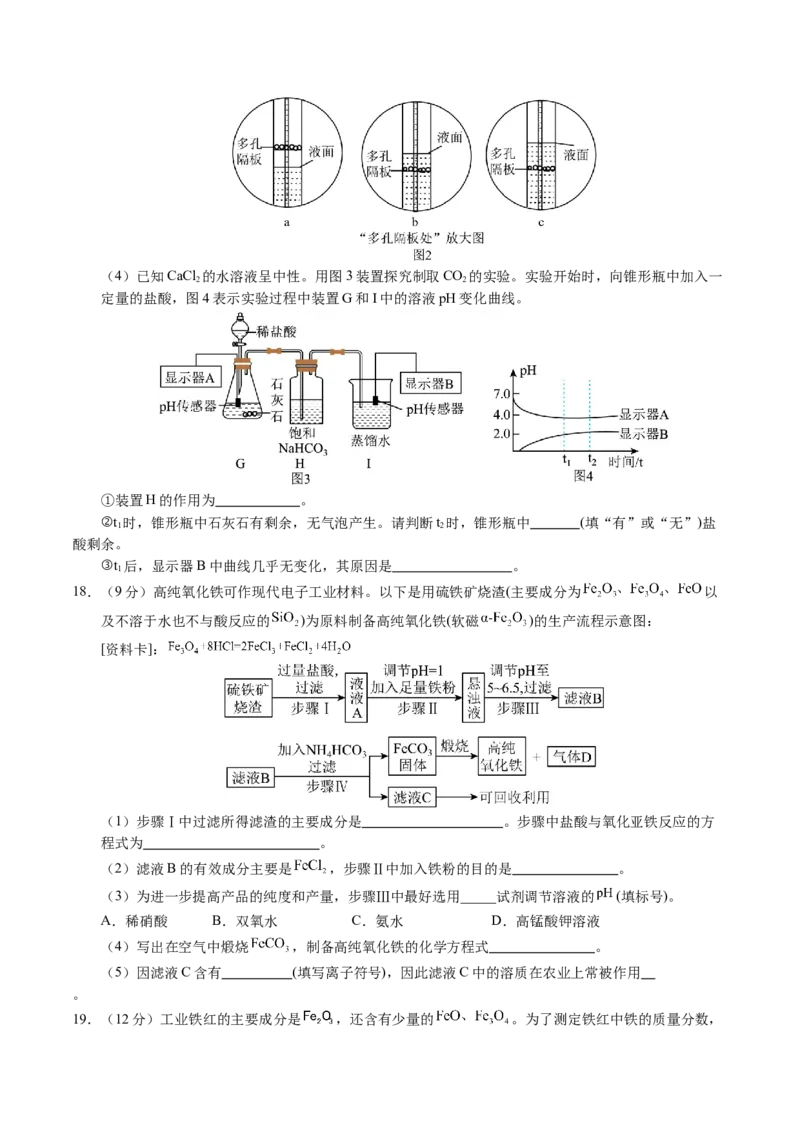
则现象出现的顺序是 (用字母a、b、c排序)。(4)已知CaCl 的水溶液呈中性。用图3装置探究制取CO 的实验。实验开始时,向锥形瓶中加入一
2 2
定量的盐酸,图4表示实验过程中装置G和I中的溶液pH变化曲线。
①装置H的作用为 。
②t 时,锥形瓶中石灰石有剩余,无气泡产生。请判断t 时,锥形瓶中 (填“有”或“无”)盐
1 2
酸剩余。
③t 后,显示器B中曲线几乎无变化,其原因是 。
1
18.(9分)高纯氧化铁可作现代电子工业材料。以下是用硫铁矿烧渣(主要成分为 以
及不溶于水也不与酸反应的 )为原料制备高纯氧化铁(软磁 )的生产流程示意图:
[资料卡]:
(1)步骤Ⅰ中过滤所得滤渣的主要成分是 。步骤中盐酸与氧化亚铁反应的方
程式为 。
(2)滤液B的有效成分主要是 ,步骤Ⅱ中加入铁粉的目的是 。
(3)为进一步提高产品的纯度和产量,步骤Ⅲ中最好选用_____试剂调节溶液的 (填标号)。
A.稀硝酸 B.双氧水 C.氨水 D.高锰酸钾溶液
(4)写出在空气中煅烧 ,制备高纯氧化铁的化学方程式 。
(5)因滤液C含有 (填写离子符号),因此滤液C中的溶质在农业上常被作用
。
19.(12分)工业铁红的主要成分是 ,还含有少量的 。为了测定铁红中铁的质量分数,化学兴趣小组的同学们进行了如下实验。
【资料1】草酸晶体 在浓 作用下受热分解,化学方程式为:
。
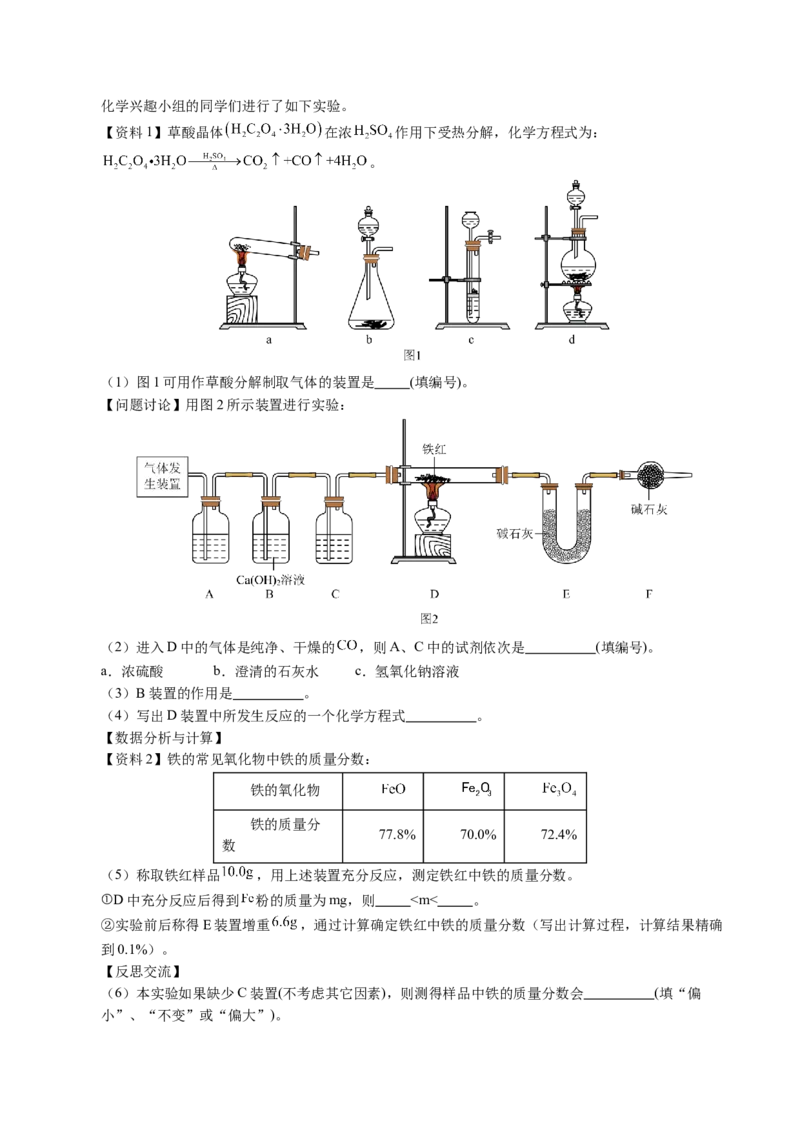
(1)图1可用作草酸分解制取气体的装置是 (填编号)。
【问题讨论】用图2所示装置进行实验:
(2)进入D中的气体是纯净、干燥的 ,则A、C中的试剂依次是 (填编号)。
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(3)B装置的作用是 。
(4)写出D装置中所发生反应的一个化学方程式 。
【数据分析与计算】
【资料2】铁的常见氧化物中铁的质量分数:
铁的氧化物
铁的质量分
77.8% 70.0% 72.4%
数
(5)称取铁红样品 ,用上述装置充分反应,测定铁红中铁的质量分数。
①D中充分反应后得到 粉的质量为mg,则