文档内容
2024 年中考第二次模拟考试(南通卷)
化 学
(考试时间:60分钟 试卷满分:60分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cu-64
第I卷(共20分)
共10小题,每小题2分,共20分。每小题给出的四个选项中,只有一个选项最符合题目的要求
1.化学在能源利用、环境保护等方面起着重要作用,下列有关说法不正确的是
A.将地沟油转化为航空油,变废为宝
B.使用新型的可降解塑料,减少白色污染
C.改进汽车尾气净化技术,减少有害气体排放
D.提高农药和化肥的使用量,以提高农作物的产量
2.“分类”是学习化学的重要方法。下列说法正确的是( )
A.单质:水银、蒸馏水、铁水 B.氧化物:二氧化锰、干冰、氯酸钾
C.碱:烧碱、消石灰、一水合氨 D.混合物:钢、石灰石、甲烷
3.下列实验操作不正确的是
A.读取液体体积 B.称量NaOH固体 C.熄灭酒精灯 D.检查装置的气密性
4.下列有关物质的性质与用途具有对应关系的是
A.铁粉锈蚀吸收氧气,可用作食品脱氧剂 B.活性炭具有吸附性,可用于硬水的软化
C.酒精具有挥发性,可用于杀菌消毒 D.浓硫酸具有脱水性,可用作干燥剂
阅读下列材料,完成下面小题:
“十四五”期间,我国将完成“天宫二号”空间实验室建造。运载火箭使用的燃料有液氢、煤油等。长期
驻留空间实验室会导致航天员肌肉萎缩、骨钙丢失。通过航天食品摄取优质蛋白质、补充钙元素有利于维
持航天员的健康。舱段建造使用的新型铝基碳化硅复合材料由颗粒状的铝和碳化硅(SiC)复合而成。制取
SiC反应为: 。
5.下列有关说法不正确的是A.氢气具有还原性 B.煤油是煤的干馏产品
C.牛奶富含蛋白质 D.钙是人体中的常量元素
6.下列说法正确的是
A.铝制品具有良好的抗腐蚀性,是因为金属铝的化学性质不活泼
B.制取SiC的反应中反应前后各元素的化合价没有改变
C.制取SiC的反应,固体减少的质量等于生成的CO质量
D.制取SiC的反应,基本反应类型属于复分解反应
7.通过下列实验探究CaCO 的性质:
3
步骤一:将CaCO 粉末灼烧一段时间,再将灼烧后的固体投入盛水的烧杯,冷却至室温,测其pH约为
3
12。
步骤二:向试管中加入少量CaCO 粉末,然后加入10mL蒸馏水,振荡后制成CaCO 悬浊液,室温时测
3 3
其pH约为9。在相同实验条件下,用电导率传感器测得蒸馏水的电导率是8.5,CaCO 悬浊液电导率为
3
74。
注:一定体积的溶液中,离子数目越多,其离子浓度越大,导电性越强,电导率越大
下列说法不正确的是
A.步骤一中加入酚酞溶液,溶液变红 B.步骤一中CaCO 不一定发生分解反应
3
C.步骤二说明有部分CaCO 溶于水 D.由实验可知盐溶液不一定呈中性
3
8.如图是MgSO 饱和溶液中溶质质量分数随温度变化的曲线图,下列正确的是
4
A.M点表示 20℃时MgSO 的饱和溶液
4
B.N点时MgSO 的溶解度为35.1g
4
C.75℃的MgSO 饱和溶液降温至20℃,析出晶体10g
4
D.100℃的MgSO 饱和溶液降温至20℃,其溶质质量分数先不变后变小
4
9.下列实验方案正确的是
实验目的 实验方案
加入适量的NaCO 溶液,过滤、洗涤滤渣、往滤渣中加
2 3
A 除去CaCl 溶液中的KCl
2
适量的稀盐酸
B 除去Fe(NO ) 溶液中的Cu(NO ) 加入足量氢氧化亚铁过滤
3 2 3 2
C 证明氢氧化钠溶液部分变质 加入足量的氢氧化钡溶液,过滤.往滤液中加入酚酞溶液
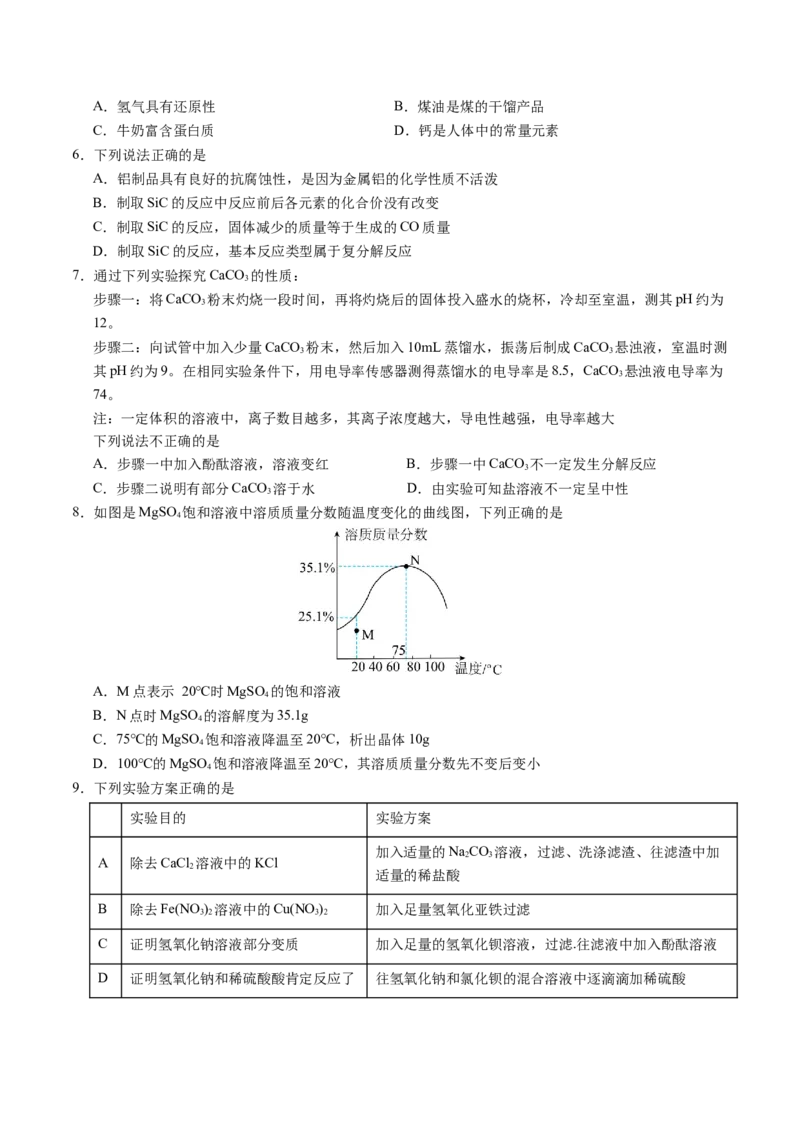
D 证明氢氧化钠和稀硫酸酸肯定反应了 往氢氧化钠和氯化钡的混合溶液中逐滴滴加稀硫酸10.取16.0gCuO在真空条件下加热分解,固体质量随温度的变化如图所示(图中a、b、c、e点对应固体
为纯净物)。当固体质量不再改变时,生成了3.2g O,下列说法不正确的是
2
A.a→b过程中,固体中铜元素的质量分数逐渐增大
B.c→d过程中产生的O 质量为0.8g
2
C.d点对应的固体中两物质的质量比为1︰1
D.c→e过程中发生的化学反应表达式为:Cu O Cu+O
2 2
第II卷(共40分)
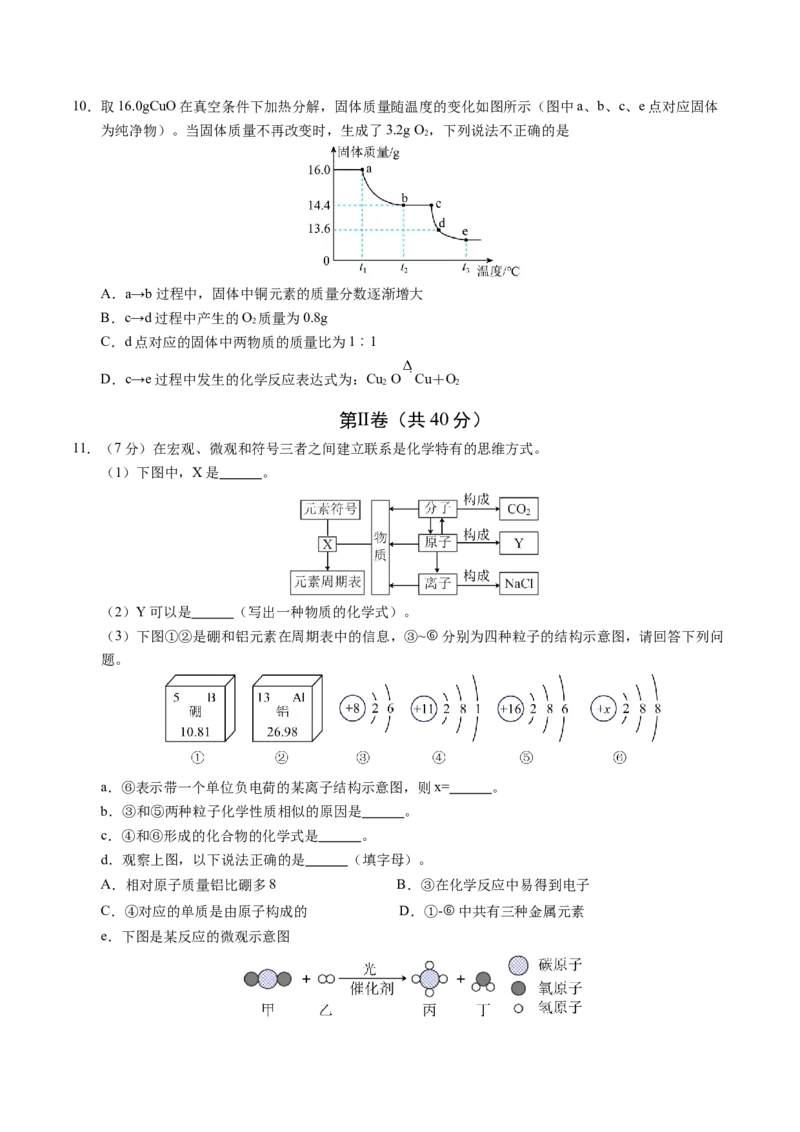
11.(7分)在宏观、微观和符号三者之间建立联系是化学特有的思维方式。
(1)下图中,X是 。
(2)Y可以是 (写出一种物质的化学式)。
(3)下图①②是硼和铝元素在周期表中的信息,③~⑥分别为四种粒子的结构示意图,请回答下列问
题。
a.⑥表示带一个单位负电荷的某离子结构示意图,则x= 。
b.③和⑤两种粒子化学性质相似的原因是 。
c.④和⑥形成的化合物的化学式是 。
d.观察上图,以下说法正确的是 (填字母)。
A.相对原子质量铝比硼多8 B.③在化学反应中易得到电子
C.④对应的单质是由原子构成的 D.①-⑥中共有三种金属元素
e.下图是某反应的微观示意图根据图示写出反应的化学方程式 。
12.(8分)工业上利用软锰矿(主要成分为MnO ,还含有Fe O、Al O、MgO、CaO、SiO 等杂质)与
2 2 3 2 3 2
葡萄糖反应制备MnO,工艺流程如图所示。
3 4
(1)“酸浸”时MnO 发生反应的化学方程式为:
2
C H O+12MnO+12H SO =12MnSO +6CO ↑+18X,X的化学式为 。
6 12 6 2 2 4 4 2
其他金属氧化物和硫酸反应生成相应的硫酸盐,写出Fe O 和硫酸反应的化学方程式 。
2 3
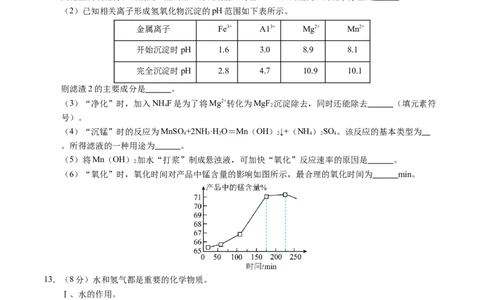
(2)已知相关离子形成氢氧化物沉淀的pH范围如下表所示。
金属离子 Fe3+ A13+ Mg2+ Mn2+
开始沉淀时pH 1.6 3.0 8.9 8.1
完全沉淀时pH 2.8 4.7 10.9 10.1
则滤渣2的主要成分是 。
(3)“净化”时,加入NH F是为了将Mg2+转化为MgF 沉淀除去,同时还能除去 (填元素符
4 2
号)。
(4)“沉锰”时的反应为MnSO +2NH·H O=Mn(OH)↓+(NH )SO 。该反应的基本类型为
4 3 2 2 4 2 4
。所得滤液的一种用途为 。
(5)将Mn(OH) 加水“打浆”制成悬浊液,可加快“氧化”反应速率的原因是 。
2
(6)“氧化”时,氧化时间对产品中锰含量的影响如图所示,最合理的氧化时间为 min。
13.(8分)水和氢气都是重要的化学物质。
Ⅰ、水的作用。
(1)有一种创可贴中间有一个凸起的小囊区,按贴伤口时,小囊区内的水和硝酸铵被挤破混合,利
用硝酸铵固体溶解时温度降低,起到快速止血的作用。水的作用是 。
Ⅱ、水的一段化学史。
(2)1785年,拉瓦锡将水蒸气通过红热的铁制枪管将水转化为氢气,同时生成某种固体。如图1所
示,则该固体中一定含有 (填元素符号)元素。若生成2g氢气,则理论上铁制枪管应增重
g。请另写一个能证明“水不是一种元素”的化学方程式: 。
Ⅲ、氢气是一种清洁能源。
(3)将制备的氢气直接加压贮存在贮氢罐中,从构成物质的微粒角度分析,氢气能被压缩的原因是
。
(4)CH—HO催化重整是目前大规模制取H 的重要方法,生产过程中涉及的重要反应有
4 2 2
, 。依据图2分析,为使制取H 的百分含量最大,方法是向
2
催化重整体系中加入 。
(5)Mg Al 是一种特殊的镁合金。
17 12
①Mg Al 合金是一种储氢材料,完全吸氢后得到MgH 和Al,则“储氢过程”属于 (填
17 12 2
“物理”或“化学”)变化。
②MgH 能分解放出氢气,温度越高,MgH 的分解速率会越快。相同质量的MgH 在不同温度(T)条件
2 2 2
下,分解产生氢气的质量随时间的变化如图3所示,则温度T、T、T 由大到小的顺序是
1 2 3
。
14.(11分)某化学兴趣小组同学将紫色石蕊滴入CuSO 溶液中,发现溶液变红。查阅资料后得知CuSO
4 4
溶液呈酸性。研究性学习小组对其展开了进一步探究。
【实验探究一】CuSO 溶液与碳酸盐反应:向足量的NaCO 溶液中滴加少量的CuSO 溶液,产生无
4 2 3 4
色气体、绿色沉淀和无色溶液。
(1)将产生的气体通入澄清石灰水,产生白色沉淀,则该气体为 。
(2)某同学经过滤、洗涤等操作后;分别获得绿色固体和无色溶液,并进行研究。
查阅资料:常见绿色固体有碱式碳酸铜[Cu (OH) CO]和碱式硫酸铜[Cu (OH) SO ],都不溶于水,但均
2 2 3 2 2 4
能与酸反应。
实验方案:
①该绿色固体的成分为 。
②步骤Ⅰ中用稀盐酸而不用稀硫酸的理由是 。
③取“足量的NaCO 溶液和少量CuSO 溶液反应”后的无色溶液于试管中,加入足量稀硝酸,产生
2 3 4
大量气泡,再滴入Ba(NO ) 溶液,产生白色沉淀,最终溶液的溶质成分为 。
3 2
④写出碳酸钠溶液与硫酸铜溶液反应的化学方程式: 。
【实验探究二】CuSO 溶液与金属Al反应:
4(3)将铝丝没入CuSO 溶液中(如图所示),一段时间后没有出现红色物质,其原因是 。
4
(4)用砂纸将铝丝表面打磨光亮,将其没入CuSO 溶液中,观察现象:
4
①铝丝表面产生少量气泡,该气体是 。24h后,铝丝表面出现少最红色物质,说明Al能
与CuSO 溶液反应,但是反应较慢。
4
查阅资料后获得:Cl-可以加快铝丝和其他物质的反应逸率。
②铝丝周围溶液逐渐变成无色,铝丝以下溶液仍为蓝色,两层溶液界面清晰,从而可以得出密度:
CuSO 溶液 Al (SO ) 溶液(填“>"或“<")。
4 2 4 3
③请设计证明Cl-可以加快铝丝和其他物质的反应速率的实验(写出实验的操作、现象和对应的结论)
(可供选用的药品:Al、CuSO 溶液和AlCl 溶液)
4 3
15.(6分)铜及其化合物广泛应用于生活生产中。
(1)青铜是金属治铸史上最早的材料,适用于铸造各种器具、机械零件、齿轮等。青铜属于
(填“金属单质”或“合金”)。
(2)氧化铜对某些化学反应具有良好的催化效果。一种制备氧化铜的方法为:将一定量的CuCl (黄棕
2
色)与NaOH固体在容器中充分研磨,可制得CuO。
①制备时还生成一种盐与氧化物,则反应的化学方程式为 。
②制备实验过程中,判断反应发生的实验现象为 。
(3)氢氧化铜一维纳米材料是一种新兴材料,具有良好的电化学、光学性能。制备原理如下:
NaO+CuSO+2H O=Cu(OH) ↓+H O+Na SO 。实验室用100g浓度为0.39%的NaO 溶液与稍过量的
2 2 4 2 2 2 2 2 4 2 2
CuSO 溶液反应,理论上可制得多少克氢氧化铜一维纳米材料?
4