文档内容
2024 年中考第二次模拟考试(扬州卷)
化 学
(满分:100分 考试时间:100分钟 )
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 O-16 Mg-24 Al-27 Fe-56 Cu-64 Ba-137
一、单项选择题:共20题,每题2分,共40分。每题只有一个选项最符合题意。
1.我国在膜法水处理技术研究设计合成了超高通量多孔石墨烯膜,利用低品质热源实现了高效可持续的
海水淡化。下列说法不正确的是
A.水分子能通过多孔石墨烯膜 B.膜法比蒸馏法节约能源
C.淡化后水分子体积减小 D.可以帮助解决水资源缺乏问题
2.空气是一种宝贵的资源,其中含量最多且可用于食品防腐的成分是
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
3.把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是
A.面粉 B.蔗糖 C.植物油 D.大理石
4.某同学用 试纸测定了生活中一些物质的 ,其中呈碱性的是
A.炉具清洁剂 B.蔗糖水
C.柠檬汁 D.厕所清洁剂
5.模型建构是化学科学研究的基本方法。如图是某同学绘制的原子结构模型和原子结构示意图,有关说
法正确的是
A.①②属于同种元素
B.③形成的阳离子符号是H+
C.①对应的原子结构示意图是④
D.②形成的单质化学性质不稳定
6.下列物质属于化石燃料的是
A.氢气 B.乙醇 C.石油 D.一氧化碳7.下列HCl参与的反应中,属于化合反应的是
A. B.
C. D.
8.神舟十六号载人飞船使用的火箭推进剂是NH(肼)和HO 反应的化学方程式为NH+2H O
2 4 2 2 2 4 2 2
4HO+X,则X的化学式是
2
A.NO B.NO C.N D.HNO
2 2 3
9.合理施用化肥是使农业增产的重要手段。下列市售化肥中,属于复合肥料的是
A.NH Cl B.KNO
4 3
C.CO(NH ) D.Ca(HPO )
2 2 2 4 2
10.碱性锌锰电池性能优越,其组成物质包括锌粉、氢氧化钾、二氧化锰、石墨等,这些物质的类别不包
括
A.酸 B.碱
C.单质 D.氧化物
11.金纳米粒子可催化某些化学反应,金元素在元素周期表中的相关信息如图。下列说法正确的是
A.金元素的原子序数为79 B.金原子的电子数为118
C.金的相对原子质量为197.0g D.金是一种非金属元素
12.鉴别、检验、除杂和分离是认识和研究物质的常用方法。下列实验方案不能达到目的的是
选项 实验目的 实验方案
A 鉴别酒精和水 闻气味
B 检验CO中是否含有CO 将气体通入澄清石灰水,观察是否变浑浊
2
C 除去MnO 中混有的少量KCl固体 加足量水溶解、过滤、洗涤、干燥
2
D 分离锌粉和铜粉 加足量的稀硫酸,过滤
13.下列物质性质和用途对应关系不正确的是
A.活性炭有吸附性,可用作除味剂
B.熟石灰有碱性,可用于治疗胃酸过多
C.油脂能溶于汽油,可用于除油污
D.生石灰有吸水性,可用作食品干燥剂14.鸡蛋壳主要成分为碳酸钙,化学兴趣小组对鸡蛋壳进行了实验探究,具体实验如图所示,下列说法中
错误的是
A.实验1中,打开分液漏斗,滴加盐酸,一段时间后,澄清石灰水会变浑浊
B.实验2中,温度计会显示溶液的温度升高
C.实验2中显示的操作都是规范的
D.实验2中,烧杯中溶液会变红
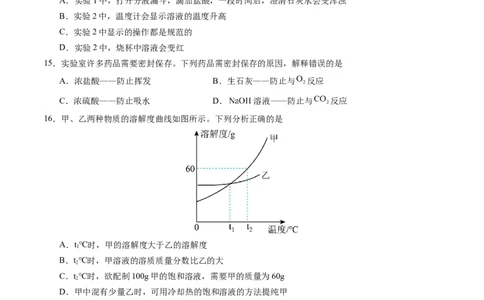
15.实验室许多药品需要密封保存。下列药品需密封保存的原因,解释错误的是
A.浓盐酸——防止挥发 B.生石灰——防止与 反应
C.浓硫酸——防止吸水 D. 溶液——防止与 反应
16.甲、乙两种物质的溶解度曲线如图所示。下列分析正确的是
A.t℃时,甲的溶解度大于乙的溶解度
1
B.t℃时,甲溶液的溶质质量分数比乙的大
2
C.t℃时,欲配制100g甲的饱和溶液,需要甲的质量为60g
2
D.甲中混有少量乙时,可用冷却热的饱和溶液的方法提纯甲
17.下列对实验现象的解释不正确的一组是
选项 实验现象 解释
A 铝制门窗比铁门窗使用寿命长 铝表面很容易形成致密氧化膜
B 向锌粒中加入稀硫酸,产生气泡 金属都能与稀硫酸反应产生气泡
C 将黄铜片和纯铜片相互刻画,纯铜片表面有明显划痕 合金的硬度往往比组成其的纯金属硬度大
D 铁丝在空气中不能燃烧,在氧气中可以燃烧 氧气的浓度对物质的燃烧有影响18.用石灰浆与双氧水反应可制备 ,反应过程包括:步骤一: ,其中O代表氧原子;
步骤二:主要发生Ca(OH)+O═CaO+H O,少量发生 。下列说法不正确的是
2 2 2
A.生成 的总反应为
B.使用石灰浆是为了增大反应混合物中 的含量
C. 中氧元素的化合价是
D.大幅度提高温度可以加快制备 的速率
阅读下列材料,完成19~20题。
近期,中国科学家在淀粉人工合成方面取得突破性进展,在国际上首次实现二氧化碳到淀粉的从头合
成,相关论文在国际学术期刊《Nature》上发表。主要过程如下:
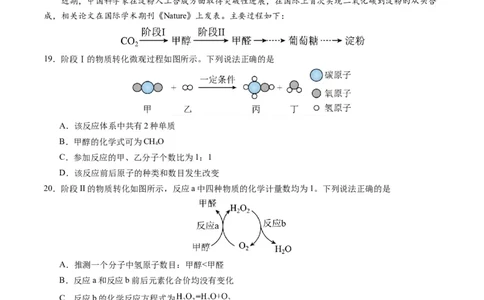
19.阶段Ⅰ的物质转化微观过程如图所示。下列说法正确的是
A.该反应体系中共有2种单质
B.甲醇的化学式可为CHO
4
C.参加反应的甲、乙分子个数比为1:1
D.该反应前后原子的种类和数目发生改变
20.阶段II的物质转化如图所示,反应a中四种物质的化学计量数均为1。下列说法正确的是
A.推测一个分子中氢原子数目:甲醇<甲醛
B.反应a和反应b前后元素化合价均没有变化
C.反应b的化学反应方程式为
D.阶段II甲醇能够持续转化为甲醛,反应b还需补充HO
2 2
二、非选择题:共5题,每题2分,共60分。
21.(10分)扬州大运河博物馆收藏了大量的文物和历史资料,展示了大运河的历史、文化等方面的丰富
内容。(1)建筑艺术——中国钢结构金奖
①钢的主要成分是 (填化学式)。
②钢在空气中容易生锈,生锈的条件是 ,写出一种防止钢生锈的措施 。
③生铁和钢性能不同的原因 。
(2)何止八怪——扬州绘画三百年
①用炭墨书绘的古代字画能保留上百年依然完好不褪色,是因为 。
②金刚石和石墨都是由碳元素组成的单质,但它们的物理性质不同,原因是 。
(3)运河古城——千载清波漾
①检验运河水是软水还是硬水,可向水样中加 来检验。
②生产自来水时,常用 吸附水中的色素和异味,通过 操作除去运河水中的难溶性杂质。
③测定运河水的酸碱度可用 。
22.(12分)能源既是国家经济发展的命脉,也是国家发展战略的重要支柱。
(一)人类目前所消耗的能量主要来自化石燃料。
(1)将石油加热炼制,是利用石油中各成分的 不同,将它们分离得到汽油、煤油、柴油等产品。
(2)天然气用途非常广泛,可作燃料直接使用。其完全燃烧的化学方程式为 。
当家用燃气灶火焰呈黄色,锅底出现黑色固体,此时可将灶具的进风口 (填“调大”或“调小”)。
(二)氢气被看作是理想的“绿色能源”,氢能产业包含氢气的制备、储存、运输和应用等多个环节。
I.制备“氢气”:
(3)用太阳能将水转化为氢能是一种理想途径。图1装置通过控制开关连接K 或K,可交替得到H 和
1 2 2
O。制H 时,连接 (填“K”或“K”);改变开关连接方式,可得O。
2 2 1 2 2
(4)CH-H O催化重整是目前大规模制取H 的重要方法,生产过程中涉及的主要反应有:CH+H O
4 2 2 4 2
CO+3H;CO+HO CO+H 。
2 2 2 2
①若将8吨CH 用于制取H,假设每一步均完全反应,理论上可制得H 吨。
4 2 2
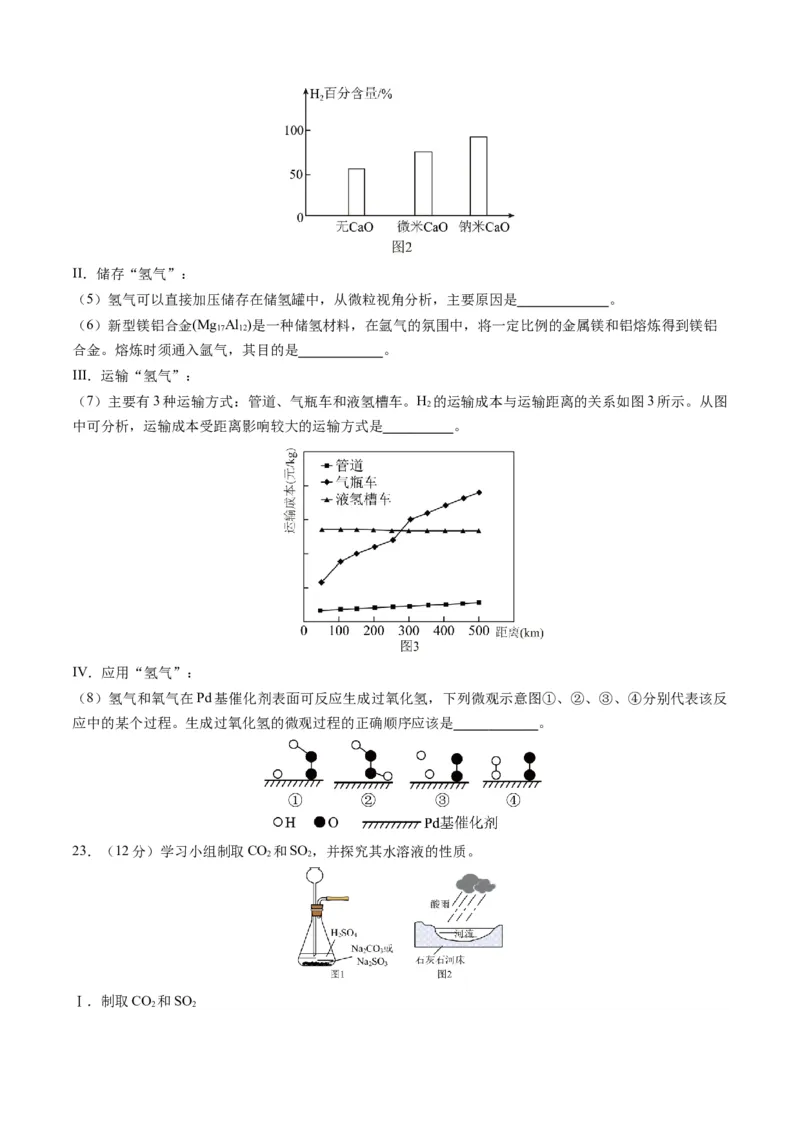
②如图2,向CH -HO催化重整体系中投入定量的CaO可提高H 百分含量。而投入纳米CaO时H 的百
4 2 2 2
分含量最大,原因可能是 。II.储存“氢气”:
(5)氢气可以直接加压储存在储氢罐中,从微粒视角分析,主要原因是 。
(6)新型镁铝合金(Mg Al )是一种储氢材料,在氩气的氛围中,将一定比例的金属镁和铝熔炼得到镁铝
17 12
合金。熔炼时须通入氩气,其目的是 。
III.运输“氢气”:
(7)主要有3种运输方式:管道、气瓶车和液氢槽车。H 的运输成本与运输距离的关系如图3所示。从图
2
中可分析,运输成本受距离影响较大的运输方式是 。
IV.应用“氢气”:
(8)氢气和氧气在Pd基催化剂表面可反应生成过氧化氢,下列微观示意图①、②、③、④分别代表该反
应中的某个过程。生成过氧化氢的微观过程的正确顺序应该是 。
23.(12分)学习小组制取CO 和SO ,并探究其水溶液的性质。
2 2
Ⅰ.制取CO 和SO
2 2在常温、气体压强为101kPa时,1体积水里最多能溶解大约1体积CO 或40体积SO 。学习小组利用图1
2 2
所示装置制取CO 和SO 。
2 2
(1)利用该装置制取CO 的化学反应方程式为 。
2
(2)不能用排水法收集SO 的理由是 。
2
Ⅱ.探究CO 和SO 水溶液的性质
2 2
(3)在通风橱中分别向100 mL H O中通入CO 和SO 至饱和,用pH计测定饱和溶液pH,静置2h后,再
2 2 2
次读取溶液pH。结果如下表所示。
饱和溶液pH 静置2h后溶液pH
CO 水溶液 3.94 4.12
2
SO 水溶液 0.88 0.79
2
①测定pH最简便的方法是使用pH试纸,操作时玻璃棒的作用是 (填字母)。
A.搅拌 B.引流 C.蘸取溶液
②静置2h后,CO 水溶液酸性 (填“增强”或“减弱”)。
2
③有同学根据溶液的pH认为CO 也是造成酸雨的重要因素。请判断该推论是否正确,并说明理由:
2
。
(4)取静置后的SO 水溶液于试管中,向其中滴加过量Ba(OH) 溶液,有沉淀产生。
2 2
【提出问题】该沉淀是什么?
【查阅资料】
①SO 水溶液、BaSO 都能与O 发生氧化反应。
2 3 2
②BaSO 和BaSO 都难溶于水。
3 4
③BaSO 能溶于浓度较大的盐酸,BaSO 不溶于盐酸。
3 4
【提出猜想】沉淀可能为BaSO 或BaSO、BaSO 的混合物。
4 4 3
【实验验证】请设计实验验证沉淀中一定含有BaSO。简述实验过程(包括操作和现象): 。
4
(实验中须使用的试剂:10%的盐酸)
(5)煤燃烧排放的SO 可能导致酸雨。南通市2021年酸雨发生率为1.7%,比2020年减少1%。你了解的
2
本地决策部门为降低SO 排放做出的举措有 (写一条)。
2
(6)酸雨对环境的影响因地区地质而异。图2中河流受酸雨损害的程度较小的原因是 。
24.(12分)金属材料在生产生活中应用广泛。
(1)高铁电传输系统的材料主要含铜,是利用了铜良好的 性。
(2)高铁轨道、车厢、附属设施使用了大量的铁合金和铝合金。小组同学探究合金中金属的化学性质。
【实验一】在分别装有质量相等和外形相同的Cu、Fe、A1和Mg的四个烧杯中,加入相同质量的溶质质
量分数为7.3%的盐酸,如图1所示。①证明金属活动性Fe>Cu的实验现象是 ,反应的化学方程式为 。
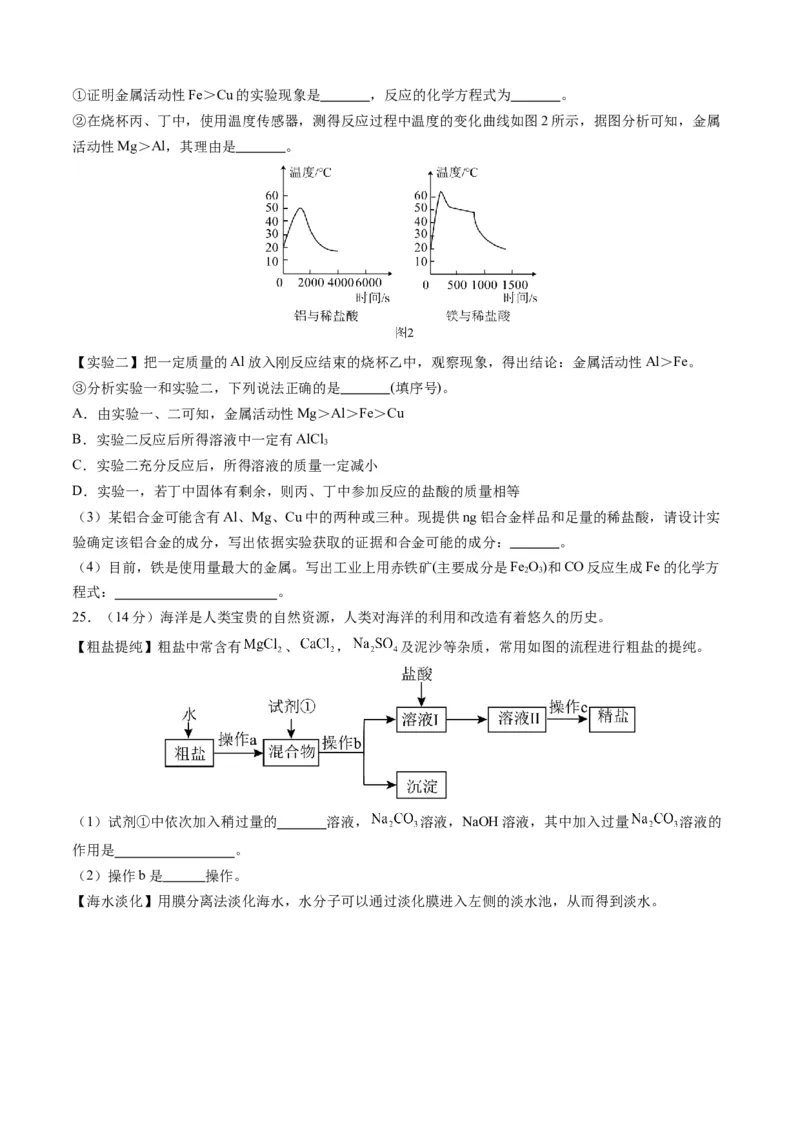
②在烧杯丙、丁中,使用温度传感器,测得反应过程中温度的变化曲线如图2所示,据图分析可知,金属
活动性Mg>Al,其理由是 。
【实验二】把一定质量的Al放入刚反应结束的烧杯乙中,观察现象,得出结论:金属活动性Al>Fe。
③分析实验一和实验二,下列说法正确的是 (填序号)。
A.由实验一、二可知,金属活动性Mg>Al>Fe>Cu
B.实验二反应后所得溶液中一定有AlCl
3
C.实验二充分反应后,所得溶液的质量一定减小
D.实验一,若丁中固体有剩余,则丙、丁中参加反应的盐酸的质量相等
(3)某铝合金可能含有Al、Mg、Cu中的两种或三种。现提供ng铝合金样品和足量的稀盐酸,请设计实
验确定该铝合金的成分,写出依据实验获取的证据和合金可能的成分: 。
(4)目前,铁是使用量最大的金属。写出工业上用赤铁矿(主要成分是Fe O)和CO反应生成Fe的化学方
2 3
程式: 。
25.(14分)海洋是人类宝贵的自然资源,人类对海洋的利用和改造有着悠久的历史。
【粗盐提纯】粗盐中常含有 、 , 及泥沙等杂质,常用如图的流程进行粗盐的提纯。
(1)试剂①中依次加入稍过量的 溶液, 溶液,NaOH溶液,其中加入过量 溶液的
作用是 。
(2)操作b是 操作。
【海水淡化】用膜分离法淡化海水,水分子可以通过淡化膜进入左侧的淡水池,从而得到淡水。(3)下列说法中正确的是______(填字母序号)。
A.膜分离法的原理与蒸馏的原理类似
B.左侧淡水中盐类物质含量减小
C.该膜分离法的目的是除去海水中的不溶物
【海水利用】我国企业用10年时间,自主研发出海水镁资源综合利用专利技术,生出碳酸镁水合物,并以
此为中间体制备各类镁产品,填补了我国高端镁产品生产空白。
工业上从弱碱性卤水(主要成分为 )中获取 的一种方法如图1:
(4)沉淀过程的pH随时间的变化如图2所示,沉淀过程的操作为 (填序号)。
a.向NaOH溶液中滴加卤水,同时通入
b.向卤水中滴加NaOH溶液,同时通入
c.向卤水中通入 至饱和,然后滴加NaOH溶液,同时继续通入
d.向NaOH溶液中通入 至饱和,然后滴加卤水,同时继续通入
(5)测定 的纯度
实验步骤:利用如图3所示装置(图中夹持仪器略去)进行实验,以确定 的纯度。已知:
。依据实验过程回答下列问题。
①C中反应的化学方程式为 ;D中碱石灰的作用为 。
②下列措施能提高测定准确度的是 (填序号)。a.在加入硫酸之前应排净装置内 气体
b.在AB之间增添盛有浓硫酸的洗气装置
c.实验结束后,再通空气一段时间
d.在C装置左侧导管末端增添多孔球泡
(6)小智认为应将C中 溶液换成 溶液,理由一:氢氧化钡的溶解度大,形成溶液的浓
度大,使 被吸收的更完全;理由二: 。
(7)①实验中准确称取三份10g样品,进行三次测定,测得生成 沉淀的平均质量为9.85g,则样品
中 的纯度为 。(写出计算过程)
②若获取样品中含有少量 ,则样品中 的纯度 (填“偏大”
“不变”或“偏小”)。