文档内容
2024 年中考第一次模拟考试(扬州卷)
化 学
(考试时间:100分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Fe-56 Cl-35.5
第Ⅰ卷(选择题 共 40 分)
一、单项选择题:本题共20个小题,每小题2分,共40分。
1.下列是我国“国家最高科学技术奖”几位获得者及其部分研究领域,其中研究领域主要涉及化石燃料
的是
A.闵恩泽,石油化工催化剂研究 B.师昌绪,材料腐蚀研究
C.赵忠贤,高温超导材料研究 D.张存浩,高能化学激光研究
2.保存文物可用空气中含量最多的气体,该气体的化学式为
A. B. C. D.
3.绿色植物通过光合作用将气体X与HO转化为葡萄糖与O,气体X是
2 2
A.N B.Ar C.CO D.SO
2 2 2
4.下列物质溶于水,所得溶液显酸性的是
A. B.KCl C. D.
5.新型高强、高塑、高稳定性铝基碳化硅( )复合材料是“祝融号”火星车中的一种重要材料。碳元
素和硅元素的根本区别是
A.相对原子质量不同 B.最外层电子数不同
C.原子核内中子数不同 D.原子核内质子数不同
6.推进能源资源、产业结构转型升级,推动经济社会绿色发展,是我国经济发展的重要举措,下列做法
符合这一理念的是
A.大力发展钢铁产业 B.加大原煤开采运输
C.增加开山采矿投资 D.建设风力发电设备
7.我国宋代《梦溪笔谈》中有“熬胆矾铁釜久之亦化为铜”的记载,其化学反应原理为Fe+CuSO=Cu+FeSO ,该反应的基本反应类型是
4 4
A.化合反应 B.置换反应 C.分解反应 D.氧化反应
8.为了减少污染,某工厂用硫化钠溶液来吸收工厂烟气中的SO ,反应的化学方程式为:
2
,则X的化学式为
A.NaSO B.NaHSO C.NaHSO D.NaSO
2 3 4 3 2 4
9.材料与人类生活密切相关。下列物品由复合材料制成的是
A.玻璃水杯 B.玻璃钢罩 C.塑料砧板 D.陶瓷餐具
10.运用分类,可以预测物质的性质及其变化的规律,下列物质中属于盐的是
A.NaOH B.NaCO C.CuO D.C HOH
2 3 2 5
11.下列物质由原子直接构成的是
A.氯化钠 B.过氧化氢 C.汞 D.C
60
12.下列实验方案设计正确的是
A.鉴别硬水和软水:取等量水样,滴加等量肥皂水,振荡,观察现象差异
B.比较铜和银的金属活动性强弱:分别向盛有铜和银的试管中加入稀盐酸
C.检验气体是否为二氧化碳:向集气瓶内伸入燃着的木条,观察是否熄灭
D.除去铁粉中的少量铜粉:加入足量稀盐酸,充分反应后过滤、洗涤、干燥
13.下列物质的用途和性质对应正确的是
A.氧气作助燃剂——可燃性 B.浓硫酸可作某些气体的干燥剂——腐蚀性
C.铜丝制作导线——导热性 D.小苏打可用于中和胃酸过多——碱性
14.规范的实验操作是实验成功的关键。下列实验操作正确的是
A.称量固体 NaOH B.倾倒液体
C.测定溶液的 pH D.稀释浓硫酸
15.下列物质的俗名、化学式、用途完全对应正确的是
A.烧碱、NaOH、改良酸性土壤 B.干冰、HO、人工降雨
2
C.纯碱、NaCO 制玻璃 D.水银、Ag、做温度计
2 3、
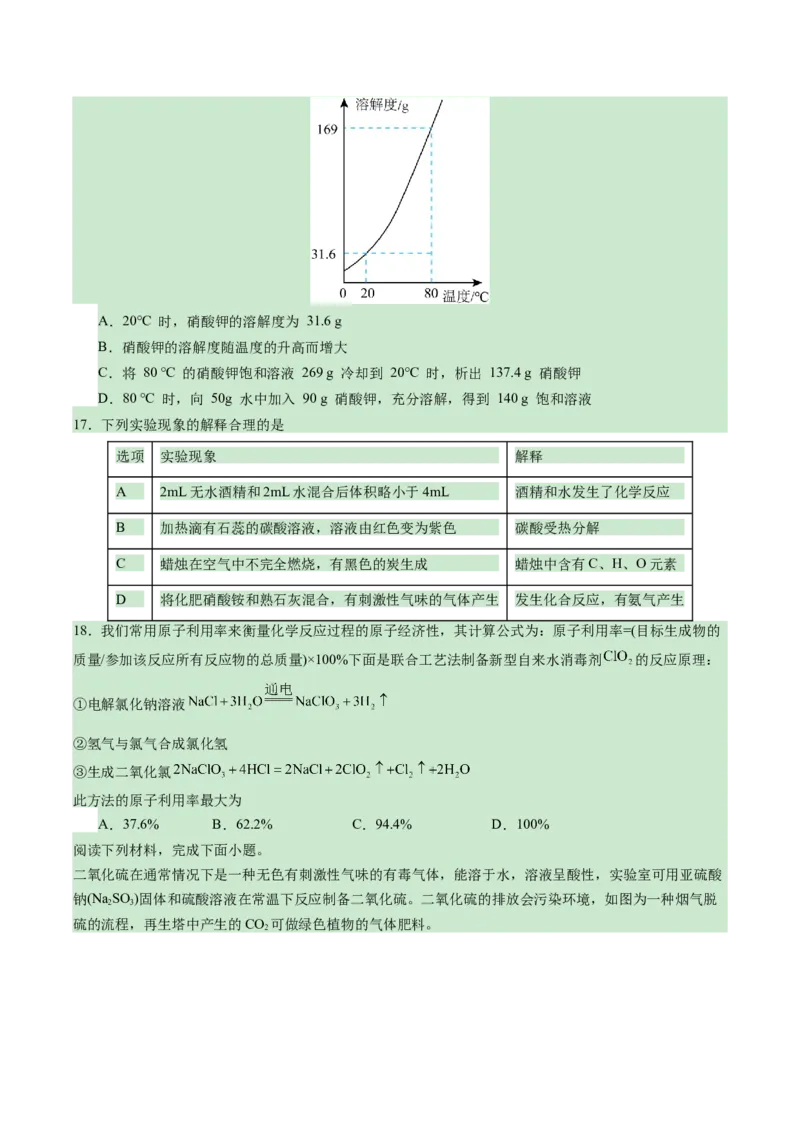
16.如图为硝酸钾的溶解度曲线,下列说法错误的是A.20℃ 时,硝酸钾的溶解度为 31.6 g
B.硝酸钾的溶解度随温度的升高而增大
C.将 80 ℃ 的硝酸钾饱和溶液 269 g 冷却到 20℃ 时,析出 137.4 g 硝酸钾
D.80 ℃ 时,向 50g 水中加入 90 g 硝酸钾,充分溶解,得到 140 g 饱和溶液
17.下列实验现象的解释合理的是
选项 实验现象 解释
A 2mL无水酒精和2mL水混合后体积略小于4mL 酒精和水发生了化学反应
B 加热滴有石蕊的碳酸溶液,溶液由红色变为紫色 碳酸受热分解
C 蜡烛在空气中不完全燃烧,有黑色的炭生成 蜡烛中含有C、H、O元素
D 将化肥硝酸铵和熟石灰混合,有刺激性气味的气体产生 发生化合反应,有氨气产生
18.我们常用原子利用率来衡量化学反应过程的原子经济性,其计算公式为:原子利用率=(目标生成物的
质量/参加该反应所有反应物的总质量)×100%下面是联合工艺法制备新型自来水消毒剂 的反应原理:
①电解氯化钠溶液
②氢气与氯气合成氯化氢
③生成二氧化氯
此方法的原子利用率最大为
A.37.6% B.62.2% C.94.4% D.100%
阅读下列材料,完成下面小题。
二氧化硫在通常情况下是一种无色有刺激性气味的有毒气体,能溶于水,溶液呈酸性,实验室可用亚硫酸
钠(Na SO )固体和硫酸溶液在常温下反应制备二氧化硫。二氧化硫的排放会污染环境,如图为一种烟气脱
2 3
硫的流程,再生塔中产生的CO 可做绿色植物的气体肥料。
219.下列关于二氧化硫的说法中,正确的是
A.二氧化硫也能使紫色石蕊溶液变红
B.二氧化硫是由硫和氧气两种单质组成
C.二氧化硫和亚硫酸钠都属于氧化物
D.实验室制取二氧化硫的装置与氯酸钾制取氧气相同
20.下列说法不正确的是
A.烟气脱硫能减少酸雨的形成
B.理论上,生产过程中需不断补充CaS
C.脱硫塔中发生的主要反应为:
D.该工业流程可以实现CO 的“零排放”
2
第 II 卷(非选择题 共 60 分)
21.(10分)扬州既是世界美食之都,也是一座历史悠久并极具现代气息的文化名城。
(1)扬州美食,传承扬州味道。美食香味四溢,说明分子在 。
(2)青砖黛瓦,诉说扬州历史。
①《天工开物》中介绍了烧制青砖的方法,其中载有“灌水其上”“水火既济”。相关反应为水蒸气
与灼热的碳生成CO和一种气体单质,其化学方程式为 。
②工匠用生石灰(CaO)和水化合生成熟石灰[Ca(OH)]。用熟石灰加水制得的石灰乳抹墙,在空气
2
中会形成白色的碳酸钙,该反应的化学方程式为 。
③长时间使用的铜制门环会发黑,是因为铜与氧气产生了黑色的 (填化学式)。
(3)汽车高铁,展现扬州速度。
①电网通过石墨电刷给动车供电,体现了石墨具有良好的 性。
②动车车身表面防锈采用的方法是 ,其防锈原理是 。
③制造铁轨的锰钢是一种铁合金,与纯铁相比,其硬度更 (填“大”或“小”)。
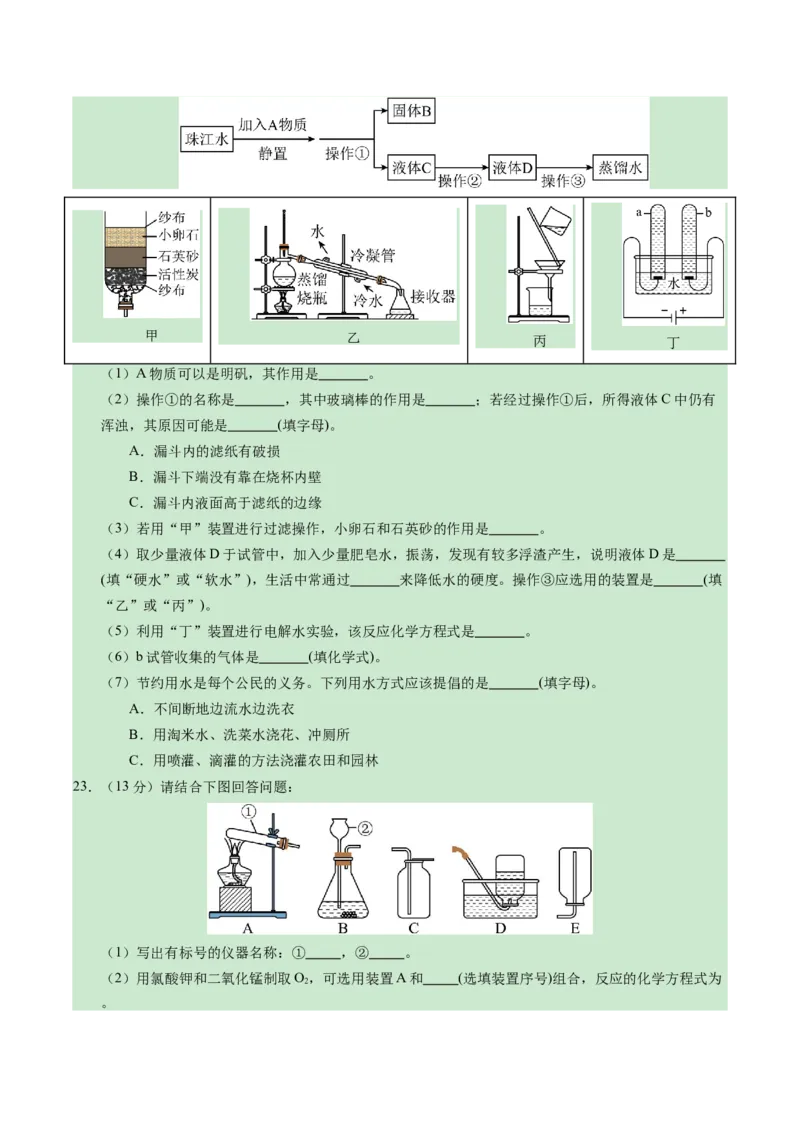
22.(12分)水是生命之源。某化学小组收集到一瓶浑浊的珠江水,并在实验室模拟自来水厂的净水过
程,
最终制成蒸馏水。其实验过程如图所示。请回答以下问题:甲 乙 丙 丁
(1)A物质可以是明矾,其作用是 。
(2)操作①的名称是 ,其中玻璃棒的作用是 ;若经过操作①后,所得液体C中仍有
浑浊,其原因可能是 (填字母)。
A.漏斗内的滤纸有破损
B.漏斗下端没有靠在烧杯内壁
C.漏斗内液面高于滤纸的边缘
(3)若用“甲”装置进行过滤操作,小卵石和石英砂的作用是 。
(4)取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,说明液体D是
(填“硬水”或“软水”),生活中常通过 来降低水的硬度。操作③应选用的装置是 (填
“乙”或“丙”)。
(5)利用“丁”装置进行电解水实验,该反应化学方程式是 。
(6)b试管收集的气体是 (填化学式)。
(7)节约用水是每个公民的义务。下列用水方式应该提倡的是 (填字母)。
A.不间断地边流水边洗衣
B.用淘米水、洗菜水浇花、冲厕所
C.用喷灌、滴灌的方法浇灌农田和园林
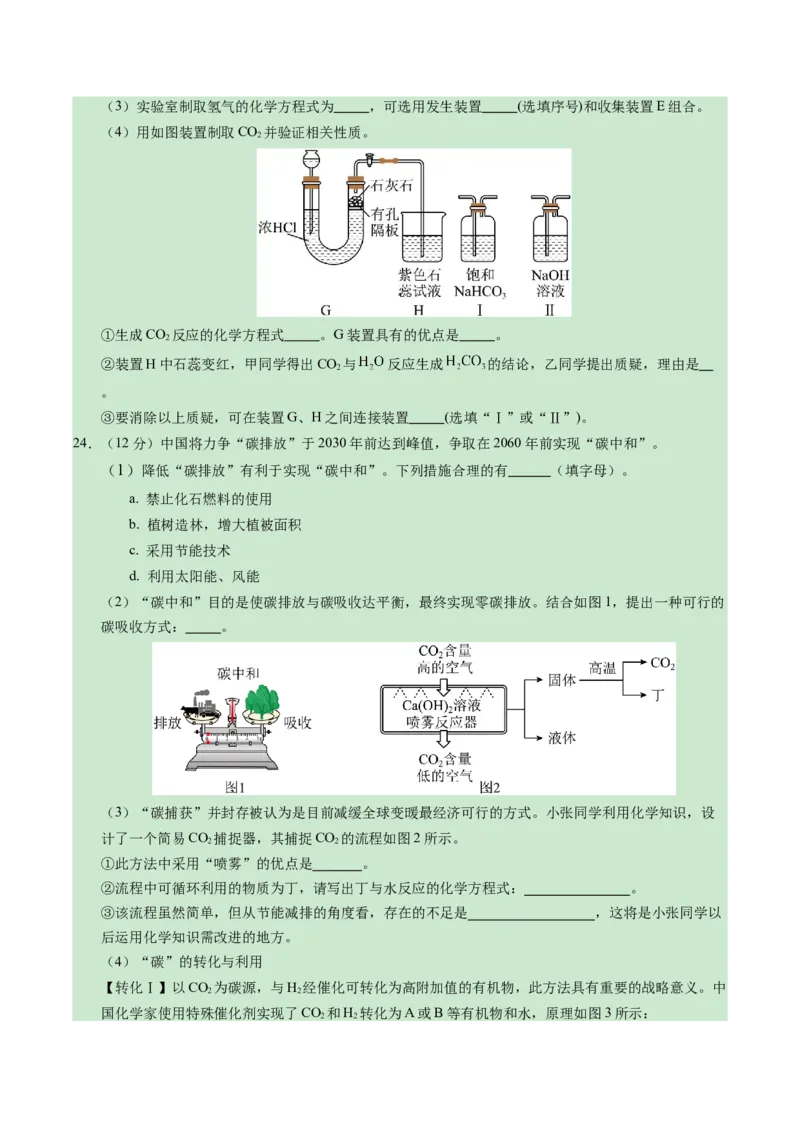
23.(13分)请结合下图回答问题:
(1)写出有标号的仪器名称:① ,② 。
(2)用氯酸钾和二氧化锰制取O,可选用装置A和 (选填装置序号)组合,反应的化学方程式为
2
。(3)实验室制取氢气的化学方程式为 ,可选用发生装置 (选填序号)和收集装置E组合。
(4)用如图装置制取CO 并验证相关性质。
2
①生成CO 反应的化学方程式 。G装置具有的优点是 。
2
②装置H中石蕊变红,甲同学得出CO 与 反应生成 的结论,乙同学提出质疑,理由是
2
。
③要消除以上质疑,可在装置G、H之间连接装置 (选填“Ⅰ”或“Ⅱ”)。
24.(12分)中国将力争“碳排放”于2030年前达到峰值,争取在2060年前实现“碳中和”。
(1)降低“碳排放”有利于实现“碳中和”。下列措施合理的有 (填字母)。
a. 禁止化石燃料的使用
b. 植树造林,增大植被面积
c. 采用节能技术
d. 利用太阳能、风能
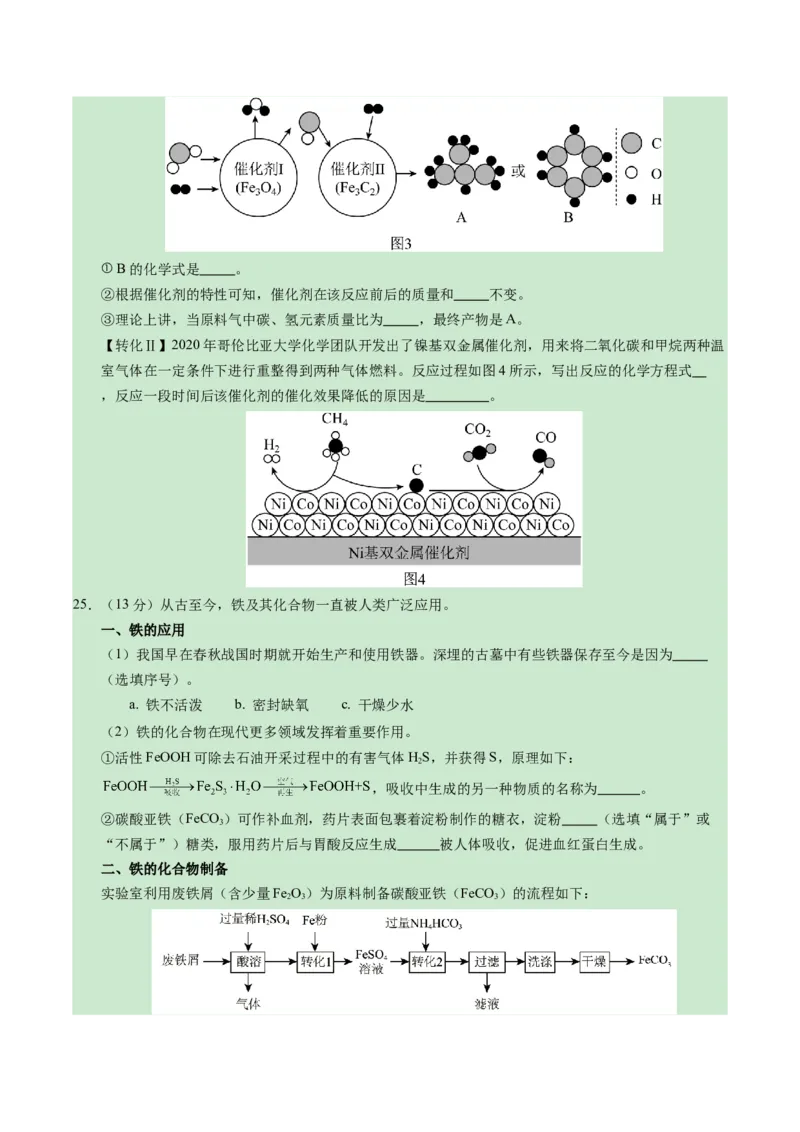
(2)“碳中和”目的是使碳排放与碳吸收达平衡,最终实现零碳排放。结合如图1,提出一种可行的
碳吸收方式: 。
(3)“碳捕获”并封存被认为是目前减缓全球变暖最经济可行的方式。小张同学利用化学知识,设
计了一个简易CO 捕捉器,其捕捉CO 的流程如图2所示。
2 2
①此方法中采用“喷雾”的优点是 。
②流程中可循环利用的物质为丁,请写出丁与水反应的化学方程式: 。
③该流程虽然简单,但从节能减排的角度看,存在的不足是 ,这将是小张同学以
后运用化学知识需改进的地方。
(4)“碳”的转化与利用
【转化Ⅰ】以CO 为碳源,与H 经催化可转化为高附加值的有机物,此方法具有重要的战略意义。中
2 2
国化学家使用特殊催化剂实现了CO 和H 转化为A或B等有机物和水,原理如图3所示:
2 2① B的化学式是 。
②根据催化剂的特性可知,催化剂在该反应前后的质量和 不变。
③理论上讲,当原料气中碳、氢元素质量比为 ,最终产物是A。
【转化Ⅱ】2020年哥伦比亚大学化学团队开发出了镍基双金属催化剂,用来将二氧化碳和甲烷两种温
室气体在一定条件下进行重整得到两种气体燃料。反应过程如图4所示,写出反应的化学方程式
,反应一段时间后该催化剂的催化效果降低的原因是 。
25.(13分)从古至今,铁及其化合物一直被人类广泛应用。
一、铁的应用
(1)我国早在春秋战国时期就开始生产和使用铁器。深埋的古墓中有些铁器保存至今是因为
(选填序号)。
a. 铁不活泼 b. 密封缺氧 c. 干燥少水
(2)铁的化合物在现代更多领域发挥着重要作用。
①活性FeOOH可除去石油开采过程中的有害气体HS,并获得S,原理如下:
2
,吸收中生成的另一种物质的名称为 。
②碳酸亚铁(FeCO)可作补血剂,药片表面包裹着淀粉制作的糖衣,淀粉 (选填“属于”或
3
“不属于”)糖类,服用药片后与胃酸反应生成 被人体吸收,促进血红蛋白生成。
二、铁的化合物制备
实验室利用废铁屑(含少量Fe O)为原料制备碳酸亚铁(FeCO)的流程如下:
2 3 3(3)酸溶时适当提高反应温度和HSO 浓度,目的是 。
2 4
(4)Fe粉可使“酸溶”产生的Fe (SO ) 转化为FeSO ,该反应的化学方程式为 。
2 4 3 4
(5)转化2中温度不宜过高的原因是 。
(6)在空气中灼烧FeCO 可获得颜料铁红(Fe O)和CO,反应的化学方程式为 。
3 2 3 2
三、铁的化合物含量测定
称取含FeCO 的Fe O 样品21.8g,放入下图所示装置中通入CO,控温在300℃,加热至质量不再改
3 2 3
变,测得剩余固体质量为19.6g。
资料:
①FeCO 在282℃分解为FeO。
3
②用CO还原Fe O 炼铁的过程大致分为三个阶段:
2 3
阶段1:
阶段2:
阶段3:
继续向装置中通CO,分阶段升温,进行CO还原铁的氧化物,加热时测得剩余固体质量随温度变化的
曲线如图所示。
(7)图中N点固体的成分及对应的质量为 。(写出计算过程)