文档内容
2024 年中考第一次模拟考试(甘肃卷)
化学·全解全析
一、选择题(每小题只有一个正确答案,第1-10小题每题1分,第11-15题每小题2分,共20分)
1. 下列物质中,目前计入“空气污染指数”项目的是
A. 二氧化碳 B. 稀有气体 C. 细颗粒物 D. 氮气
【答案】C
【解析】目前计入我国“空气污染指数”的监测项目有:二氧化硫、一氧化碳、二氧化氮、可吸入颗粒及
臭氧等。故选C。
2. 从变化角度看下列诗句中与其它三句有本质区别的是
A. 千锤万凿出深山,烈火焚烧若等闲
B. 爆竹声中一岁除,春风送暖入屠苏
C. 美人首饰侯王印,尽是沙中浪底来
D. 春蚕到死丝方尽,蜡炬成灰泪始干
【答案】C
【解析】A、烈火焚烧若等闲中石灰石高温煅烧时能生成氧化钙和二氧化碳等新物质,属于化学变化;
B、燃放烟花爆竹能生成二氧化碳等新物质,属于化学变化;C、“美人首饰侯王印,尽是沙中浪底
来”过程中没有新物质生成,只是物质的形态发生了改变,属于物理变化;D、蜡烛燃烧能生成水和二
氧化碳等新物质,属于化学变化。故选C。
3. 保护环境,节约资源,从我做起。下列做法不符合这一理念的是
A. 纸张要双面使用
B. 随手关灯
C. 农业和园林灌溉采用大水浸灌
D. 外卖、网购等包装用品分类回收,综合利用
【答案】C
【解析】A、纸张要双面使用,利于节约资源,不符合题意;B、随手关灯利于节约电能资源,不符合
题意;C、农业和园林灌溉采用大水浸灌,不利于节约水资源,符合题意;D、外卖、网购等包装用品
分类回收,综合利用,利于节约资源,不符合题意;故选C。
4. 下列对实验现象的描述或实验操作正确的是
A. 棉花灼烧后会产生烧焦羽毛的气味
B. 铁丝在空气中剧烈燃烧生成黑色固体C. 硫在空气中燃烧,火焰呈淡蓝色
D. 氢氧化钠固体放在纸片上进行称量
【答案】C
【解析】A、棉花灼烧时有烧纸的气味,而不是烧焦羽毛的气味,该选项描述不正确;B、铁丝在空气
中不燃烧,只能在纯氧中燃烧,该选项描述不正确;C、硫在空气中燃烧,产生淡蓝色火焰,放热,该
选项描述正确;D、氢氧化钠固体易潮解,且具有腐蚀性,称量时不能放在纸上称量,应放在玻璃器皿
中,该选项操作不正确。故选C。
5. 化学与生活、健康、环境密切相关。下列有关说法错误的是
A. 蔬菜、水果富含维生素
B. 霉变大米含有黄曲霉素,用热水洗净后再煮饭
C. 青少年缺钙,易患佝偻病
D. 垃圾分类,有利减少废弃污染,变废为宝
【答案】B
【解析】A、蔬菜、水果富含维生素,选项说法正确; B、霉变大米含有有毒的黄曲霉素,用水洗净后
也不能食用,选项说法错误; C、青少年缺钙,易患佝偻病,选项说法正确; D、垃圾分类,有利减少
废弃污染,变废为宝,选项说法正确。 故选B。
6. 下列物质中,氮元素的化合价最低的是
A. NO B. NH C. NO D. HNO
3 2 3
【答案】B
【解析】A、NO中氧元素为-2价,氮元素的化合价为+2价;B、NH 中氢元素的化合价为+1价,则
3
氮元素的化合价为-3价;C、NO中氧元素的化合价为-2价,则氮元素的化合价为+1价;D、HNO 中
2 3
氢元素的化合价为+1价,氧元素的化合价为-2价,设氮元素化合价为x,根据化合物中正负化合价代
数为0,则有(+1)+ x+(-2)×3=0,得x=+5价;所以氮元素的化合价最低的化合物是NH ,故选B。
3
7. 下列对分子、原子、离子的认识正确的是
A. 离子一定是带电的原子
B. 原子是最小的粒子,不可再分
C. 由分子构成的物质,分子是保持其化学性质的最小微粒
D. CO 和CO性质的差异主要是由于分子间的间隔不同
2
【答案】C
【解析】A、离子是带电的原子或原子团,不符合题意;B、原子可分为原子核和核外电子,在化学变
化中,原子不可分,不符合题意;C、由分子构成的物质,分子是保持其化学性质的最小微粒,符合题意;D、CO 和CO性质的差异是因为分子构成不同,一个二氧化碳分子比一个一氧化碳分子多一个氧原
2
子,不符合题意。故选C。
8. 下图是钠元素在元素周期表中的信息和钠原子结构示意图。下列说法正确的是
A. 钠原子的相对原子质量是22.989
B. 钠元素的中子数为11
C. 钠元素为非金属元素
D. 化学反应中,钠原子易得到电子变为钠离子
【答案】A
【解析】A、根据元素周期表中的一格中获取的信息,可知元素的相对原子质量为 22.989,相对原子质
量单位是“1”,省略不写,故选项说法正确;B、根据元素周期表中的一格中获取的信息,该元素的原
子序数为11;根据原子序数=核电荷数=质子数,则该元素的质子数为11;或由原子的结构示意图,知
其质子数为11,中子数不是11,故选项说法错误;C、根据元素周期表中的一格中获取的信息,该元
素的名称是钠,属于金属元素,故选项说法错误;D、钠原子的最外层电子数是1,在化学反应中易失
去1个电子而形成阳离子,故选项说法错误;故选B。
9. 为防控疫情,通常在公共场所使用84消毒液(土要成分是NaClO)进行消毒。NaClO中氯元素的化合
价是
A. -3 B. +1 C. +3 D. +5
【答案】B
【解析】NaClO中钠元素的化合价为+1价,氧元素的化合价为-2价,设NaClO中氯元素的化合价为a,
则+1+a+(-2)=0,a=+1,故NaClO中氯元素的化合价为+1价。故选B。
10. 碳与浓硫酸在加热条件下发生如下反应: ,其中X的化学式
是
A. B. C. D.
【答案】B
【解析】化学反应前后原子的种类和个数不变,等号左边有1个碳原子、4个氢原子、2个硫原子和8
个氧原子,等号右边除2X外,有1个碳原子、4个氢原子和4个氧原子,则2X中含有2个硫原子和4个氧原子,则X的化学式为SO ,故选B。
2
11. 某化学反应的微观示意图如下,根据该图得出的结论,不正确的是
A. 四种物质中丙、丁属于氧化物
B. 化学反应前后分子种类没有发生变化
C. 该反应是氧化反应
D. 反应生成的丙、丁分子个数比为2:3
【答案】B
【解析】由化学反应的微观示意图可知,该反应是氨气和氧气反应生成了一氧化氮和水,反应的化学
方程式是:4NH +5O 4NO+6H O。A、由方程式可知,该反应中的NO、H O属于氧化物,故A
3 2 2 2
正确;B、由微粒的变化可知,化学反应前后分子种类发生变化,故B错误;C、该反应有氧气参加,
是氧化反应,故C正确;D、由化学方程式可知,反应中甲和丁的分子个数比是4:6=2:3,故D正确。
故选B。
12. 构建化学基本观念是学好化学的基础,下列对化学基本观念的认识错误的是( )
A. 元素观:一氧化碳、二氧化碳都是由碳元素和氧元素组成的
B. 微粒观:保持石墨化学性质的最小微粒是碳原子
C. 转化观:二氧化碳在一定条件下可以转化为一氧化碳
D. 守恒观:9g氢气和9g氧气反应,一定生成18g水
【答案】D
【解析】A、一氧化碳、二氧化碳都是由碳元素和氧元素组成的,该选项说法正确;B、构成物质的微
粒就是保持物质化学性质的微粒,石墨是由碳原子构成的物质,保持石墨化学性质的最小微粒是碳原
子,该选项说法正确;C、二氧化碳在一定条件下可以转化为一氧化碳,例如高温条件下二氧化碳和碳
反应生成一氧化碳,该选项说法正确;D、氢气燃烧生成水,反应过程中氢气和氧气的质量比是1:8,
因此9g氢气和9g氧气不能恰好完全反应,生成水的质量小于18g,该选项说法不正确。故选D。
13. 元素化合价和物质类别是认识物质的两个重要维度。如图表示硫元素的化合价与含硫物质类别之间的关系,已知A点表示SO ,则下列说法错误的是
3
A. B点表示的物质在空气中燃烧产生淡蓝色火焰
B. C点表示的物质是大气污染物之一
C. D点表示的物质和硝酸钡在溶液中不能大量共存
D. E点表示的物质的化学式为NaSO
2 3
【答案】D
【解析】A、B点表示物质属于单质,故B点表示的物质为硫,硫在空气中燃烧,发出淡蓝色火焰,不
符合题意;B、C点表示物质属于氧化物,且硫元素的化合价为+4价,故C点表示二氧化硫,二氧化硫
会导致酸雨,属于空气污染物,不符合题意;C、D点表示物质属于酸,且硫元素的化合价为+6价,故
D点表示硫酸,硫酸能与硝酸钡反应生成硫酸钡沉淀和硝酸,不能大量共存,不符合题意;D、E点表
示物质属于盐,且硫元素的化合价为+6价,表示硫酸钠,化学式为:Na SO ,符合题意。故选D。
2 4
14. “证据推理与模型认知”是化学学科核心素养的重要组成部分。下列推理正确的是
A. CO和 的分子构成不同,则两种物质的化学性质不同
B. 铝的金属活动性比铁强,则铝制品比铁制品更容易受腐蚀
C. 阴离子带负电,所以带负电的粒子都是阴离子
D. 向某物质中加入稀盐酸产生气泡,则原物质一定含有
【答案】A
【解析】A、一氧化碳和二氧化碳的分子构成不同,由分子构成的物质,分子是保持其化学性质的最小
粒子,则它们的化学性质不同,该选项推理正确;B、虽然铝的金属活动性比铁强,由于铝在常温下能
和氧气反应生成一层致密的氧化铝薄膜,则铝比铁耐腐蚀,该选项推理不正确;C、阴离子带负电,电
子也带负电,则带负电的粒子不都是阴离子,该选项推理不正确;D、碳酸盐或碳酸氢盐和盐酸反应生
成二氧化碳气体,而活泼金属能和盐酸反应生成氢气,则向某物质中加入稀盐酸产生气泡,原物质不
一定含有碳酸根,该选项推理不正确。故选A。
15. 除去括号内杂质的操作方法正确的是A. N(O ) :放入木炭燃烧
2 2
B. CaO(CaCO ) :加稀盐酸
3
.
C CO(CO ) :通过灼热氧化铜
2
D.MnO (NaCl) :溶解,过滤,洗涤,干燥
2
【答案】D
【解析】A、除去N 中的氧气不能放入木炭燃烧,木炭燃烧会产生二氧化碳气体,会引入新的新杂质,
2
N(不能燃烧、不能支持燃烧)大量存在时,若氧气少量时,木炭是不会燃烧的;A错误,不符合题意;
2
B、CaO和CaCO )均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,B错
3
误,不符合题意;C、CO 能与灼热氧化铜反应生成铜和二氧化碳,反而会把原物质除去,不符合除杂
原则,C错误,不符合题意;D、氯化钠易溶于水,MnO 难溶于水,可采取加水溶解、过滤、洗涤、
2
干燥的方法进行分离除杂,D正确,符合题意。故选D。
二、填空与简答
16. 化学与生活息息相关。某兴趣小组的同学对厨房中的化学(柴-米-水-盐)进行调查后,得到了如下信
息:
(1)柴——厨房燃料的变迁:①上世纪60年代以前,我国城市家庭以煤为燃料,煤属于_______(填
“可再生”或“不可再生”)资源;②到70年代虽然仍以煤为主,但已将“蜂窝煤”取代了“煤球”,这样能
使煤充分燃烧,请用化学知识解释其原因:______;③到了80-90年代管道煤气又取代了“蜂窝煤”;
④今天,绿色上海世博会的亮点之一就是二氧化碳的零排放,衣食住行均与低碳密切相关,此时使用
的能源多为清洁能源,例如_______(请举1个例子)。
(2)米——分子料理中的米饭主要为我们提供的营养素是 (填序号)。
A. 蛋白质 B. 糖类 C. 无机盐 D. 维生素
(3)水——喝水的主要目的是解渴、补水,因此以白开水、矿泉水为宜,尽量少喝饮料。从物质分类
的角度,白开水属于______(填“纯净物”或“混合物”);从含有可溶性钙、镁离子量的多少,白开水属
于______(填“硬水”或“软水”)。
(4)盐——厨房里的两只调料瓶中都放有白色固体,只知道它们分别是精盐(NaCl)和碱面
(NaCO)中的某一种,可用厨房中的______将它们区分开来。调料瓶的盖子是由塑料加工而成的,
2 3
属于______材料(填“天然”或“合成”)。
【答案】(1) ①. 不可再生 ②. 增大与氧气的接触面积,使煤燃烧更充分 ③. 太阳能(合
理即可) (2)B (3) ①. 混合物 ②. 软水
(4) ①. 醋(合理即可) ②. 合成
【解析】(1)煤、石油、天然气属于三大化石能源,属于不可再生资源;将“蜂窝煤”取代了“煤球”是增大与氧气的接触面积,煤燃烧更加充分;清洁能源有:太阳能、风能、潮汐能、氢能、生物质能
等;故填:不可再生;增大与氧气的接触面积,使煤燃烧更加充分;太阳能(合理即可);(2)米主要
有糖类;故填:A;(3)白开水中含有水和无机盐;故属于混合物;故填:混合物;(4)厨房中含有
醋,醋中含有醋酸,氯化钠与醋酸不反应,碳酸钠与醋酸反应生成醋酸钠、水和二氧化碳;因此可用
醋酸区分;三大合成材料:合成纤维、合成橡胶、塑料;塑料属于合成材料;故填:醋;合成。
17. 食盐是人类生存的必需品,盐在自然界中无处不在。人们很早就发现,从海里,盐湖里、盐井里和盐
矿里,都能够开采出食盐。
(1)《汉代古火井碑序》记载:“诸葛丞相躬莅视察,改进技法,刳斑竹以导气(气指沼气),引井
火以煮盐”,请写出文中涉及到的化学反应的化学方程式:_________。
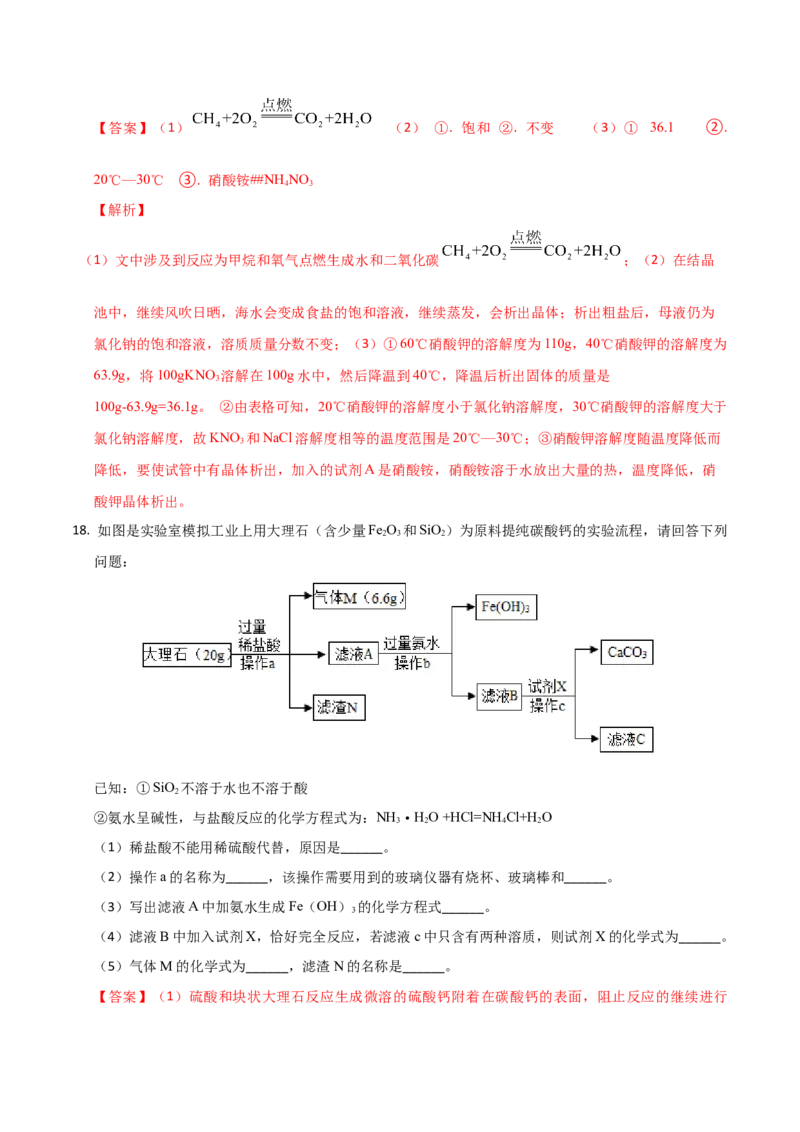
(2)通过晾晒海水可以得到粗盐和卤水,上图为海水提取粗盐的过程,在结晶池中,继续风吹日晒,
海水会变成食盐的_____溶液(填“饱和”或“不饱和”)。析出粗盐后,母液中氯化钠的溶质质量分数
____(填“变大”、“变小”或“不变”)。
(3)氯化钠和硝酸钾在不同温度下的溶解度如下表所示。请根据下表回答:
温度/℃ 20 30 40 50 60 70 80
NaCl 36.0 36.3 36.6 37.0 37.3 37.8 38.4
溶解度/g
KNO 31.6 45.5 63.9 85.5 110 138 169
3
①60℃将100gKNO 溶解在100g水中,然后降温到40℃,降温后析出固体的质量是________g。
3
②KNO 和NaCl溶解度相等的温度范围是________。
3
③如下图所示,要使试管中有晶体析出,加入的试剂A是__________。
A.生石灰 B.氢氧化钠 C.硝酸铵固体 D.氯化钠固体.
【答案】(1) (2) ①. 饱和 ②. 不变 (3)① 36.1 ②.
20℃—30℃ ③. 硝酸铵##NH NO
4 3
【解析】
(1)文中涉及到反应为甲烷和氧气点燃生成水和二氧化碳 ;(2)在结晶
池中,继续风吹日晒,海水会变成食盐的饱和溶液,继续蒸发,会析出晶体;析出粗盐后,母液仍为
氯化钠的饱和溶液,溶质质量分数不变;(3)①60℃硝酸钾的溶解度为110g,40℃硝酸钾的溶解度为
63.9g,将100gKNO 溶解在100g水中,然后降温到40℃,降温后析出固体的质量是
3
100g-63.9g=36.1g。 ②由表格可知,20℃硝酸钾的溶解度小于氯化钠溶解度,30℃硝酸钾的溶解度大于
氯化钠溶解度,故KNO 和NaCl溶解度相等的温度范围是20℃—30℃;③硝酸钾溶解度随温度降低而
3
降低,要使试管中有晶体析出,加入的试剂A是硝酸铵,硝酸铵溶于水放出大量的热,温度降低,硝
酸钾晶体析出。
18. 如图是实验室模拟工业上用大理石(含少量Fe O 和SiO)为原料提纯碳酸钙的实验流程,请回答下列
2 3 2
问题:
已知:①SiO 不溶于水也不溶于酸
2
②氨水呈碱性,与盐酸反应的化学方程式为:NH ·HO +HCl=NH Cl+H O
3 2 4 2
(1)稀盐酸不能用稀硫酸代替,原因是______。
(2)操作a的名称为______,该操作需要用到的玻璃仪器有烧杯、玻璃棒和______。
(3)写出滤液A中加氨水生成Fe(OH) 的化学方程式______。
3
(4)滤液B中加入试剂X,恰好完全反应,若滤液c中只含有两种溶质,则试剂X的化学式为______。
(5)气体M的化学式为______,滤渣N的名称是______。
【答案】(1)硫酸和块状大理石反应生成微溶的硫酸钙附着在碳酸钙的表面,阻止反应的继续进行(2) ①. 过滤 ②. 漏斗
(3) (4)(NH )CO (5) ①. CO ②. 二氧化硅
4 2 3 2
【解析】根据题干可知大理石中含有碳酸钙、氧化铁和二氧化硅,将20g大理石中加入过量稀盐酸后,
大理石中的碳酸钙能够与稀盐酸充分反应,产生二氧化碳、水和氯化钙,氧化铁与稀盐酸反应生成氯
化铁和水,大理石中的二氧化硅剩余,操作a能够将溶液中的不溶物和溶液分开,操作a应为过滤操作,
滤渣N的成分应为二氧化硅,滤液A中含有的溶质包括盐酸、氯化钙、氯化铁;滤液 A中加入过量氨
水后,氨水能够与盐酸反应生成氯化铵和水,氨水和氯化铁发生反应,生成氢氧化铁沉淀和氯化铵,
经过操作b,固体和液体分离,滤液B中的溶质包括氨水、氯化铵和氯化钙,滤液B中加入X,恰好完
全反应,X能够与氯化钙完全反应生成碳酸钙沉淀,若反应后滤液C中的溶质只有两种,可以判断X
与氯化钙反应生成的物质为碳酸钙和氯化氨,因此X应为碳酸铵,滤液C中的溶质为氨水和氯化铵。
(1)实验室制取二氧化碳时,若使用稀硫酸代替会生成硫酸钙微溶于水,包裹在大理石表面阻止反应
继续进行;(2)操作a将固体和液体分离,为过滤操作,需要用到的玻璃仪器为烧杯、玻璃棒和漏斗;
(3)根据分析可知,滤液A中的溶质为HCl、CaCl 和FeCl ,FeCl 能够与氨水反应生成氢氧化铁沉淀,
2 3 3
化学方程式为: ;(4)根据分析可知,滤液B 中含有的
溶质包括氨水、氯化钙和氯化铵,滤液B中加入试剂X,恰好完全反应,除去氯化钙后,若滤液c中只
含有两种溶质,试剂X应为碳酸铵,化学式为(NH )CO,完全反应后,溶液中只含氯化铵和氨水;
4 2 3
(5)大理石中的碳酸钙与稀盐酸反应产生二氧化碳,因此M的化学式为CO,大理石中的二氧化硅不
2
能与稀盐酸反应,因此滤渣N为二氧化硅;
三、实验与探究题(本大题包括2小题,每空1分,共16分)
19. 实验室利用如图所示装置进行相关实验,请回答问题:
(1)写出标有序号的仪器名称:①_______;②_______。
(2)实验室制取二氧化碳,可选择的装置组合是_______(填字母),写出该反应的化学方程式_______
(3)实验室利用装置AE制取氧气,写出该反应的化学方程式_______,用装置 E收集氧气,操作的正
确顺序是_______(填序号)。
①将导管伸入集气瓶口
②观察导管口气泡
③将装满水的集气瓶倒扣在水槽中
④当气体收集满时,用毛玻璃片盖上瓶口,将集气瓶移出水面放置
(4)图 F是某同学利用塑料瓶和其它用品设计的制取二氧化碳的发生装置,该设计与 B装置比较除了
废物利用的优点外,请另写一个优点_______。
【答案】(1) ①. 锥形瓶 ②. 长颈漏斗 (2)BC CaCO +2HCl=CaCl +CO +H O (3)
3 2 2 2
2KMnO K MnO +MnO +O ↑ ③②①④ (4) 控制反应的发生与停止
4 2 4 2 2
【解析】(1)仪器①的名称为:锥形瓶,仪器②的名称为:长颈漏斗;故填:锥形瓶;长颈漏斗;
(2)实验室石灰石或大理石与稀盐酸反应制取二氧化碳,属于固液常温型,选用的发生装置为B,二
氧化碳的密度比空气大,二氧化碳可溶于水,选用的收集装置为C;石灰石或大理石与稀盐酸反应,生
成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO +2HCl=CaCl +H O+CO ↑;故填:BC;
3 2 2 2
CaCO +2HCl=CaCl +H O+CO ↑;(3)装置适合于固固加热型,试管口放有棉花,是采用加热高锰酸钾制
3 2 2 2
取氧气,反应的化学方程式为:2KMnO K MnO +MnO +O ↑;用装置 E收集氧气,正确的顺序为:③
4 2 4 2 2
将装满水的集气瓶倒扣在水槽中;②观察导管口气泡;①将导管伸入集气瓶口;④当气体收集满时,
用毛玻璃片盖上瓶口,将集气瓶移出水面放置,故填:2KMnO K MnO +MnO +O ↑;③②①④;
4 2 4 2 2
(4)在F装置中,打开开关时,固液接触,反应发生,关闭开关时,瓶中的气体增多,压强增大,把
液体压入塑料瓶,固体和液体分离,反应停止,故装置F的优点是:能够控制反应的发生与停止。故填:
控制反应的发生与停止。
20. 某化学兴趣小组在整理实验室时发现失去标签的两瓶无色溶液,已知一瓶是稀盐酸或稀硫酸,另一瓶
是氢氧化钠溶液或氢氧化钙溶液。请你和同学们一起完成探究活动(每种方案或实验的1、2号试管中,都事先分别加入等量的上述两种无色溶液);
探究一:鉴别酸溶液与碱溶液
【设计实验】
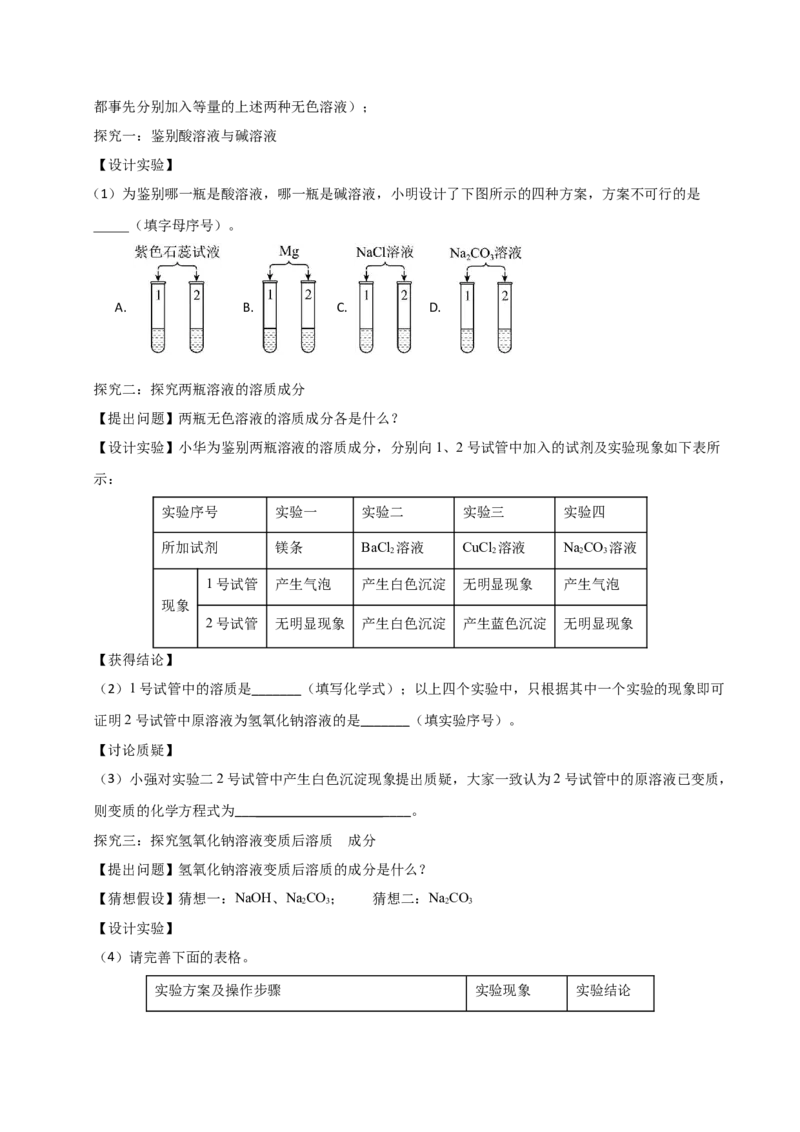
(1)为鉴别哪一瓶是酸溶液,哪一瓶是碱溶液,小明设计了下图所示的四种方案,方案不可行的是
_____(填字母序号)。
A. B. C. D.
探究二:探究两瓶溶液的溶质成分
【提出问题】两瓶无色溶液的溶质成分各是什么?
【设计实验】小华为鉴别两瓶溶液的溶质成分,分别向1、2号试管中加入的试剂及实验现象如下表所
示:
实验序号 实验一 实验二 实验三 实验四
所加试剂 镁条 BaCl 溶液 CuCl 溶液 NaCO 溶液
2 2 2 3
1号试管 产生气泡 产生白色沉淀 无明显现象 产生气泡
现象
2号试管 无明显现象 产生白色沉淀 产生蓝色沉淀 无明显现象
【获得结论】
(2)1号试管中的溶质是_______(填写化学式);以上四个实验中,只根据其中一个实验的现象即可
证明2号试管中原溶液为氢氧化钠溶液的是_______(填实验序号)。
【讨论质疑】
(3)小强对实验二2号试管中产生白色沉淀现象提出质疑,大家一致认为2号试管中的原溶液已变质,
则变质的化学方程式为___ ____。
探究三:探究氢氧化钠溶液变质后溶质 的成分
【提出问题】氢氧化钠溶液变质后溶质的成分是什么?
【猜想假设】猜想一:NaOH、NaCO; 猜想二:NaCO
2 3 2 3
【设计实验】
(4)请完善下面的表格。
实验方案及操作步骤 实验现象 实验结论步骤一:取瓶中变质后的氢氧化钠溶液少量于试
产生白色沉淀
管中,加入足量BaCl 溶液充分反应,过滤。
2
猜想一成立
步骤二:取步骤一中的滤液少量于试管中,向其
溶液变红色
中滴加_______。
【反思评价】
(5)小明认为可用Ba(OH) 溶液代替步骤一中的BaCl 溶液进行实验,大家一致认为此方案不可行,
2 2
理由是_______。
【答案】(1)C (2) ①. H SO ②. 实验四 (3)2NaOH+CO =Na CO +H O (4)2~3滴酚酞溶液
2 4 2 2 3 2
(5)Ba(OH) 溶液与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,由于生成了氢氧化钠,无法验证原溶
2
液中是否有氢氧化钠。
【解析】
(1)A、酸使紫色石蕊溶液变红,碱使紫色石蕊溶液变蓝。A方案可行,不符合题意;
B、镁和酸反应生成盐和氢气,和碱不反应。B方案可行,不符合题意;C、酸、碱与氯化钠溶液均不发
生反应,无法鉴别。C方案不可行,符合题意;D、酸与碳酸钠反应由二氧化碳生成,氢氧化钠与碳酸
钠不反应,氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠。所以D方案可行,不符合题意。综上
所述:选择C。
(2)根据实验一、1号试管与镁条反应生成氢气,则1号试管为酸,实验二,BaCl 溶液与硫酸反应生成
2
硫酸钡白色沉淀,所以1号试管中的溶液是硫酸溶液,1号试管中的溶质是硫酸,化学式H SO 。氢氧
2 4
化钠溶液与碳酸钠不反应,而盐酸、硫酸与碳酸钠反应生成二氧化碳气体,氢氧化钙和碳酸钠反应生
成碳酸钙沉淀,所以四个实验中,只根据其中一个实验的现象即可证明2号试管中原溶液为氢氧化钠溶
液的是实验四。
(3)氢氧化钠变质,即氢氧化钠与二氧化碳反应生成碳酸钠,化学方程式2NaOH+CO =Na CO +H O。变
2 2 3 2
质后的碳酸钠可以和氯化钡反应生成碳酸钡沉淀。
(4)变质后的氢氧化钠溶液中的碳酸钠,与氯化钡反应生成碳酸钙沉淀和氯化钠。余下的溶液中含有
氢氧化钠,滴加酚酞溶液,溶液变红。所以,步骤二:取步骤一中的滤液少量于试管中,向其中滴加2
~3滴酚酞溶液。(5)由于Ba(OH) 溶液与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,生成了氢氧化
2
钠,无法验证原溶液中是否有氢氧化钠。所以用Ba(OH) 溶液代替步骤一中的BaCl 溶液进行实验,
2 2
不可行。
四、计算题(本大题共1小题,共6分)
21. 2022年2月,中山市某工厂的锅炉发生爆炸,造成数人伤亡和重大经济损失。锅炉爆炸的一重要原因
是锅炉内有大量水垢(主要成分之一为碳酸钙)未及时清理。某同学取一定量的水垢放入烧杯中,逐滴加入120g的稀盐酸进行反应(水垢中的其他杂质不与稀盐酸反应,也不溶于稀盐酸),反应关系如
下图所示。请回答下列问题:
(1)在上图______点处反应恰好完全。
(2)产生 的总质量为______g。
(3)计算所加稀盐酸中溶质的质量分数(写出计算过程)。
【答案】21.(1) B (2) 8.8
(3) 设HCl的质量为x,则
x=14.6g
则所加稀盐酸中溶质的质量分数为
答:所加稀盐酸中溶质的质量分数为14.6%
【解析】
(1)由图可知,B点后加入的稀盐酸的质量和烧杯中物质增加的质量相同,则说明B点处反应恰好完全。
(2)根据反应前后物质的总质量不变,产生的二氧化碳的质量为22g+100g-113.2g=8.8g。(3)见答案。