文档内容
2024 年中考第二次模拟考试(上海卷)
化 学
(考试时间:40分钟 试卷满分:50分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号填
写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Ag 108 Cl 35.5 Na 23
第 I 卷(选择题 共 20 分)
一、选择题:(共20分)
本题共20个小题,21-34题,每小题1分,在每小题给出的四个选项中,只有一项是符合题目要求的。35-37
题,每小题2分,每题有一个或两个选项符合题意.
21.发生化学变化的是
A.玻璃破碎 B.盐酸挥发 C.铁钉生锈 D.冰雪融化
22.属于有机物的是
A. CO B. CH C. KCO D. NaHCO
2 4 2 3 3
23..A、B、C、D表示四种物质,其微观示意图如下所示,表示单质的是
A. B. C. D.
24.有关铁丝燃烧现象描述不正确的是
A.火星四射 B.发出耀眼白光 C.放出热量 D.生成黑色固体
25.化学方程式书写正确的是
A.2HO 2H↑+O ↑ B.2Fe+6HCl=2FeCl +3H
2 2 2 3 2C.2NaOH+SO =Na SO +H O D.C+CuO Cu+CO ↑
2 2 3 2 2
26.下列各组中物质的俗称、学名与化学式表示同一种物质的是
A.氯化氢 盐酸 HCl
B.苛性钠 氢氧化钠 NaOH
C.胆矾 硫酸铜 CuSO4·5H O
2
D.苏打 碳酸氢钠 NaCO
2 3
27.关于水的说法正确的是
A.水蒸气可以用胆矾来检验 B.水的反常膨胀跟水分子之间的缔合有关
C.电解水实验证明水是由氢气和氧气组成的 D.自来水生产中通入氯气的作用是吸附微生物
28.属于复合肥的是
A.Ca (PO ) B.CO(NH) C.KNO D.KCl
2 3 2 2 2 3
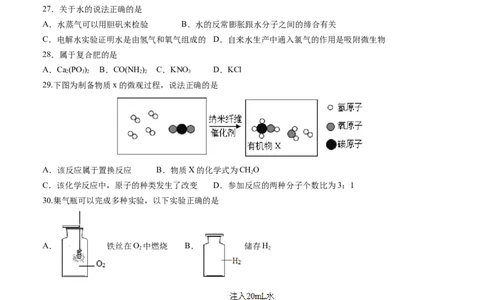
29.下图为制备物质x的微观过程,说法正确的是
A.该反应属于置换反应 B.物质X的化学式为CHO
2
C.该化学反应中,原子的种类发生了改变 D.参加反应的两种分子个数比为3:1
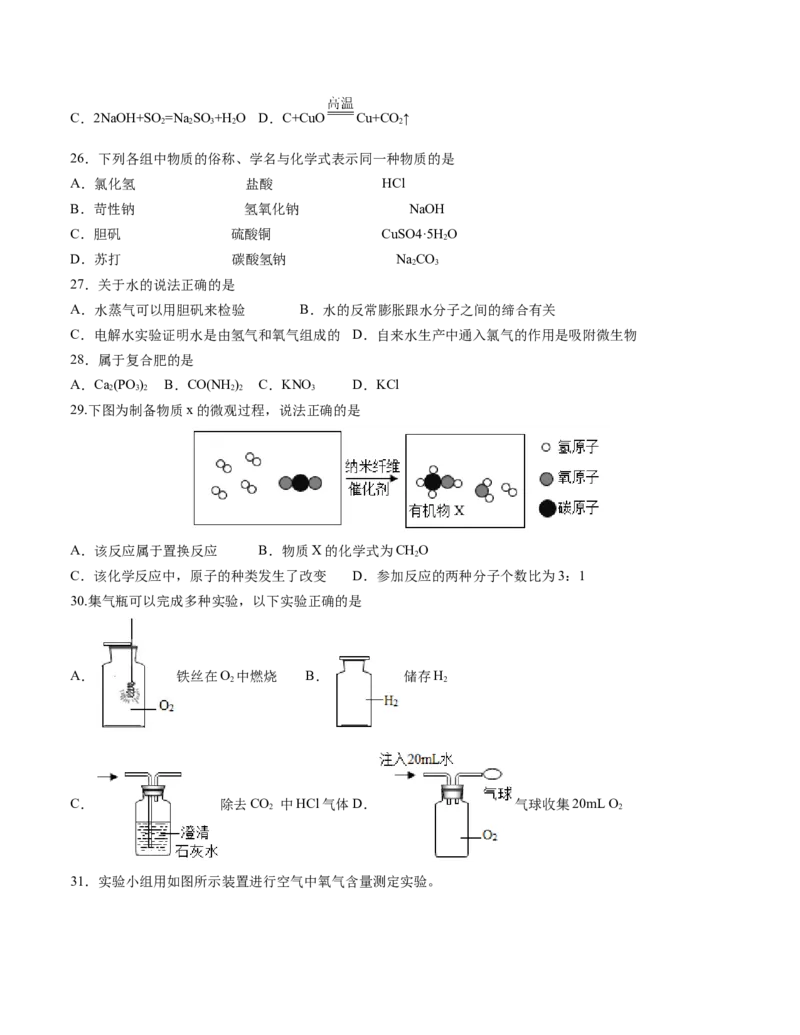
30.集气瓶可以完成多种实验,以下实验正确的是
A. 铁丝在O 中燃烧 B. 储存H
2 2
C. 除去CO 中HCl气体D. 气球收集20mL O
2 2
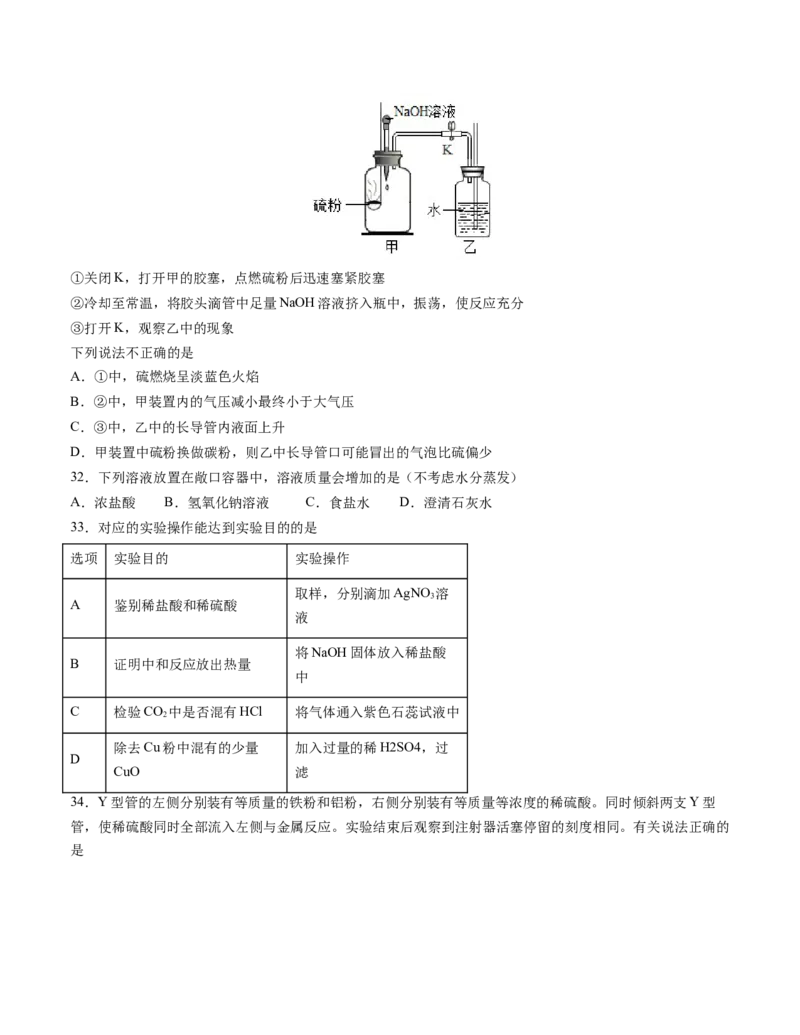
31.实验小组用如图所示装置进行空气中氧气含量测定实验。①关闭K,打开甲的胶塞,点燃硫粉后迅速塞紧胶塞
②冷却至常温,将胶头滴管中足量NaOH溶液挤入瓶中,振荡,使反应充分
③打开K,观察乙中的现象
下列说法不正确的是
A.①中,硫燃烧呈淡蓝色火焰
B.②中,甲装置内的气压减小最终小于大气压
C.③中,乙中的长导管内液面上升
D.甲装置中硫粉换做碳粉,则乙中长导管口可能冒出的气泡比硫偏少
32.下列溶液放置在敞口容器中,溶液质量会增加的是(不考虑水分蒸发)
A.浓盐酸 B.氢氧化钠溶液 C.食盐水 D.澄清石灰水
33.对应的实验操作能达到实验目的的是
选项 实验目的 实验操作
取样,分别滴加AgNO 溶
3
A 鉴别稀盐酸和稀硫酸
液
将NaOH固体放入稀盐酸
B 证明中和反应放出热量
中
C 检验CO 中是否混有HCl 将气体通入紫色石蕊试液中
2
除去Cu粉中混有的少量 加入过量的稀H2SO4,过
D
CuO 滤
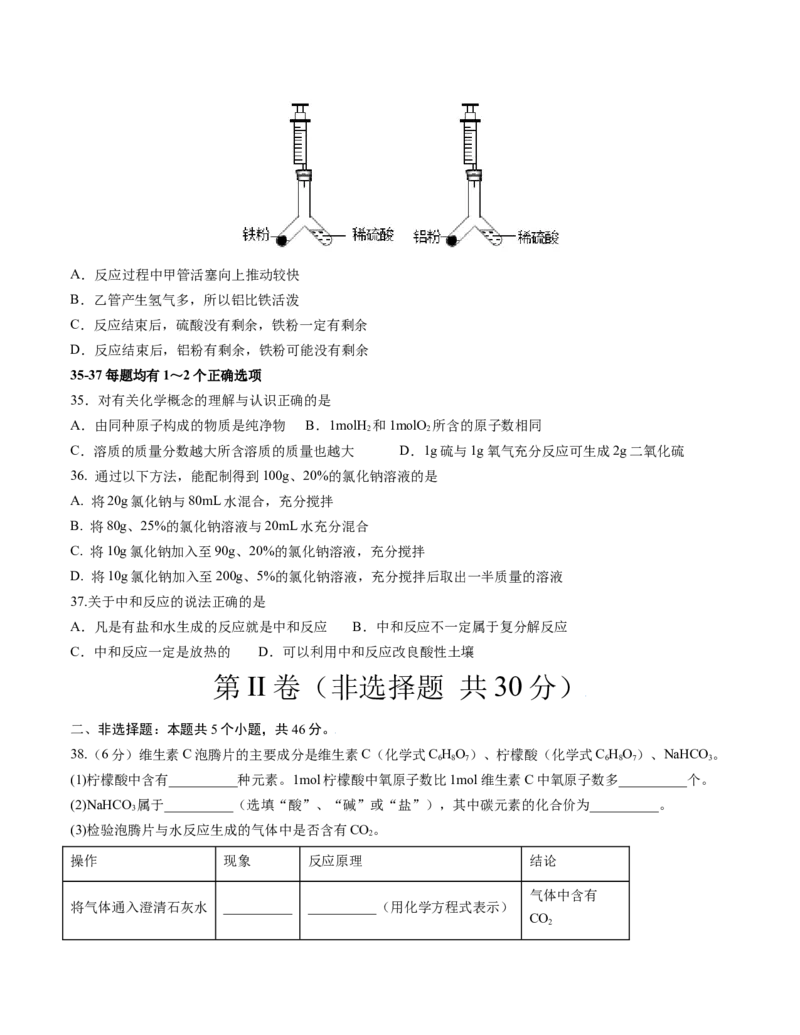
34.Y型管的左侧分别装有等质量的铁粉和铝粉,右侧分别装有等质量等浓度的稀硫酸。同时倾斜两支Y型
管,使稀硫酸同时全部流入左侧与金属反应。实验结束后观察到注射器活塞停留的刻度相同。有关说法正确的
是A.反应过程中甲管活塞向上推动较快
B.乙管产生氢气多,所以铝比铁活泼
C.反应结束后,硫酸没有剩余,铁粉一定有剩余
D.反应结束后,铝粉有剩余,铁粉可能没有剩余
35-37每题均有1~2个正确选项
35.对有关化学概念的理解与认识正确的是
A.由同种原子构成的物质是纯净物 B.1molH 和1molO 所含的原子数相同
2 2
C.溶质的质量分数越大所含溶质的质量也越大 D.1g硫与1g氧气充分反应可生成2g二氧化硫
36. 通过以下方法,能配制得到100g、20%的氯化钠溶液的是
A. 将20g氯化钠与80mL水混合,充分搅拌
B. 将80g、25%的氯化钠溶液与20mL水充分混合
C. 将10g氯化钠加入至90g、20%的氯化钠溶液,充分搅拌
D. 将10g氯化钠加入至200g、5%的氯化钠溶液,充分搅拌后取出一半质量的溶液
37.关于中和反应的说法正确的是
A.凡是有盐和水生成的反应就是中和反应 B.中和反应不一定属于复分解反应
C.中和反应一定是放热的 D.可以利用中和反应改良酸性土壤
第 II 卷(非选择题 共 30 分)
二、非选择题:本题共5个小题,共46分。
38.(6分)维生素C泡腾片的主要成分是维生素C(化学式C HO)、柠檬酸(化学式C HO)、NaHCO 。
6 8 7 6 8 7 3
(1)柠檬酸中含有__________种元素。1mol柠檬酸中氧原子数比1mol维生素C中氧原子数多__________个。
(2)NaHCO 属于__________(选填“酸”、“碱”或“盐”),其中碳元素的化合价为__________。
3
(3)检验泡腾片与水反应生成的气体中是否含有CO。
2
操作 现象 反应原理 结论
气体中含有
将气体通入澄清石灰水 __________ __________(用化学方程式表示)
CO
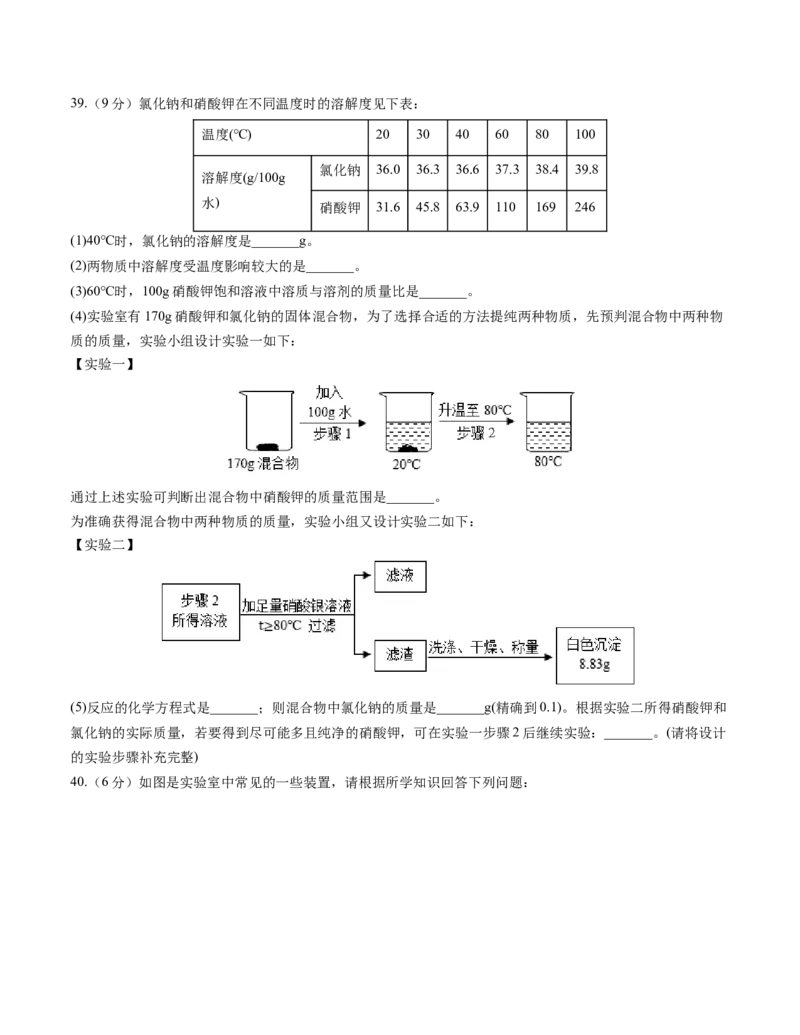
239.(9分)氯化钠和硝酸钾在不同温度时的溶解度见下表:
温度(℃) 20 30 40 60 80 100
氯化钠 36.0 36.3 36.6 37.3 38.4 39.8
溶解度(g/100g
水)
硝酸钾 31.6 45.8 63.9 110 169 246
(1)40℃时,氯化钠的溶解度是_______g。
(2)两物质中溶解度受温度影响较大的是_______。
(3)60℃时,100g硝酸钾饱和溶液中溶质与溶剂的质量比是_______。
(4)实验室有170g硝酸钾和氯化钠的固体混合物,为了选择合适的方法提纯两种物质,先预判混合物中两种物
质的质量,实验小组设计实验一如下:
【实验一】
通过上述实验可判断出混合物中硝酸钾的质量范围是_______。
为准确获得混合物中两种物质的质量,实验小组又设计实验二如下:
【实验二】
(5)反应的化学方程式是_______;则混合物中氯化钠的质量是_______g(精确到0.1)。根据实验二所得硝酸钾和
氯化钠的实际质量,若要得到尽可能多且纯净的硝酸钾,可在实验一步骤2后继续实验:_______。(请将设计
的实验步骤补充完整)
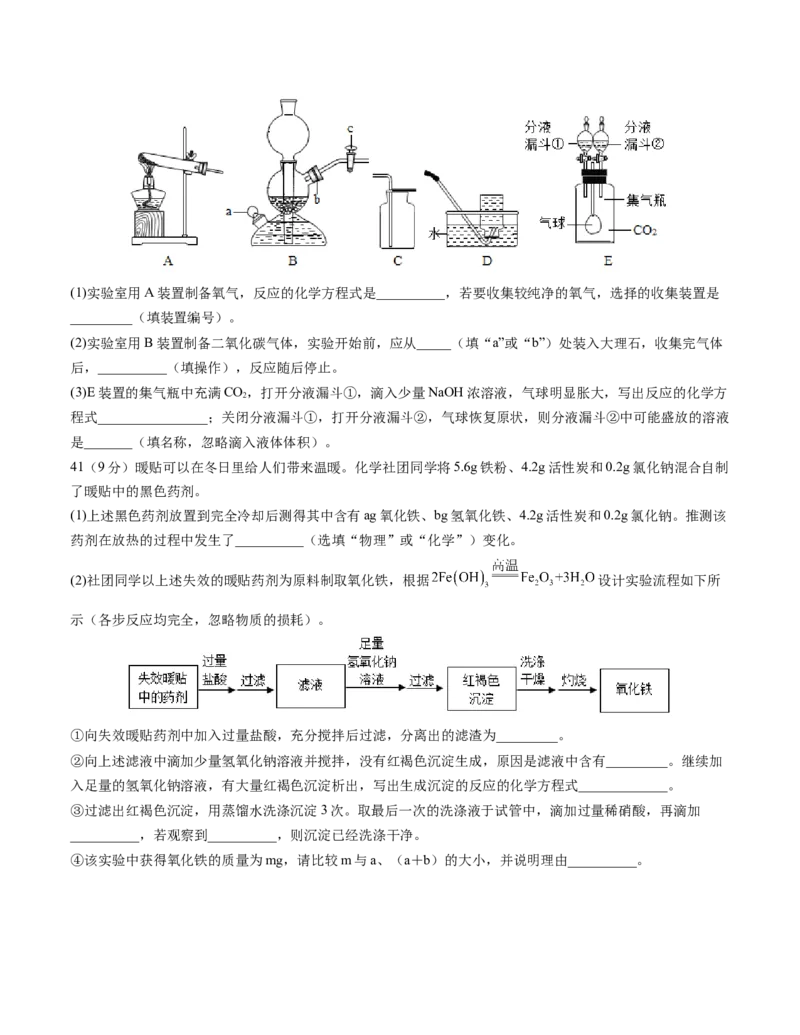
40.(6分)如图是实验室中常见的一些装置,请根据所学知识回答下列问题:(1)实验室用A装置制备氧气,反应的化学方程式是__________,若要收集较纯净的氧气,选择的收集装置是
_________(填装置编号)。
(2)实验室用B装置制备二氧化碳气体,实验开始前,应从_____(填“a”或“b”)处装入大理石,收集完气体
后,__________(填操作),反应随后停止。
(3)E装置的集气瓶中充满CO,打开分液漏斗①,滴入少量NaOH浓溶液,气球明显胀大,写出反应的化学方
2
程式________________;关闭分液漏斗①,打开分液漏斗②,气球恢复原状,则分液漏斗②中可能盛放的溶液
是_______(填名称,忽略滴入液体体积)。
41(9分)暖贴可以在冬日里给人们带来温暖。化学社团同学将5.6g铁粉、4.2g活性炭和0.2g氯化钠混合自制
了暖贴中的黑色药剂。
(1)上述黑色药剂放置到完全冷却后测得其中含有ag氧化铁、bg氢氧化铁、4.2g活性炭和0.2g氯化钠。推测该
药剂在放热的过程中发生了__________(选填“物理”或“化学”)变化。
(2)社团同学以上述失效的暖贴药剂为原料制取氧化铁,根据 设计实验流程如下所
示(各步反应均完全,忽略物质的损耗)。
①向失效暖贴药剂中加入过量盐酸,充分搅拌后过滤,分离出的滤渣为_________。
②向上述滤液中滴加少量氢氧化钠溶液并搅拌,没有红褐色沉淀生成,原因是滤液中含有_________。继续加
入足量的氢氧化钠溶液,有大量红褐色沉淀析出,写出生成沉淀的反应的化学方程式_____________。
③过滤出红褐色沉淀,用蒸馏水洗涤沉淀3次。取最后一次的洗涤液于试管中,滴加过量稀硝酸,再滴加
__________,若观察到__________,则沉淀已经洗涤干净。
④该实验中获得氧化铁的质量为mg,请比较m与a、(a+b)的大小,并说明理由__________。