文档内容
2024 年中考第二次模拟考试(海南卷)
化 学
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Si-28 S-32
一、选择题:每小题只有一个选项符合题意,每小题3分,共42分。
1.大米为我们提供的营养素主要是( )
A.油脂 B.无机盐
C.糖类 D.蛋白质
【答案】C
【解析】大米中含有较多淀粉,淀粉属于糖类。故选:C。
2.下列变化前者是物理变化,后者是化学变化的是( )
A.煤的燃烧 B.雕刻石像
C.丝绸制衣 D.工业制氧
【答案】A
【解析】A、煤燃烧过程中有二氧化碳等新物质生成,属于化学变化;
B、雕刻石像过程中没有新物质的生成,属于物理变化;
C、丝绸制衣过程中没有新物质的生成,属于物理变化;
D、工业制氧,是利用氧气与其它气体的沸点不一样,通过控制温度将氧气从液态空气中分离出来,过程
中没有新物质生成,属于物理变化;
故选A。
3.下列化学用语表述正确的是( )
A.2H: 2个氢元素
B. : 水中氢元素的化合价为+1 价
C.FeSO : 硫酸铁
4
D.Zn+2: 带两个单位正电荷的锌离子
【答案】B
【解析】A、2H: 2个氢原子;故选项错误;
B、 : 水中氢元素的化合价为+1 价;故选项正确;C、FeSO : 硫酸亚铁;故选项错误;
4
D、Zn2+: 带两个单位正电荷的锌离子;故选项错误;
故选:B。
4.下列是配制一定溶质质量分数的氢氧化钠溶液的部分操作,其中正确的是( )
A. 称量NaOH固体 B. 读取液体体积
C. 溶解 D. 装瓶
【答案】C
【解析】A、氢氧化钠有腐蚀性,称量时要将氢氧化钠放在玻璃器皿中,故选项A错误;
B、读取量筒内液体的体积时,视线应与凹液面的最低处保持水平,故选项B错误;
C、溶解固体时应使用玻璃棒搅拌,故选项C正确;
D、液体试剂要用细口瓶盛放,故选项D错误;
故选:C。
5.下列化肥中,从外观即可与其他化肥相区别的是( )
A.硫酸钾 B.过磷酸钙
C.硝酸铵 D.氯化钾
【答案】B
【解析】氮肥和钾肥是白色晶体,磷肥是灰白色的;A硫酸钾、D氯化钾属于钾肥、C硝酸铵属于氮肥,
都是白色晶体,B过磷酸钙属于磷肥,是灰白色粉末。故从外观即可与其他化肥区别的是B。
故选B。
6.下列排序正确的是( )
A.溶液的pH:
B.金属的熔点:
C.地壳中元素的含量:
D.空气中气体的含量:
【答案】C
【解析】A、洗洁精显碱性,pH>7;苹果法显酸性,pH<7;食盐水显中性,pH=7,故A错误;
B、汞常温下为液体,熔点最低,故B错误;
C、地壳中元素含量由高到低是:O、Si、Al、Fe,故C正确;D、空气中氮气约占78%,氧气约占21%,二氧化碳约占0.03%,故D错误。
故选C。
7.下列有关空气及其成分说法正确的是( )
A.铁丝在空气中剧烈燃烧,生成黑色固体
B.CO 是空气污染物之一,是因为会引起温室效应
2
C.酸雨的pH<5.6
D.空气中的氮气可以用做保护气,因为它的化学性质不稳定
【答案】C
【解析】A、铁丝在空气中不能燃烧,错误;
B、二氧化碳是空气的成分之一,空气污染物不包括二氧化碳,错误;
C、酸雨的pH<5.6,正确;
D、氮气的化学性质稳定,可做保护气,错误。
故选C。
8.金、铜、银按一定比例制成合金,具有柔和的粉红玫瑰色彩,被称为“玫瑰金”,广泛用于首饰设计
和加工。下列叙述不正确的是( )
A.“玫瑰金”的硬度比金、铜、银大 B.“玫瑰金”是一种混合物
C.“玫瑰金”的熔点比金、铜、银高 D.“玫瑰金”属于金属材料
【答案】C
【解析】A、“玫瑰金”为金、铜、银的合金,合金的硬度比纯金属大,该选项叙述正确;
B、“玫瑰金”中含有多种物质,属于混合物,该选项叙述正确;
C、合金的熔点比组成的纯金属的熔点低,该选项叙述不正确;
D、合金属于金属材料,该选项叙述正确。
故选C。
9.化学与我们的生产、生活息息相关。下列说法正确的是( )
A.遇到室内起火,迅速打开门窗通风
B.甲醛有防腐作用,可用于浸泡食材
C.为节约粮食,霉变大米蒸煮后食用
D.为了预防缺碘性疾病,可食用适量海带
【答案】D
【解析】A、遇到室内起火,迅速打开门窗通风,会进入更多氧气,使火燃烧更旺,A选项错误;
B、甲醛有防腐作用,但甲醛能破坏人体内的蛋白质结构,所以甲醛不能用于浸泡食材,B选项错误;
C、霉变大米有毒,不能食用,C选项错误;
D、海带中含有碘元素,为了预防缺碘性疾病,可食用适量海带,D选项正确。
故选:D。
10.下列说法错误的是( )
A.(NH )SO 肥料不能与碱性物质混用,以免肥效降低
4 2 4B.风把蜡烛火焰吹灭了,是因为蜡烛的着火点降低了
C.过度使用化肥会造成土壤酸化,可用熟石灰改良
D.放学回到家中,还未进入厨房就闻到了妈妈炒菜的香味,说明分子在不断运动
【答案】B
【解析】A、铵态氮肥与碱性肥料混用能产生氨气,降低肥效,故A说法正确,不符合题意;
B、风把蜡烛火焰吹灭了,是因为降低温度到蜡烛的着火点以下,故B说法错误,符合题意;
C、过度使用化肥会造成土壤酸化,可用熟石灰改良酸性土壤,故C说法正确,不符合题意;
D、放学回到家中,还未进入厨房就闻到了妈妈炒菜的香味,说明分子在不断运动,故D说法正确,不符
合题意。
故选:B。
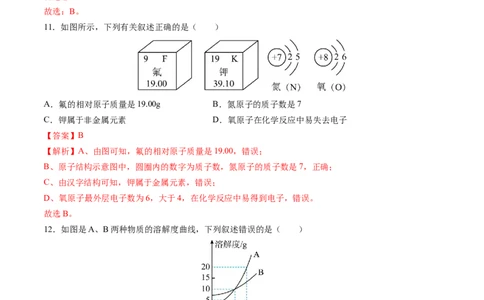
11.如图所示,下列有关叙述正确的是( )
A.氟的相对原子质量是19.00g B.氮原子的质子数是7
C.钾属于非金属元素 D.氧原子在化学反应中易失去电子
【答案】B
【解析】A、由图可知,氟的相对原子质量是19.00,错误;
B、原子结构示意图中,圆圈内的数字为质子数,氮原子的质子数是7,正确;
C、由汉字结构可知,钾属于金属元素,错误;
D、氧原子最外层电子数为6,大于4,在化学反应中易得到电子,错误。
故选B。
12.如图是A、B两种物质的溶解度曲线,下列叙述错误的是( )
A.A物质的溶解度大于B物质的溶解度
B.A物质的饱和溶液从30℃降温到20℃,其溶质质量分数减小
C.30℃时,向100克水中加入25克A物质,充分溶解后所得的溶液是饱和溶液
D.30℃时,将B物质的不饱和溶液转变为饱和溶液,可用恒温蒸发溶剂的方法
【答案】A
【解析】A、A物质的溶解度大于B物质的溶解度错误,因为没有指明温度;故选项错误;
B、A物质的饱和溶液从30℃降温到20℃,其溶质质量分数变小,故选正确;C、30℃时,A物质的溶解度为20g,25g固体不能完全溶解,得到的溶液是饱和溶液,故正确;
D、30℃时,将B物质的不饱和溶液转变为饱和溶液,可用恒温蒸发溶剂的方法、加溶质的方法等;故正
确;
故选A。
13.下列实验不能达到实验目的是( )
实
验
实
验 A.验证生石灰与水反 B.探究 能否加快 C.证明呼出气体中 D.测定空气中 的
目 应放出热量 的分解 含量比空气中多 含量
的
【答案】B
【解析】A、氧化钙和水反应放热,大试管内压强会增大,使得墨水的液面发生变化,所以可用此装置验
证生石灰与水反应放热,故选项实验能达到实验目的;
B、根据对比实验的要求,两组实验所用的过氧化氢溶液的浓度不一样,无法完成实验,故选项实验不能
达到实验目的;
C、通过观察澄清石灰水变浑浊的程度可以判断两种气体中二氧化碳含量的高低,故选项实验能达到实验
目的;
D、红磷本身是固体,能在空气中燃烧,生成五氧化二磷固体,没有生成新的气体,可用于测定空气中氧
气的含量,故选项实验能达到实验目的。
故选B。
14.如图的反应中,甲、乙、丙三种分子的个数比为1:3:2,则从图示中获得的信息正确的是( )
A.甲物质是由原子构成的
B.原子种类在化学反应中发生了变化
C.该反应不可能是分解反应
D.乙分子中A与B的原子个数比为1:2
【答案】C
【解析】由题中信息知,A. 甲物质分子是由原子构成的。故A错误。B. 原子种类,数目,性质在化学反应
中都不会发生变化。故B错误。C. 该反应不可能是分解反应,是化合反应。故C正确。D. 根据质量守恒定律,乙分子中不可能含有A.原子。故D错误。
二、填空题(每空2分,共28分)
15.(8分)生活中处处有化学。现有以下常见的物质:
A.生石灰 B.活性炭 C.一氧化碳 D.石墨 E.石灰石;
请按要求填空(填字母编号)。
(1)煤气的主要成分,能使人中毒的是 ;
(2)常用于冰箱除臭的 ;
(3)用作电池电极的是 ;
(4)用作某些食品防止受潮的干燥剂的是 。
【答案】(1)C;(2)B;(3)D;(4)A
【解析】(1)煤气的主要成分是一氧化碳,一氧化碳有毒,极易与血液中的血红蛋白结合,从而使血红
蛋白不能再与氧气结合,造成生物体缺氧,故填:C;
(2)活性炭结构疏松多孔,具有吸附性,可用于冰箱除臭,故填:B;
(3)石墨具有良好的导电性,可用作电池电极,故填:D;
(4)生石灰是氧化钙的俗称,氧化钙和水反应生成氢氧化钙,可用作食品干燥剂,故填:A。
16.(8分)积极参加家庭劳动,提升生活技能,感受到化学与生活息息相关。请回答下列问题。
(1)小明洗衬衣时,为确定洗涤方式,仔细观察了衣服的标签(如图所示)。面料成分中属于合成材料
的是 ;
(2)小明闻到冰箱内有异味,放入活性炭包除味,这是利用活性炭的 性;
(3)小明准备为家人做一顿丰盛的午餐:米饭、清蒸鱼、红烧排骨。从营养均衡的角度分析,为补充该
营养素,建议增加______(选填字母序号)
A.炒青菜 B.酱牛肉 C.煮鸡蛋
(4)洗碗时,加入洗洁精除去油污,这是利用了洗洁精的 作用。
【答案】(1)涤纶
(2)吸附
(3)A
(4)乳化
【解析】(1)面料中棉属于天然材料,涤纶属于合成材料;
(2)小明闻到冰箱内有异味,放入活性炭包除味,这是利用活性炭的吸附性;
(3)米饭中富含糖类、清蒸鱼中富含蛋白质和油脂、红烧排骨中富含蛋白质和油脂等,则该午餐中还缺
少维生素,炒青菜中富含维生素,酱牛肉中富含油脂和蛋白质,煮鸡蛋中富含蛋白质,为补充维生素,建
议增加炒青菜;故:A。
(4)洗碗时,加入洗洁精除去油污,这是利用了洗洁精的乳化作用。
17.(4分)将锌粉和铁粉的混合物加入盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤渣和
滤液。
(1)写出一定发生反应的化学方程式 。
(2)向滤渣中加入稀盐酸,有气泡冒出,试分析滤渣的成分 。
【答案】(1)
(2)滤渣中一定含有Fe和Ag,可能含有Zn
【解析】锌、铁、银三种金属的活动性顺序为锌>铁>银,将锌粉和铁粉的混合物加入盛有一定量硝酸银
溶液的烧杯中,锌优先与硝酸银反应生成硝酸锌和银,若锌反应完,硝酸银有剩余,铁粉再与硝酸银反应
生成硝酸亚铁和银;(1)由分析可知,一定发生反应是锌与硝酸银反应生成硝酸锌和银,反应的化学方
程式为 ,故填: ;
(2)向滤渣中加入稀盐酸,有气泡冒出,说明滤渣中一定含有能与稀盐酸反应的铁,可能含有锌,滤渣
里还一定含有生成的银,故填:滤渣中一定含有Fe和Ag,可能含有Zn。
18.(8分)消毒与清洁对公共场所和家庭是至关重要的。
(1)二氧化氯(ClO )可作水处理消毒剂,二氧化氯中氯元素的化合价为 。
2
(2)“洁厕灵”与“漂白剂”不能混用,二者若混合易产生一种有毒气体X,反应原理为:
,则X的化学式为 。
(3)使用洗涤剂清洗餐具上的油污时,利用了洗涤剂对油污的 作用;
(4)用炉具清洁剂(含有NaOH)清洗炉具时,应避免接触皮肤,其原因是 。
【答案】(1)+4
(2)Cl
2
(3)乳化
(4)氢氧化钠具有强腐蚀性
【解析】(1)二氧化氯(ClO )中,氧元素的化合价为-2价,设氯元素的化合价为x,根据“化合物中各元
2
素化合价代数和为零”,则x+(-2)×2=0,解得x=+4。
(2)反应前后原子的种类和个数不变,等号左边有1个钠原子、3个氯原子、2个氢原子和1个氧原子,
等号右边除X,有1个钠原子、1个氯原子、2个氢原子和1个氧原子,还少2个氯原子,则X为Cl。
2
(3)洗涤剂具有乳化作用,可除去餐具上的油污。
(4)氢氧化钠具有强腐蚀性,则应避免接触皮肤。
三、简答题(共10分)
19.(4分)随着人类对能源的需求日益增长,开发和利用新能源成为越来越迫切的需求。请回答:
(1)目前,我国的一些地区正在使用乙醇汽油(在汽油中加入适量乙醇)作为汽车燃料,这样做的优点是什
么?
(2)为缓解全球性能源危机,人们正积极开发利用新能源,请列举出一种新能源。
【答案】(1)可适当节省石油资源(2)太阳能(合理即可)
【解析】(1)在汽油中加入适量乙醇,能节约石油资源,且乙醇燃烧不产生有害气体,从而能减少汽车
尾气的污染。
(2)新能源有太阳能、地热能、潮汐能、氢能等。
20.(6分)溶液在生产和科研中具有广泛的用途,与人们的生活密不可分。请用所学知识回答下列问题:
(1)喝了冰镇的汽水以后,常常会打嗝,其原因是什么?
(2)常温下,一瓶合格的氯化钠注射液密封放置一段时间后,是否会出现浑浊现象?为什么?
(3)为什么各盐场从海水制取氯化钠时往往采用风吹日晒的方法?
【答案】(1)汽水温度升高,溶解度减小,则气体会逸出。
(2)不会出现浑浊现象,因为溶液具有均一性。
(3)氯化钠的溶解度受温度影响比较小。
四、实验题(共12分)
21.(6分)化学是一门以实验为基础的科学。请根据下列实验装置完成相关问题。
(1)写出仪器a的名称 ;
(2)写出利用A装置加热固体混合物制取氧气的化学方程式 ;
(3)制取二氧化碳时,要获得平稳气流,最佳发生装置是 (填装置序号)。
【答案】(1)铁架台
(2)
(3)B
【解析】(1)仪器a是铁架台;
(2)A装置为固体加热型装置,试管口没有棉花,应用氯酸钾制氧气,氯酸钾在二氧化锰的作用下加热生
成氯化钾和氧气,化学方程式为: ;
(3)制取二氧化碳时,要获得平稳气流,最佳发生装置是B,B中用分液漏斗可以控制滴加液体的速率,
从而控制反应速率。
22.(6分)某校化学社团采用图1装置将注射器中等质量等浓度的氢氧化钠溶液分别注入用排水法和排
空气法收集的CO 的锥形瓶内(氢氧化钠溶液均过量)得到所示的压强随时间变化的曲线图。
2(1)用化学方程式说明锥形瓶内压强发生变化的原因 。
(2)结合图2判断哪种方法收集到的CO 含量高并解释原因 。
2
(3)设计实验证明,反应进行到300s时锥形瓶内溶液中溶质的成分(写出实验操作、现象、结论)
。
【答案】 排水法收集到的CO 含量高,因为排水法收集的CO 与
2 2
足量NaOH溶液反应,压强变化大 取300s时溶液少量,滴加过量的氯化钙溶液,产生白色沉淀静置
后取上层清液,滴加无色酚酞试液,溶液变红,说明溶质成分是NaOH和NaCO
2 3
【解析】(1)随着氢氧化钠溶液的加入,氢氧化钠与二氧化碳反应生成碳酸钠和水,瓶中的二氧化碳越
来越少,瓶中的压强逐渐降低,故反应的化学方程式写为:2NaOH+CO =Na CO+H O。
2 2 3 2
(2)由图可知,排水法收集的CO 与足量NaOH溶液反应后瓶中的压强差较大,说明排水法收集的二氧
2
化碳的含量较高,故填排水法收集到的CO 含量高,因为排水法收集的CO 与足量NaOH溶液反应,压强
2 2
变化大。
(3)由题文可知,反应后氢氧化钠溶液均过量,由图可知,300s时反应均已完成,则锥形瓶内溶液中溶
质的成分是生成的碳酸钠和过量的氢氧化钠,检验方法是取300s时溶液少量,滴加过量的氯化钙溶液,产
生白色沉淀,静置后取上层清液,滴加无色酚酞试液,溶液变红,说明溶质成分是NaOH和NaCO,故填
2 3
取300s时溶液少量,滴加过量的氯化钙溶液,产生白色沉淀,静置后取上层清液,滴加无色酚酞试液,溶
液变红,说明溶质成分是NaOH和NaCO。
2 3
五、计算题(共8分)
23.(8分)“中国天眼”是世界上口径最大的单天线射电望远镜,其“眼镜片”由金刚砂(SiC)制造。
生产SiC的化学方程式为SiO+3C SiC+2CO↑。
2
(1)SiO 中Si元素的化合价为 。
2
(2)生产160kg 的SiC,理论上消耗C的质量为多少?
【答案】(1)+4
(2)解:设生产160kg 的SiC,理论上消耗C的质量为xx=144kg
答:生产160kg 的SiC,理论上消耗C的质量为144kg。