文档内容
第五讲 有关溶质的质量分数的计算
模块一 溶液稀释的计算
知识精讲
知识点一 溶液稀释的计算
1.稀释
(1)计算依据:溶液稀释前后,溶质的质量不变。
(2)若设浓溶液质量为A g,溶质的质量分数为a%,加水稀释成溶质的质量分数为 b%的稀溶液B g,
则
A g×a%=Bg×b%(其中B=A+m )
水
【练1】把100 g质量分数为98%的浓硫酸稀释成10%的稀硫酸,需要水的质量( )
A.800 g B.880 g C.980 g D.98 g
【答案】B
【练2】双氧水(HO )既是工业上的重要的绿色氧化剂,又是常用的医药消毒剂。小明从试剂商店购得
2 2
一瓶质量分数为30%的双氧水,用于制取氧气。若要配制5%的双氧水600g,需要30%的双氧水的质量为
___________。 100g 500ml
【答案】100g;
2.浓缩
1、向原溶液中添加溶质
(1)计算依据:溶液增加溶质前后,溶剂的质量不变。
(2)增加溶质后,溶液中溶质的质量=原溶液中溶质的质量+增加的溶质的质量,而溶液的质量=原溶
液的质量+增加的溶质的质量。
若设原溶液质量为A g,溶质的质量分数为a%,加溶质Bg后变成溶质的质量分数为b%的溶液,则
Ag×a%+Bg=(A g+Bg)×b%。
【练1】有含盐8%的盐水40千克,要配制成含盐20%的盐水,须加盐多少千克? 6千克【答案】6
【解析】40 8%+x=(40+x) 20%,x=6kg。
× ×
2、将原溶液蒸发掉部分溶剂
(1)溶液蒸发溶剂前后,溶质的质量不变。
(2)若设原溶液质量为A g,溶质的质量分数为a%,蒸发Bg水后变成溶质的质量分数为b%的溶液,则
Ag×a%=(Ag一Bg)×b%。
【练2】在含盐0.5%的盐水中蒸去了236千克水,就变成了含盐30%的盐水,问原来的盐水是多少千克?
【答案】240
【解析】x ( ) , 。
×0.5%= x-236 ×30% x=240kg
3、与浓溶液混合
(1)混合后溶液的总质量等于两混合溶液的质量之和,混合后溶液中溶质质量等于两混合溶液的溶质质
量之和。
(2)若设原溶液质量为 A g,溶质的质量分数为a%,浓溶液质量为B g,溶质的质量分数为b%,两溶
液混合后得到溶质的质量分数为c%的溶液,则
Ag×a%+B g× b%=(Ag+Bg)×c%。
【练1】将含酒精量5%的溶液400克,与含酒精量60%的溶液600克混合,求混合后溶液的浓度是多少?
【答案】38%
【解析】400 5%+600 ( ) ,解得 。
× ×60%= 400+600 ×x% x=38%
经典例题
溶液稀释
【例1】硝酸钾可作为无土栽培的营养液。现将100g 25%的硝酸钾溶液稀释到l0%用于培植营养液,需加
水的质量是( C )
A.50g B.100g C.150g D.250g
【答案】C
【例1】将100g20%氯化钾溶液稀释到500g,稀释后所得溶液中溶剂的质量是( )质量分数是(C )A.100g 5 % B.400g 4% C.480 g 4% D.500 g 5%
【答案】C
溶液浓缩
【例1】现有含盐16%的盐水30千克,要配制成含盐20%的盐水,需要加盐多少千克?
【答案】1.5
【解析】(30 16%+x) (30+x)= 20%,解得x=1.5.
× ÷ ×
【例2】要从含盐12.5%的盐水40千克中蒸去多少水分才能制出含盐20%的盐水?
【答案】15
【解析】40-(40 12.5% )=40-25,解得x=15.
× ÷20%
【例2】有40g质量分数为5%的氯化钙溶液,若将其质量分数增加到10%,应采用的方法是( C )
A.把溶剂蒸发掉一半 B.加入40g质量分数为20%的氯化钙溶液
C.把溶剂蒸发掉20g D.加入2g氯化钙固体
【答案】C
专项训练
【训1】用20%过氧化氢溶液配制600克5%的过氧化氢溶液用于消毒,则需要20%过氧化氢溶液多少克?
需要水多少毫升?
【答案】150g;450mL。
【解析】设需要20%过氧化氢溶液的质量为x,根据溶液稀释前后溶质的质量不变,
则600g×5%=x×20% x=150g。
水的质量=稀溶液的质量﹣浓溶液的质量,需要水的质量为600g﹣150g=450g(合450mL)。
【训2】现有300g溶质质量分数为10%的氯化钠溶液。
(1)若蒸发掉150克水,溶液中溶质质量分数为 。
(2)若要使此溶液的溶质质量分数变成20%,需向溶液中加入 氯化钠。
(3)若要使此溶液的溶质质量分数变成5%,需向溶液中加入 水。
【答案】(1)20%;(2)37.5g;(3)300g。
【解析】(1)该溶液中氯化钠的质量为300g×10%=30g;若蒸发掉150克水,溶液中溶质质量分数为:
×100%=20%
(2)设加入的氯化钠的质量为x,则: ×100%=20%,解得:x=37.5g。(3)设需向溶液中加入的质量为y, ×100%=5%,解得:y=300g.
模块二 用化学方程式计算质量分数
知识精讲
知识点二 用化学方程式计算质量分数
【练1】一定量的镁与100g硫酸溶液恰好反应,生成氢气0.4g,计算:
(1)参加反应的镁的质量。 13g
(2)硫酸溶液溶质的质量分数。 9.8%
(3)反应后所得溶液的溶质质量分数。 15.1%
解:设参加反应的Mg的质量为x。HSO 的质量为y。产物MgSO 的质量为z。
2 4 4
Mg+HSO ===MgSO +H
2 4 4 2
24 98 120 2
x g y g z g 0.4g
解得:x=4.8g,y=19.6g,z=24g。
(1)参加反应的镁的质量:4.8g。
(2)硫酸溶液溶质的质量分数: 。
(3)反应后所得溶液的溶质质量分数:
经典例题
可能用到的相对原子质量:O-16、Na-23、Mg-24、Cl-35.5、Ca-40、Sr-88。
【例1】4 g氧化镁与100 g稀盐酸恰好完全反应,反应的化学方程式为MgO+2HCl===MgCl +HO。计算
2 2
该稀盐酸中溶质的质量分数。(结果精确到0.1%)解:设参加反应的HCl的质量为x。
MgO+2HCl===MgCl +HO
2 2
40 73
4 g x
= x=7.3 g
该稀盐酸中溶质的质量分数为×100%=7.3%。
答:该稀盐酸中溶质的质量分数为7.3%。
【例2】实验室常用大理石和稀盐酸制取二氧化碳。现取25 g含碳酸钙的大理石于烧杯中,缓慢加入稀盐酸
(大理石中的杂质不溶于水,也不与稀盐酸反应),剩余固体质量与加入稀盐酸的质量关系如图所示。求:
(1)25 g大理石中碳酸钙的质量。
(2)恰好完全反应时所得溶液中溶质的质量分数。
(1)25 g大理石中碳酸钙的质量为25 g-5 g=20 g。
(2)设恰好完全反应时生成二氧化碳的质量为x,生成氯化钙的质量为y。
CaCO +2HCl CaCl +H O+CO↑
3 2 2 2
100 111 44
20 g y x
100 20 g
= x=8.8 g
44 x
100 20 g
= y=22.2 g
111 y
22.2 g
恰好完全反应时所得溶液中溶质的质量分数为 ×100%=11.1%。
20 g+188.8 g-8.8 g
答:(1)25 g大理石中碳酸钙的质量为20 g;(2)恰好完全反应时所得溶液中溶质的质量分数为11.1%。
【例3】 碳酸锶(SrCO )可用于制造红色火焰、荧光玻璃等。小赵同学为测定某SrCO 和NaCl固体混合物
3 3
中SrCO 的质量分数,在三只烧杯中进行相关实验,实验所用稀盐酸的溶质质量分数相同。所得数据如下
3
表所示。试求:
烧杯编号 ① ② ③
稀盐酸质量/g 100 200 300
固体混合物质量/g 100 100 100反应后烧杯中物质的质量/g 195.6 291.2 391.2
(1)烧杯②中产生CO 的质量为________g。
2
(2)原固体混合物中SrCO 的质量分数。(计算结果精确到0.1%)
3
(提示:SrCO +2HCl===SrCl +CO↑+HO)
3 2 2 2
(1)8.8
(2)解:设固体混合物中SrCO 的质量为x。
3
SrCO +2HCl===SrCl +CO↑+HO
3 2 2 2
148 44
x 8.8 g
=
x=29.6 g
原固体混合物中SrCO 的质量分数为
3
×100%=29.6%。
答:原固体混合物中SrCO 的质量分数为29.6%。
3
【例4】向6 g氯化钠和碳酸钠的固体混合物中不断加入稀盐酸,发生反应的化学方程式为 NaCO +
2 3
2HCl===2NaCl+HO+CO↑,反应过程中生成气体的质量与加入稀盐酸的质量关系如图所示。求:
2 2
(1)恰好完全反应时,生成气体的质量为______g。
(2)恰好完全反应时,所得溶液的溶质质量分数。
(1)2.2
(2)解:设原混合物中碳酸钠的质量为x,生成氯化钠的质量为y。
NaCO+2HCl===2NaCl+HO+CO↑
2 3 2 2
106 117 44
x y 2.2 g
= x=5.3 g
= y=5.85 g
所得溶液的溶质质量分数为
×100%=12.2%。
答:恰好完全反应时,所得溶液的溶质质量分数为12.2%。
【例5】某化学兴趣小组的同学到化学实验室,完成了如下实验,请计算:
(已知:2Al+2NaOH+2H O 2NaAlO +3H ↑)
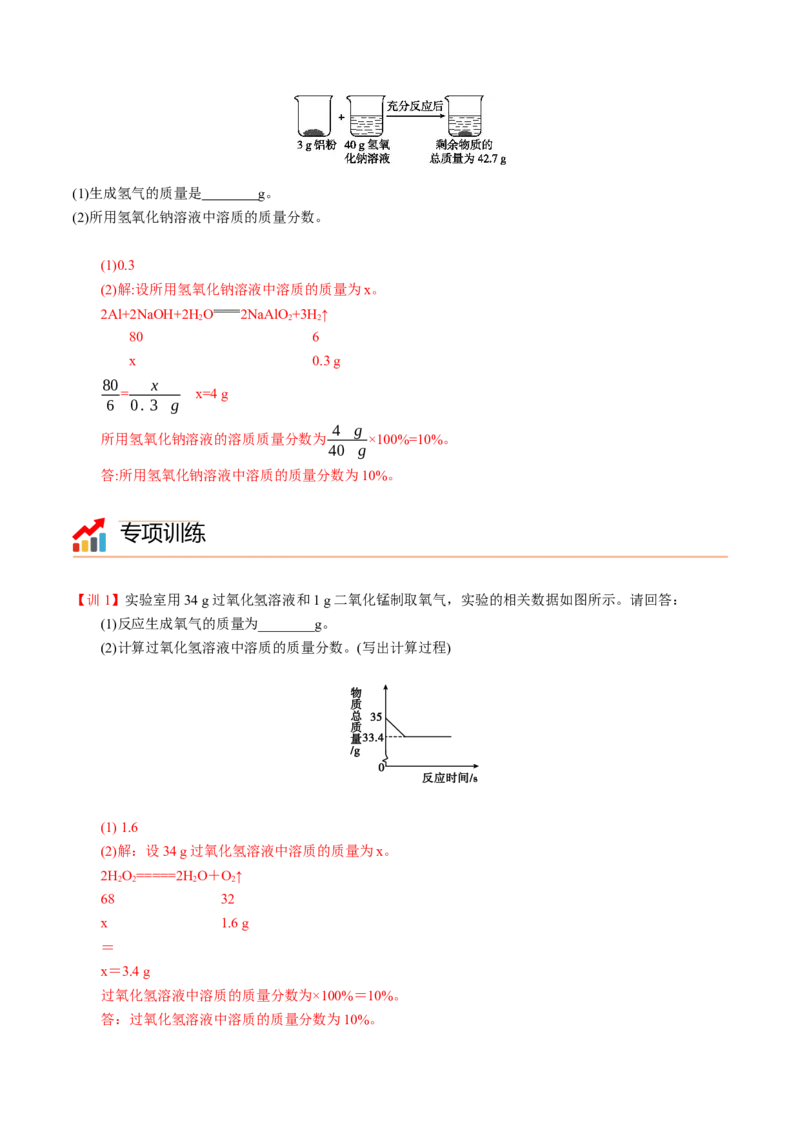
2 2 2(1)生成氢气的质量是 g。
(2)所用氢氧化钠溶液中溶质的质量分数。
(1)0.3
(2)解:设所用氢氧化钠溶液中溶质的质量为x。
2Al+2NaOH+2H O 2NaAlO +3H ↑
2 2 2
80 6
x 0.3 g
80 x
= x=4 g
6 0.3 g
4 g
所用氢氧化钠溶液的溶质质量分数为 ×100%=10%。
40 g
答:所用氢氧化钠溶液中溶质的质量分数为10%。
专项训练
【训1】实验室用34 g过氧化氢溶液和1 g二氧化锰制取氧气,实验的相关数据如图所示。请回答:
(1)反应生成氧气的质量为________g。
(2)计算过氧化氢溶液中溶质的质量分数。(写出计算过程)
(1) 1.6
(2)解:设34 g过氧化氢溶液中溶质的质量为x。
2HO=====2HO+O↑
2 2 2 2
68 32
x 1.6 g
=
x=3.4 g
过氧化氢溶液中溶质的质量分数为×100%=10%。
答:过氧化氢溶液中溶质的质量分数为10%。【训2】我州石灰石资源丰富,某课外小组同学为了测定石灰石中碳酸钙的质量分数,取某地石灰石样品
9.0g于烧杯中,将50g稀盐酸分5次加入烧杯中,充分反应后(杂质不与稀盐酸反应),测得剩余固体的
质量记录如下。
次数 1 2 3 4 5
加入稀盐酸质量/g 10 10 10 10 10
剩余固体质量/g 7.0 5.0 3.0 1.5 1.5
请计算:
(1)所用稀盐酸溶质的质量分数。(写出计算过程)__________
【答案】(1)根据前三次每次加入10g盐酸都是减少固体2g,可见每10g盐酸和2g碳酸钙完全反应。
设10g盐酸中HCl的质量为y。
CaCO + 2HCl=CaCl + H O+ CO
3 2 2 2
100 73
2g y
100 2g
=
73 y
解得y=1.46g
1.46g
100%
所用稀盐酸溶质的质量分数为 10g =14.6%
提分作业
1.将50g质量分数为98%的浓硫酸稀释为20%的稀硫酸,需要加水的质量为( )
A.245g B.195g C.100g D.无法计算
【答案】B
【解析】溶质质量不变,50 98%=(50+x) 20%,解得x=195g。
× ×
2.为了控制新冠疫情,每天需要喷洒大量的消毒液。
(1)800kg 质量分数为0.5% 的过氧乙酸消毒液中,过氧乙酸的质量为__________kg。 4
(2)要配制 800kg 质量分数为0.5% 的过氧乙酸消毒液,需要质量分数为16% 的过氧乙酸溶液的质量是
多少? 25kg
【答案】(1)4;(2)25kg。
【解析】(1)溶质质量=溶液质量 质量分数,800 0.5%=4kg;(2)溶质质量不变,
800 0.5%=x 16%,x=25kg。
× ×
× ×3.为测定某碳酸钙样品中碳酸钙的质量分数,某学习小组进行了如下实验探究。取10g碳酸钙样品放入烧
杯中,加入稀盐酸至不再产生气泡为止(样品中的杂质仅有 CaCl ),并绘制了加入稀盐酸的质量与放出
2
气体质量的坐标图(如图).
(1)所用稀盐酸的溶质质量分数是多少?______
(2)该样品中碳酸钙的质量分数为多少?______
(3)当盐酸和样品恰好完全反应,所得溶液中溶质质量分数是多少?(规范写出计算过程)______
【答案】(1)6.9% (2) 80% (3)12.0%
【解析】
由题意碳酸钙与稀盐酸反应生成二氧化碳的质量为3.52g,设反应消耗的HCl质量为x,参加反应的CaCO
3
的质量为y,反应生成的CaCl 质量为z,则有:
2
CaCO + 2HCl = CaCl + H O + CO
3 2 2 2
100 73 111 44
y x z 3.52g
73 44
=
由 x 3.52g 解得x=5.84g
100 44
=
由 y 3.52g 解得y=8g
111 44
=
由 z 3.52g 解得z=8.88g
5.84g
100%6.9%
(1)所用稀盐酸的溶质质量分数为84.32g
8g
100%=80%
(2)样品中CaCO 的质量分数为10g
3
(3)样品中所含氯化钙的质量为10g-8g=2g,反应后的溶液溶质质量分数为
2g+8.88g
100%12.0%
10g+84.32g-3.52g
答:(1)稀盐酸的溶质质量分数为6.9%。(2)样品中CaCO 的质量分数为80%。
3
(3)反应后的溶液溶质质量分数为12.0%。