文档内容
凉山州 2026 届高中毕业班第二次诊断性考试
化 学
全卷共8页,满分100分,考试时间75分钟。
注意事项:
1. 答题前,考生务必将自己的姓名、座位号、准考证号用0.5毫米的黑色签字笔填写在答题卡
上,并检查条形码粘贴是否正确。
2.选择题使用2B铅笔涂在答题卡对应题目标号的位置上;非选择题用0.5毫米黑色签字笔
书写在答题卡的对应框内,超出答题区域书写的答案无效;在草稿纸、试卷上答题无效。
3.考试结束后,将答题卡收回。
可能用到的相对原子质量:
H 1 B 11 C 12 N 14 Na 23 Cu 64
一、单项选择题(本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项
是最符合题目要求的。)
三星堆是中华文明的重要组成部分。下列出土文物的材料属于合金的是( )
1. 银
象牙雕刻 青铜神树 丝绸“黑炭” 商玉边璋
A援 B援 C援 D援
化学与人类社会发展息息相关。下列说法不正确的是( )
2. 银
维生素 可用作食品抗氧化剂
A援 C
煤的气化是通过化学变化将煤转化为可燃性气体的过程
B援
添入牙膏中能起到预防龋齿的作用是因为 有强氧化性
C援 NaF NaF
泡腾片和酒精均可灭杀病毒,二者消毒原理不同
D援 ClO2
下列表示不正确的是( )
3. 银
的电子式:
A援 CO2
分子的球棍模型:
B援 CH4
用电子云轮廓图表示 键的形成:
C援 p-p 仔
溶液中的水合离子:
D援 NaCl
抗癌药物 的结构如图。关于该药物的说法不正确的是( )
4. CADD522 银
能发生水解反应
A援
含有 个手性碳原子
B援 4
化学式为
C援 C15H11Cl2NO3
碳原子杂化方式有 和
2 3
D援 sp sp
化学试题卷 第 页(共 页)
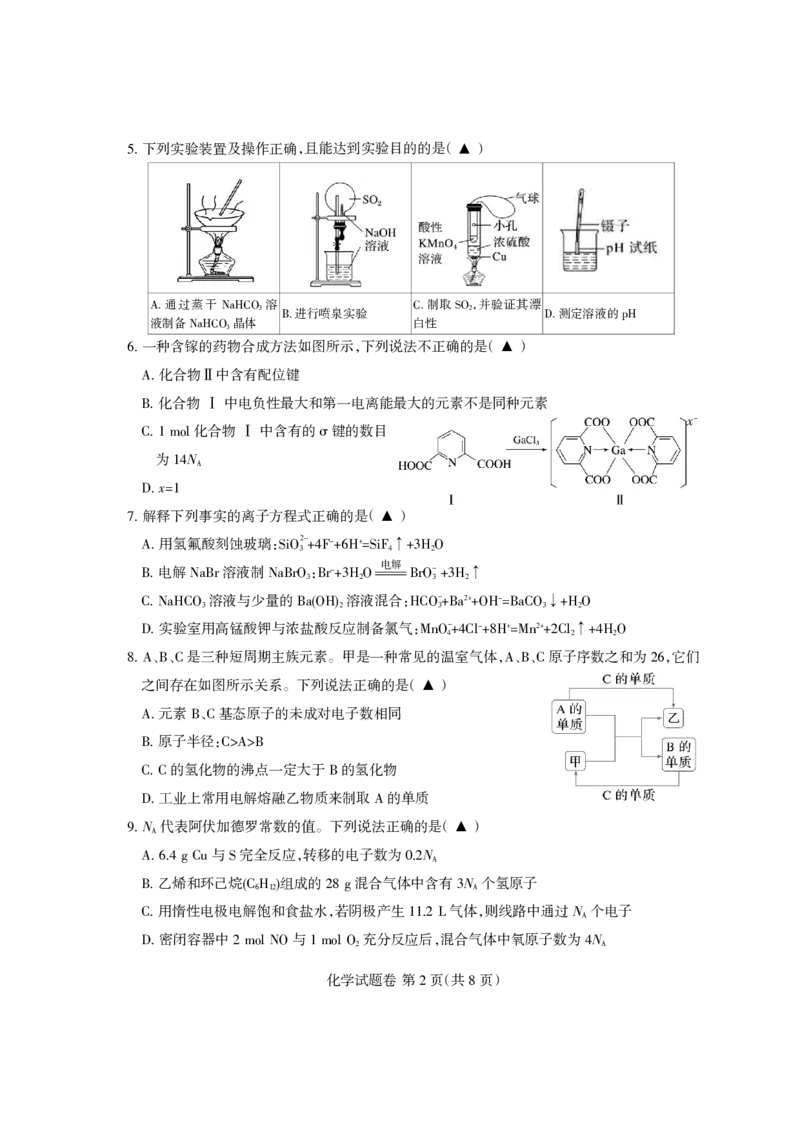
1 8下列实验装置及操作正确,且能达到实验目的的是( )
5援 银
A. 通过蒸干 NaHCO 溶 C.制取SO,并验证其漂
3 2
B.进行喷泉实验 D.测定溶液的pH
液制备NaHCO 晶体 白性
3
一种含镓的药物合成方法如图所示,下列说法不正确的是( )
6援 银
化合物 中含有配位键
A援 域
化合物 中电负性最大和第一电离能最大的元素不是同种元素
B援 玉
x
-
化合物 中含有的 键的数目
C援 1 mol 玉 滓
为 N
14 A
x
D援 =1
解释下列事实的离子方程式正确的是( )
7. 银
用氢氟酸刻蚀玻璃: 2- - +
A援 SiO3 +4F+6H=SiF4尹+3H2O
电解
电解 溶液制 : - -
B. NaBr NaBrO3 Br+3H2O越BrO3 +3H2尹
溶液与少量的 溶液混合: - 2+ -
C. NaHCO3 Ba(OH)2 HCO3+Ba +OH=BaCO3引+H2O
实验室用高锰酸钾与浓盐酸反应制备氯气: - - + 2+
D. MnO4+4Cl+8H=Mn +2Cl2尹+4H2O
、、 是三种短周期主族元素。甲是一种常见的温室气体,、、 原子序数之和为 ,它们
8援 A B C A B C 26
之间存在如图所示关系。下列说法正确的是( )
银
元素 、 基态原子的未成对电子数相同
A援 B C
原子半径:
B援 C>A>B
的氢化物的沸点一定大于 的氢化物
C援 C B
工业上常用电解熔融乙物质来制取 的单质
D援 A
N 代表阿伏加德罗常数的值。下列说法正确的是( )
9援 A 银
与 完全反应,转移的电子数为 N
A援 6.4 g Cu S 0.2 A
乙烯和环己烷 组成的 混合气体中含有 N 个氢原子
B援 (C6H12) 28 g 3 A
用惰性电极电解饱和食盐水,若阴极产生 气体,则线路中通过N 个电子
C援 11.2 L A
密闭容器中 与 充分反应后,混合气体中氧原子数为 N
D援 2 mol NO 1 mol O2 4 A
化学试题卷 第 页(共 页)
2 8下列有关物质检验“操作、现象、结论”的逻辑关系正确的是( )
10援 银
实验操作及现象 结论
A 蘸有浓氨水的玻璃棒靠近溶液X,有白烟产生 X一定是浓盐酸
向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO 溶液,均
4
B 蛋白质均发生变性
有固体析出
C 向NaHS溶液中滴入酚酞,溶液变红色 HS-水解程度大于其电离程度
溴乙烷与NaOH水溶液共热后,滴加AgNO 溶液,未出现浅黄色
3
D 溴乙烷未发生水解
沉淀
一种利用 和 直接合成 的反应历程如图所示。下列说法不正确的是( )
11. H2 O2 H2O2 银
总反应的原子利用率理论上可达
A. 100%
步骤 中,若 完全反应,则理论上转移电子数目为 N
B援 2 1 mol O2 2 A
在此过程中作为催化剂
2原
C援 [PdCl4]
和 中 的化合价不相同
D援 Pd
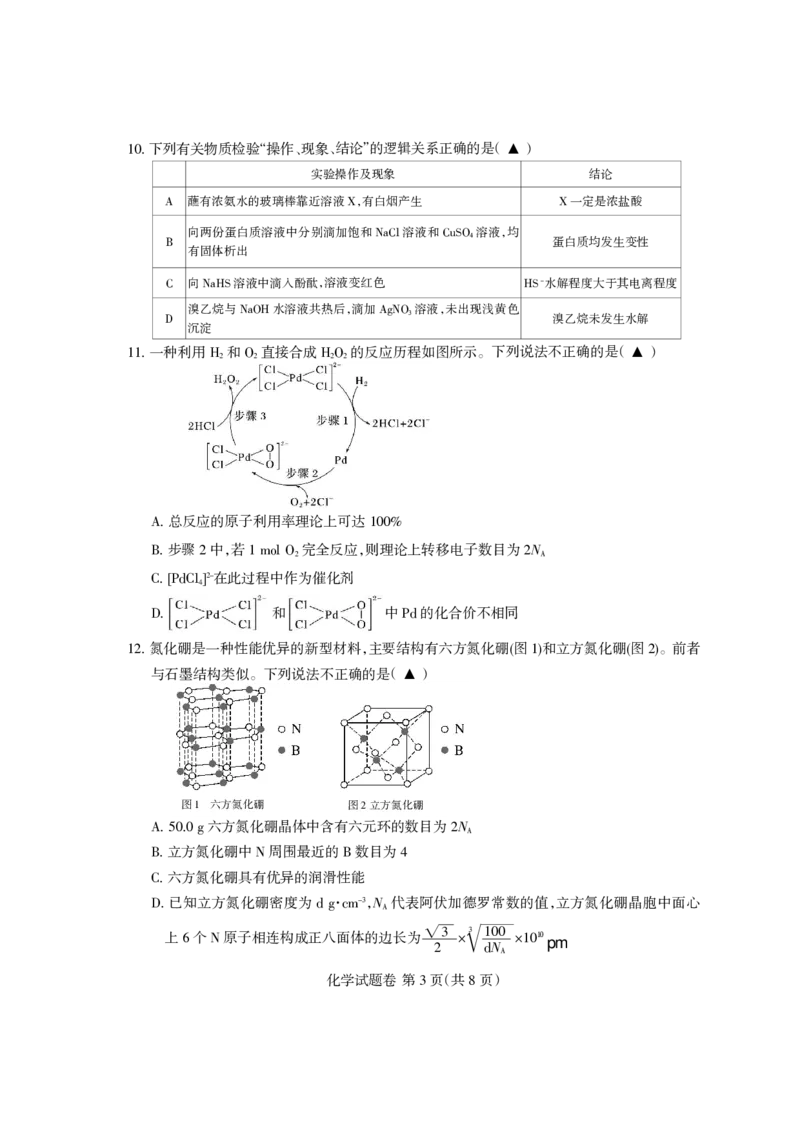
氮化硼是一种性能优异的新型材料,主要结构有六方氮化硼图 和立方氮化硼图 。前者
12援 ( 1) ( 2)
与石墨结构类似。下列说法不正确的是( )
银
图 六方氮化硼 图 立方氮化硼
1 2
六方氮化硼晶体中含有六元环的数目为 N
A援 50.0 g 2 A
立方氮化硼中 周围最近的 数目为
B援 N B 4
六方氮化硼具有优异的润滑性能
C援
已知立方氮化硼密度为 · ,N 代表阿伏加德罗常数的值,立方氮化硼晶胞中面心
原3
D援 d g cm A
上
6
个
N
原子相连构成正八面体的边长为 姨3
伊
3 10
N
0
伊10
10pm
2 姨d A
化学试题卷 第 页(共 页)
3 8以铅精矿含 、 等为主要原料提取金属 和 的工艺流程如下:
13. ( PbS Ag2S ) Pb Ag
已知:“热浸”时,难溶的 和 转化为 和 及单质硫。
2- -
PbS Ag2S [PbCl4] [AgCl2]
下列说法不正确的是( )
银
溶解等物质的量的 和 时,消耗 物质的量之比为
3垣
A援 PbS Ag2S Fe 1:1
热浸中盐酸浓度不宜过大,可以有效防止产生有毒气体
B援 H2S
将“过滤 ”得到的 沉淀反复用饱和食盐水热溶,电解所得溶液可在阳极获得金属
C援 域 PbCl2 Pb
“还原”中加入铅精矿可以提高铅精矿利用率,同时减少试剂 的用量,降低生产成本
D援 X
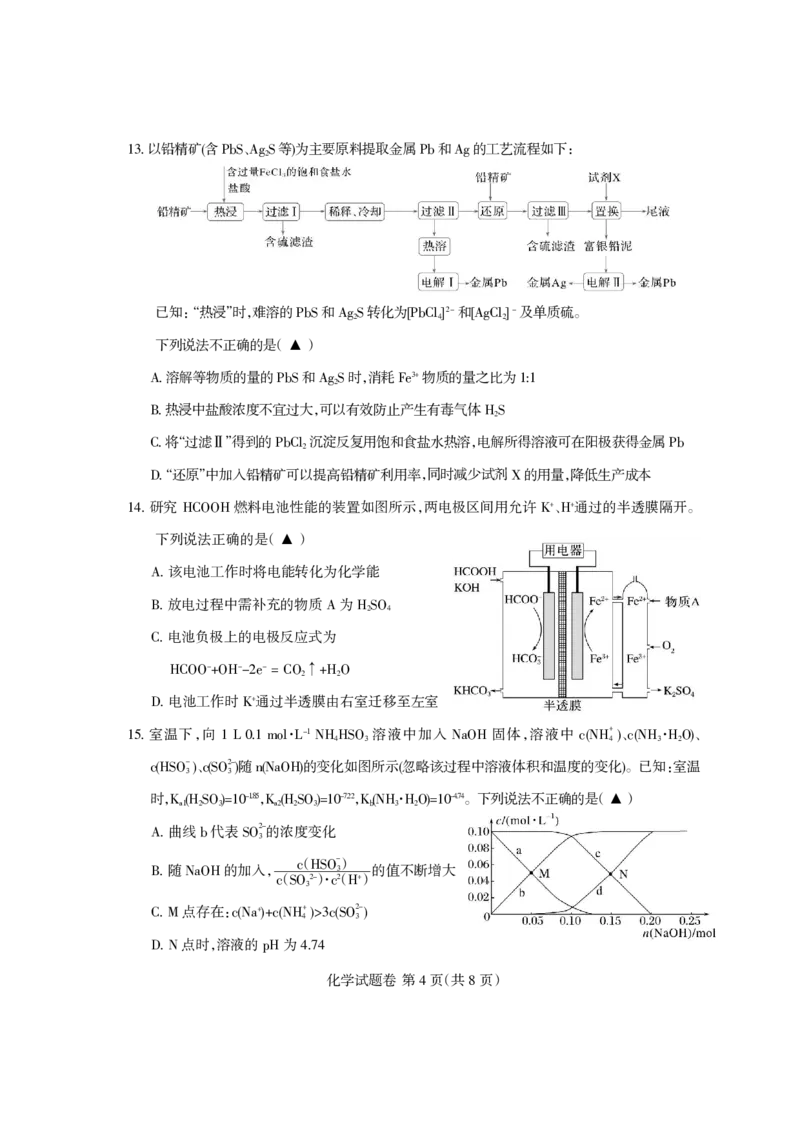
研究 燃料电池性能的装置如图所示,两电极区间用允许 、 通过的半透膜隔开。
+ +
14. HCOOH K H
下列说法正确的是( )
银
该电池工作时将电能转化为化学能
A援
放电过程中需补充的物质 为
B援 A H2SO4
电池负极上的电极反应式为
C援
- - -
HCOO+OH-2e = CO2尹+H2O
电池工作时 通过半透膜由右室迁移至左室
+
D援 K
室温下,向 · -1 溶液中加入 固体,溶液中 + 、 · 、
15. 1 L 0.1 mol L NH4HSO3 NaOH c(NH4 ) c(NH3 H2O)
- 、 2-随 的变化如图所示忽略该过程中溶液体积和温度的变化。已知:室温
c(HSO3) c(SO3) n(NaOH) ( )
时, , , · 。下列说法不正确的是( )
-1.85 -7.22 -4.74
Ka1(H2SO3)=10 Ka2(H2SO3)=10 Kb(NH3 H2O)=10 银
曲线 代表 2-的浓度变化
A援 b SO3
( -)
随 的加入, 的值不断增大
B援 NaOH ( c 2 H - )· SO (3 2 + )
c SO3 c H
点存在: + + 2-
C援 M c(Na)+c(NH4 )>3c(SO3 )
点时,溶液的 为
D援 N pH 4.74
化学试题卷 第 页(共 页)
4 8二、非选择题(共55分)
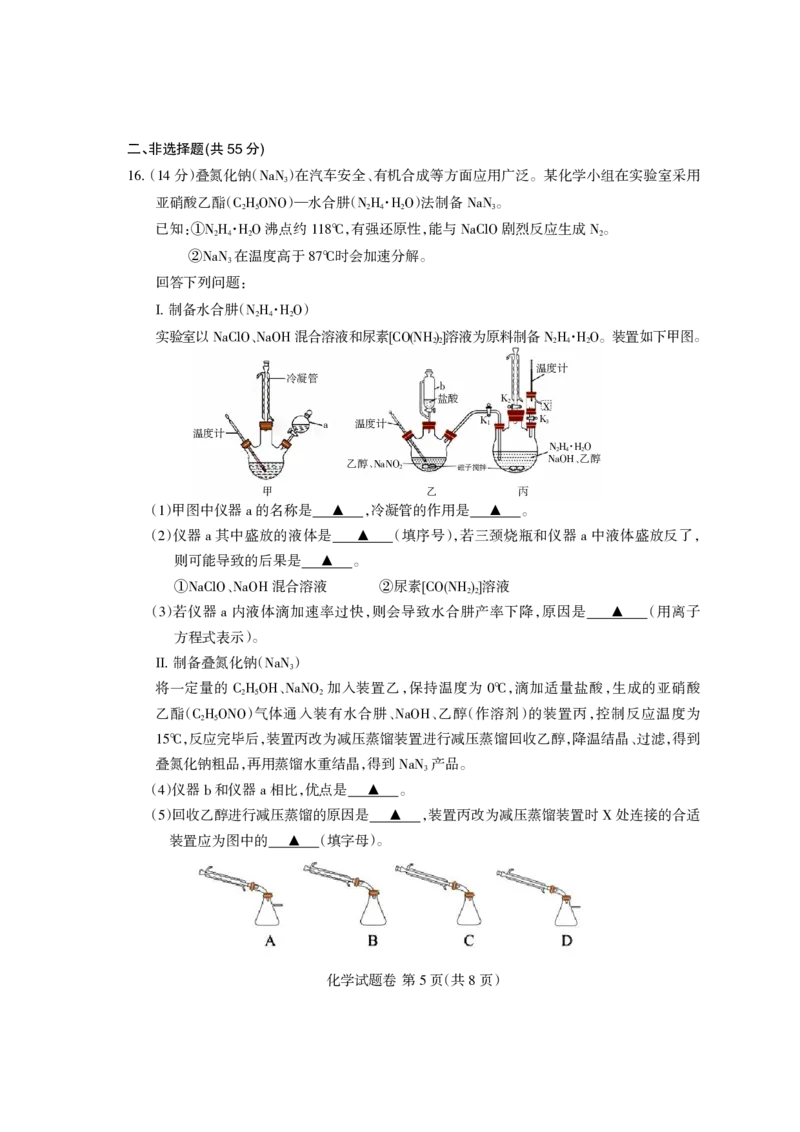
( 分)叠氮化钠( )在汽车安全、有机合成等方面应用广泛。某化学小组在实验室采用
16援 14 NaN3
亚硝酸乙酯( )—水合肼( · )法制备 。
C2H5ONO N2H4 H2O NaN3
已知: · 沸点约 ,有强还原性,能与 剧烈反应生成 。
淤N2H4 H2O 118益 NaClO N2
在温度高于 时会加速分解。
于NaN3 87益
回答下列问题:
制备水合肼( · )
I援 N2H4 H2O
实验室以 、 混合溶液和尿素 溶液为原料制备 · 。装置如下甲图。
NaClO NaOH [CO(NH2)2] N2H4 H2O
温度计
冷凝管
b
盐酸
K2
X
温度计 a
温度计 K1 K3
·
N2H4 H 、乙2O
醇
乙醇、 NaNO2 磁子搅拌 NaOH
甲 乙 丙
()甲图中仪器 的名称是 ,冷凝管的作用是 。
1 a 银 银
()仪器 其中盛放的液体是 (填序号),若三颈烧瓶和仪器 中液体盛放反了,
2 a 银 a
则可能导致的后果是 。
银
、 混合溶液 尿素 溶液
淤NaClO NaOH 于 [CO(NH2)2]
()若仪器 内液体滴加速率过快,则会导致水合肼产率下降,原因是 (用离子
3 a 银
方程式表示)。
制备叠氮化钠( )
II援 NaN3
将一定量的 、 加入装置乙,保持温度为 ,滴加适量盐酸,生成的亚硝酸
C2H5OH NaNO2 0益
乙酯( )气体通入装有水合肼、 、乙醇(作溶剂)的装置丙,控制反应温度为
C2H5ONO NaOH
,反应完毕后,装置丙改为减压蒸馏装置进行减压蒸馏回收乙醇,降温结晶、过滤,得到
15益
叠氮化钠粗品,再用蒸馏水重结晶,得到 产品。
NaN3
()仪器 和仪器 相比,优点是 。
4 b a 银
()回收乙醇进行减压蒸馏的原因是 ,装置丙改为减压蒸馏装置时 处连接的合适
5 银 X
装置应为图中的 (填字母)。
银
化学试题卷 第 页(共 页)
5 8测定叠氮化钠纯度
III援
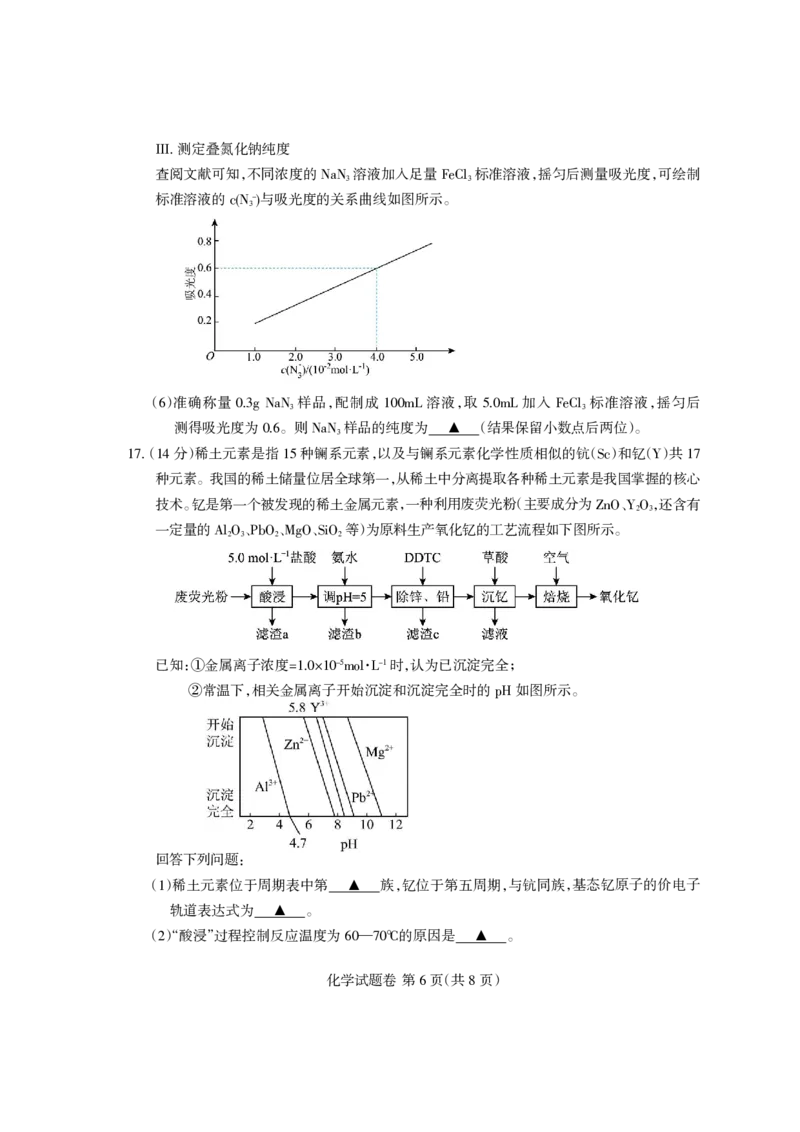
查阅文献可知,不同浓度的 溶液加入足量 标准溶液,摇匀后测量吸光度,可绘制
NaN3 FeCl3
标准溶液的 与吸光度的关系曲线如图所示。
-
c(N3)
()准确称量 样品,配制成 溶液,取 加入 标准溶液,摇匀后
6 0.3g NaN3 100mL 5.0mL FeCl3
测得吸光度为 。则 样品的纯度为 (结果保留小数点后两位)。
0.6 NaN3 银
( 分)稀土元素是指 种镧系元素,以及与镧系元素化学性质相似的钪( )和钇( )共
17援 14 15 Sc Y 17
种元素。我国的稀土储量位居全球第一,从稀土中分离提取各种稀土元素是我国掌握的核心
技术。钇是第一个被发现的稀土金属元素,一种利用废荧光粉(主要成分为 、 ,还含有
ZnO Y2O3
一定量的 、 、 、 等)为原料生产氧化钇的工艺流程如下图所示。
Al2O3 PbO2 MgO SiO2
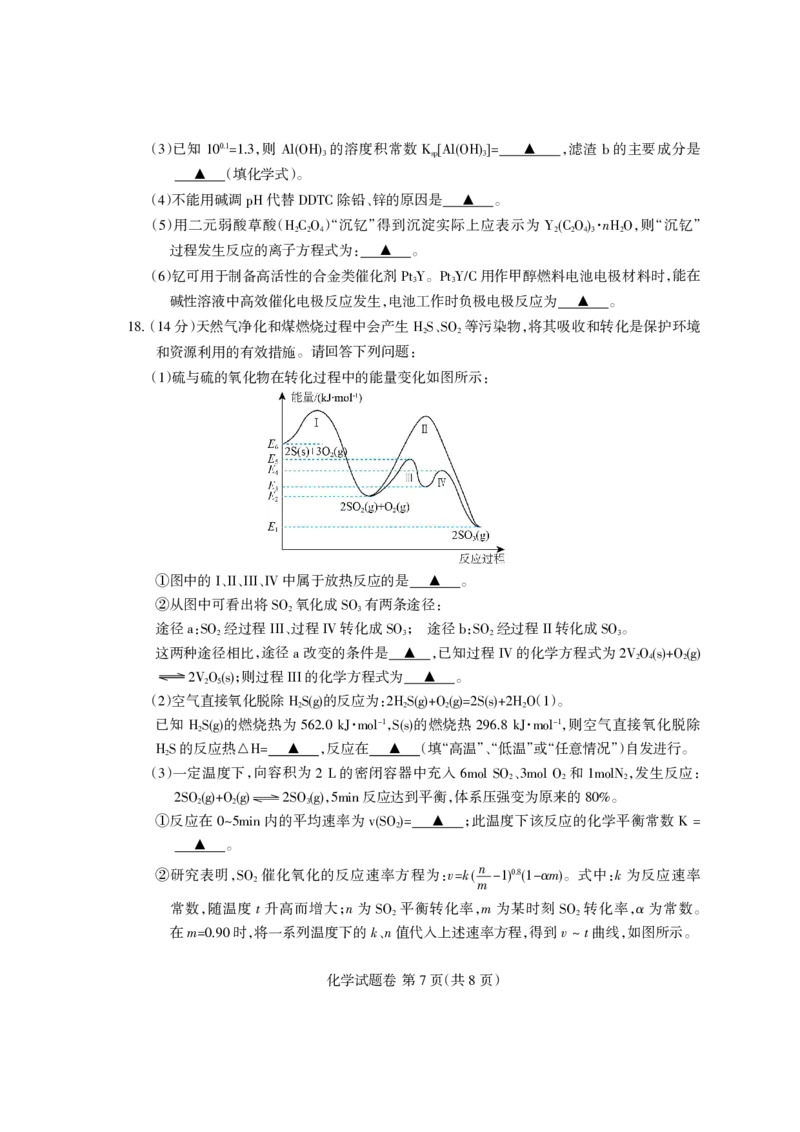
已知: 金属离子浓度 · 时,认为已沉淀完全;
-5 -1
淤 =1.0伊10 mol L
常温下,相关金属离子开始沉淀和沉淀完全时的 如图所示。
于 pH
回答下列问题:
()稀土元素位于周期表中第 族,钇位于第五周期,与钪同族,基态钇原子的价电子
1 银
轨道表达式为 。
银
()“酸浸”过程控制反应温度为 — 的原因是 。
2 60 70益 银
化学试题卷 第 页(共 页)
6 8()已知 ,则 的溶度积常数 ,滤渣 的主要成分是
0.1
3 10 越1.3 Al(OH)3 Ksp[Al(OH)3]越 银 b
(填化学式)。
银
()不能用碱调 代替 除铅、锌的原因是 。
4 pH DDTC 银
()用二元弱酸草酸( )“沉钇”得到沉淀实际上应表示为 ·n ,则“沉钇”
5 H2C2O4 Y2(C2O4)3 H2O
过程发生反应的离子方程式为: 。
银
()钇可用于制备高活性的合金类催化剂 。 用作甲醇燃料电池电极材料时,能在
6 Pt3Y Pt3Y/C
碱性溶液中高效催化电极反应发生,电池工作时负极电极反应为 。
银
( 分)天然气净化和煤燃烧过程中会产生 、 等污染物,将其吸收和转化是保护环境
18援 14 H2S SO2
和资源利用的有效措施。请回答下列问题:
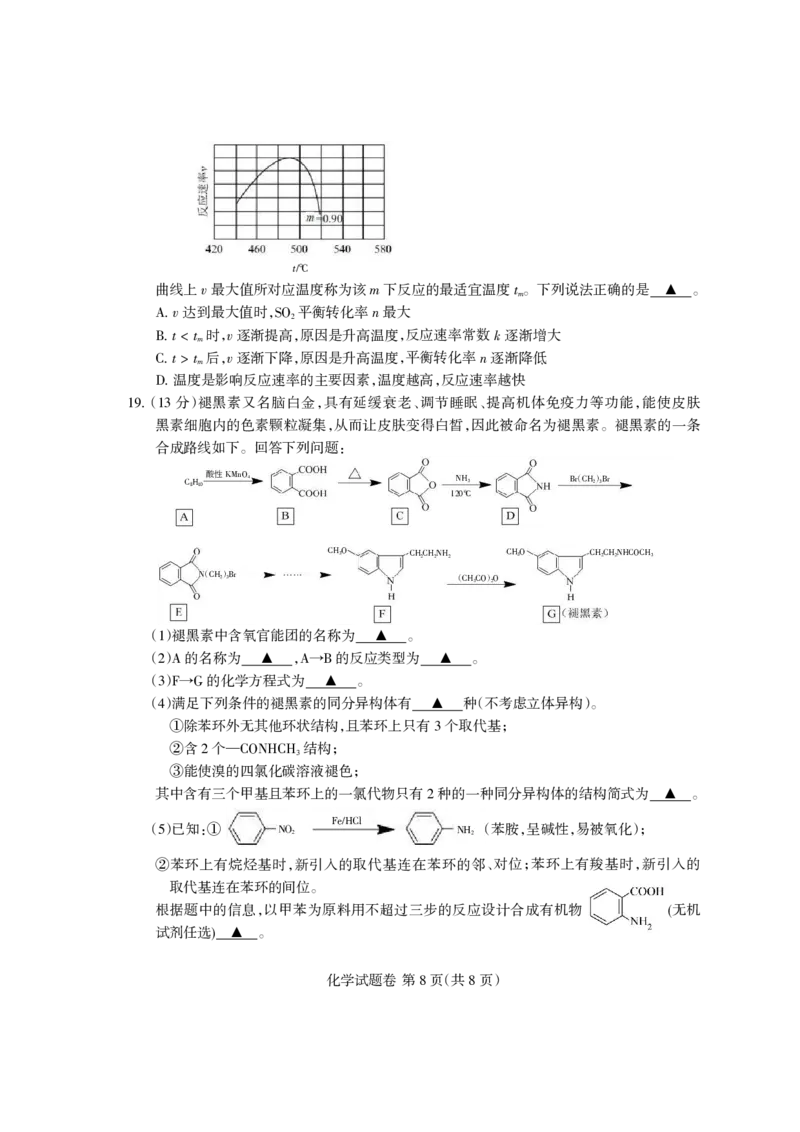
()硫与硫的氧化物在转化过程中的能量变化如图所示:
1
图中的 、、 、 中属于放热反应的是 。
淤 I II III IV 银
从图中可看出将 氧化成 有两条途径:
于 SO2 SO3
途径 : 经过程 、过程 转化成 ; 途径 : 经过程 转化成 。
a SO2 III IV SO3 b SO2 II SO3
这两种途径相比,途径 改变的条件是 ,已知过程 的化学方程式为
a 银 IV 2V2O4(s)垣O2(g)
;则过程 的化学方程式为 。
2V2O5(s) III 银
()空气直接氧化脱除 的反应为: ()。
2 H2S(g) 2H2S(g)垣O2(g)越2S(s)垣2H2O 1
已知 的燃烧热为 · , 的燃烧热 · ,则空气直接氧化脱除
-1 -1
H2S(g) 562.0 kJ mol S(s) 296.8 kJ mol
的反应热 ,反应在 (填“高温”、“低温”或“任意情况”)自发进行。
H2S 吟H越 银 银
()一定温度下,向容积为 的密闭容器中充入 、 和 ,发生反应:
3 2 L 6mol SO2 3mol O2 1molN2
, 反应达到平衡,体系压强变为原来的 。
2SO2(g)垣O2(g) 2SO3(g) 5min 80%
反应在 内的平均速率为 ;此温度下该反应的化学平衡常数
淤 0耀5min v(SO2)= 银 K =
。
银
n
研究表明, 催化氧化的反应速率方程为:v k 琢m。式中:k 为反应速率
0.8
于 SO2 = (m 原1) (1原 )
常数,随温度 t 升高而增大;n 为 平衡转化率,m 为某时刻 转化率,琢 为常数。
SO2 SO2
在m 时,将一系列温度下的k、n值代入上述速率方程,得到v ~ t曲线,如图所示。
=0.90
化学试题卷 第 页(共 页)
7 8t
/益
曲线上v 最大值所对应温度称为该m下反应的最适宜温度t 。下列说法正确的是 。
m 银
v 达到最大值时, 平衡转化率n最大
A援 SO2
t < t 时,v 逐渐提高,原因是升高温度,反应速率常数k 逐渐增大
B援 m
t > t 后,v 逐渐下降,原因是升高温度,平衡转化率n逐渐降低
C援 m
温度是影响反应速率的主要因素,温度越高,反应速率越快
D援
( 分)褪黑素又名脑白金,具有延缓衰老、调节睡眠、提高机体免疫力等功能,能使皮肤
19援 13
黑素细胞内的色素颗粒凝集,从而让皮肤变得白皙,因此被命名为褪黑素。褪黑素的一条
合成路线如下。回答下列问题:
酸性
C8H10 KMnO4 NH3 B ( r CH2 ) 3Br
120益
CH3O CH2CH2NH2 CH3O CH2CH2NHCOCH3
N ( CH2 ) 3Br ( CH3CO ) 2O
()褪黑素中含氧官能团的名称为 。
1 银
() 的名称为 , 的反应类型为 。
2 A 银 A寅B 银
() 的化学方程式为 。
3 F寅G 银
()满足下列条件的褪黑素的同分异构体有 种(不考虑立体异构)。
4 银
除苯环外无其他环状结构,且苯环上只有 个取代基;
淤 3
含 个— 结构;
于 2 CONHCH3
能使溴的四氯化碳溶液褪色;
盂
其中含有三个甲基且苯环上的一氯代物只有 种的一种同分异构体的结构简式为 。
2 银
()已知: Fe/HCl (苯胺,呈碱性,易被氧化);
5 淤 NO2 NH2
苯环上有烷烃基时,新引入的取代基连在苯环的邻、对位;苯环上有羧基时,新引入的
于
取代基连在苯环的间位。
根据题中的信息,以甲苯为原料用不超过三步的反应设计合成有机物 无机
(
试剂任选 。
) 银
化学试题卷 第 页(共 页)
8 8