文档内容
2024 灌南高中协作体高一月考联考
化学试题(12.2)
一、单选题
1.化学来源于生活,也服务于生活。下列有关生活中的化学知识叙述不正确的是
A.水果罐头中添加维生素C作抗氧化剂,是因为维生素C易被氧化
B.漂白粉露置于空气中变质,该过程未涉及化学变化
C.洁厕灵(主要成分为 )与“84”消毒液不能混合使用,因为会产生有毒气体
D.区别氯化钾和氯化钠可以利用焰色反应原理
2.制取 的反应为 ,下列有关化学用语表示不正确的
是
A.中子数为10的氧原子: B.钠离子的结构示意图:
C. 的电子式: D. 的电离方程式:
3.下列有关物质的性质与用途具有对应关系的是
A. 能与碱反应,可用作焙制糕点的膨松剂
试卷第1页,共3页
学科网(北京)股份有限公司B.碱石灰具有吸水性,可用作实验室干燥
C.氢氧化铝具有弱碱性,可用于制胃酸中和剂
D.浓硫酸有脱水性,可作气体干燥剂
氮元素及其化合物在自然界广泛存在且具有重要应用。氮的氧化物有 等,氮的氢化物有
等。 易液化,能与多种物质发生反应。将金属钠投入液氮中有 产生, 可与酸反应
制得铵盐,可通过催化氧化生产 ,强碱条件下能被 氧化生成水合肼 ,其制备的
反应原理为 。回答下列问题:
4.下列说法正确的是
A.液 具有碱性,可用作制冷剂
B. 转化为其它含氮的化合物,可看作氮的固定
C.氨气可以用湿润的蓝色石荦试纸来检验
D.金属钠与液氨反应体现了 的氧化性
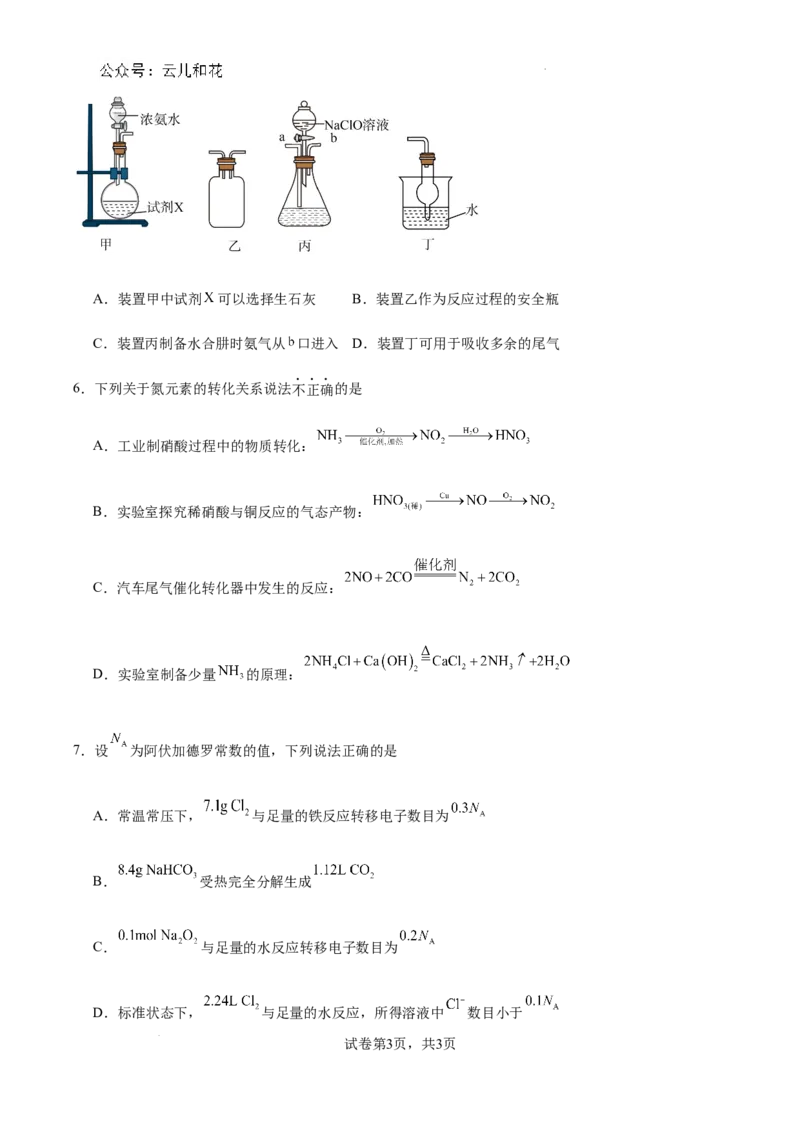
5.下列关于实验室制备水合肼的装置、操作或原理不正确的是
试卷第2页,共3页A.装置甲中试剂 可以选择生石灰 B.装置乙作为反应过程的安全瓶
C.装置丙制备水合肼时氨气从 口进入 D.装置丁可用于吸收多余的尾气
6.下列关于氮元素的转化关系说法不正确的是
A.工业制硝酸过程中的物质转化:
B.实验室探究稀硝酸与铜反应的气态产物:
C.汽车尾气催化转化器中发生的反应:
D.实验室制备少量 的原理:
7.设 为阿伏加德罗常数的值,下列说法正确的是
A.常温常压下, 与足量的铁反应转移电子数目为
B. 受热完全分解生成
C. 与足量的水反应转移电子数目为
D.标准状态下, 与足量的水反应,所得溶液中 数目小于
试卷第3页,共3页
学科网(北京)股份有限公司8.室温下,下列各组离子在指定溶液中能大量共存的是
A.饱和氯水: 、 、 、
B.无色透明溶液中: 、 、 、
C.能使酚酞变红的溶液: 、 、 、
D. 溶液: 、 、 、
9. 将逐渐取代 成为生产自来水的消毒剂。工业上常通过如下反应制取:
(未配平)。下列说法正确的是
A.反应中氯元素被氧化,硫元素被还原
B.还原性:
C.氧化剂和还原剂的物质的量之比为2:1
D.每生成 转移2mol电子
10.硫及其化合物的转化具有重要应用。下列说法不正确的是
A.实验室探究浓硫酸与硫反应的气态产物:
B.工业制硫酸过程中的物质转化:
C.用生石灰进行“钙基固硫”的主要反应为:
试卷第4页,共3页D. 通入少量氨水中的离子方程式为:
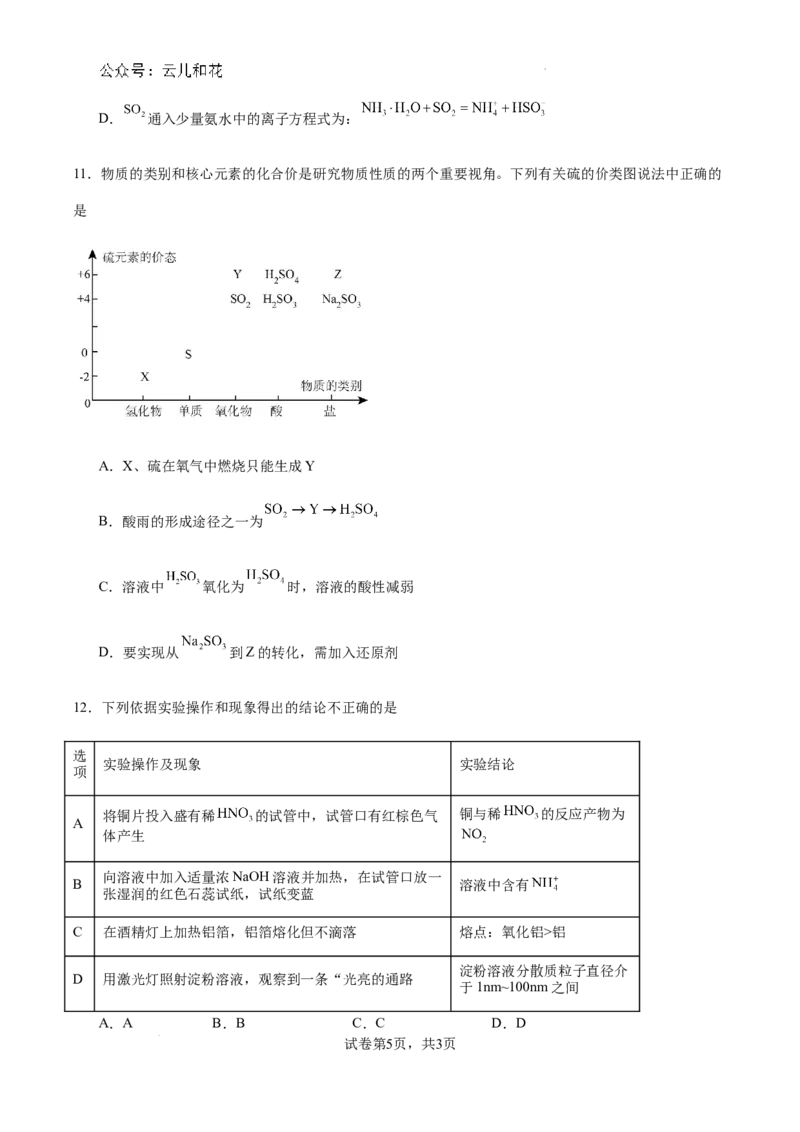
11.物质的类别和核心元素的化合价是研究物质性质的两个重要视角。下列有关硫的价类图说法中正确的
是
A.X、硫在氧气中燃烧只能生成Y
B.酸雨的形成途径之一为
C.溶液中 氧化为 时,溶液的酸性减弱
D.要实现从 到Z的转化,需加入还原剂
12.下列依据实验操作和现象得出的结论不正确的是
选
实验操作及现象 实验结论
项
将铜片投入盛有稀 的试管中,试管口有红棕色气 铜与稀 的反应产物为
A
体产生
向溶液中加入适量浓NaOH溶液并加热,在试管口放一
B 溶液中含有
张湿润的红色石蕊试纸,试纸变蓝
C 在酒精灯上加热铝箔,铝箔熔化但不滴落 熔点:氧化铝>铝
淀粉溶液分散质粒子直径介
D 用激光灯照射淀粉溶液,观察到一条“光亮的通路
于1nm~100nm之间
A.A B.B C.C D.D
试卷第5页,共3页
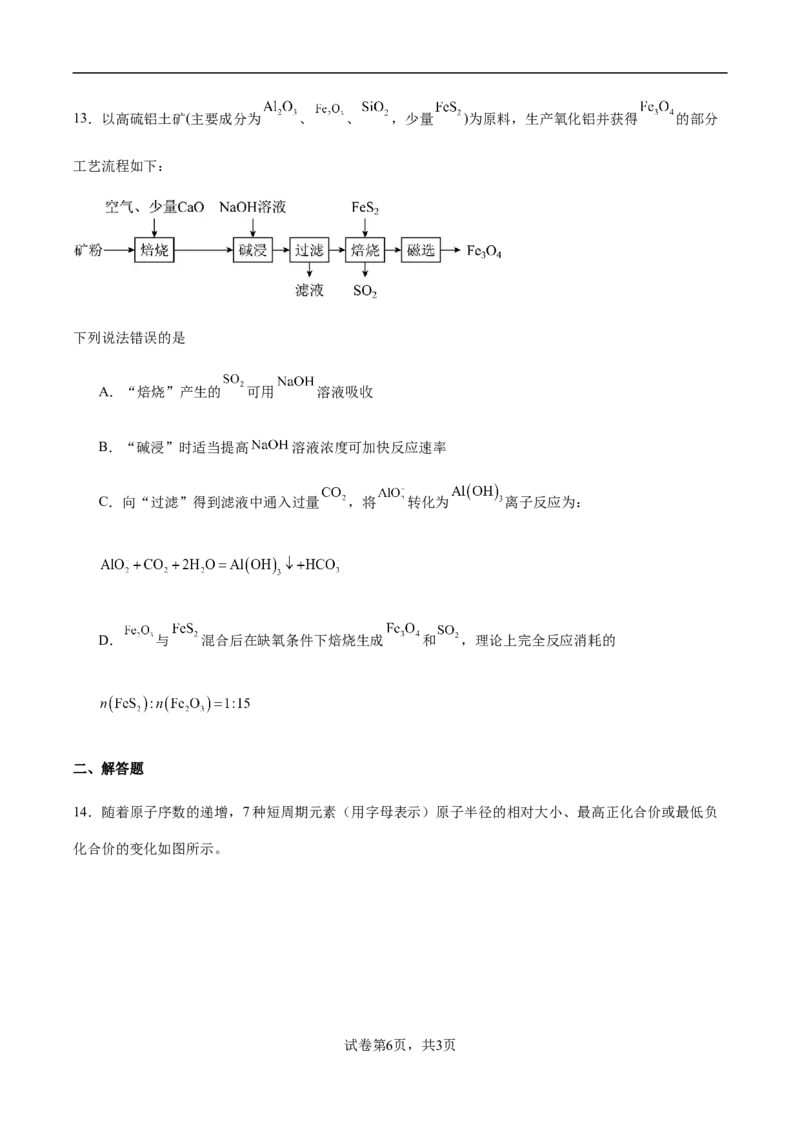
学科网(北京)股份有限公司13.以高硫铝土矿(主要成分为 、 、 ,少量 )为原料,生产氧化铝并获得 的部分
工艺流程如下:
下列说法错误的是
A.“焙烧”产生的 可用 溶液吸收
B.“碱浸”时适当提高 溶液浓度可加快反应速率
C.向“过滤”得到滤液中通入过量 ,将 转化为 离子反应为:
D. 与 混合后在缺氧条件下焙烧生成 和 ,理论上完全反应消耗的
二、解答题
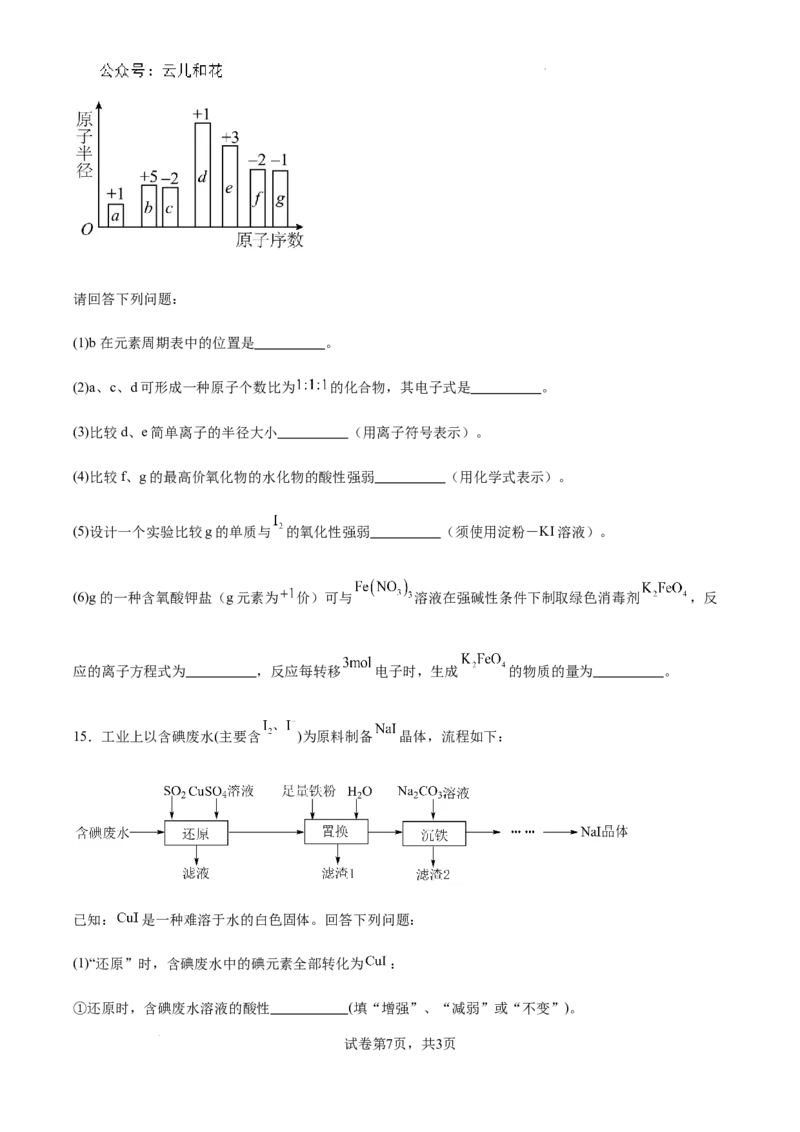
14.随着原子序数的递增,7种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负
化合价的变化如图所示。
试卷第6页,共3页请回答下列问题:
(1)b在元素周期表中的位置是 。
(2)a、c、d可形成一种原子个数比为 的化合物,其电子式是 。
(3)比较d、e简单离子的半径大小 (用离子符号表示)。
(4)比较f、g的最高价氧化物的水化物的酸性强弱 (用化学式表示)。
(5)设计一个实验比较g的单质与 的氧化性强弱 (须使用淀粉-KI溶液)。
(6)g的一种含氧酸钾盐(g元素为 价)可与 溶液在强碱性条件下制取绿色消毒剂 ,反
应的离子方程式为 ,反应每转移 电子时,生成 的物质的量为 。
15.工业上以含碘废水(主要含 )为原料制备 晶体,流程如下:
已知: 是一种难溶于水的白色固体。回答下列问题:
(1)“还原”时,含碘废水中的碘元素全部转化为 :
①还原时,含碘废水溶液的酸性 (填“增强”、“减弱”或“不变”)。
试卷第7页,共3页
学科网(北京)股份有限公司②检验滤液中存在的主要阴离子的实验方法是 。
(2)“置换”时生成 ,滤渣1的主要成分为 。
(3)“沉铁”时,若溶液碱性太强, 会转化为胶状物吸附 ,造成损失。则 溶液与 溶液的
加料方式为 。
a. 溶液逐滴加入 溶液中
b. 溶液逐滴加入 溶液
(4)向 (强酸)酸化的 的 溶液中通一定量空气,溶液呈黄色。用 萃取,下层 为无色;
取萃取后的上层溶液加入淀粉,溶液变蓝色。
①写出溶液呈黄色时发生的离子方程式 。
②查阅相关资料得知,上述实验中下层 为无色,是因为生成的 易溶解于 溶液中,请设计实验验
证这个结论 。(必须选用的试剂为:碘水、 溶液)
16.工业烟气中的 会造成环境问题。可通过多种方法进行脱除并获得含硫产品,实现 资源化利用。
(1)“氨脱硫法”。将含有 的烟气通入过量氨水中,写出发生主要反应的化学方程式: 。
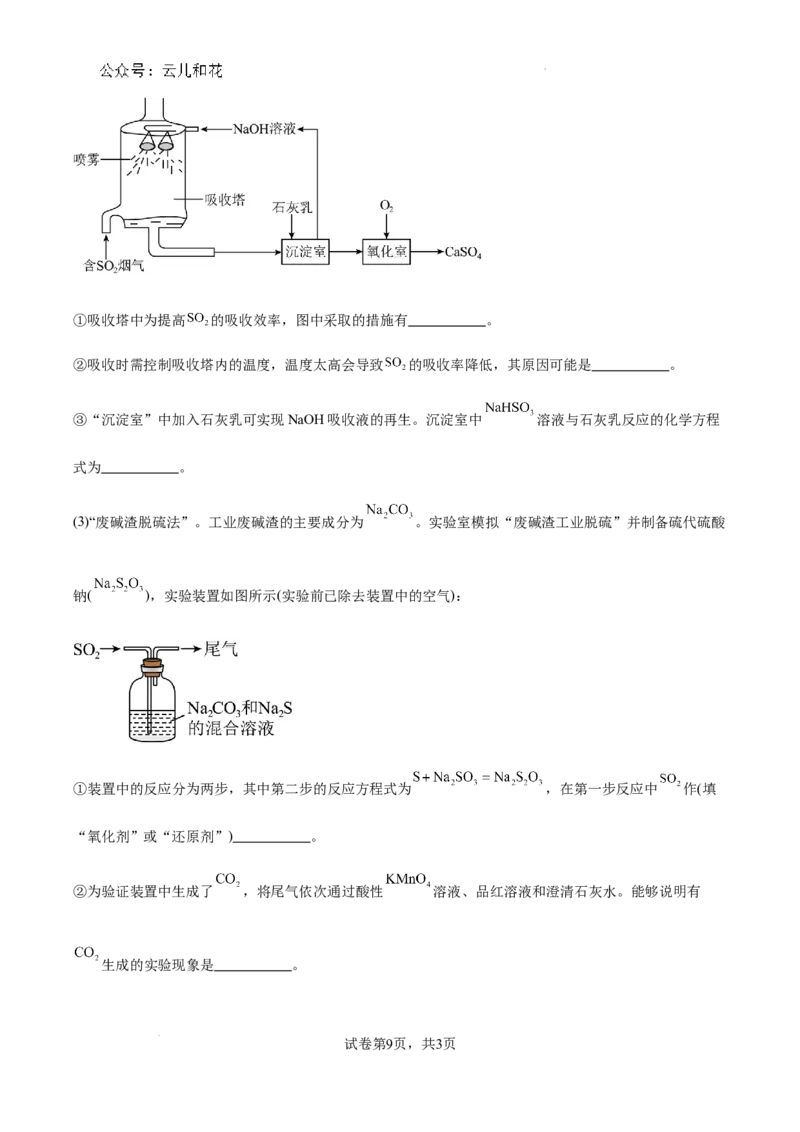
(2)“钠钙双碱脱硫法”。其部分工艺流程如图所示:
试卷第8页,共3页①吸收塔中为提高 的吸收效率,图中采取的措施有 。
②吸收时需控制吸收塔内的温度,温度太高会导致 的吸收率降低,其原因可能是 。
③“沉淀室”中加入石灰乳可实现NaOH吸收液的再生。沉淀室中 溶液与石灰乳反应的化学方程
式为 。
(3)“废碱渣脱硫法”。工业废碱渣的主要成分为 。实验室模拟“废碱渣工业脱硫”并制备硫代硫酸
钠( ),实验装置如图所示(实验前已除去装置中的空气):
①装置中的反应分为两步,其中第二步的反应方程式为 ,在第一步反应中 作(填
“氧化剂”或“还原剂”) 。
②为验证装置中生成了 ,将尾气依次通过酸性 溶液、品红溶液和澄清石灰水。能够说明有
生成的实验现象是 。
试卷第9页,共3页
学科网(北京)股份有限公司③ 可用于去除水中的 得到含硫酸盐的酸性溶液,该反应的离子方程式为 。
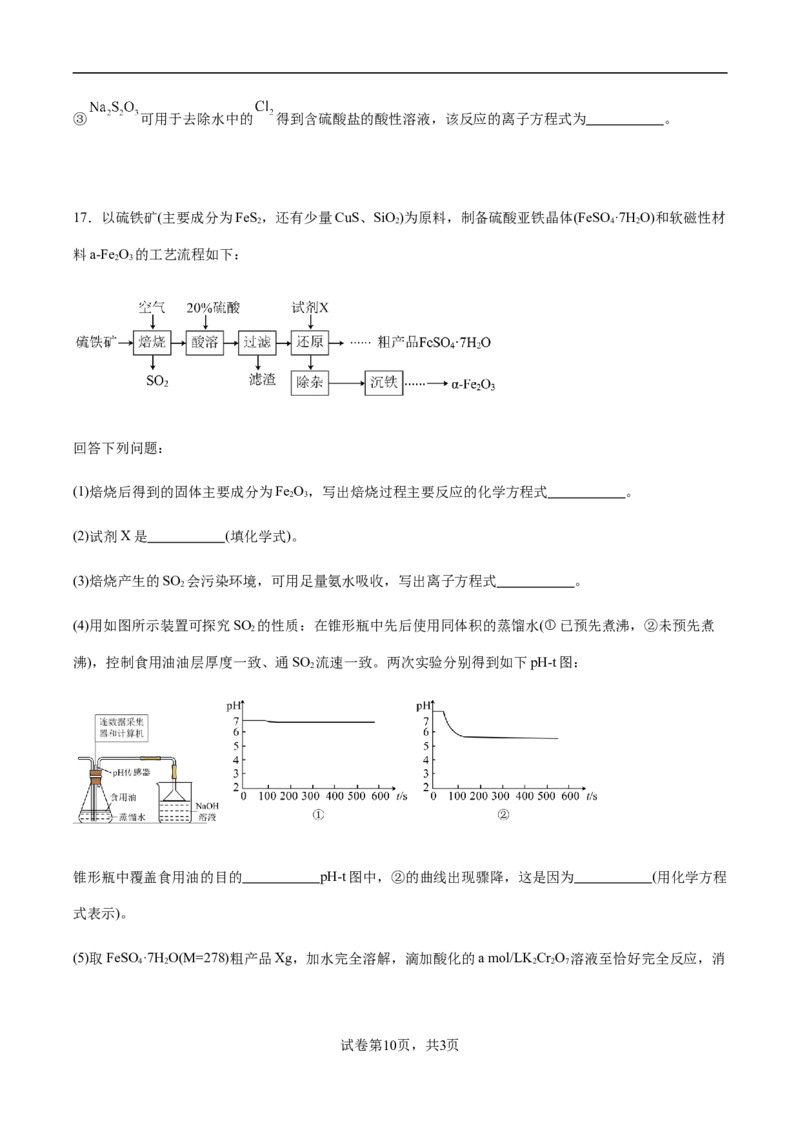
17.以硫铁矿(主要成分为FeS,还有少量CuS、SiO)为原料,制备硫酸亚铁晶体(FeSO ·7H O)和软磁性材
2 2 4 2
料a-Fe O 的工艺流程如下:
2 3
回答下列问题:
(1)焙烧后得到的固体主要成分为Fe O,写出焙烧过程主要反应的化学方程式 。
2 3
(2)试剂X是 (填化学式)。
(3)焙烧产生的SO 会污染环境,可用足量氨水吸收,写出离子方程式 。
2
(4)用如图所示装置可探究SO 的性质:在锥形瓶中先后使用同体积的蒸馏水(①已预先煮沸,②未预先煮
2
沸),控制食用油油层厚度一致、通SO 流速一致。两次实验分别得到如下pH-t图:
2
锥形瓶中覆盖食用油的目的 pH-t图中,②的曲线出现骤降,这是因为 (用化学方程
式表示)。
(5)取FeSO ·7H O(M=278)粗产品Xg,加水完全溶解,滴加酸化的a mol/LKCr O 溶液至恰好完全反应,消
4 2 2 2 7
试卷第10页,共3页耗KCr O 溶液bmL(已知Cr O 被还原为Cr3+),则FeSO ·7H O的纯度为 。
2 2 7 2 4 2
(6)“沉铁”操作时,将提纯后的FeSO 溶液与氨水-NH HCO 混合溶液反应,生成FeCO 沉淀。
4 4 3 3
①生成FeCO 沉淀的离子方程式为 。
3
②以FeSO 溶液、氨水-NH HCO 混合溶液为原料,制备FeCO 的实验方案为:边搅拌边缓慢向FeSO 溶液
4 4 3 3 4
中滴加氨水NH HCO 混合溶液, ;静置后 所得沉淀用蒸馏水洗涤2~3次;
4 3
,干燥。【Fe(OH) 开始沉淀的pH=6.5,FeCO 沉淀需“洗涤完全”,实验中须使用的实验仪器为pH计,
2 3
选用的试剂有:稀盐酸、稀硫酸、BaCl 溶液、NaOH溶液】。
2
试卷第11页,共3页
学科网(北京)股份有限公司