文档内容
余姚中学 2024 学年第二学期期中检测高一化学(选考)试卷
命题教师:王琦凯 审题教师:张建勤
本试题卷分选择题和非选择题两部分,满分 100分,考试时间 90分钟。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5 K-39
Ca-40 Fe-56 Cu-64 Ag-108 I-127 Ba-137
一、选择题(本大题共 25小题,每题 2分,总共 50分。每个小题列出的四个备选项中只有一
个是符合题目要求的,不选、多选、错选均不得分)
1.下列表示方法正确的是( )
分子的空间填充模型: 四氯化碳分子的电子式:
���� �
乙烯的结构简式: 丙烷分子的球棍模型:
� ������ �
A. B. C. D.
2.汽车剧烈碰撞时,安全气囊中发生反应: 。若氧化产物比还
�� ��� ���� ��
原产物多 ,则下列判断正确的是( )
1��⺁����h��� �h�����⺁���1��� �
A.生成 标准状况 B.有 被氧化
�若8化产物
C.转移电子的物质的量为 D.被氧化的 原子的物质的量为
��若8�撞���� � �若�化产物�h���
3.用 表示阿伏加德罗常数的值。下列叙述正确的是( )
�若�化产物 � �化产物
A.钠作除水剂时,每消耗 ,生成 的分子数为
��
B.工业合成氨时,每反应 标准状况下 ,生成的极性共价键数目为
1化产物�⺁ �� ��
C.60g冰醋酸晶体中,含阴离子数目为
��若�撞� ��� ���
D.明矾净水时, 形成的 胶粒的数目为
��
4. 年 月 日,嫦娥 号��在长征 号火箭巨大的推力下前往月球,经过 多天旅程后带着月壤返
�撞�若��化产物晶撞�物 �物����� �若1��
回。这是中国航天“探月工程”向世界展示出的“中国力量”,下列有关说法正确的是( )
���� 11 �� � � ��
A.月壤中含有珍贵的3He,它与地球上的4He互为同素异形体
B.火箭采用液氢、煤油、液氧作为推进剂,液氢、煤油、液氧都属于纯净物
C.登月中所用北斗系统的导航卫星,其计算机芯片材料是高纯度的二氧化硅
D.航天员穿的航天服具有“耐热性、耐高低温、抗静电”等特点,它可能使用了多种合成纤维
5.下列化学或离子方程式不正确的是( )
A.过氧化钠与水反应:
B.过量铁与稀硝酸的反应:
��⺁�����������⺁����� �
C. 通入氯水中漂白作用减弱: � � ��
�ܨ��8� ����� ��ܨ� ���� ������
� �� �
��� �����物��������� 浓硫 � 酸 ��� ���物
D.硬脂酸与乙醇的酯化反应:
6.分子式为 的有机物共 � 有1��不��含 �� 立 � 体 � 异 � 构 ����( 18 �)� �� �1�������������� 18 �
A. 种 B. 种 C. 种 D. 种
���8�物� � �
� 8 � 1�
第 页,共 页
1 87.下列说法正确的是 ( )
A.大豆蛋白纤维属于天然纤维
B.为了提高橡胶的强度可以用硫与橡胶作用,硫原子和高分子链之间形成分子间作用力
C.聚甲基丙烯酸甲酯俗称有机玻璃,可用于制备光学仪器
D.植物油含较多的饱和脂肪酸甘油酯,熔点较低
8.下列叙述正确的是 ( )
A.甲醇既可发生取代反应也可发生加成反应 B.用饱和碳酸氢钠溶液可以鉴别乙酸和乙醇
C.含有苯环的化合物称为芳香烃 D.戊二烯与环戊烷互为同分异构体
9.1,1-联环戊烯( )是重要的有机合成中间体。下列关于该有机物的说法错误的是 ( )
A. 分子式为C H ,属于不饱和烃 B.能使酸性高锰酸钾溶液和溴水褪色,且褪色原理不同
10 14
C. 能与溴发生取代反应 D.最多和2molH 发生加成反应
2
10.已知常温常压下,断裂下列气态分子的化学键需要吸收的能量: 为 , 为
, 为 。下列说法中正确的是 ( ) �1
��� �����t�化产物 ܨ�ܨ
A. 与 反�应1的热化学方程式为 �1
1����t�化产物 ��ܨ �����t�化产物
B. 气体分解成 和 吸收 的热量
�� ܨ� �� � �ܨ� � ���ܨ � ������1�t
C. 与 反应生成 液态 放出的热量小于
��若8�撞��ܨ ��若��撞�� ��若��撞ܨ� ��1��t
D.在相同条件下, 与 的能量总和大于 气体的能量
1�化产物����� 1�化产物ܨ���� ��化产物 �ܨ ��1��t
11.通过以下反应可获得新型能源二甲醚 。下列说法不正确的是 ( )
1�化产物����� 1�化产物ܨ���� ��化产物��ܨ���
���������
�1
������������������������� ��1 �⺁�t�化产物
�1
��������������������������� ��� �t�t�化产物
�1
������������������������������� ��� �t�t�化产物
A.反应 为反应 提供原料气 �1
����������������������������� ��� �t�t�化产物
B.反应 是 资源化利用的方法之一
���� ��
C.已知��>0,�则�反� 应 的
1 1 t �1
D.反应t ��������� ������������的�����物� ��� � �t�化产物
12.利用CO (g)与H (g)反应生成CH OCH (g)和H O(g)有利于实现碳中和,其反应�过1程中的能量变化如图所
���2�����2������������3 ����3�����2�� ��� �t��t�t �t�化产物
示。下列有关说法正确的是( )
A.若该反应在绝热密闭容器中进行,则反应过程中体系温度会降低
B.1molH (g)在O (g)中完全燃烧生成H O(g)时放出的热量大于20.45kJ
2 2 2
C.若反应消耗0.4molCO (g)和1.2molH (g),则该反应放出49.08kJ热量
2 2
D.CH OCH (g)+3H O(g)=2CO (g)+6H (g) ΔH=-122.7kJ·mol-1
3 3 2 2 2
第 页,共 页
� 813.电池是人类生产和生活中的重要能量来源,各式各样电池的发展是化学对人类的一大贡献。下列有关电
池的叙述正确的是( )
A.碱性锌锰电池比普通锌锰电池的性能更好
B.氢氧燃料电池工作时氢气在正极被氧化
C.铅蓄电池在放电过程中,负极质量减少,正极质量增加
D.镍氢电池、锂离子电池和锌锰干电池都是二次电池
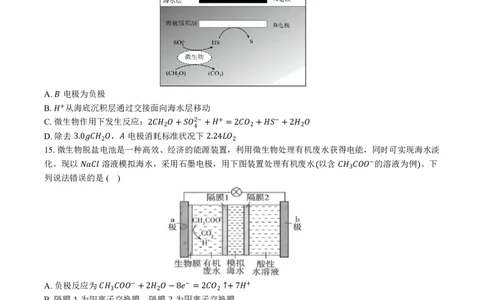
14.“海泥电池”既可用于深海水下仪器的电源补给,又有利于海洋环境污染治理。电池工作原理如图所示,
其中微生物代谢产物显酸性。下列说法错误的是 ( )
A. 电极为负极
B. 从海底沉积层通过交接面向海水层移动
�
C.微�生物作用下发生反应:
�
D.除去 , 电极消
��
耗
�
标
��
准
�
状
�
况
��
�下�
��
�
��������
�
�����
15.微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡
�若������ � �若��撞��
化。现以 溶液模拟海水,采用石墨电极,用下图装置处理有机废水 以含 的溶液为例 。下
列说法错误的是 ( ) �
�⺁�物 � ������ �
A.负极反应为
B.隔膜 为阳离
��
子
��
交
�
换
�
�膜
�
,
�
隔
��
膜
��
为
8�
阴� 离
�
子
��
交
��
换
�
膜
���
�
C.当电路中转移 电子时,模拟海水理论上除盐
1 �
D.电池工作一段时间后,正、负极产生气体的物质的量之比为
1化产物 �8若��
16.已知反应X(g)+3Y(g) 2Z(g) ΔH=-akJ·mol-1,一定条件下,1molX和3molY在2L恒容密闭容器中
�t1
发生反应,10min时测得Y的物质的量为2.4mol。下列说法正确的是( )
A. 10min时,容器内的压强是反应前的0.9倍
B.10min时,X的转化率为80%
C.0~10min内,用Y表示的平均反应速率为0.06mol∙L-1∙min-1
D.前5min内,X和Y反应放出的热量等于0.1akJ
第 页,共 页
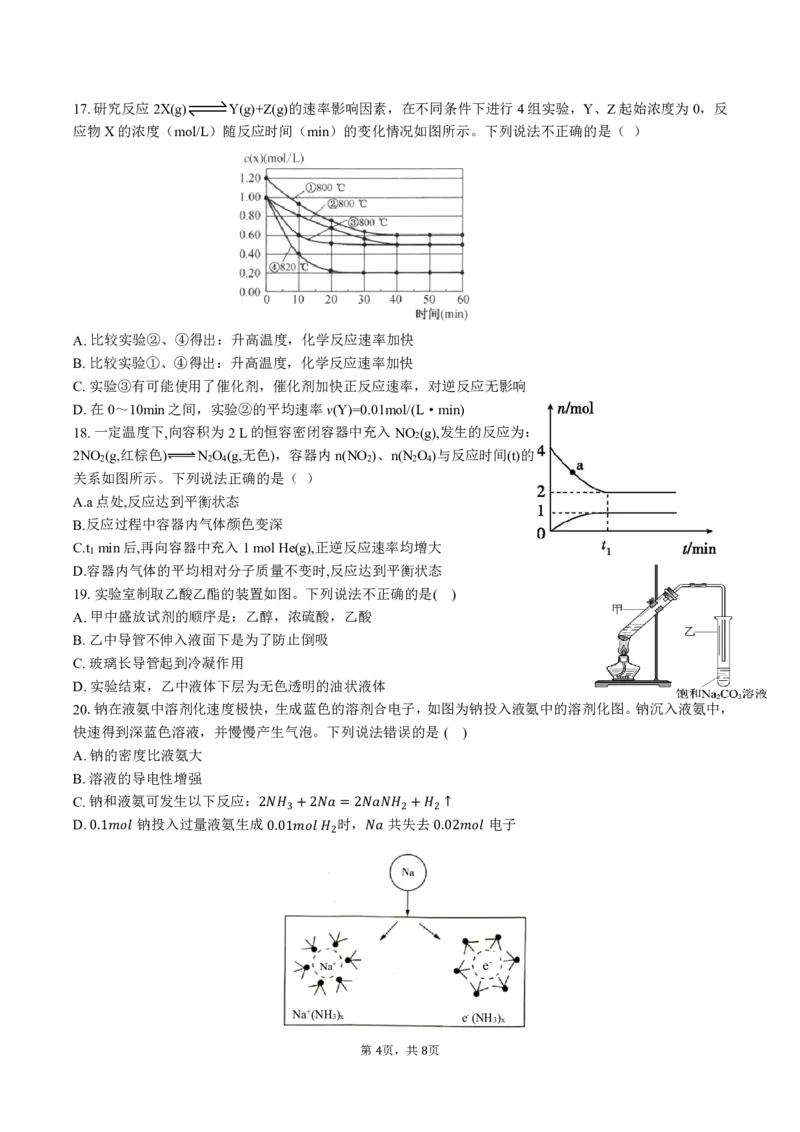
� 817.研究反应2X(g) Y(g)+Z(g)的速率影响因素,在不同条件下进行4组实验,Y、Z起始浓度为0,反
应物X的浓度(mol/L)随反应时间(min)的变化情况如图所示。下列说法不正确的是( )
A.比较实验②、④得出:升高温度,化学反应速率加快
B.比较实验①、④得出:升高温度,化学反应速率加快
C.实验③有可能使用了催化剂,催化剂加快正反应速率,对逆反应无影响
D.在0~10min之间,实验②的平均速率v(Y)=0.01mol/(L·min)
18.一定温度下,向容积为2L的恒容密闭容器中充入NO (g),发生的反应为:
2
2NO (g,红棕色) N O (g,无色),容器内n(NO )、n(N O )与反应时间(t)的
2 2 4 2 2 4
关系如图所示。下列说法正确的是( )
A.a点处,反应达到平衡状态
B.反应过程中容器内气体颜色变深
C.t min后,再向容器中充入1molHe(g),正逆反应速率均增大
1
D.容器内气体的平均相对分子质量不变时,反应达到平衡状态
19.实验室制取乙酸乙酯的装置如图。下列说法不正确的是( )
A.甲中盛放试剂的顺序是:乙醇,浓硫酸,乙酸
B.乙中导管不伸入液面下是为了防止倒吸
C.玻璃长导管起到冷凝作用
D.实验结束,乙中液体下层为无色透明的油状液体
20.钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,如图为钠投入液氨中的溶剂化图。钠沉入液氨中,
快速得到深蓝色溶液,并慢慢产生气泡。下列说法错误的是 ( )
A.钠的密度比液氨大
B.溶液的导电性增强
C.钠和液氨可发生以下反应:
D. 钠投入过量液氨生成 时, 共失去 电子
�������⺁���⺁������ �
�若1化产物 �若�1化产物��� �⺁ �若��化产物
Na+ e-
Na+(NH3)x e-(NH3)x
第 页,共 页
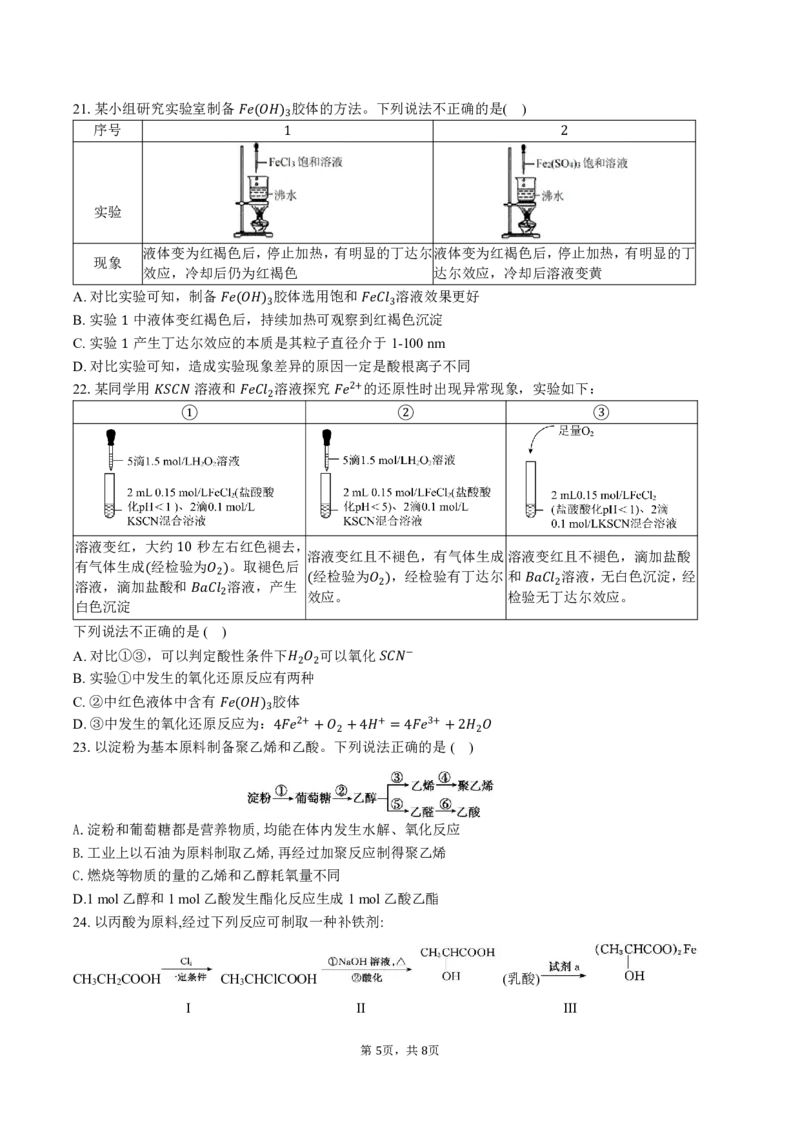
� 821.某小组研究实验室制备 胶体的方法。下列说法不正确的是( )
序号
ܨ������
1 �
实验
液体变为红褐色后,停止加热,有明显的丁达尔液体变为红褐色后,停止加热,有明显的丁
现象
效应,冷却后仍为红褐色 达尔效应,冷却后溶液变黄
A.对比实验可知,制备 胶体选用饱和 溶液效果更好
B.实验 中液体变红褐色后,持续加热可观察到红褐色沉淀
ܨ������ ܨ��物�
C.实验 产生丁达尔效应的本质是其粒子直径介于1-100nm
1
D.对比实验可知,造成实验现象差异的原因一定是酸根离子不同
1
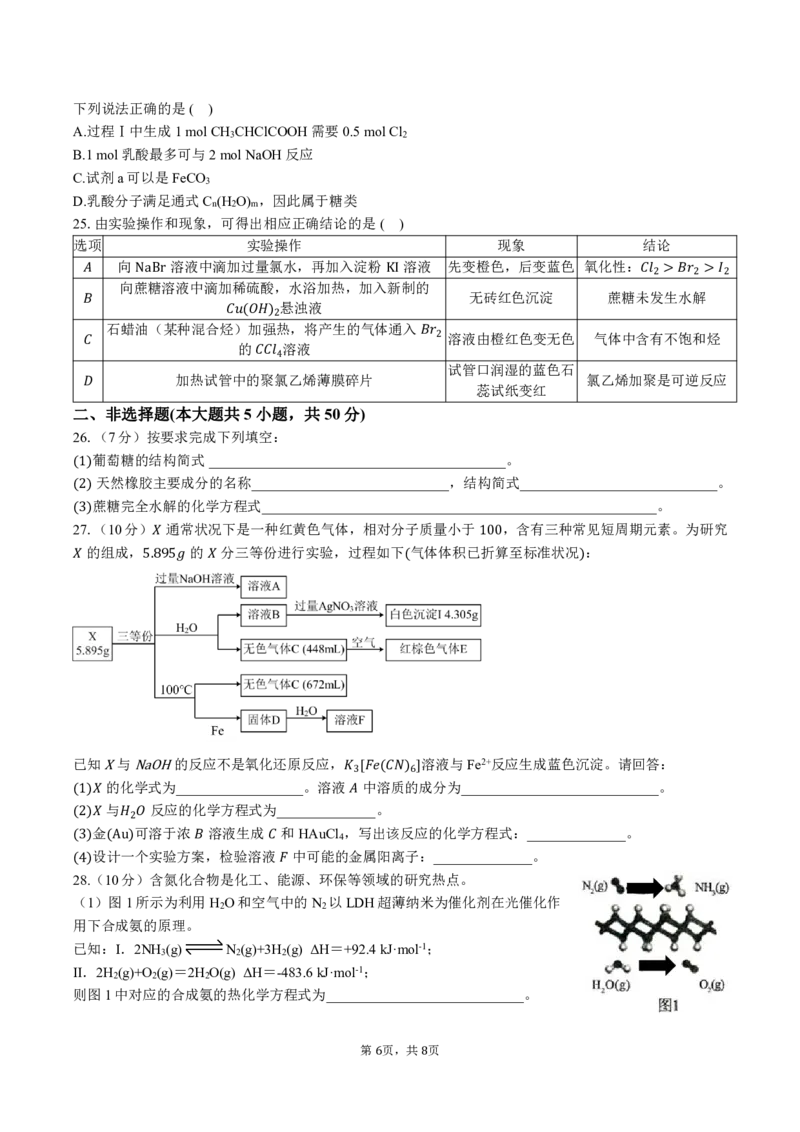
22.某同学用 溶液和 溶液探究 的还原性时出现异常现象,实验如下:
��
h��� ܨ��物� ܨ�
� � �
溶液变红,大约 秒左右红色褪去,
溶液变红且不褪色,有气体生成溶液变红且不褪色,滴加盐酸
有气体生成 经检验为 。取褪色后
1� 经检验为 ,经检验有丁达尔和 溶液,无白色沉淀,经
溶液,滴加盐酸和 溶液,产生
� ��� 效应。 检验无丁达尔效应。
白色沉淀 � ��� �⺁�物�
�⺁�物�
下列说法不正确的是( )
A.对比①③,可以判定酸性条件下 可以氧化
B.实验①中发生的氧化还原反应有两种 �
���� ���
C.②中红色液体中含有 胶体
D.③中发生的氧化还原反应为:
ܨ������
23.以淀粉为基本原料制备聚乙烯和乙��酸。下列说法� 正确的�是� ( )
�ܨ� ������ ��ܨ� �����
A.淀粉和葡萄糖都是营养物质,均能在体内发生水解、氧化反应
B.工业上以石油为原料制取乙烯,再经过加聚反应制得聚乙烯
C.燃烧等物质的量的乙烯和乙醇耗氧量不同
D.1mol乙醇和1mol乙酸发生酯化反应生成1mol乙酸乙酯
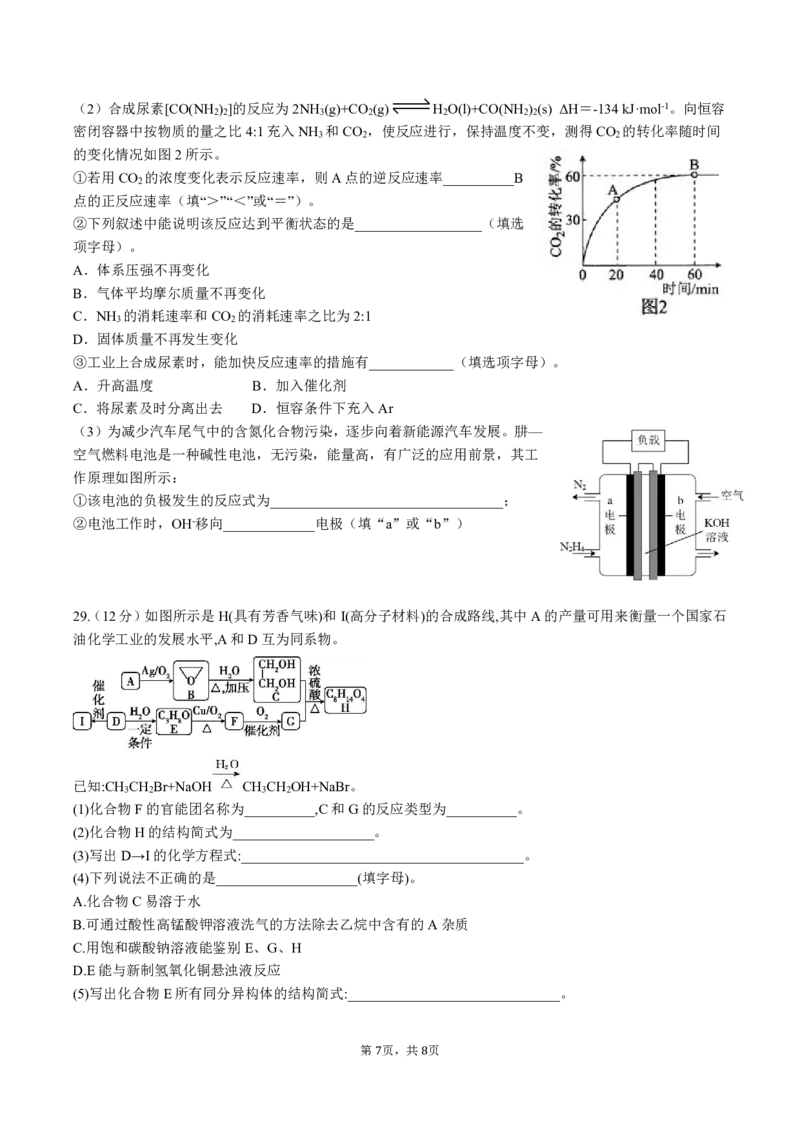
24.以丙酸为原料,经过下列反应可制取一种补铁剂:
CH CH COOH CH CHClCOOH (乳酸)
3 2 3
I II III
第 页,共 页
� 8下列说法正确的是( )
A.过程Ⅰ中生成1molCH CHClCOOH需要0.5molCl
3 2
B.1mol乳酸最多可与2molNaOH反应
C.试剂a可以是FeCO
3
D.乳酸分子满足通式C (H O) ,因此属于糖类
n 2 m
25.由实验操作和现象,可得出相应正确结论的是 ( )
选项 实验操作 现象 结论
向 溶液中滴加过量氯水,再加入淀粉 溶液 先变橙色,后变蓝色 氧化性:
向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的
� NaBr KI 无砖红色沉淀 蔗糖未�物发� �生�水�解� ���
悬浊液
� 石蜡油(某种混合烃)加强热,将产生的气体通入
�t����� 溶液由橙红色变无色 气体中含有不饱和烃
的 溶液
���
� 试管口润湿的蓝色石
加热试管中的�聚�物氯� 乙烯薄膜碎片 氯乙烯加聚是可逆反应
蕊试纸变红
二�、非选择题(本大题共5小题,共 50分)
26.(7分)按要求完成下列填空:
葡萄糖的结构简式 __________________________________________。
天然橡胶主要成分的名称____________________________,结构简式____________________________。
�1�
蔗糖完全水解的化学方程式________________________________________________________。
���
27.(10分) 通常状况下是一种红黄色气体,相对分子质量小于 ,含有三种常见短周期元素。为研究
���
的组成, 的 分三等份进行实验,过程如下 气体体积已折算至标准状况 :
� 1��
� �若8��� � � �
已知 与 的反应不是氧化还原反应, 溶液与Fe2+反应生成蓝色沉淀。请回答:
的化学式为__________________。溶液 中溶质的成分为____________________________。
X NaOH h��ܨ�������
与 反应的化学方程式为______________。
�1�� �
金 可溶于浓 溶液生成 和HAuCl ,写出该反应的化学方程式:______________。
���� ��� 4
设计一个实验方案,检验溶液 中可能的金属阳离子:______________。
��� �Au� � �
28.(10分)含氮化合物是化工、能源、环保等领域的研究热点。
��� ܨ
(1)图1所示为利用H O和空气中的N 以LDH超薄纳米为催化剂在光催化作
2 2
用下合成氨的原理。
已知:I.2NH (g) N (g)+3H (g) ΔH=+92.4kJ·mol-1;
3 2 2
Ⅱ.2H (g)+O (g)=2H O(g) ΔH=-483.6kJ·mol-1;
2 2 2
则图1中对应的合成氨的热化学方程式为____________________________。
第 页,共 页
� 8(2)合成尿素[CO(NH ) ]的反应为2NH (g)+CO (g) H O(l)+CO(NH ) (s) ΔH=-134kJ·mol-1。向恒容
2 2 3 2 2 2 2
密闭容器中按物质的量之比4:1充入NH 和CO ,使反应进行,保持温度不变,测得CO 的转化率随时间
3 2 2
的变化情况如图2所示。
①若用CO 的浓度变化表示反应速率,则A点的逆反应速率__________B
2
点的正反应速率(填“>”“<”或“=”)。
②下列叙述中能说明该反应达到平衡状态的是__________________(填选
项字母)。
A.体系压强不再变化
B.气体平均摩尔质量不再变化
C.NH 的消耗速率和CO 的消耗速率之比为2:1
3 2
D.固体质量不再发生变化
③工业上合成尿素时,能加快反应速率的措施有____________(填选项字母)。
A.升高温度 B.加入催化剂
C.将尿素及时分离出去 D.恒容条件下充入Ar
(3)为减少汽车尾气中的含氮化合物污染,逐步向着新能源汽车发展。肼—
空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,其工
作原理如图所示:
①该电池的负极发生的反应式为_________________________________;
②电池工作时,OH-移向_____________电极(填“a”或“b”)
29.(12分)如图所示是H(具有芳香气味)和I(高分子材料)的合成路线,其中A的产量可用来衡量一个国家石
油化学工业的发展水平,A和D互为同系物。
已知:CH CH Br+NaOH CH CH OH+NaBr。
3 2 3 2
(1)化合物F的官能团名称为__________,C和G的反应类型为__________。
(2)化合物H的结构简式为____________________。
(3)写出D→I的化学方程式:________________________________________。
(4)下列说法不正确的是____________________(填字母)。
A.化合物C易溶于水
B.可通过酸性高锰酸钾溶液洗气的方法除去乙烷中含有的A杂质
C.用饱和碳酸钠溶液能鉴别E、G、H
D.E能与新制氢氧化铜悬浊液反应
(5)写出化合物E所有同分异构体的结构简式:______________________________。
第 页,共 页
� 8(6)根据题目所给信息,以A为原料,设计一条不同于上述题干中合成C的反应路线。(用流程图表示,流程写法
参照上述题干中流程,无机试剂任选)。
30.(11分)某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如图所示:
I.取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu (OH) CO ]。
2 2 3
Ⅱ.将洗涤后的铜丝做成匝数较多的螺旋状。
Ⅲ.按如图所示装置连接仪器、检查气密性、装入化学试剂。
(1)过程I发生反应的离子方程式是__________________________。
(2)写出过程Ⅲ中检查气密性的方法__________________________。
(3)过程Ⅲ的后续操作如下:
①打开止水夹a和b,轻推注射器,使浓硝酸与铜丝接触后关闭a,观察到的现象是________________,一
段时间后使反应停止的操作是____________________________________,关闭a,取下注射器.
②打开b和分液漏斗活塞,当玻璃管充满稀硝酸后,关闭分液漏斗活塞,观察到有无色气泡产生,反应的
离子方程式是______________________,稀硝酸充满玻璃管的实验目的是__________________________。
(4)另取3支盛满NO 气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的
2
高度明显不一致。结果如表所示(忽略温度对气体体积的影响):
实验编号 水温/℃ 液面上升高度
1 25 超过试管的2/3
2 50 不足试管的2/3
3 0 液面上升超过实验1
①根据上表得出的结论是温度越______(填“高”或“低”),进入试管中的溶液越多。
②查阅资料:
a.NO 与水反应的实际过程为:2NO +H O=HNO +HNO ,3HNO =HNO +2NO↑+H O;
2 2 2 3 2 2 3 2
b.HNO 不稳定。
2
则产生上述现象的原因是________________________________________________________。
第 页,共 页
8 8