文档内容
2024-2025学年高一协作体期中联考
化学试卷
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5 Mn-55
第Ⅰ卷(选择题 共42 分)
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1. 下列有关说法或解释不合理的是
A.《本草经集注》记载区分硝石(KNO )和朴消(Na SO )方法:“以火烧之,紫青烟起,乃真硝石
3 2 4
也”,这是古人利用焰色试验鉴别物质
B.《神农本草经》中记载的石胆能化铁为“铜”,该过程涉及氧化还原反应
C.活字印刷胶泥的成分CaO、Al O ,两者都是碱性氧化物,同时也是金属氧化物
2 3
D.《周礼》中记载沿海古人“煤饼烧蛎房成灰”(“蛎房”即指牡蛎壳之类的贝壳),并把这种灰称
为“蜃”,“蜃”的主要成分可以作干燥剂
2. 下列物质转化(“→”表示一种物质转化为另一种物质)中,每次转化只通过一步反应,不可能全部实
现的是
A.H O →O →CO →H CO B.NaOH→NaNO →Na CO →NaCl
2 2 2 2 2 3 3 2 3
C.CaCO →CaO→Ca(OH) →NaOH D.Mg→MgCl →Mg(OH) →Mg(NO )
3 2 2 2 3 2
3. 下列关于分散系的说法错误的是
A.《江楼夜话》中“江雾秋楼白,灯花夜雨青”,描写的雾是一种气溶胶
B.河流入海处形成三角洲是由于胶体聚沉导致
C.硫酸铜溶液和液氯都是分散系,均属于溶液
D.浊液与溶液的本质区别是分散质粒子直径大小不同
1
{#{QQABIQIEogggAAIAABgCUwEwCACQkhCACagGQBAEIAIASBNABAA=}#}4. 下列指定的溶液中,能大量共存的离子组是
A.遇石蕊变红的溶液中:Ca2+、HCO−、NO−、K+ B.碱性溶液中: Fe3+、Cl-、Na+、SO2-
3 3 4
C.与铁反应放氢气的溶液:NO−、Mg2+、Na+、I− D.澄清透明的溶液中:Cu2+、Cl−、Br−、Na+
3
5. 下列反应的离子方程式书写正确的是
A. 澄清石灰水与足量NaHCO 溶液反应:Ca2+ +2OH− +2HCO− =CaCO ↓+CO2− +2H O
3 3 3 3 2
B 将水滴在少量过氧化钠固体上:Na O +2H O=2Na+ +2OH− +O ↑
2 2 2 2
C.向足量的碳酸钠溶液中滴入两滴稀盐酸:CO2-+2H+=CO↑+HO
3 2 2
D. 氯气与水反应:Cl +HO == 2H+ + ClO- +Cl-
2 2
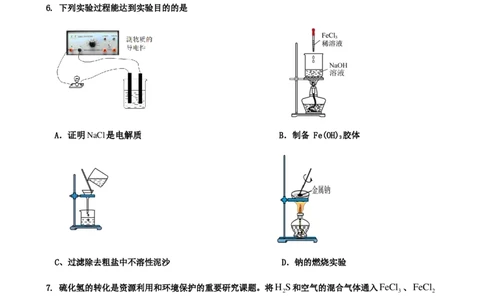
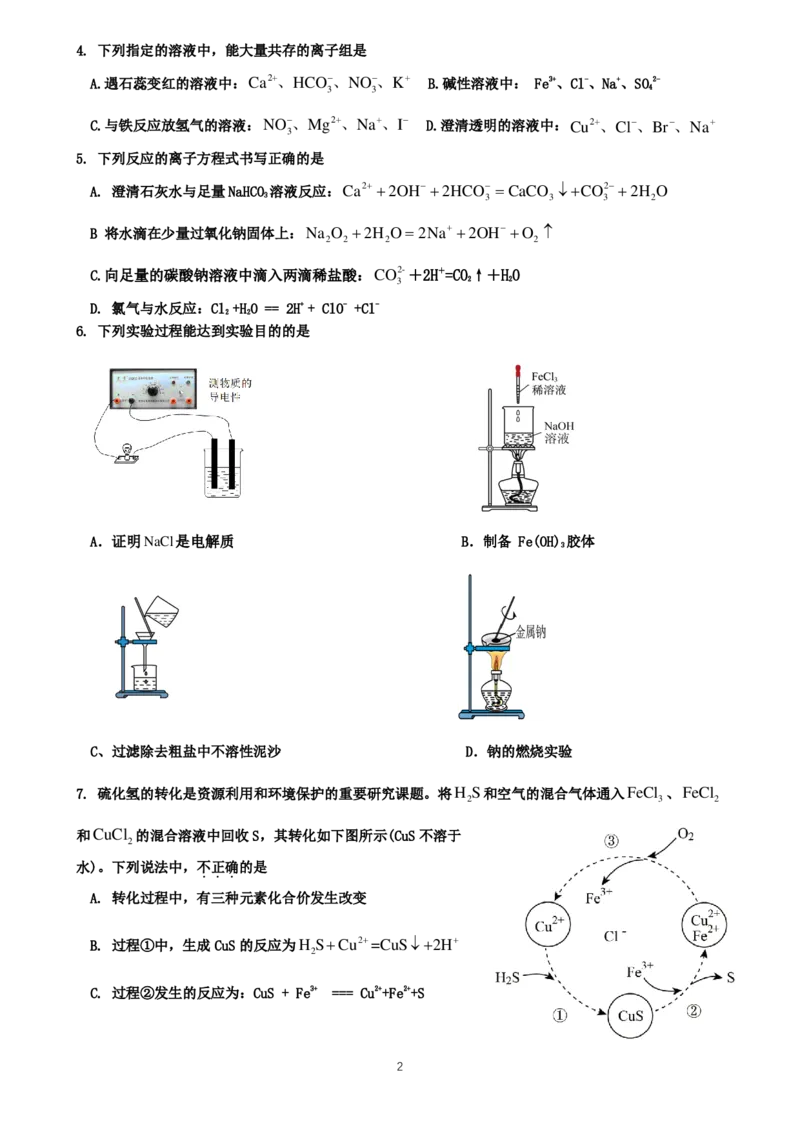
6. 下列实验过程能达到实验目的的是
A.证明NaCl是电解质 B.制备 Fe(OH) 胶体
3
C、过滤除去粗盐中不溶性泥沙 D.钠的燃烧实验
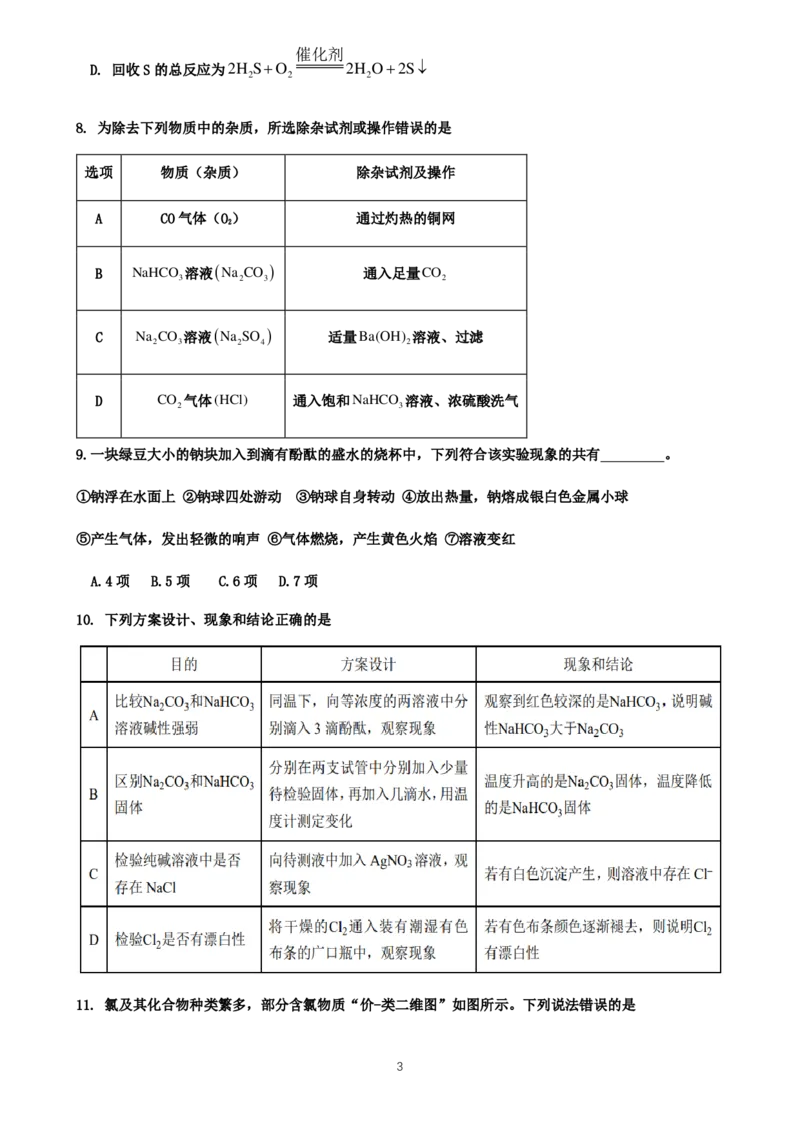
7. 硫化氢的转化是资源利用和环境保护的重要研究课题。将H S和空气的混合气体通入FeCl 、FeCl
2 3 2
和CuCl 的混合溶液中回收S,其转化如下图所示(CuS不溶于
2
水)。下列说法中,不正确的是
...
A. 转化过程中,有三种元素化合价发生改变
B. 过程①中,生成CuS的反应为H S+Cu2+=CuS↓+2H+
2
C. 过程②发生的反应为:CuS + Fe3+ === Cu2++Fe2++S
2
{#{QQABIQIEogggAAIAABgCUwEwCACQkhCACagGQBAEIAIASBNABAA=}#}催化剂
D. 回收S的总反应为2H S+O 2H O+2S↓
2 2 2
8. 为除去下列物质中的杂质,所选除杂试剂或操作错误的是
选项 物质(杂质) 除杂试剂及操作
A CO气体(O) 通过灼热的铜网
2
B NaHCO 溶液(Na CO ) 通入足量CO
3 2 3 2
C Na CO 溶液(Na SO ) 适量Ba(OH) 溶液、过滤
2 3 2 4 2
D CO 气体(HCl) 通入饱和NaHCO 溶液、浓硫酸洗气
2 3
9.一块绿豆大小的钠块加入到滴有酚酞的盛水的烧杯中,下列符合该实验现象的共有 。
①钠浮在水面上 ②钠球四处游动 ③钠球自身转动 ④放出热量,钠熔成银白色金属小球
⑤产生气体,发出轻微的响声 ⑥气体燃烧,产生黄色火焰 ⑦溶液变红
A.4项 B.5项 C.6项 D.7项
10. 下列方案设计、现象和结论正确的是
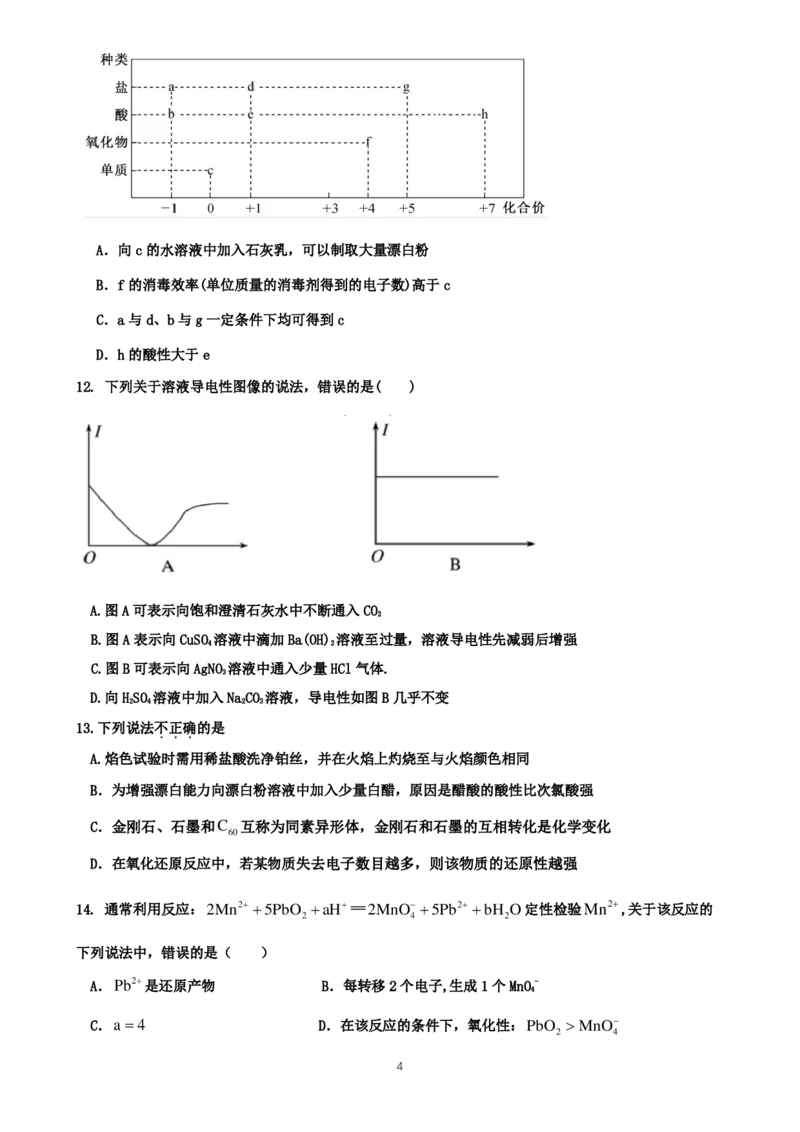
11. 氯及其化合物种类繁多,部分含氯物质“价-类二维图”如图所示。下列说法错误的是
3
{#{QQABIQIEogggAAIAABgCUwEwCACQkhCACagGQBAEIAIASBNABAA=}#}A.向c的水溶液中加入石灰乳,可以制取大量漂白粉
B.f的消毒效率(单位质量的消毒剂得到的电子数)高于c
C.a与d、b与g一定条件下均可得到c
D.h的酸性大于e
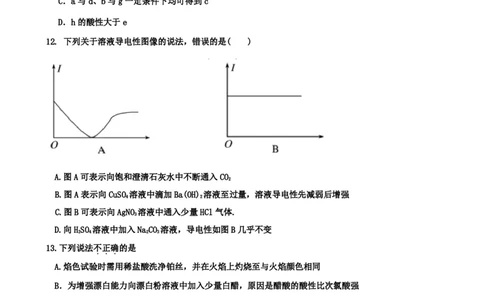
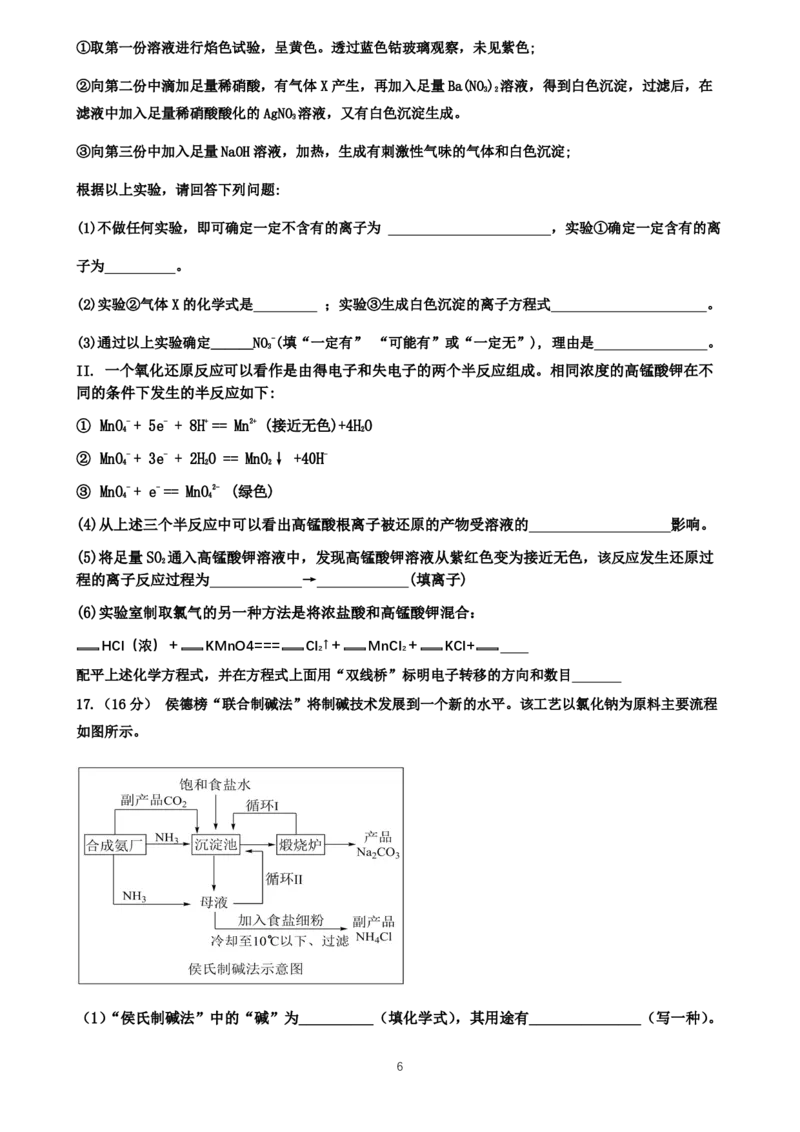
12. 下列关于溶液导电性图像的说法,错误的是( )
A.图A可表示向饱和澄清石灰水中不断通入CO
2
B.图A表示向CuSO 溶液中滴加Ba(OH) 溶液至过量,溶液导电性先减弱后增强
4 2
C.图B可表示向AgNO 溶液中通入少量HCl气体.
3
D.向HSO 溶液中加入NaCO 溶液,导电性如图B几乎不变
2 4 2 3
13.下列说法不正确的是
...
A.焰色试验时需用稀盐酸洗净铂丝,并在火焰上灼烧至与火焰颜色相同
B.为增强漂白能力向漂白粉溶液中加入少量白醋,原因是醋酸的酸性比次氯酸强
C.金刚石、石墨和C 互称为同素异形体,金刚石和石墨的互相转化是化学变化
60
D.在氧化还原反应中,若某物质失去电子数目越多,则该物质的还原性越强
14. 通常利用反应:2Mn2+ +5PbO +aH+ 2MnO− +5Pb2+ +bH O定性检验Mn2+,关于该反应的
2 4 2
下列说法中,错误的是( )
A.Pb2+是还原产物 B.每转移2个电子,生成1个MnO-
4
C.a =4 D.在该反应的条件下,氧化性:PbO >MnO−
2 4
4
{#{QQABIQIEogggAAIAABgCUwEwCACQkhCACagGQBAEIAIASBNABAA=}#}第 II 卷(非选择题 58 分)
二、非选择题(共4题,58分)
15.(15分)I.生活中离不开化学,市面上有许多商品的主要成分是中学化学常见的物质,括号内为商
品的主要成分:
①食盐(NaCl);②料酒(乙醇);③食醋(乙酸);④纯碱(Na CO );⑤小苏打(NaHCO );⑥84消毒液
2 3 3
(NaClO);⑦洁厕灵(HCl);⑧净水剂(明矾);⑨铁锅(Fe) ⑩呼吸面具(NaO)
2 2
回答下列问题:
(1)明矾的化学式为KAl(SO ) ⋅12H O,属于 (填“纯净物”或“混合物”)。
4 2 2
(2)厨卫用品的主要成分(括号内的物质)属于电解质的有 (填序号,下同), 属于盐
的有 。
(3)食醋在水溶液的电离方程式为 。
(4)生活中⑥和⑦不能混用,混用将产生有毒气体,因为
(用离子方程式表示)。
(5)呼吸面具工作原理的化学方程式
II. (1)现有甲、乙、丙三名同学分别进行硅酸胶体的制备实验:
分组 实验操作 实验现象
甲 将1%硅酸钠溶液滴入沸水中,冷却后用激光笔进行照射 无明显现象
向1%硅酸钠溶液中加入几滴酚酞溶液,缓慢滴入稀盐酸,溶液红
乙
色褪去后停止滴加,用激光笔进行照射
未出现“光亮的通路”,
丙 向1%硅酸钠溶液中加入等体积的稀盐酸,用激光笔进行照射
溶液中出现浑浊
已知:硅酸钠(Na SiO )溶液呈碱性,遇酚酞变红;常温下硅酸(H SiO )难溶于水。试回答:乙同学成
2 3 2 3
功制备硅酸胶体,其实验现象是 ,根据三位同学
的实验操作可知,成功制备硅酸胶体的关键在于 ,丙同学实验中出现
浑浊的原因是 。
(2)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。现将制得的硅酸胶体
装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计一个实验证明硅酸胶体中的杂质Cl-已经透过
半透膜: 。
16.(13分)I.某无色溶液中仅由K+、Mg2+、Na+、NH+、Fe2+、SO2-、OH-、HCO-、Cl-、NO-中的若干种
4 4 3 3
离子组成,且各种离子的个数相等。现取该溶液若干份,进行如下实验:
5
{#{QQABIQIEogggAAIAABgCUwEwCACQkhCACagGQBAEIAIASBNABAA=}#}①取第一份溶液进行焰色试验,呈黄色。透过蓝色钴玻璃观察,未见紫色;
②向第二份中滴加足量稀硝酸,有气体X产生,再加入足量Ba(NO) 溶液,得到白色沉淀,过滤后,在
3 2
滤液中加入足量稀硝酸酸化的AgNO 溶液,又有白色沉淀生成。
3
③向第三份中加入足量NaOH溶液,加热,生成有刺激性气味的气体和白色沉淀;
根据以上实验,请回答下列问题:
(1)不做任何实验,即可确定一定不含有的离子为 ,实验①确定一定含有的离
子为 。
(2)实验②气体X的化学式是 ;实验③生成白色沉淀的离子方程式 。
(3)通过以上实验确定______NO-(填“一定有” “可能有”或“一定无”), 理由是 。
3
II. 一个氧化还原反应可以看作是由得电子和失电子的两个半反应组成。相同浓度的高锰酸钾在不
同的条件下发生的半反应如下:
① MnO
4
- + 5e- + 8H+ == Mn2+ (接近无色)+4H
2
O
② MnO
4
- + 3e- + 2H
2
O == MnO
2
↓ +40H-
③ MnO
4
- + e- == MnO
4
2- (绿色)
(4)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的 影响。
(5)将足量SO 通入高锰酸钾溶液中,发现高锰酸钾溶液从紫红色变为接近无色,该反应发生还原过
2
程的离子反应过程为 → (填离子)
(6)实验室制取氯气的另一种方法是将浓盐酸和高锰酸钾混合:
HCl(浓)+ KMnO4=== Cl ↑+ MnCl + KCl+
2 2
配平上述化学方程式,并在方程式上面用“双线桥”标明电子转移的方向和数目
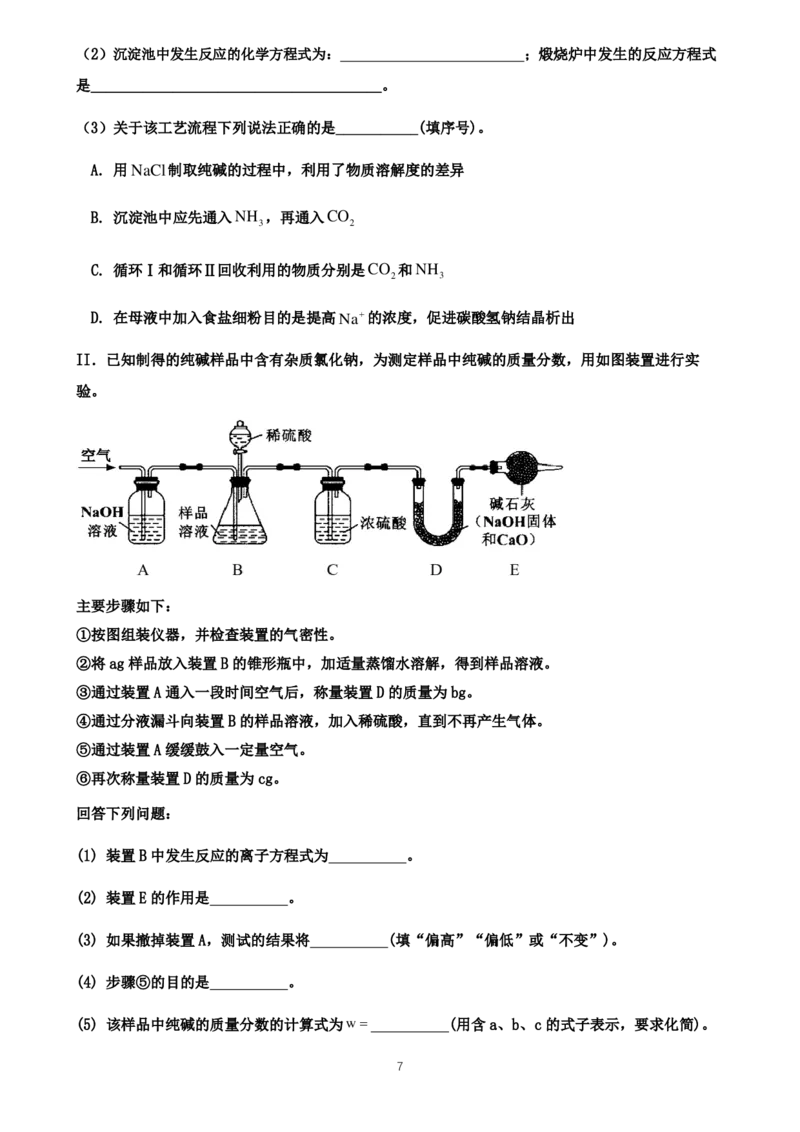
17.(16分) 侯德榜“联合制碱法”将制碱技术发展到一个新的水平。该工艺以氯化钠为原料主要流程
如图所示。
(1)“侯氏制碱法”中的“碱”为__________(填化学式),其用途有_______________(写一种)。
6
{#{QQABIQIEogggAAIAABgCUwEwCACQkhCACagGQBAEIAIASBNABAA=}#}(2)沉淀池中发生反应的化学方程式为: ;煅烧炉中发生的反应方程式
是_______________________________________。
(3)关于该工艺流程下列说法正确的是___________(填序号)。
A. 用NaCl制取纯碱的过程中,利用了物质溶解度的差异
B. 沉淀池中应先通入NH ,再通入CO
3 2
C. 循环Ⅰ和循环Ⅱ回收利用的物质分别是CO 和NH
2 3
D. 在母液中加入食盐细粉目的是提高Na+的浓度,促进碳酸氢钠结晶析出
II.已知制得的纯碱样品中含有杂质氯化钠,为测定样品中纯碱的质量分数,用如图装置进行实
验。
主要步骤如下:
①按图组装仪器,并检查装置的气密性。
②将ag样品放入装置B的锥形瓶中,加适量蒸馏水溶解,得到样品溶液。
③通过装置A通入一段时间空气后,称量装置D的质量为bg。
④通过分液漏斗向装置B的样品溶液,加入稀硫酸,直到不再产生气体。
⑤通过装置A缓缓鼓入一定量空气。
⑥再次称量装置D的质量为cg。
回答下列问题:
(1) 装置B中发生反应的离子方程式为 。
(2) 装置E的作用是 。
(3) 如果撤掉装置A,测试的结果将 (填“偏高”“偏低”或“不变”)。
(4) 步骤⑤的目的是 。
(5) 该样品中纯碱的质量分数的计算式为w= (用含a、b、c的式子表示,要求化简)。
7
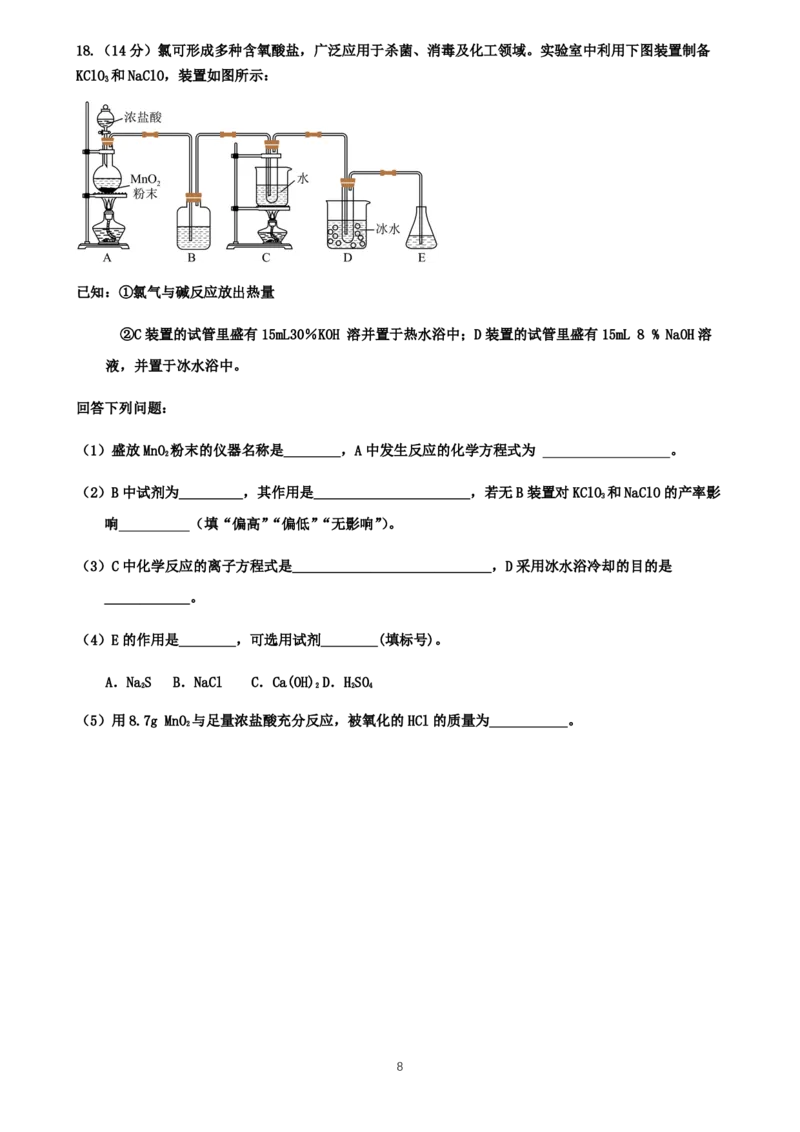
{#{QQABIQIEogggAAIAABgCUwEwCACQkhCACagGQBAEIAIASBNABAA=}#}18.(14分)氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置制备
KClO 和NaClO,装置如图所示:
3
已知:①氯气与碱反应放出热量
②C装置的试管里盛有15mL30%KOH 溶并置于热水浴中;D装置的试管里盛有15mL 8 % NaOH溶
液,并置于冰水浴中。
回答下列问题:
(1)盛放MnO 粉末的仪器名称是________,A中发生反应的化学方程式为 。
2
(2)B中试剂为_________,其作用是______________________,若无B装置对KClO 和NaClO的产率影
3
响 (填“偏高”“偏低”“无影响”)。
(3)C中化学反应的离子方程式是____________________________,D采用冰水浴冷却的目的是
____________。
(4)E的作用是________,可选用试剂________(填标号)。
A.NaS B.NaCl C.Ca(OH) D.HSO
2 2 2 4
(5)用8.7g MnO 与足量浓盐酸充分反应,被氧化的HCl的质量为___________。
2
8
{#{QQABIQIEogggAAIAABgCUwEwCACQkhCACagGQBAEIAIASBNABAA=}#}