文档内容
2025年秋期高一年级期中模拟考试(三)
化学试题
(时间:75分钟 满分:100分)
可能用到的相对原子质量:N 14 O 16 Cl 35.5 Na 23
一、单选题(本题共16小题,每题3分,共48分)
1.中国历史悠久,文化灿烂。下列有关说法或解释不合理的是 ( )
A.我国古代用明矾净水,是因为明矾溶于水生成一种能凝聚水中悬浮物的胶
状物质
B.《抱朴子内篇·黄白》记载“曾青(硫酸铜)涂铁,铁赤色如铜”,该过程
涉及置换反应
C.《江楼夜话》中有诗句“江雾秋楼白,灯花夜雨青”,描写的雾是一种液溶胶
D.《周礼》中记载沿海古人“煤饼烧蛎房成灰”(“蛎房”即指牡蛎壳之类
的贝壳),并把这种灰称为“蜃”,“蜃”的主要成分可以作干燥剂
2.分类是化学研究中常用的方法。下列分类方法正确的是 ( )
A.干冰、冰、胆矾都属于化合物 B.金属氧化物一定是碱性氧化物
C.混合物一定含两种或两种以上的元素 D.氨水能导电,故NH3属于电解质
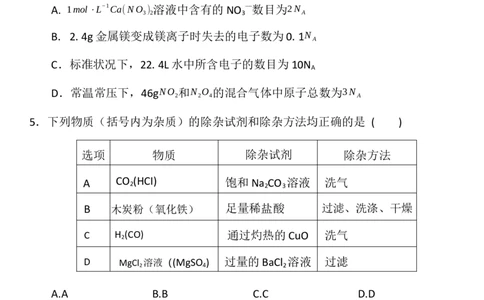
3.下列实验能够达到相应目的的是
A.将FeCl 饱和溶液滴入热NaOH溶液中
3
B.验证钠与水反应为放热反应
制备胶体
澄清石灰水
D.装置可用于比较碳酸钠和碳酸
C.制备过氧化钠
氢钠的热稳定性
4.表示下列反应的离子方程式正确的是 ( )A.铁跟稀硫酸反应: 2Fe+6H+=2Fe3++3H ↑
2
B.向NaHSO 溶液中逐滴加入Ba(OH) 溶液至SO2−刚好沉淀完
4 2 4
H++SO2−+Ba2++OH−=H O+BaSO ↓
4 2 4
C.氢氧化钡溶液和稀硫酸反应: Ba2++SO2−=BaSO ↓
4 4
D.NH HCO 溶液与足量NaOH溶液反应: N H++OH−=N H ⋅H O
4 3 4 3 2
5.用N 表示阿伏加德罗常数的值。下列说法正确的是 ( )
A
A. 1mol⋅L−1Ca(NO ) 溶液中含有的NO —数目为2N
3 2 3 A
B. 2.4g金属镁变成镁离子时失去的电子数为0.1N
A
C.标准状况下,22.4L水中所含电子的数目为10N
A
D.常温常压下,46gNO 和N O 的混合气体中原子总数为3N
2 2 4 A
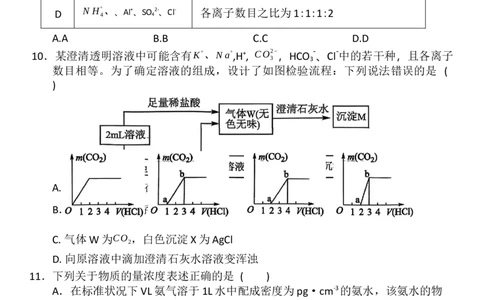
5.下列物质(括号内为杂质)的除杂试剂和除杂方法均正确的是 ( )
选项 物质 除杂试剂 除杂方法
A CO 2 (HCI) 饱和Na 2 CO 3 溶液 洗气
B 木炭粉(氧化铁) 足量稀盐酸 过滤、洗涤、干燥
C H (CO) 通过灼热的CuO 洗气
2
D MgCl 溶液((MgSO ) 过量的BaCl 溶液 过滤
2 4 2
A.A B.B C.C D.D
7.由 O 和 H 组成的混合气体平均相对分子质量为 28,则该混合气体中 O 和 H
2 2 2 2
的体积比为 ( )
A.1:1 B. 16:1 C.13:2 D.2:13
8.下列叙述正确的是 ( )
A.金属钠着火时,可用泡沫灭火器灭火
B.红热的铁丝在氯气中燃烧生成FeCl
2
C.向某待测溶液中滴入盐酸酸化的 AAgNO 溶液,产生白色沉淀,说明待测溶液
3
中含CI-
D. Na O与Na O 中阳、阴离子的个数比均为2:1
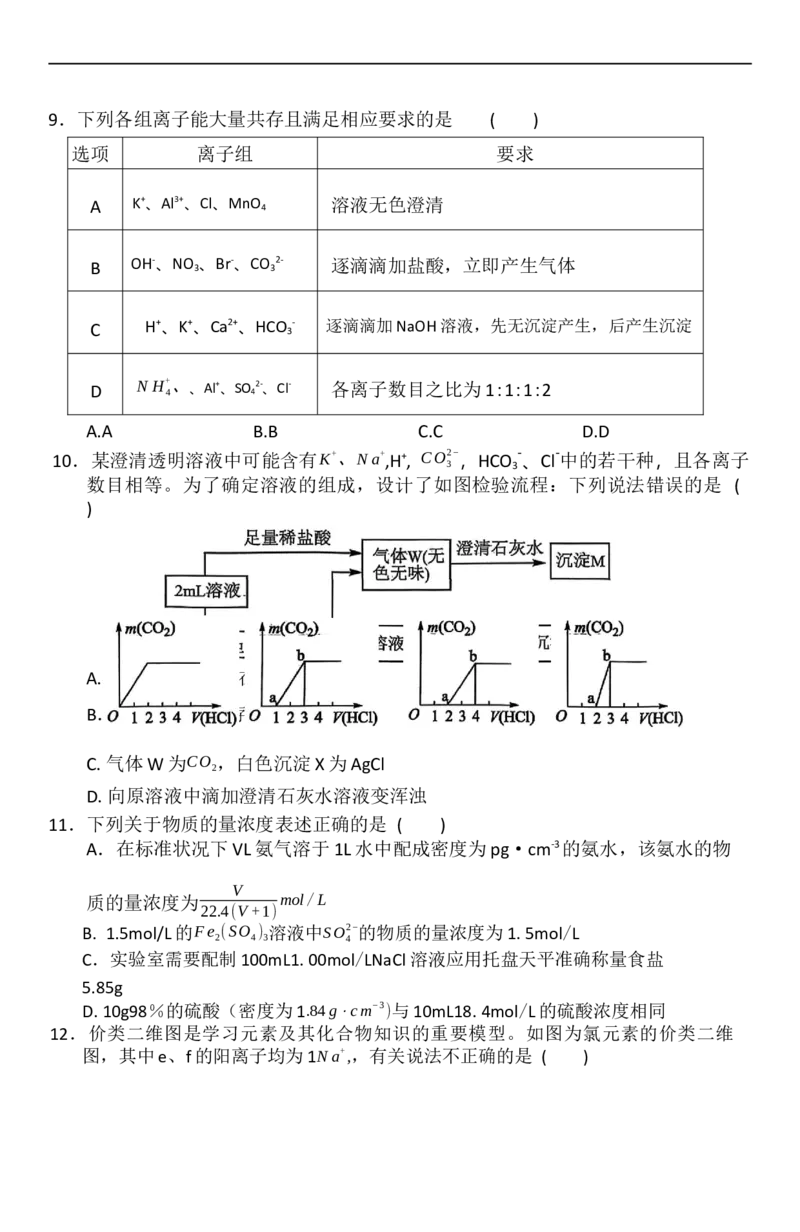
2 2 29.下列各组离子能大量共存且满足相应要求的是 ( )
选项 离子组 要求
A K+、Al3+、Cl、MnO 溶液无色澄清
4
B OH-、NO 3 、Br-、CO 3 2- 逐滴滴加盐酸,立即产生气体
C
H+、K+、Ca2+、HCO - 逐滴滴加NaOH溶液,先无沉淀产生,后产生沉淀
3
D N H+ 、、Al+、SO 2-、Cl- 各离子数目之比为1:1:1:2
4 4
A.A B.B C.C D.D
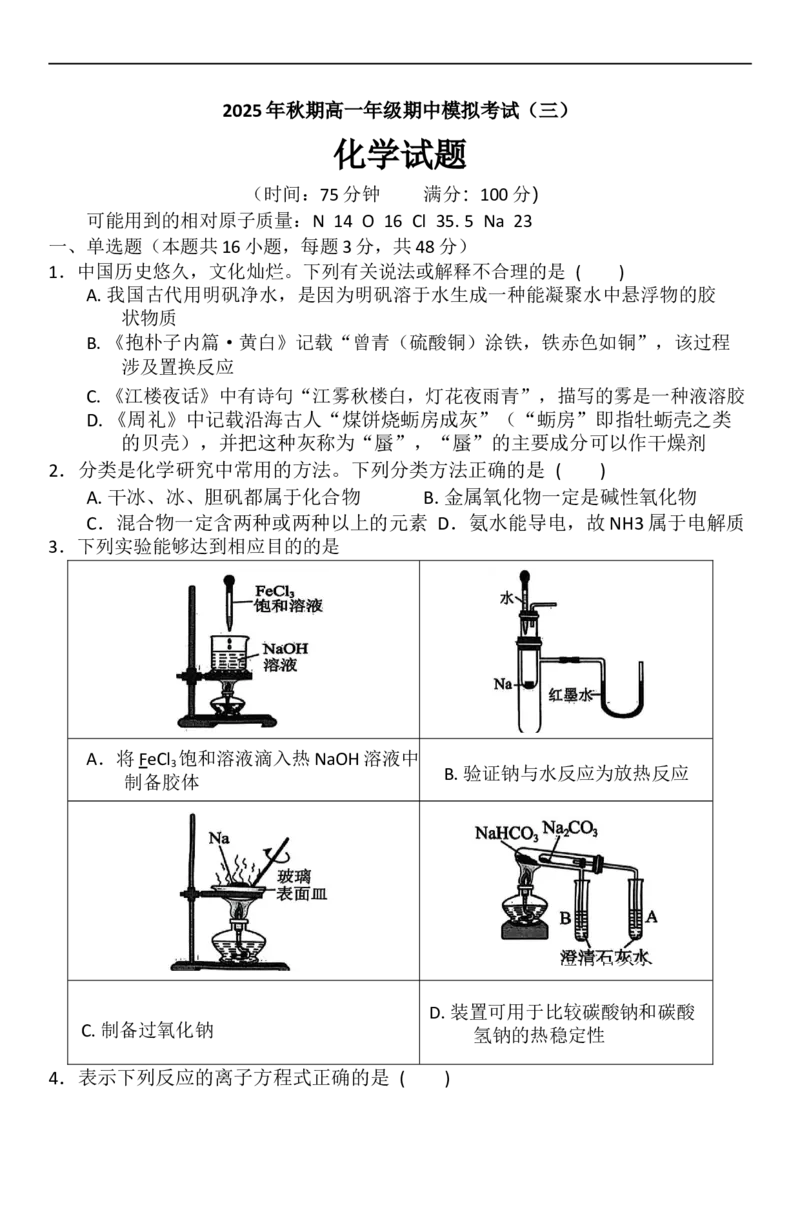
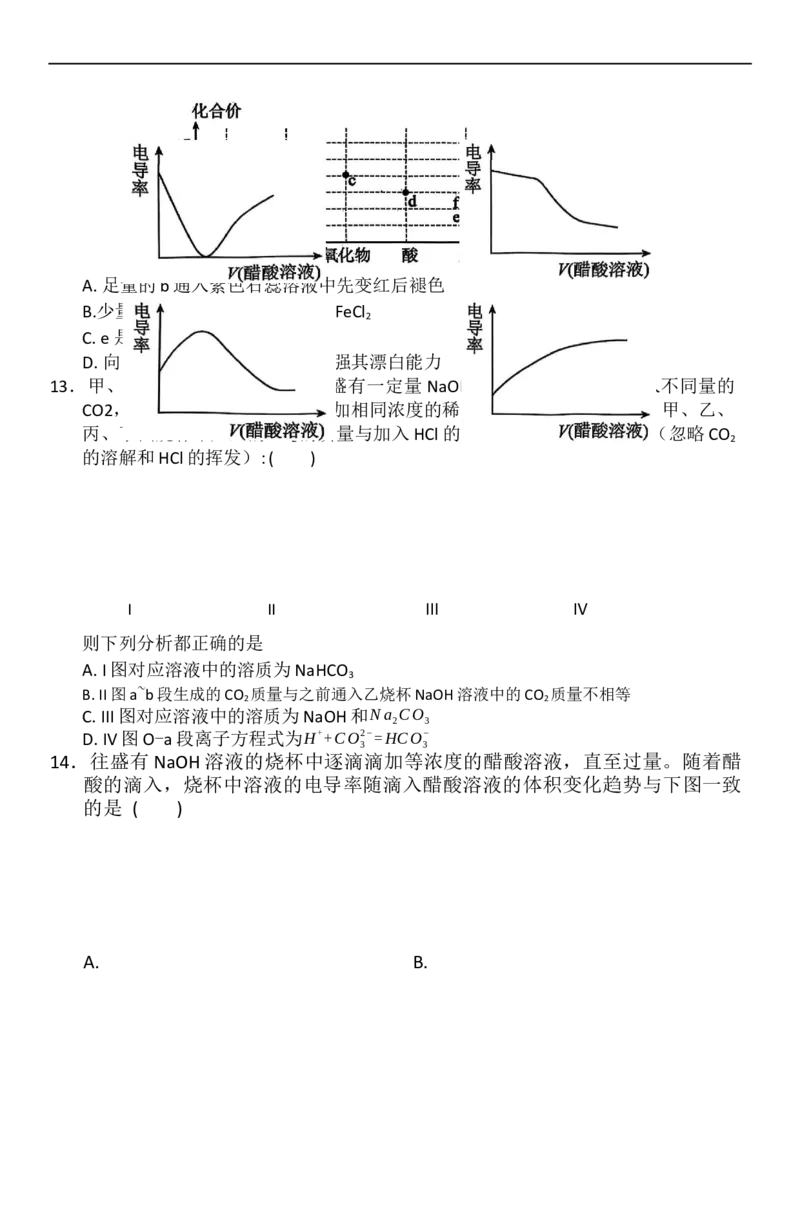
10.某澄清透明溶液中可能含有K+ 、Na+ ,H+, CO2− ,HCO - 、Cl -中的若干种,且各离子
3 3
数目相等。为了确定溶液的组成,设计了如图检验流程:下列说法错误的是 (
)
A.原溶液中一定存在Na+ 、K+
B.原溶液中可能存在HCO -
3
C.气体W为CO ,白色沉淀X为AgCl
2
D.向原溶液中滴加澄清石灰水溶液变浑浊
11.下列关于物质的量浓度表述正确的是 ( )
A.在标准状况下VL氨气溶于1L水中配成密度为pg·cm-3的氨水,该氨水的物
V
质的量浓度为 mol/L
22.4(V +1)
B. 1.5mol/L的Fe (SO ) 溶液中SO2−的物质的量浓度为1.5mol/L
2 4 3 4
C.实验室需要配制100mL1.00mol/LNaCl溶液应用托盘天平准确称量食盐
5.85g
D.10g98%的硫酸(密度为1.84g⋅cm−3 )与10mL18.4mol/L的硫酸浓度相同
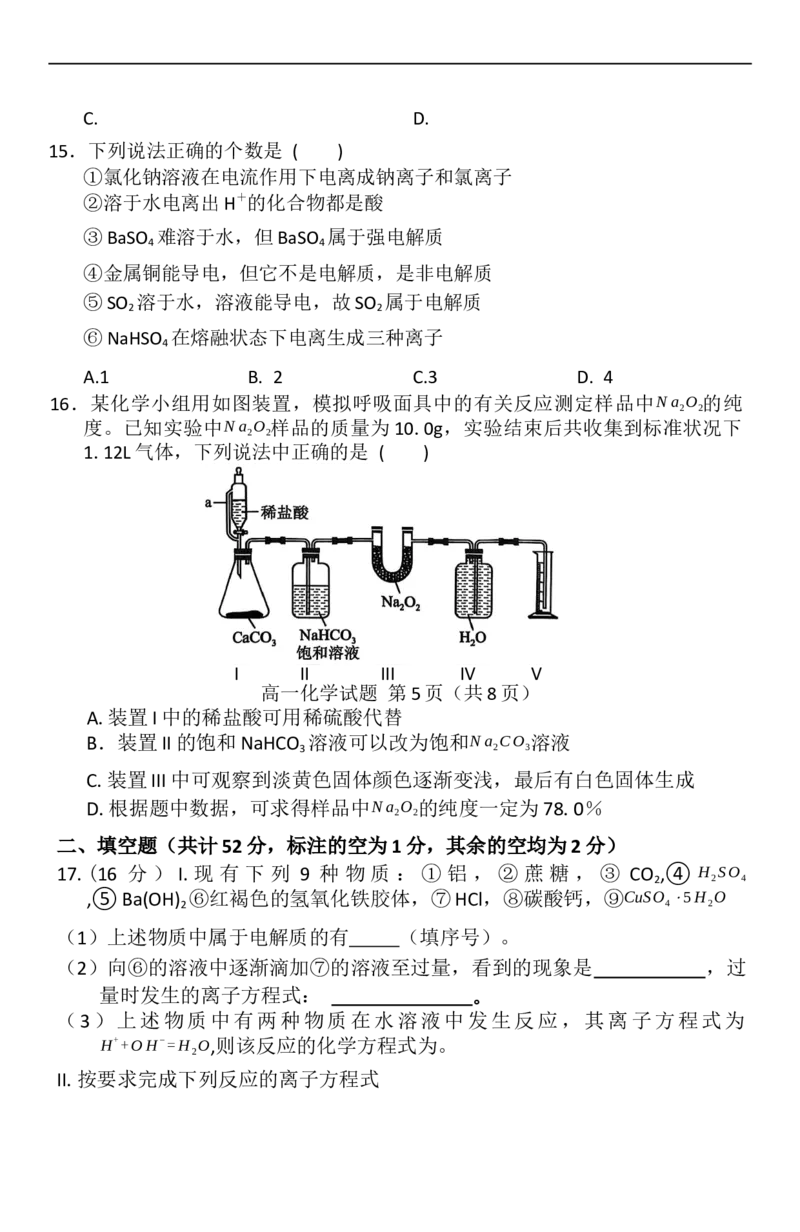
12.价类二维图是学习元素及其化合物知识的重要模型。如图为氯元素的价类二维
图,其中e、f的阳离子均为1Na+,,有关说法不正确的是 ( )A.足量的b通入紫色石蕊溶液中先变红后褪色
B.少量的b与足量的铁反应生成FeCl
2
C.e是侯氏制碱法的原料之一
D.向f溶液中通入二氧化碳可增强其漂白能力
13.甲、乙、丙、丁四烧杯中分别盛有一定量 NaOH 溶液,向其中分别通入不同量的
CO2,再向所得溶液中分别逐滴加相同浓度的稀盐酸至过量,加热溶液,甲、乙、
丙、丁四烧杯中产生的 CO 的质量与加入 HCl的体积关系如图I-IV 所示(忽略CO
2 2
的溶解和HCl的挥发):( )
I II III IV
则下列分析都正确的是
A.I图对应溶液中的溶质为NaHCO
3
B.II图a~b段生成的CO 质量与之前通入乙烧杯NaOH溶液中的CO 质量不相等
2 2
C.III图对应溶液中的溶质为NaOH和Na CO
2 3
D.IV图O-a段离子方程式为H++CO2−=HCO−
3 3
14.往盛有 NaOH 溶液的烧杯中逐滴滴加等浓度的醋酸溶液,直至过量。随着醋
酸的滴入,烧杯中溶液的电导率随滴入醋酸溶液的体积变化趋势与下图一致
的是 ( )
A. B.C. D.
15.下列说法正确的个数是 ( )
①氯化钠溶液在电流作用下电离成钠离子和氯离子
②溶于水电离出H+的化合物都是酸
③BaSO 难溶于水,但BaSO 属于强电解质
4 4
④金属铜能导电,但它不是电解质,是非电解质
⑤SO 溶于水,溶液能导电,故SO 属于电解质
2 2
⑥NaHSO 在熔融状态下电离生成三种离子
4
A.1 B. 2 C.3 D. 4
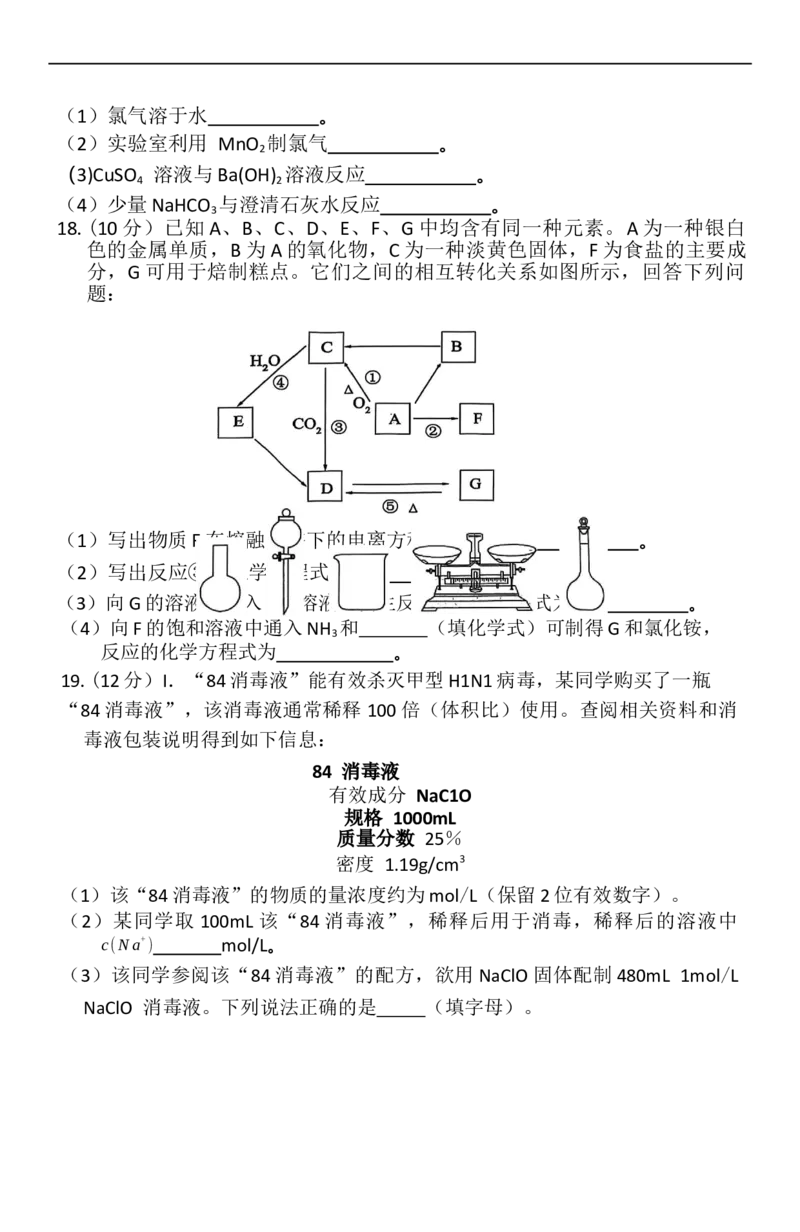
16.某化学小组用如图装置,模拟呼吸面具中的有关反应测定样品中Na O 的纯
2 2
度。已知实验中Na O 样品的质量为 10.0g,实验结束后共收集到标准状况下
2 2
1.12L气体,下列说法中正确的是 ( )
I II III IV V
高一化学试题 第5页(共8页)
A.装置I中的稀盐酸可用稀硫酸代替
B.装置II 的饱和NaHCO 溶液可以改为饱和Na CO 溶液
3 2 3
C.装置III 中可观察到淡黄色固体颜色逐渐变浅,最后有白色固体生成
D.根据题中数据,可求得样品中Na O 的纯度一定为78.0%
2 2
二、填空题(共计52 分,标注的空为1 分,其余的空均为2 分)
17.(16 分 ) I. 现 有 下 列 9 种 物 质 : ① 铝 , ② 蔗 糖 , ③ CO ,④ H SO
2 2 4
,⑤Ba(OH) ⑥红褐色的氢氧化铁胶体,⑦HCl,⑧碳酸钙,⑨CuSO ⋅5H O
2 4 2
(1)上述物质中属于电解质的有 (填序号)。
(2)向⑥的溶液中逐渐滴加⑦的溶液至过量,看到的现象是 ,过
量时发生的离子方程式: 。
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为
H++OH−=H O,则该反应的化学方程式为。
2
II.按要求完成下列反应的离子方程式(1)氯气溶于水 。
(2)实验室利用 MnO 制氯气 。
2
(3)CuSO 溶液与Ba(OH) 溶液反应 。
4 2
(4)少量NaHCO 与澄清石灰水反应 。
3
18.(10 分)已知 A、B、C、D、E、F、G 中均含有同一种元素。A 为一种银白
色的金属单质,B 为 A 的氧化物,C 为一种淡黄色固体,F 为食盐的主要成
分,G 可用于焙制糕点。它们之间的相互转化关系如图所示,回答下列问
题:
(1)写出物质F在熔融状态下的电离方程式: 。
(2)写出反应③的化学方程式: 。
(3)向G的溶液中滴入E的溶液,发生反应的离子方程式为 。
(4)向 F的饱和溶液中通入 NH 和 (填化学式)可制得 G和氯化铵,
3
反应的化学方程式为 。
19.(12分)I.“84消毒液”能有效杀灭甲型H1N1病毒,某同学购买了一瓶
“84 消毒液”,该消毒液通常稀释 100 倍(体积比)使用。查阅相关资料和消
毒液包装说明得到如下信息:
84 消毒液
有效成分 NaC1O
规格 1000mL
质量分数 25%
密度 1.19g/cm3
(1)该“84消毒液”的物质的量浓度约为mol/L(保留2位有效数字)。
(2)某同学取 100mL 该“84 消毒液”,稀释后用于消毒,稀释后的溶液中
c(Na+ ) mol/L。
(3)该同学参阅该“84 消毒液”的配方,欲用 NaClO 固体配制 480mL 1mol/L
NaClO 消毒液。下列说法正确的是 (填字母)。① ② ③ ④ ⑤
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制溶液定容时仰视凹液面可能导致结果偏低
D.需要称量NaClO固体的质量为35.7g
II.有 A、B、C、D 四种可溶性盐,它们的阳离子分别是Ba2+ 、Ag+ 、Na+ 、Cu2+中的
某一种,阴离子分别是NO 3 -、SO 4 2-、 Cl- 、 CO 3 2-中的一种(离子不重复出现)。
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向四支试管中分别加入盐酸,B 盐的溶液有沉淀生成,D 盐的溶液有无色
无味的气体逸出。
(4)B的化学式为 (1分),C的化学式为 (1分)。
(5)写出D与足量盐酸反应的化学方程式 。
(6)检验A溶液中阴离子的方法是 。
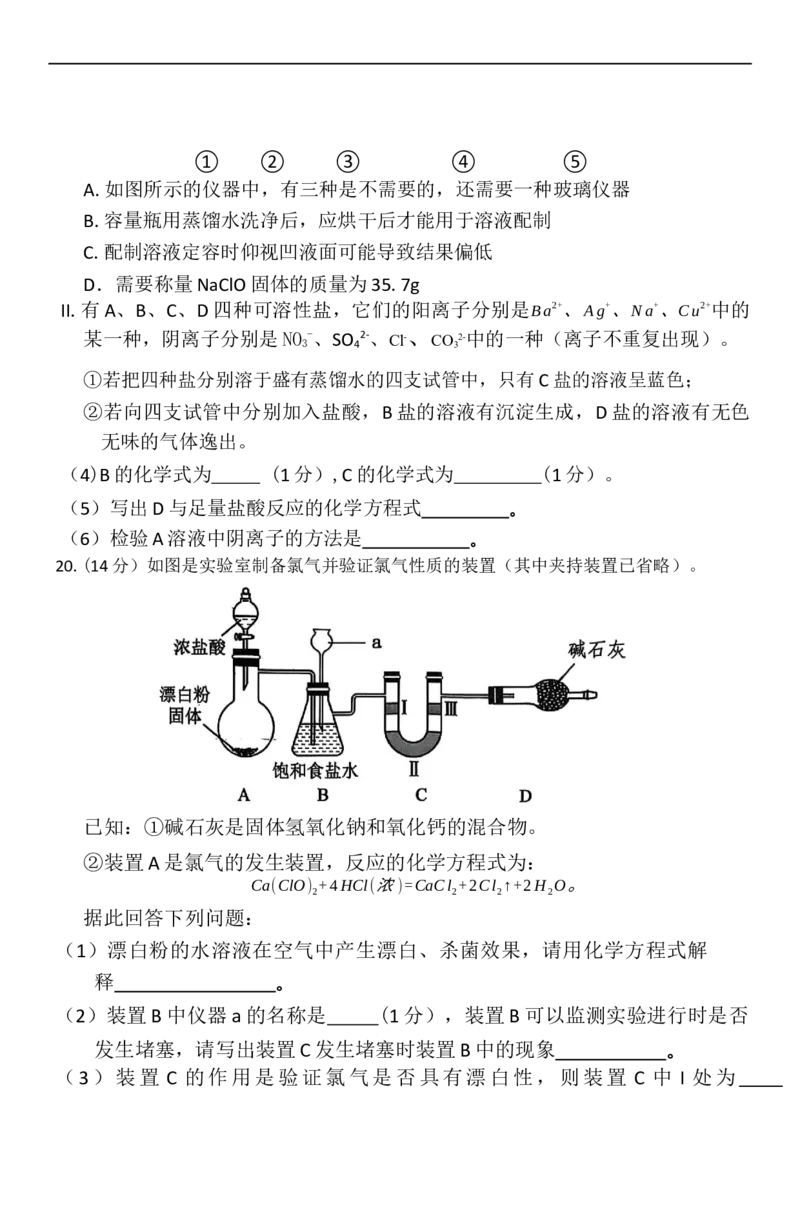
20.(14分)如图是实验室制备氯气并验证氯气性质的装置(其中夹持装置已省略)。
已知:①碱石灰是固体氢氧化钠和氧化钙的混合物。
②装置A是氯气的发生装置,反应的化学方程式为:
Ca(ClO) +4HCl(浓)=CaCl +2Cl ↑+2H O。
2 2 2 2
据此回答下列问题:
(1)漂白粉的水溶液在空气中产生漂白、杀菌效果,请用化学方程式解
释 。
(2)装置 B 中仪器 a 的名称是 (1 分),装置 B 可以监测实验进行时是否
发生堵塞,请写出装置C发生堵塞时装置B 中的现象 。
(3)装置 C 的作用是验证氯气是否具有漂白性,则装置 C 中 I 处为(填“湿润的有色布条”或“干燥的有色布条”),II 处为氯化钙固体,其
作用是 (1 分),用方程式解释氯气能使布条褪色的原因 。
(4)装置D的作用是 。
(5)工业上可用氢氧化钠与氯气反应制取 84 消毒液,在生活中 84 消毒液不可
与洁厕灵(其主要成分为盐酸)混用,其原因是: (用离
子方程式解释)。