文档内容
2024 年 12月
绵阳南山中学高 2024 级高一上期 12 月月考试题
化学试题
命题人:陈雅涵 审题人:汪桃先
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分 100 分,考试时间 75 分
钟。答题前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第 I 卷时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂
黑。如需改动,用橡皮擦干净后,再选涂其它答案标号。写在本试卷上无效。
可能用到的相对原子质量:H1 O16 S32 Ni59
第Ⅰ卷
(选择题,共 45 分)
一、选择题(本题包括15小题,每小题3分,共45分。每小题只有一个选项最符合题意)
1.金属材料的应用促进了人类社会的发展。下列不
.
属
.
于
.
金属材料的是
A.青铜戈 B.说唱陶俑 C.航母钢甲板 D.储氢合金
2.化学与生产、生活密切相关。下列说法错误的是
A.二氧化氯与臭氧可用于自来水消毒 B.合金的硬度一般比其成分金属的大
C.碳酸钠常用于治疗胃酸过多 D.铁粉可用作食品脱氧剂
3.下列变化不
.
能
.
通过一步反应实现的是
A.Na CO →NaOH B.Fe O →Fe(OH) C.Fe→FeCl D.Al→AlCl
2 3 2 3 3 2 3
4.硒(Se)是人体必须微量元素之一。下列关于80Se的说法不正确的是
34
A. 质量数为46 B. 质子数为34 C. 中子数为46 D. 核外电子数为34
5.下列各离子组在指定溶液中一定能大量共存的是
A.澄清透明的溶液:Mg2+、K+、MnO-、CO2-
4 3
B.与Al反应放出H 的溶液:K+、Fe3+、SO2- 、NO-
2 4 3
C.0.1mol/L的Al (SO ) 溶液:Na+、NH+、Cl-、SO2-
2 4 3 4 4
D.氯水:Ca2+、Fe2+、NO-、HCO-
3 3
6.用N 表示阿伏加德罗常数的值,下列说法中正确的是
A
A.标况下,3.6gH O与4.48LNH 的分子数均为0.2N
2 3 A
B.18gD O所含质子数为10N
2 A
C.标况下,11.2LCl 通入水中,溶液中N(Cl-)+N(HClO)+N(ClO-)=1N
2 A
D.0.1mol/LK SO 溶液中含有的K+数为0.2N
2 4 A
第 1 页 共 6 页7.磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性。制备时将含等量的FeSO 和
4
Fe (SO ) 的溶液混合再滴入稍过量的NaOH溶液,随后加入油酸钠溶液,即可生成黑色的、分散质粒
2 4 3
子直径为5.5~36nm的磁流体。下列说法中正确的是
A. 该磁流体与NaCl溶液的分散质粒子直径相同
B. 用光束照射磁流体时,可以产生丁达尔效应
C. 该磁流体可以通过过滤的方法提纯
D. 该磁流体的制备过程只涉及物理变化
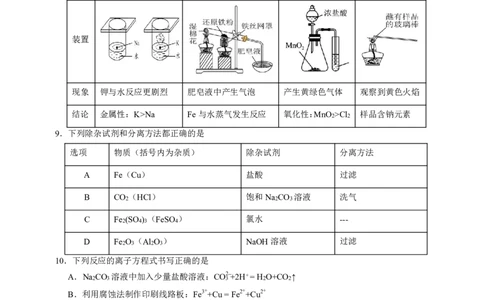
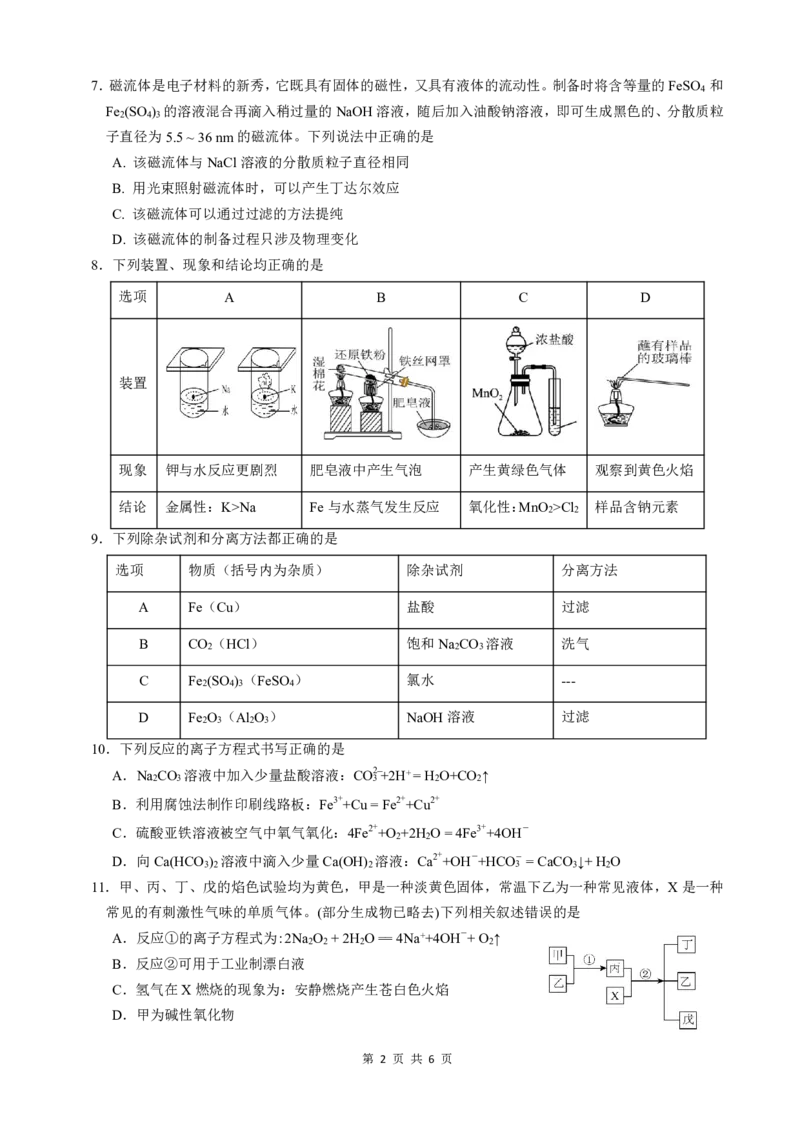
8.下列装置、现象和结论均正确的是
选项 A B C D
装置
现象 钾与水反应更剧烈 肥皂液中产生气泡 产生黄绿色气体 观察到黄色火焰
结论 金属性:K>Na Fe与水蒸气发生反应 氧化性:MnO >Cl 样品含钠元素
2 2
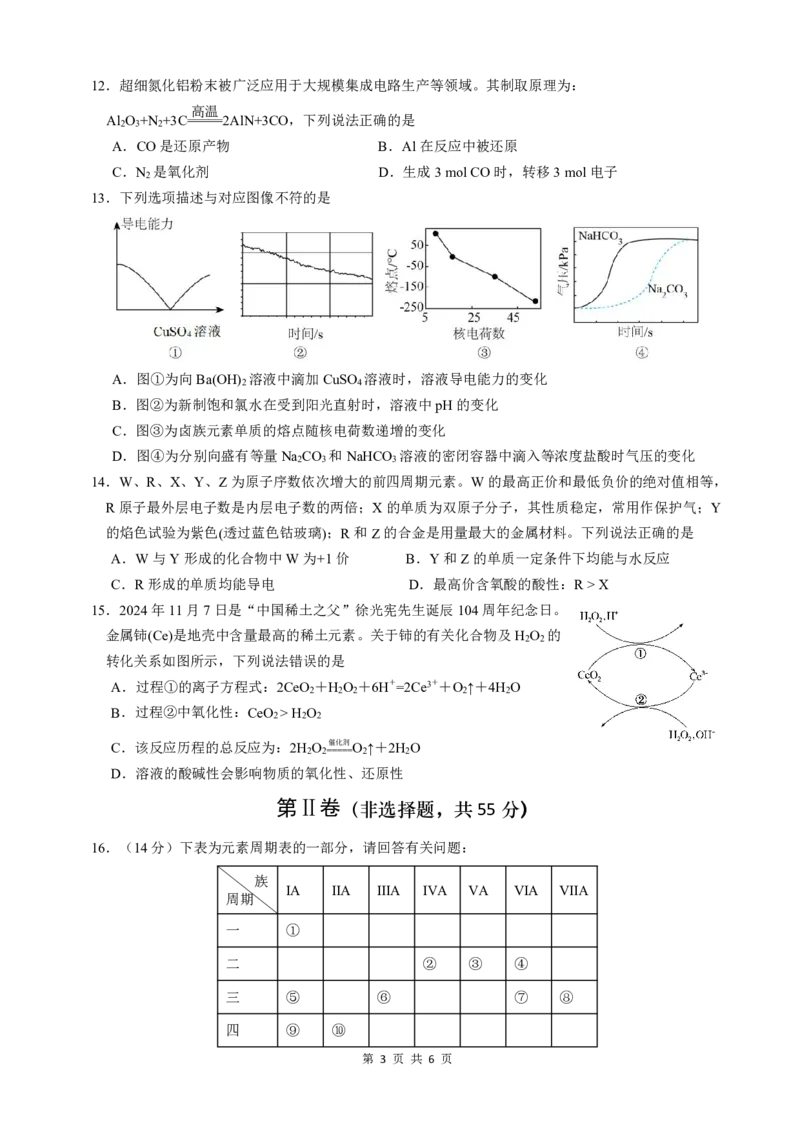
9.下列除杂试剂和分离方法都正确的是
选项 物质(括号内为杂质) 除杂试剂 分离方法
A Fe(Cu) 盐酸 过滤
B CO (HCl) 饱和Na CO 溶液 洗气
2 2 3
C Fe 2 (SO 4 ) 3 (FeSO 4 ) 氯水 ---
D Fe 2 O 3 (Al 2 O 3 ) NaOH溶液 过滤
10.下列反应的离子方程式书写正确的是
A.Na CO 溶液中加入少量盐酸溶液:CO2-+2H+=H O+CO ↑
2 3 3 2 2
B.利用腐蚀法制作印刷线路板:Fe3+ +Cu=Fe2+ +Cu2+
C.硫酸亚铁溶液被空气中氧气氧化:4Fe2+ +O +2H O=4Fe3+ +4OH-
2 2
D.向Ca(HCO ) 溶液中滴入少量Ca(OH) 溶液:Ca2+ +OH-+HCO-=CaCO ↓+H O
3 2 2 3 3 2
11.甲、丙、丁、戊的焰色试验均为黄色,甲是一种淡黄色固体,常温下乙为一种常见液体,X是一种
常见的有刺激性气味的单质气体。(部分生成物已略去)下列相关叙述错误的是
A.反应①的离子方程式为:2Na O +2H O==4Na++4OH-+O ↑
2 2 2 2
B.反应②可用于工业制漂白液
C.氢气在X燃烧的现象为:安静燃烧产生苍白色火焰
D.甲为碱性氧化物
第 2 页 共 6 页12.超细氮化铝粉末被广泛应用于大规模集成电路生产等领域。其制取原理为:
高温
Al O +N +3C=====2AlN+3CO,下列说法正确的是
2 3 2
A.CO是还原产物 B.Al在反应中被还原
C.N 是氧化剂 D.生成3molCO时,转移3mol电子
2
13.下列选项描述与对应图像不符的是
A.图①为向Ba(OH) 溶液中滴加CuSO 溶液时,溶液导电能力的变化
2 4
B.图②为新制饱和氯水在受到阳光直射时,溶液中pH的变化
C.图③为卤族元素单质的熔点随核电荷数递增的变化
D.图④为分别向盛有等量Na CO 和NaHCO 溶液的密闭容器中滴入等浓度盐酸时气压的变化
2 3 3
14.W、R、X、Y、Z为原子序数依次增大的前四周期元素。W的最高正价和最低负价的绝对值相等,
R原子最外层电子数是内层电子数的两倍;X的单质为双原子分子,其性质稳定,常用作保护气;Y
的焰色试验为紫色(透过蓝色钴玻璃);R和Z的合金是用量最大的金属材料。下列说法正确的是
A.W与Y形成的化合物中W为+1价 B.Y和Z的单质一定条件下均能与水反应
C.R形成的单质均能导电 D.最高价含氧酸的酸性:R>X
15.2024年11月7日是“中国稀土之父”徐光宪先生诞辰104周年纪念日。
金属铈(Ce)是地壳中含量最高的稀土元素。关于铈的有关化合物及H O 的
2 2
转化关系如图所示,下列说法错误的是
A.过程①的离子方程式:2CeO +H O +6H+=2Ce3++O ↑+4H O
2 2 2 2 2
B.过程②中氧化性:CeO >H O
2 2 2
C.该反应历程的总反应为:2H O 催化剂O ↑+2H O
2 2===== 2 2
D.溶液的酸碱性会影响物质的氧化性、还原性
第Ⅱ卷
(非选择题,共 55 分)
16.(14分)下表为元素周期表的一部分,请回答有关问题:
族
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
周期
一 ①
二 ② ③ ④
三 ⑤ ⑥ ⑦ ⑧
四 ⑨ ⑩
第 3 页 共 6 页(1)⑧的原子结构示意图为 。
(2)气态氢化物的稳定性:④ ⑦,与水反应的剧烈程度⑤ ⑨填(填“>”或“<”)。
(3)⑥单质与⑤的最高价氧化物的水化物是家庭厨卫管道疏通剂的主要成分,疏通管道时发生反应
的化学方程式是 。
(4)工业生产中主要利用⑤与⑧形成的化合物,通过电解其水溶液制备化合物烧碱,不采用⑤和④
形成的化合物制备的原因是 。
(5)向纯碱溶液中,逐滴滴加①和⑦形成的化合物的稀溶液的现象为 。
(6)6Li和7Li可作核反应堆最佳热载体,7LiH和7LiD用作高温堆减速剂。下列说法正确的是
3 3 3 3
(填字母)。
A.等物质的量的7LiH和7LiD中电子总数相同 B.6Li和7Li属于同种核素
3 3 3 3
C.等物质的量的7LiH和7LiD中质子总数相同 D.6Li和7Li互为同位素
3 3 3 3
(7)实验室中⑤的单质为避免接触空气保存在 中;锂电池使用时需要注意防水,其原因用
化学反应方程式表示为 。
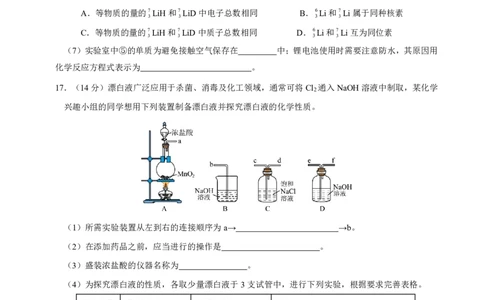
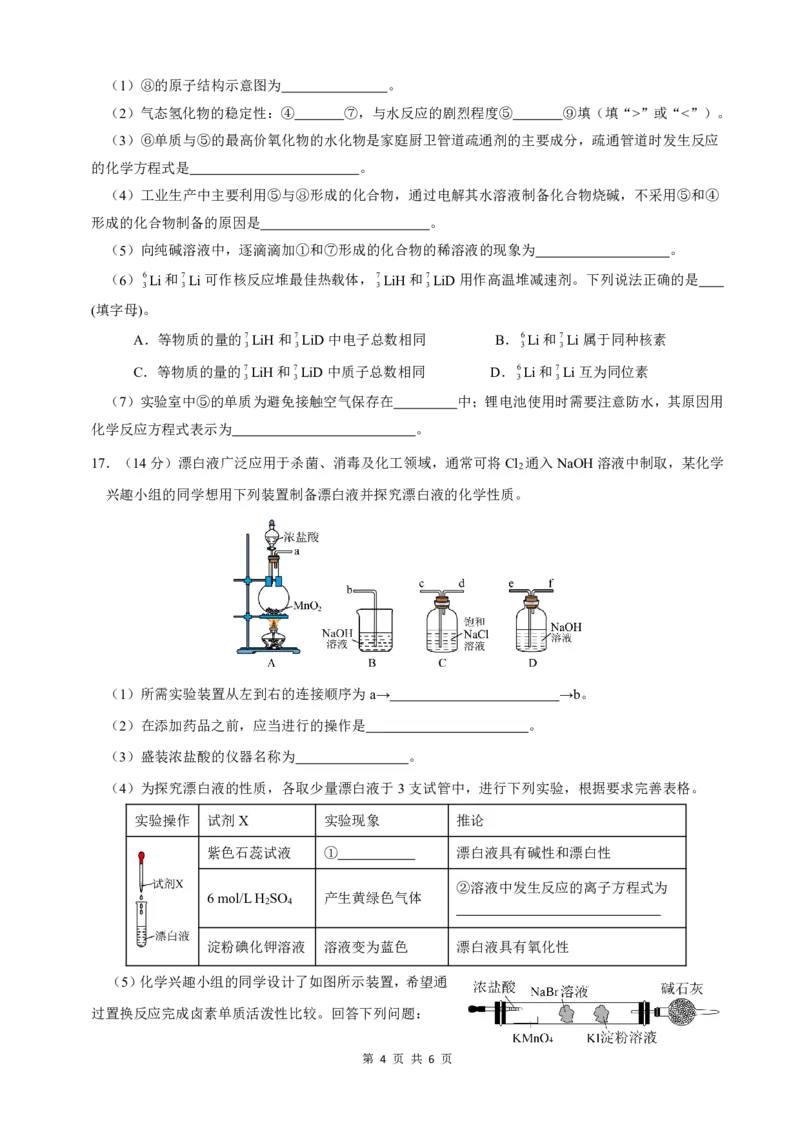
17.(14分)漂白液广泛应用于杀菌、消毒及化工领域,通常可将Cl 通入NaOH溶液中制取,某化学
2
兴趣小组的同学想用下列装置制备漂白液并探究漂白液的化学性质。
(1)所需实验装置从左到右的连接顺序为a→ →b。
(2)在添加药品之前,应当进行的操作是 。
(3)盛装浓盐酸的仪器名称为 。
(4)为探究漂白液的性质,各取少量漂白液于3支试管中,进行下列实验,根据要求完善表格。
实验操作 试剂X 实验现象 推论
紫色石蕊试液 ① 漂白液具有碱性和漂白性
②溶液中发生反应的离子方程式为
6mol/LH SO 产生黄绿色气体
2 4
淀粉碘化钾溶液 溶液变为蓝色 漂白液具有氧化性
(5)化学兴趣小组的同学设计了如图所示装置,希望通
过置换反应完成卤素单质活泼性比较。回答下列问题:
第 4 页 共 6 页①吸有NaBr溶液的棉球中发生的离子反应为 。
②该实验是否可以说明氧化性Br I : (填“是”或“否”),并说明你的理由 。
2 2
18.(14分)某工厂以镍废渣(主要成分为Ni,含少量Fe、Fe O 、Al O 等)为原料制备翠矾(NiSO ·7H O),
3 4 2 3 4 2
其生产工艺如图。
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Ni2+ Al3+ Fe3+ Fe2+
开始沉淀时的pH 7.2 3.7 2.2 7.5
沉淀完全时的pH 8.7 4.7 3.2 9.0
(1)用NaOH溶液处理镍废渣时发生反应的化学方程式为_________________________。
(2)实验室进行操作1需要用的玻璃仪器除了烧杯还有________。
(3)已知溶液1中含有金属阳离子主要有Ni2+、 。
(4)滤渣B为___________。
(5)滤渣B过滤后经过洗涤可回收利用,检验滤渣B已洗净的方法是 。
(6)加“沉淀剂”时,最适宜的 pH 范围是 。
(7)NiSO 在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH,该反应的离子
4
方程式为: Ni2++ ClO-+ == NiOOH+ Cl-+ 。
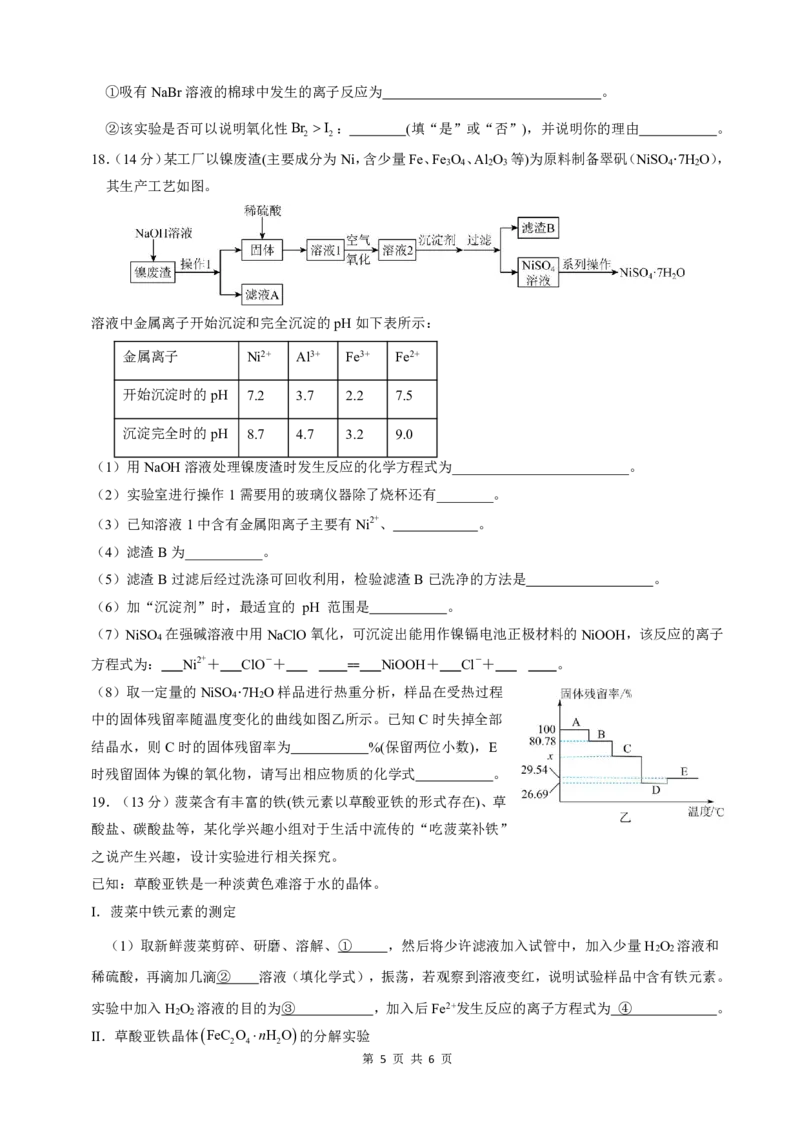
(8)取一定量的NiSO ·7H O样品进行热重分析,样品在受热过程
4 2
中的固体残留率随温度变化的曲线如图乙所示。已知C时失掉全部
结晶水,则C时的固体残留率为 %(保留两位小数),E
时残留固体为镍的氧化物,请写出相应物质的化学式 。
19.(13分)菠菜含有丰富的铁(铁元素以草酸亚铁的形式存在)、草
酸盐、碳酸盐等,某化学兴趣小组对于生活中流传的“吃菠菜补铁”
之说产生兴趣,设计实验进行相关探究。
已知:草酸亚铁是一种淡黄色难溶于水的晶体。
I.菠菜中铁元素的测定
(1)取新鲜菠菜剪碎、研磨、溶解、① ,然后将少许滤液加入试管中,加入少量H O 溶液和
2 2
稀硫酸,再滴加几滴② 溶液(填化学式),振荡,若观察到溶液变红,说明试验样品中含有铁元素。
实验中加入H O 溶液的目的为③ ,加入后Fe2+发生反应的离子方程式为 ④ 。
2 2
II.草酸亚铁晶体FeC O nH O的分解实验
2 4 2
第 5 页 共 6 页(2)加热反应开始前,需要先通一段时间的N ,目的是 。
2
(3)实验开始后:装置B中出现浑浊,证明分解产物中存在CO ;出现 现象,证
2
明分解产物中存在CO。
(4)将充分反应后的固体残余物投入经煮沸的稀硫酸中,固体完全溶解且无气体放出,取反应液,
向其中加入KSCN溶液无血红色出现,写出装置A中发生反应的化学方程式: 。
(5)从环保角度考虑,该套实验装置的明显缺陷是 。
第 6 页 共 6 页