文档内容
2025 年秋期六校第一次联考
高一年级化学试题
命题学校:内乡实验高中 审题学校:南召一中
(考试时间:75 分钟 试卷满分:100分)
注意事项:
1.答题前,考生务必将自己的姓名、准考证号、考场号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其它答案标号。回答非选择题时,将答案写在答题卡
上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Cl-35.5
一、选择题(本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是
符合题目要求的)
1.下列有关说法正确的是
A.我国科学家屠呦呦发现了青霉素,获得了诺贝尔医学奖
B.意大利科学家阿伏加德罗于1811年发现元素周期律,使化学的研究变得有规律
C.俄国科学家门捷列夫提出氧化学说,使近代化学取得了革命性的进展
D.1965年,我国科学家成功地合成了结晶牛胰岛素,这是世界上首次人工合成的、具有生理
活性的蛋白质
2.下列有关说法正确的是
A.1mol 苹果 B.氯原子的结构示意图:
C. Na O₂中阴离子:O²⁻ D. NH₃的摩尔质量:17g
2
3.某学习小组的同学在研究金属钠的性质时发现,金属钠暴露在空气中生成白色的氧化钠,在
空气中燃烧生成淡黄色的过氧化钠。你认为该小组同学在研究金属钠的性质时没有运用的基
本方法是
A.实验法 B.观察法 C.分类法 D.比较法
4.设NA为阿伏加德罗常数的值,下列有关说法正确的是
A.标准状况下,22.4 L 乙醇中分子数为N
A
B.2mol⋅L−1的 MgCl₂溶液中含氯离子数为4N
A
C.1L2mol⋅L−1Na CO 溶液中含氧原子总数为6N
2 3 A
D.标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为N
A
5.某兴趣小组将钠与水的反应装置改进如下图所示,下列说法错误的是
高一年级化学试题第1 页(共6页)
学科网(北京)股份有限公司A.钠块始终保持在a处,直至完全消失
B.本实验中,如果把水换成稀盐酸,除了反应快些,其他现象基本相同
C.随反应的进行,左侧漏斗中液面上升
D.钠处于煤油和水的交界处上下浮动
6.下列关于金属钠的叙述正确的是
A.钠与水反应的现象可以说明钠的硬度小、熔点低、密度比水小
B.钠可以保存在煤油中
C.把一小块金属钠放入稀硫酸中时,钠先与水剧烈反应
D.当钠与硫酸铜溶液反应时,有大量红色固体铜出现
7.下列叙述中正确的是
A.工业上用电解氯化钠溶液的方法生产金属钠
B. Na O₂和Na O都是碱性氧化物
2 2
C.过量的Na O₂放入到加有酚酞的水中,溶液中出现的颜色变化是变红
2
D. Na O₂是淡黄色固体,Na O是白色固体,二者都能与水反应生成NaOH
2 2
8.下列有关氯气及其化合物叙述正确的是
A.足量的铁丝在氯气中燃烧,生成 FeCl₂
B.大量氯气泄漏时,用浸有烧碱溶液的毛巾捂住口鼻向高处跑
C.红热的铜丝在氯气中剧烈燃烧,生成棕黄色的烟
D.工业上把氯气通入澄清的石灰水制漂白粉
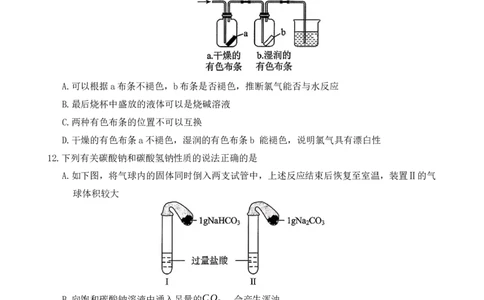
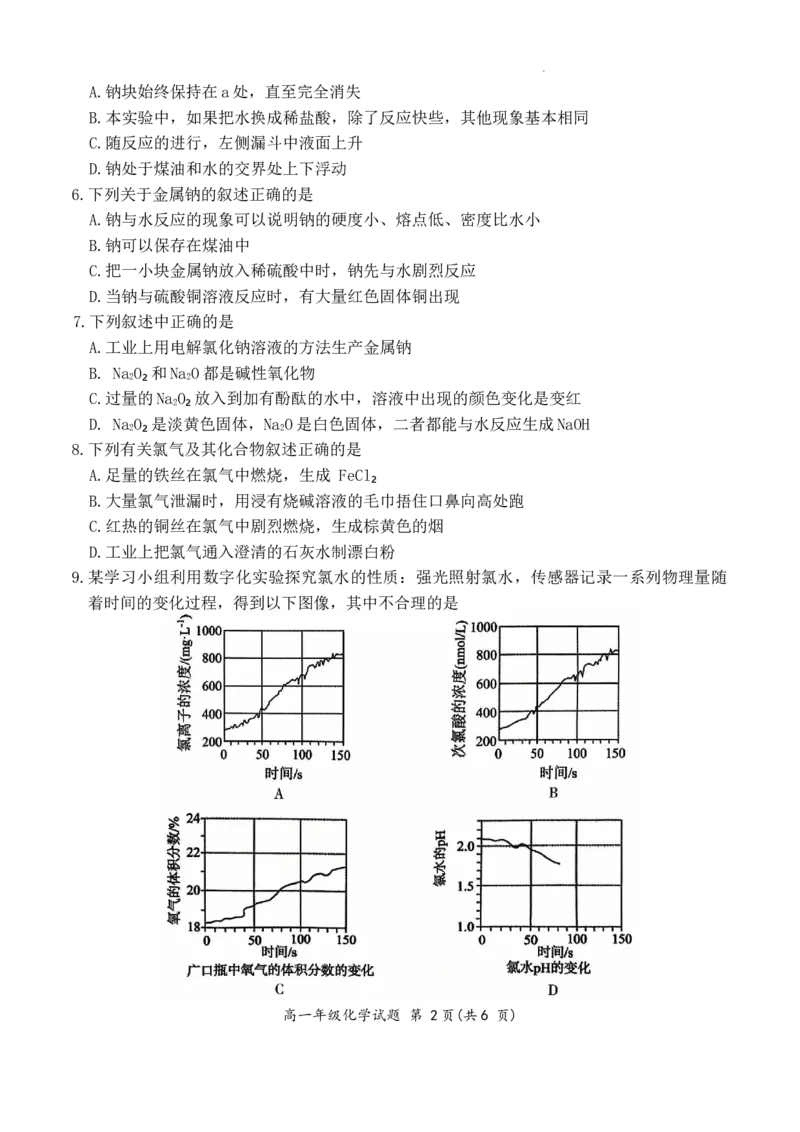
9.某学习小组利用数字化实验探究氯水的性质:强光照射氯水,传感器记录一系列物理量随
着时间的变化过程,得到以下图像,其中不合理的是
高一年级化学试题 第 2页(共6 页)
学科网(北京)股份有限公司10.下表是小华在人民医院体检结果报告单的部分数据:
分析项目 检测结果 单位
葡萄糖 4.00 mmol⋅L⁻¹
甘油三酯 2.94 mmol⋅L⁻¹
报告单中 是哪种物理量的单位
A.质量 B.物质的量 C.浓度 D.体积
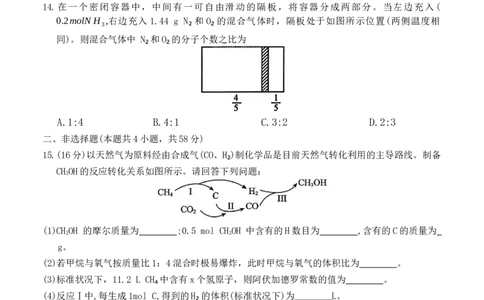
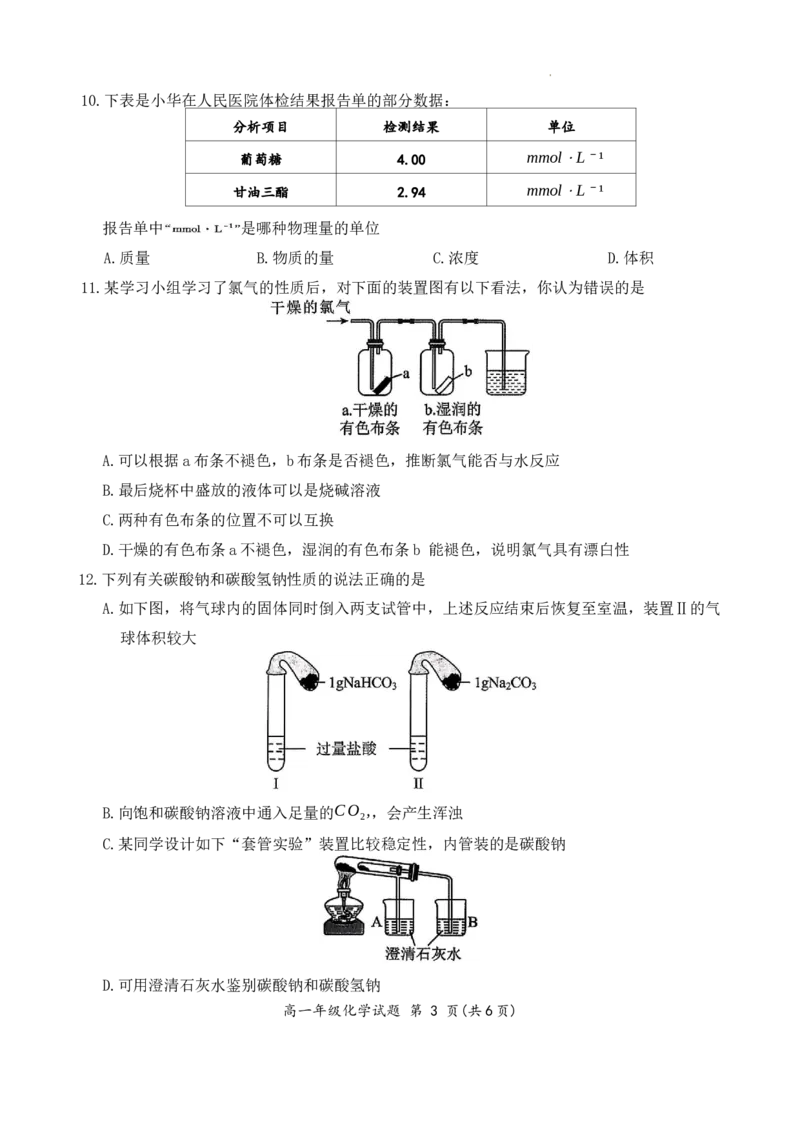
11.某学习小组学习了氯气的性质后,对下面的装置图有以下看法,你认为错误的是
A.可以根据a布条不褪色,b布条是否褪色,推断氯气能否与水反应
B.最后烧杯中盛放的液体可以是烧碱溶液
C.两种有色布条的位置不可以互换
D.干燥的有色布条a不褪色,湿润的有色布条b 能褪色,说明氯气具有漂白性
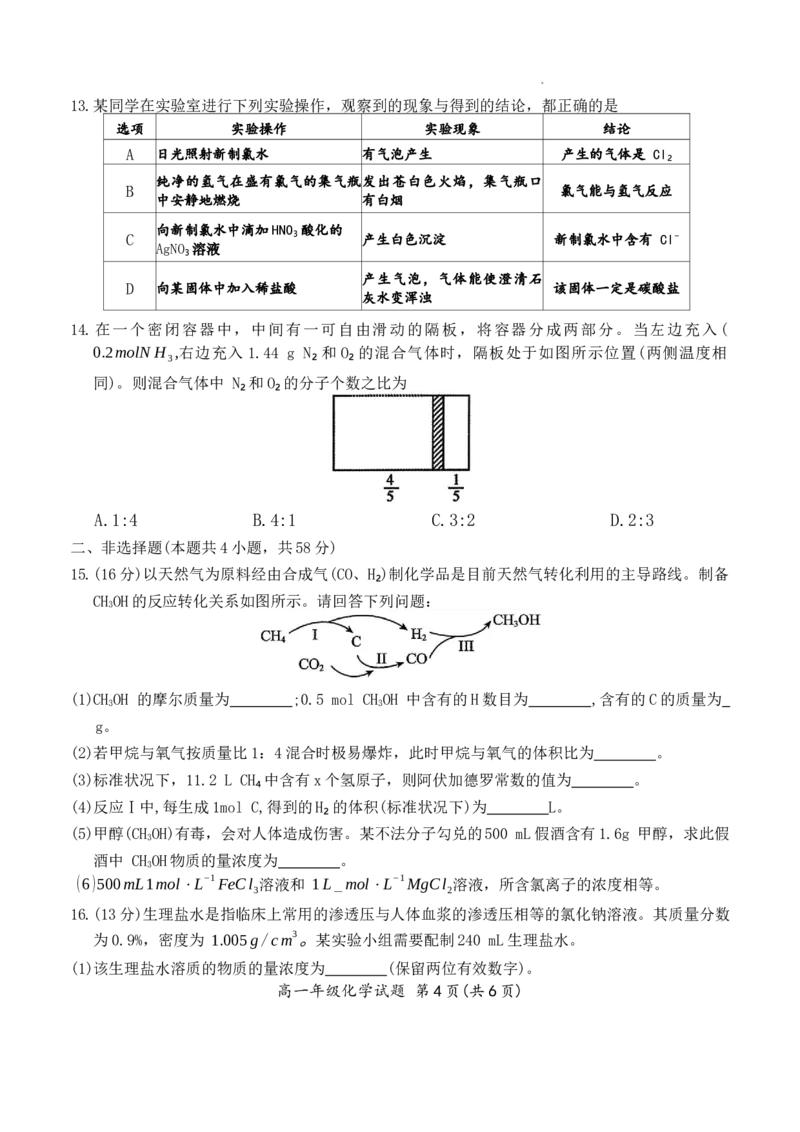
12.下列有关碳酸钠和碳酸氢钠性质的说法正确的是
A.如下图,将气球内的固体同时倒入两支试管中,上述反应结束后恢复至室温,装置Ⅱ的气
球体积较大
B.向饱和碳酸钠溶液中通入足量的CO ,,会产生浑浊
2
C.某同学设计如下“套管实验”装置比较稳定性,内管装的是碳酸钠
D.可用澄清石灰水鉴别碳酸钠和碳酸氢钠
高一年级化学试题 第 3 页(共6页)
学科网(北京)股份有限公司13.某同学在实验室进行下列实验操作,观察到的现象与得到的结论,都正确的是
选项 实验操作 实验现象 结论
A 日光照射新制氯水 有气泡产生 产生的气体是 Cl₂
纯净的氢气在盛有氯气的集气瓶发出苍白色火焰,集气瓶口
B 氯气能与氢气反应
中安静地燃烧 有白烟
向新制氯水中滴加HNO₃酸化的
C 产生白色沉淀 新制氯水中含有 Cl⁻
AgNO₃溶液
产生气泡,气体能使澄清石
D 向某固体中加入稀盐酸 该固体一定是碳酸盐
灰水变浑浊
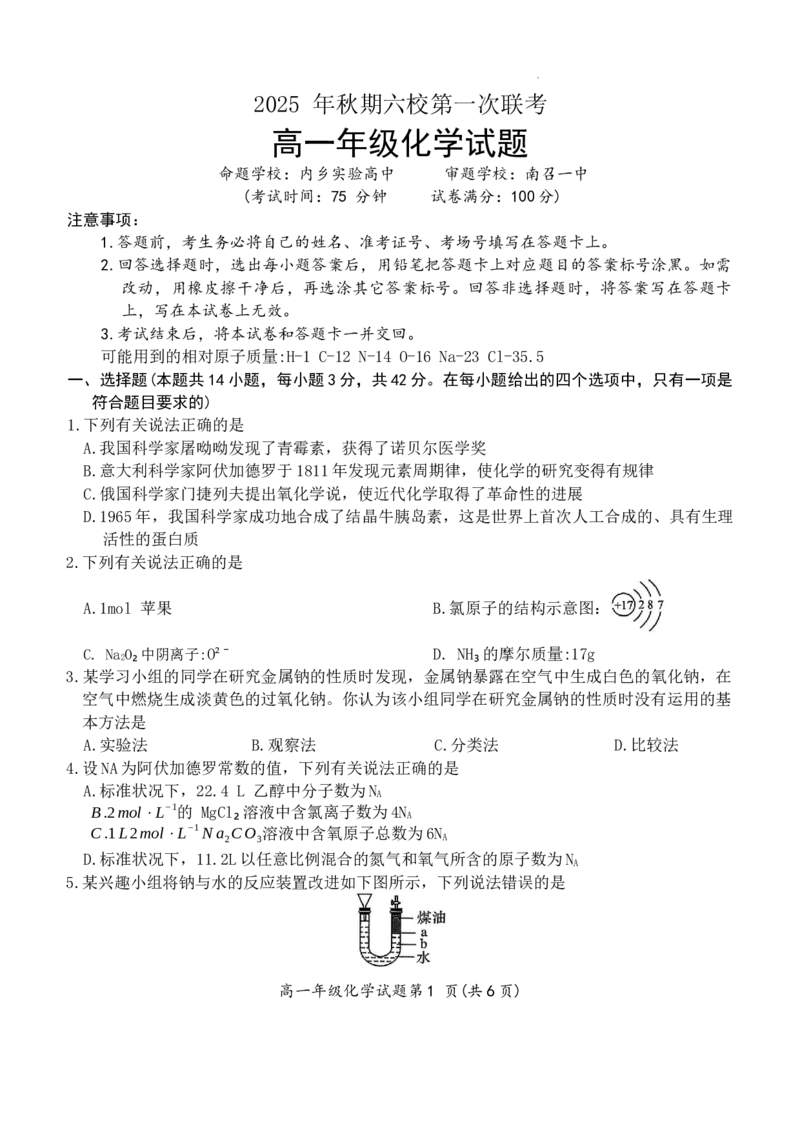
14.在一个密闭容器中,中间有一可自由滑动的隔板,将容器分成两部分。当左边充入(
0.2molN H ,右边充入 1.44 g N₂ 和O₂的混合气体时,隔板处于如图所示位置(两侧温度相
3
同)。则混合气体中 N₂和O₂的分子个数之比为
A.1:4 B.4:1 C.3:2 D.2:3
二、非选择题(本题共4小题,共58分)
15.(16分)以天然气为原料经由合成气(CO、H₂)制化学品是目前天然气转化利用的主导路线。制备
CH OH的反应转化关系如图所示。请回答下列问题:
3
(1)CH OH 的摩尔质量为 ;0.5 mol CH OH 中含有的H数目为 ,含有的C的质量为
3 3
g。
(2)若甲烷与氧气按质量比1:4混合时极易爆炸,此时甲烷与氧气的体积比为 。
(3)标准状况下,11.2 L CH₄中含有x个氢原子,则阿伏加德罗常数的值为 。
(4)反应Ⅰ中,每生成1mol C,得到的H₂的体积(标准状况下)为 L。
(5)甲醇(CH OH)有毒,会对人体造成伤害。某不法分子勾兑的500 mL假酒含有1.6g 甲醇,求此假
3
酒中 CH OH物质的量浓度为 。
3
(6)500mL1mol⋅L−1FeCl 溶液和 1L_mol⋅L−1MgCl 溶液,所含氯离子的浓度相等。
3 2
16.(13分)生理盐水是指临床上常用的渗透压与人体血浆的渗透压相等的氯化钠溶液。其质量分数
为0.9%,密度为 1.005g/cm3 。某实验小组需要配制240 mL生理盐水。
(1)该生理盐水溶质的物质的量浓度为 (保留两位有效数字)。
高一年级化学试题 第4页(共6页)
学科网(北京)股份有限公司(2)配制该溶液时,提供的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管。
①要完成该实验,还需使用到的玻璃仪器为 。
②该实验中,玻璃棒的作用为 。
(3)下图为溶液配制的过程,请将下列操作排序:a→b→ →c→e→ → 。
在f步骤中,不小心加水超过了刻度线,应如何处理 。
(4)下列操作会引起所配溶液浓度偏高的是 (填字母)。
A.称量时所用的砝码生锈
B.转移时操作如右图
C.烧杯未进行洗涤
D.定容时俯视刻度线
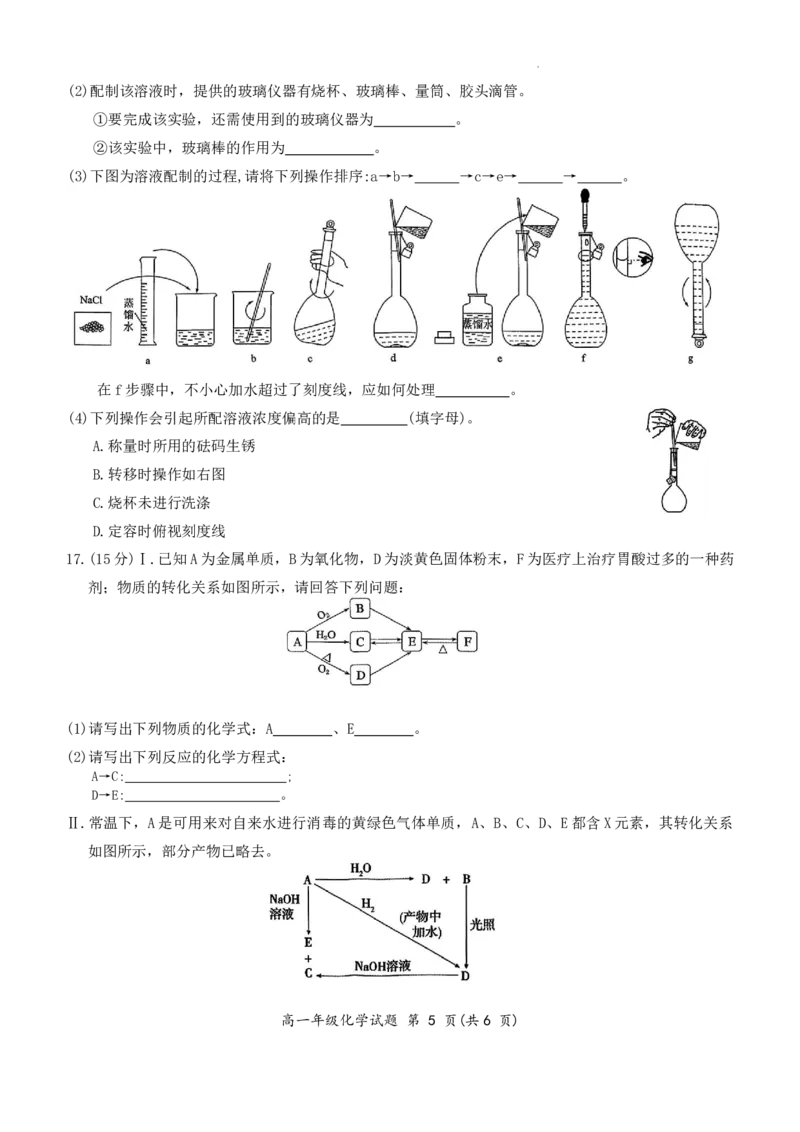
17.(15分)Ⅰ.已知A为金属单质,B为氧化物,D为淡黄色固体粉末,F为医疗上治疗胃酸过多的一种药
剂;物质的转化关系如图所示,请回答下列问题:
(1)请写出下列物质的化学式:A 、E 。
(2)请写出下列反应的化学方程式:
A→C: ;
D→E: 。
Ⅱ.常温下,A是可用来对自来水进行消毒的黄绿色气体单质,A、B、C、D、E都含X元素,其转化关系
如图所示,部分产物已略去。
高一年级化学试题 第 5 页(共6 页)
学科网(北京)股份有限公司(3)请分别写出A、E的化学式(如为溶液请写出溶质的化学式):A ,E 。
(4)A常用于合成漂白粉,漂白粉的有效成分为 (填物质名称);写出工业生产漂白粉的化
学方程式: 。
(5)漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及反应的化学方程式:
、 。
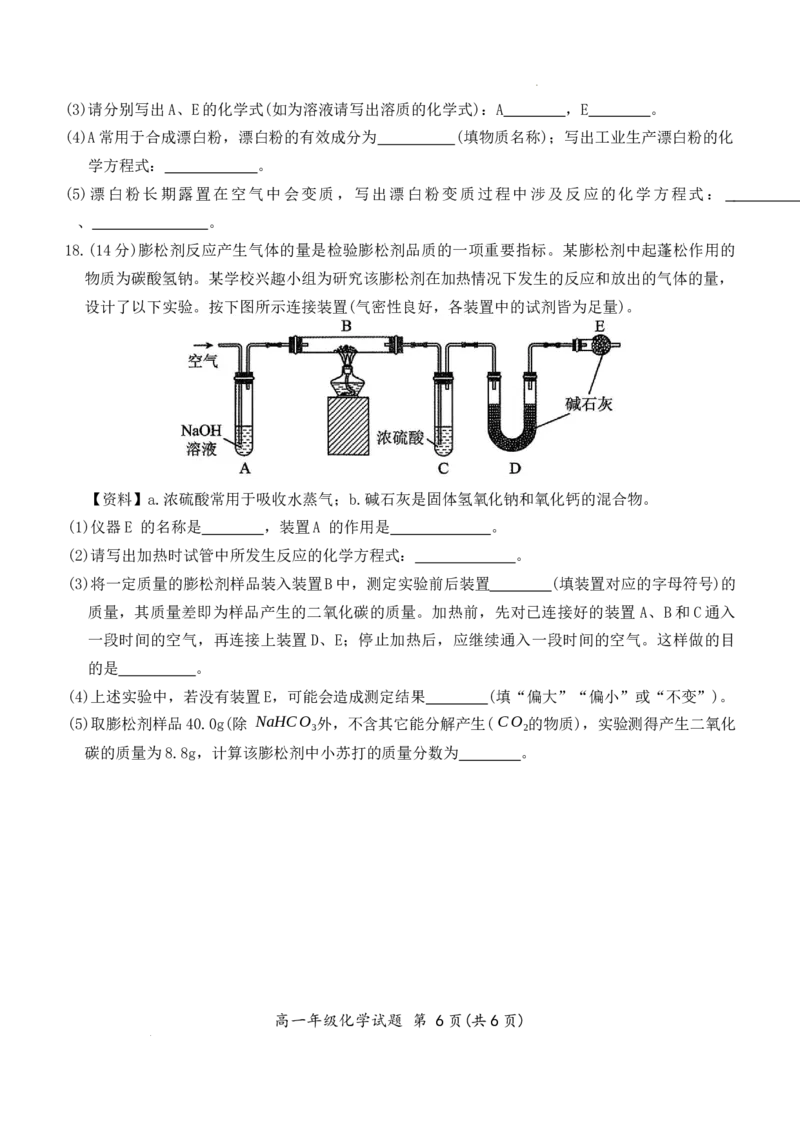
18.(14分)膨松剂反应产生气体的量是检验膨松剂品质的一项重要指标。某膨松剂中起蓬松作用的
物质为碳酸氢钠。某学校兴趣小组为研究该膨松剂在加热情况下发生的反应和放出的气体的量,
设计了以下实验。按下图所示连接装置(气密性良好,各装置中的试剂皆为足量)。
【资料】a.浓硫酸常用于吸收水蒸气;b.碱石灰是固体氢氧化钠和氧化钙的混合物。
(1)仪器E 的名称是 ,装置A 的作用是 。
(2)请写出加热时试管中所发生反应的化学方程式: 。
(3)将一定质量的膨松剂样品装入装置B中,测定实验前后装置 (填装置对应的字母符号)的
质量,其质量差即为样品产生的二氧化碳的质量。加热前,先对已连接好的装置 A、B和C通入
一段时间的空气,再连接上装置D、E;停止加热后,应继续通入一段时间的空气。这样做的目
的是 。
(4)上述实验中,若没有装置E,可能会造成测定结果 (填“偏大”“偏小”或“不变”)。
(5)取膨松剂样品40.0g(除 NaHCO 外,不含其它能分解产生( CO 的物质),实验测得产生二氧化
3 2
碳的质量为8.8g,计算该膨松剂中小苏打的质量分数为 。
高一年级化学试题 第 6页(共6页)
学科网(北京)股份有限公司