文档内容
河南省实验中学 学年上期期中试卷
2025——2026
高一化学
(时间:75分钟,满分:100 分)
可能用到相对原子质量:
C-12 N-14 O-16 Na-23 Al-27 S-32 Cl-35.5 Cu-64
一、选择题:(本大题共14小题,每小题3分,共42分,每小题只有一个正确选项)
1.下列说法不正确的是
A.徐光宪提出的稀土串级萃取理论使我国稀土提取技术取得重大进步
B.我国合成结晶牛胰岛素,为人类揭开生命奥秘作出了贡献
C.英国科学家道尔顿提出分子学说,为近代化学的发展奠定了坚实的基础
D.俄国化学家门捷列夫发现了元素周期律,使化学的研究变得有规律可循
2.下列关于电解质的说法正确的是
A.NaCl是电解质,所以NaCl固体能导电
B.NH 溶于水形成的溶液能导电,所以NH 是电解质
3 3
C.Cl 溶于水形成的溶液能导电,但Cl 是非电解质
2 2
D.熔融BaSO 能导电,因此BaSO 是电解质
4 4
3.下列各组物质的分类正确的是
A.氨水、水银、冰水混合物均属于混合物
B.含有氧元素的化合物叫氧化物
C.CO 、CO为酸性氧化物,Na O、Na O 为碱性氧化物
2 2 2 2
D.根据反应中所含元素化合价的改变情况,将物质分为氧化剂和还原剂
4.下列物质性质、用途及对应关系正确的是
A.钠具有还原性,可用于冶炼金属钛
B.碳酸钠受热分解产生大量气体,可作膨松剂
C.Cl 具有强氧化性,可用于漂白和自来水的杀菌消毒
2
D.过氧化钠为淡黄色固体,可用作呼吸面具中的供氧剂
5.下列关于氯的说法正确的是
A.氯气泄漏,可用浸有NaOH溶液的毛巾捂住口鼻,逃离现场
B.向新制氯水中滴入几滴石蕊溶液,溶液先变红后褪色
C.红热的铜丝在氯气里剧烈燃烧,生成棕红色的烟
D.氯元素在自然界中既有游离态又有化合态存在
学科网(北京)股份有限公司6.下列有关单质钠及其化合物的说法,正确的是
A.相同温度时,饱和Na CO 溶液碱性强于饱和NaHCO 溶液
2 3 3
B.少量CO 气体通入NaOH溶液中能生成NaHCO
2 3
C.反应温度高低和O 的用量共同决定Na转化为Na O或Na O
2 2 2 2
D.钠投入到CuSO 溶液中,有紫红色固体析出
4
7.下列各组粒子在指定溶液中能大量共存的是
A.“84”消毒液中:Fe2+、Cl-、Ca2+、H+
B.烧碱溶液中:K+、Br-、HCO -、CO 2-
3 3
C.澄清透明的溶液中:Cu2+、Mg2+、SO 2-、Cl-
4
D.0.1mol·L-1新制氯水中:Ba2+、Na+、CH COO-、OH-
3
8.下列离子方程式书写正确的是
A.将CO 通入BaCl 溶液中:CO +Ba2++H O=BaCO ↓+2H+
2 2 2 2 3
B.小苏打溶液滴加少量澄清石灰水Ca2++2OH-+2HCO=CaCO ↓+CO2+2H O
3 3 3 2
C.醋酸溶液除去水垢中的CaCO :CaCO +2H+=Ca2++H O+CO ↑
3 3 2 2
D.将钠投入到盛有水的烧杯中:Na+H O=Na++OH-+H ↑
2 2
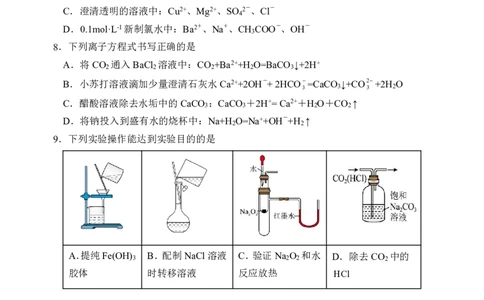
9.下列实验操作能达到实验目的的是
A.提纯Fe(OH)
3
B.配制NaCl溶液 C.验证Na
2
O
2
和水 D.除去CO
2
中的
胶体 时转移溶液 反应放热 HCl
10.设N 表示阿伏加德罗常数,下列说法正确的是
A
A.0.1molFeCl 在热水中完全反应,形成的Fe(OH) 胶体粒子数为0.1N
3 3 A
B.常温常压下,22.4LH 和22.4LN 的分子数相同
2 2
C.常温下,46gNO 和N O 组成的混合气体所含的分子数是3N
2 2 4 A
D.0.3mol·L-1Na
2
SO
4
溶液中含有Na的数目为0.6N
A
11.一定条件下,硝酸铜发生分解反应:
2C
2C
u
u(
N
N
O
O 3)
2
2
2
C
C
u
u
O
O+
4
4
N
N
O
O2
↑+
O
2O
↑ 收
集产生的所有
3 2 2 2
气体(NO 、O )共11.2L(已折算成标准状况)。关于这11.2L气体,下列叙述错误的是
2 2
学科网(北京)股份有限公司A.mNO :mO 23:4 B.VNO :VO 4:1
2 2 2 2
C.平均相对分子质量为44 D.N(N):N(O)2:5
12.根据实验目的,下列实验操作、现象及结论都正确的是
选项 实验目的 实验操作及现象 结论
A 制备FeOH 胶体
向沸水中逐滴加入5~6滴饱和FeCl
3
溶液, FeCl
3
与水反应产
3 持续加热,生成红褐色固体 生FeOH 胶体
3
将有色鲜花放入盛有干燥氯气的集气瓶中,
B 验证Cl 的漂白性 Cl 有漂白性
2 2
盖上玻璃瓶。一段时间后有色鲜花褪色
检验某无色溶液 取少量该无色溶液于试管中,加盐酸酸化的 该无色溶液中一
C
中是否含有SO2 氯化钡溶液,有白色沉淀生成 定含有SO2
4 4
探究物质燃烧的 把红热的铁丝伸进装满氯气的集气瓶中,反 燃烧不一定需要
D
条件 应剧烈,产生红棕色的烟 氧气
13.下列说法正确的是
A.将25g胆矾(CuSO 5H O)溶于1L水,该溶液的物质的量浓度为0.1molL1
4 2
B.VLAl (SO ) 溶液中含Al3+ag,则溶液中SO2-的物质的量浓度为 mol·L-1
2 4 3 4
C.同浓度的NaCl、MgCl 、AlCl 溶液体积之比为3:2:1,则Cl−浓度之比为3:4:3
2 3 18
D.将wga%的NaCl饱和溶液蒸发掉 g水,得到2a%的NaCl溶液
14.PH 常作为一种熏蒸剂,在贮粮中用于防治害虫,一种制备PH 的流程如图所示:
3 2 3
下列说法错误的是
A.上述流程中每一步均属于氧化还原反应
B.流程中,PH 都属于还原产物
3
C.次磷酸钠(NaH PO )属于正盐
2 2
D.次磷酸分解时既被还原成PH ,又被氧化成H PO
3 3 4
学科网(北京)股份有限公司二、非选择题(每空 2分,共58分)
15.(14分)有下列物质:①BaOH 固体;②KHSO 溶液;③HCl气体;④氨水;
2 4
⑤FeCl 固体;⑥冰醋酸;⑦Ca(ClO) 固体
3 2
(1)上述状态下的物质可导电的是 (填序号,下同)。
(2)写出KHSO 在熔融状态下电离方程式: 。
4
(3)写出用⑤制备FeOH 胶体的化学方程式: 。将③通入到FeOH 胶
3 3
体中至过量的实验现象是 。
(4)将⑥加入④中至恰好完全反应,则溶液导电能力的变化为 。(填“增大”或“减
小”或“不变”)
(5)写出①的溶液与②的溶液恰好中和时的离子方程式: 。
(6)漂白粉的有效成分是⑦,漂白粉生效的化学方程式为: 。
16.(14分)下图是化学实验室浓盐酸试剂标签上的部分内容。某化学小组同学计划用
该浓盐酸配制0.1mol/L的稀盐酸,现需要稀盐酸230mL。
盐酸
分子式:HCl
相对分子质量:36.5
密度:1.25g/cm3
HCl的质量分数:36.5%
(1) 该浓盐酸的物质的量浓度为 mol/L
(2) 现有该浓盐酸100g,需要加入一定量的水将其物质的量浓度稀释为原来的1/2,则加
入水的体积是 。
A.大于100mL B.小于100mL C.等于100mL
(3)配制稀盐酸时用到的玻璃仪器包括烧杯、玻璃棒、量筒,还有 、 。
(4)配制0.1mol/L的稀盐酸需要用量筒量取上述浓盐酸的体积为 mL
(5)测定所配制的稀盐酸,发现其浓度大于0.1mol/L,引起误差的原因可能是 。
A.量取浓盐酸时俯视刻度线
B.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入容量瓶
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容时俯视容量瓶刻度线
E.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
学科网(北京)股份有限公司(6)将所配制的稀盐酸100mL倒入 Na CO 和NaHCO 的固体混合物中,固体恰好全部
2 3 3
溶解,产生标准状况下气体体积为179.2mL,原混合物中Na CO 的物质的量为 mol
2 3
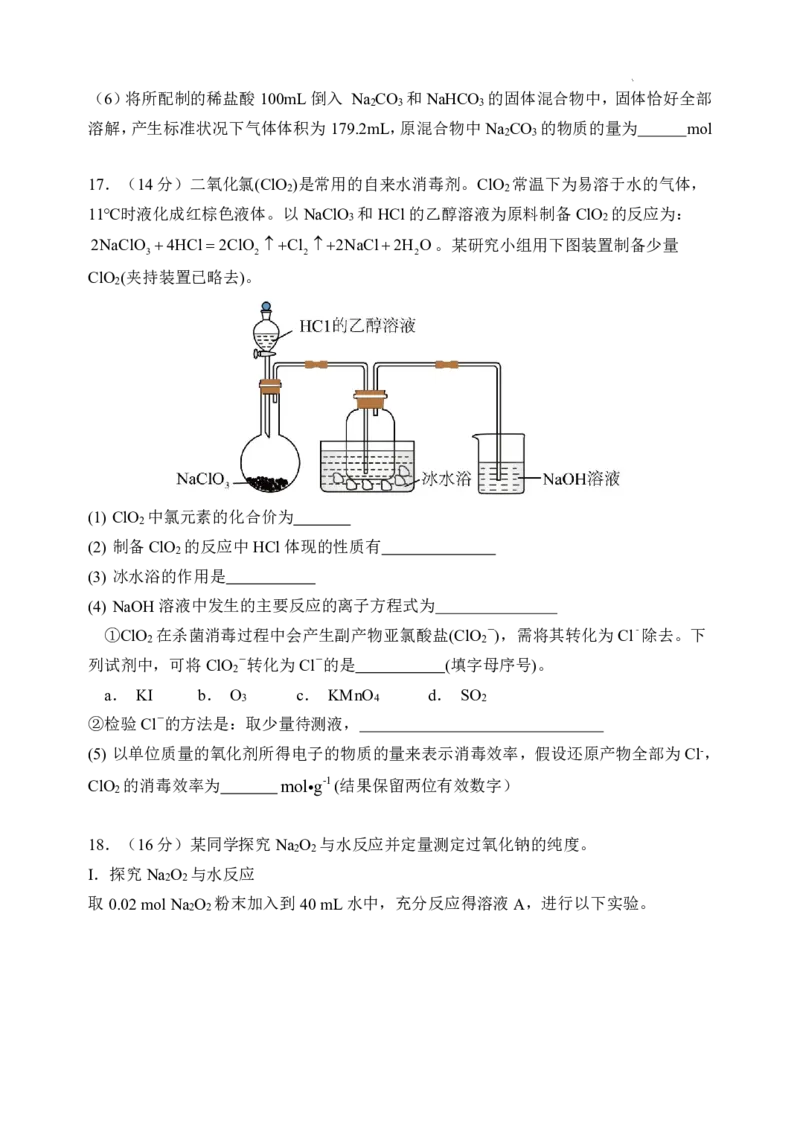
17.(14分)二氧化氯(ClO )是常用的自来水消毒剂。ClO 常温下为易溶于水的气体,
2 2
11℃时液化成红棕色液体。以NaClO 和HCl的乙醇溶液为原料制备ClO 的反应为:
3 2
2NaClO 4HCl2ClO Cl 2NaCl2H O。某研究小组用下图装置制备少量
3 2 2 2
ClO (夹持装置已略去)。
2
(1) ClO 中氯元素的化合价为
2
(2) 制备ClO 的反应中HCl体现的性质有
2
(3) 冰水浴的作用是
(4) NaOH溶液中发生的主要反应的离子方程式为
①ClO 在杀菌消毒过程中会产生副产物亚氯酸盐(ClO -),需将其转化为Cl﹣除去。下
2 2
列试剂中,可将ClO -转化为Cl-的是 (填字母序号)。
2
a. KI b. O c. KMnO d. SO
3 4 2
②检验Cl-的方法是:取少量待测液,
(5) 以单位质量的氧化剂所得电子的物质的量来表示消毒效率,假设还原产物全部为Cl-,
ClO 的消毒效率为 molg-1(结果保留两位有效数字)
2
18.(16分)某同学探究Na O 与水反应并定量测定过氧化钠的纯度。
2 2
I.探究Na O 与水反应
2 2
取0.02molNa O 粉末加入到40mL水中,充分反应得溶液A,进行以下实验。
2 2
学科网(北京)股份有限公司(1)由实验 中现象可知,Na O 与H O反应有H O 生成;
2 2 2 2 2
(2)由实验ⅱ、ⅲ、ⅳ可知,实验ⅱ中溶液褪色与 有关;
(3)由实验ⅳ、ⅴ可知,实验ⅳ中溶液褪色的原因是 。
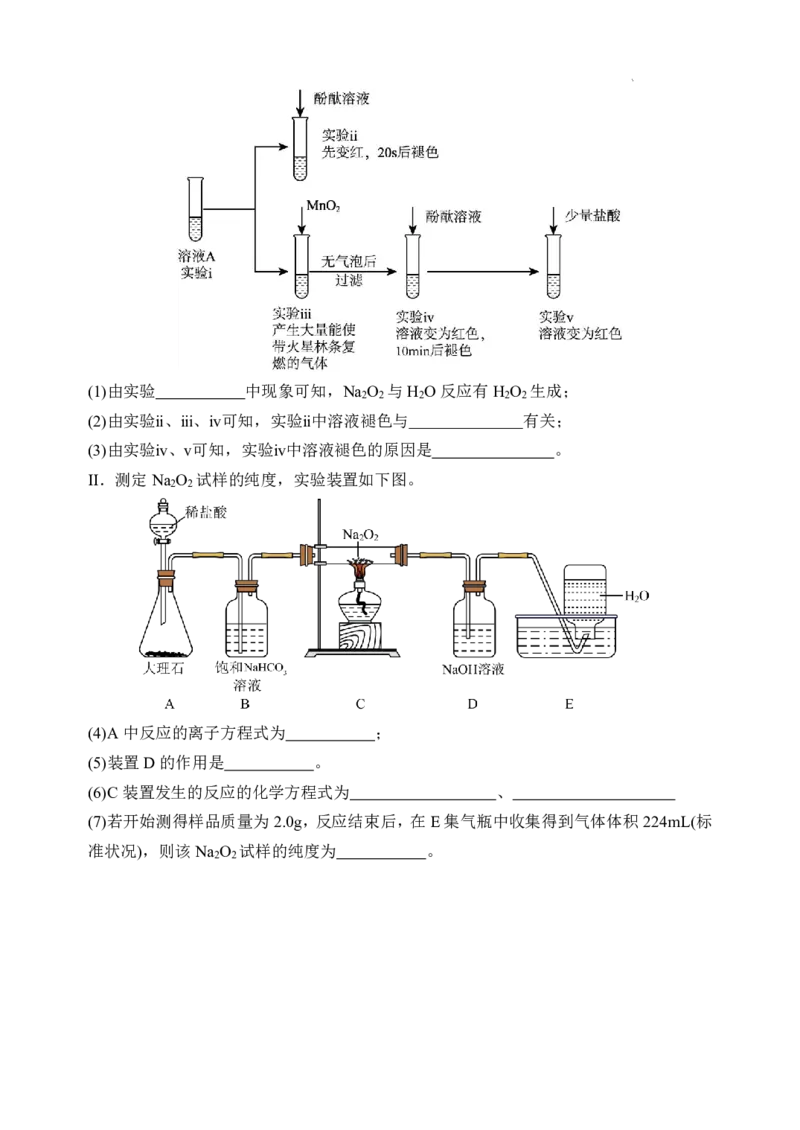
II.测定Na O 试样的纯度,实验装置如下图。
2 2
(4)A中反应的离子方程式为 ;
(5)装置D的作用是 。
(6)C装置发生的反应的化学方程式为 、
(7)若开始测得样品质量为2.0g,反应结束后,在E集气瓶中收集得到气体体积224mL(标
准状况),则该Na O 试样的纯度为 。
2 2
学科网(北京)股份有限公司