文档内容
2024 年兰州一中高一第一学期期中学业质量检测卷
化 学
时长:75分钟 总分:100分
第 I 卷(选择题 共 45 分)
一、单选题(每题3分,共45分)
1.剧烈运动时大量出汗,为维持体内电解质平衡,运动后应及时补充的离子是( )
A.Mg2+ B.Ca2+
C.Na+ D.Fe3+
【答案】C
2.电解质是( )
A.在水溶液里或熔融状态下全部电离的化合物
B.可溶性盐类
C.在水溶液里或熔融状态下能导电的化合物
D.导电性很强的物质
【答案】C
3.下列物质中,能够导电的电解质是( )
A.铜丝 B.熔融的MgCl
2
C.NaCl溶液 D.SO
3
【答案】B
4.下列物质的水溶液能导电,但属于非电解质的是( )
A.CHCOOH B.Cl
3 2
C.NHHCO D.NH
4 3 3
【答案】D
5.下列叙述正确的是( )
①NaO与NaO 都能和水反应生成碱,它们都是碱性氧化物
2 2 2
②NaO与CO 发生化合反应生成NaCO,NaO 与CO 发生置换反应生成O
2 2 2 3 2 2 2 2
③NaO是淡黄色物质,NaO 是白色物质
2 2 2
④NaO 可作供氧剂,而NaO不可
2 2 2
⑤NaO 和NaO焰色反应均为黄色
2 2 2
A.都正确 B.②③④⑤ C.②③⑤ D.④⑤
【答案】D6.下列说法中正确的是( )
A.非金属单质燃烧时火焰均为无色
B.NaCl与NaCO 灼烧时火焰颜色相同
2 3
C.焰色反应均应透过蓝色钴玻璃观察
D.只有金属单质灼烧时火焰才有颜色
【答案】B
7.有两份质量相同的NaHCO ,向第一份中加入盐酸使其充分反应;将第二份加热使其完全分解,冷却
3
至原温度再加入相同浓度的盐酸充分反应,则它们所耗用的盐酸的体积比为( )
A.2∶1 B.1∶1 C.1∶2 D.4∶1
【答案】B
8.用光洁的铂丝蘸取某无色溶液在无色火焰上灼烧,直接观察到火焰呈黄色,下列各判断正确的是(
)
A.只含有Na+
B.一定含有Na+,可能含有K+
C.既含有Na+,又含有K+
D.可能含有Na+,可能还含有K+
【答案】B
7.下列物质的分类正确的是( )
选项 碱 酸 盐 碱性氧化物 酸性氧化物
A NaOH HSO BaCO SO CO
2 4 3 2 2
B NaOH HCl NaCl NaO CO
2
C NaOH CHCOOH CaCl CO SO
3 2 2
D KOH HNO CaCO CaO SO
3 3 3
【答案】D
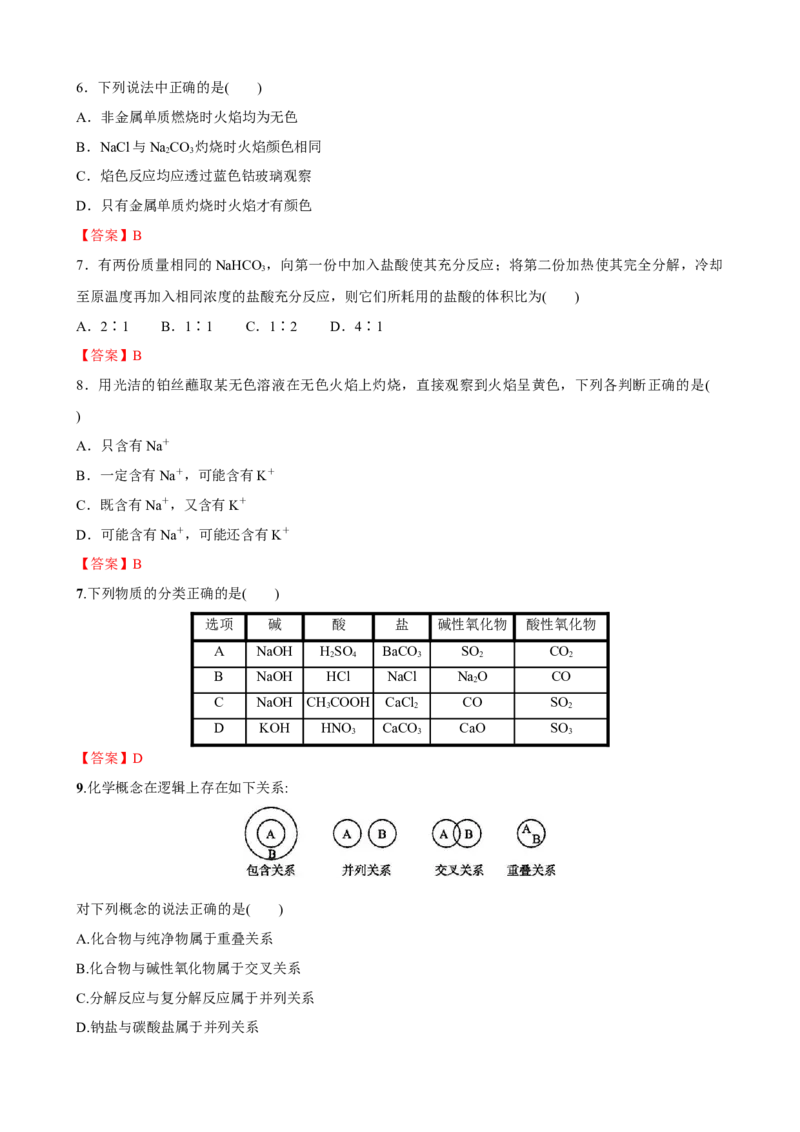
9.化学概念在逻辑上存在如下关系:
对下列概念的说法正确的是( )
A.化合物与纯净物属于重叠关系
B.化合物与碱性氧化物属于交叉关系
C.分解反应与复分解反应属于并列关系
D.钠盐与碳酸盐属于并列关系【答案】C
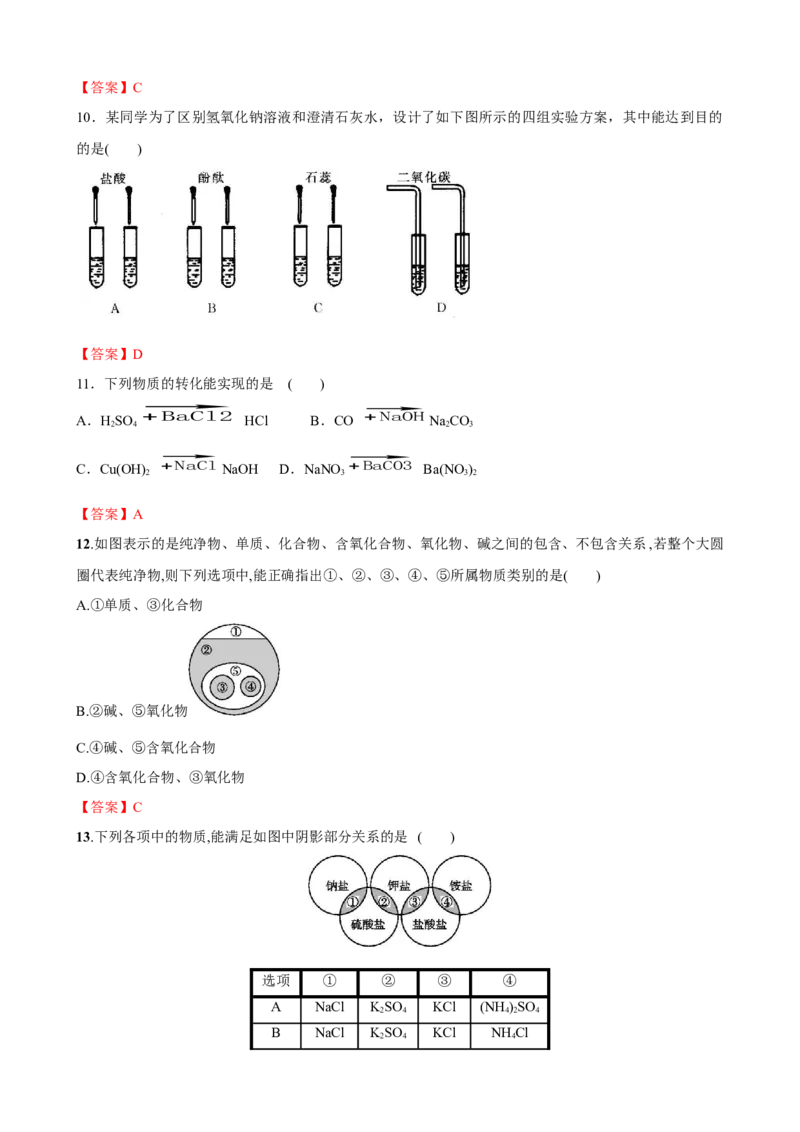
10.某同学为了区别氢氧化钠溶液和澄清石灰水,设计了如下图所示的四组实验方案,其中能达到目的
的是( )
【答案】D
11.下列物质的转化能实现的是 ( )
A.HSO ⃗ +BaCl2 HCl B.CO ⃗ +NaOH NaCO
2 4 2 3
C.Cu(OH) ⃗ +NaClNaOH D.NaNO ⃗ +BaCO3 Ba(NO )
2 3 3 2
【答案】A
12.如图表示的是纯净物、单质、化合物、含氧化合物、氧化物、碱之间的包含、不包含关系,若整个大圆
圈代表纯净物,则下列选项中,能正确指出①、②、③、④、⑤所属物质类别的是( )
A.①单质、③化合物
B.②碱、⑤氧化物
C.④碱、⑤含氧化合物
D.④含氧化合物、③氧化物
【答案】C
13.下列各项中的物质,能满足如图中阴影部分关系的是 ( )
选项 ① ② ③ ④
A NaCl KSO KCl (NH )SO
2 4 4 2 4
B NaCl KSO KCl NH Cl
2 4 4C NaSO KSO KCl NH Cl
2 4 2 4 4
D NaSO KSO KCl (NH )SO
2 4 2 4 4 2 4
【答案】C
14.已知KMnO 与浓盐酸在常温下反应生成Cl 。若用如图所示的实验装置来制备纯净、干燥的Cl ,并
4 2 2
试验它与金属的反应。每个虚线框表示一个单元装置,其中有错误的是( )
A.①和②处 B.②处
C.②和③处 D.②③④处
【答案】D
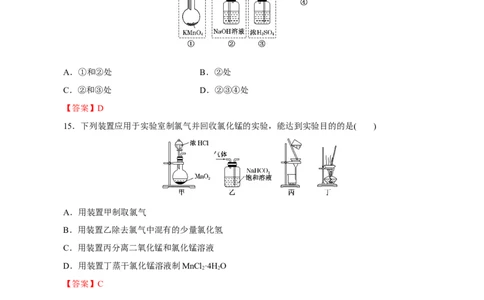
15.下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是( )
A.用装置甲制取氯气
B.用装置乙除去氯气中混有的少量氯化氢
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制MnCl ·4H O
2 2
【答案】C
第 II 卷(非选择题 共 55 分)
二、非选择题:包括第16题~第19题4个大题,共55分。
16.(10分)某溶液中可能含有K+、Na+、CO、Cl-中的一种或几种,为鉴别其中所含离子,现进
行如下实验:
序号 实验操作及现象
步骤① 取原溶液,进行焰色反应,显黄色,透过蓝色钴玻璃观察无紫色步骤② 取原溶液,向溶液中加入盐酸,有气体产生
请回答下列问题:
(1)原溶液中一定存在的离子是________(填离子符号,下同),一定不存在的离子是________,可能存
在的离子是________。
(2)为进一步确定原溶液中可能存在的离子是否存在,应进行的实验操作及判断依据是
________________________________________________________________________
【答案】(1)Na+、CO K+ Cl-
(2)取原溶液,向溶液中加入AgNO 溶液,有白色沉淀生成,再加入足量稀HNO ,若白色沉淀不消
3 3
失,则原溶液中存在Cl-,若白色沉淀消失,则原溶液中不存在Cl-
17.(10分)实验室里用如图所示仪器和药品来制取纯净的无水氯化铜(Cu+Cl CuCl )。图中A、
2 2
B、C、D、E、F表示玻璃管接口,接口的弯曲和伸长等部分未画出。根据要求填写下列各小题空白。
(1)如果所制气体从左向右流向时,上述各仪器装置的正确连接顺序是(填各装置的序号)( )接(
)接( )接( )接( )接( ),其中②与④装置相连时,玻璃管接口(用装置中字母表示)应
是________接________。
(2)装置②的作用是_______________________________________________________;
装置④的作用是__________________________________________________________。
(3)实验开始时,应首先检验装置的________,实验结束时,应先熄灭________处的酒精灯。
(4)在装置⑤的烧瓶中,发生反应的化学方程式为________________________________
【答案】(1)③ ⑤ ④ ② ① ⑥ C B
(2)除去Cl 中的水蒸气 除去Cl 中的HCl气体
2 2
(3)气密性 ①
(4)MnO +4HCl(浓) MnCl +Cl↑+2HO
2 2 2 2
18.(10分)Fe O 又称铁红,请根据要求完成下列问题。
2 3
(1)Fe O 固体(红棕色)属于 (填“混合物”或“纯净物”)。将其加入适量盐酸,发生反应的化学方程
2 3
式为 。
(2)用上述所得溶液进行以下实验:
取少量溶液置于试管中,滴入 NaOH 溶液,可观察到有红褐色沉淀生成,反应的化学方程式为,此反应属于 反应。
(3)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl 溶液,继续煮沸直至溶液呈
3
色,即可制得Fe(OH) 胶体。
3
(4)另取一小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL FeCl 溶液,振荡摇匀后,将此烧杯(编号甲)与盛有
3
Fe(OH) 胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到 烧杯中的液
3
体产生丁达尔效应,这个实验可以用来区别 。
【答案】(1)纯净物 Fe O+6HCl==2FeCl +3H O
2 3 3 2
(2)FeCl +3NaOH==Fe(OH) ↓+3NaCl 复分解
3 3
(3)红褐
(4)乙 溶液与胶体
19.(15分)如图所示,是一个制取氯气并以氯气为原料进行特定反应的装置,其中各试剂瓶装的试剂
为:B(氢硫酸)C(溴化亚铁溶液)D(碘化钾淀粉溶液)E(混有二氧化硫的氯化钡溶液)F(水)H
(紫色石蕊试液)
(1)A是氯气发生装 置,其化学反应方程式可以是:
; ;
;
(2)Ⅰ中b瓶内宜加入的液体一般是 。关闭Ⅰ中的活塞,在选取试剂正确且
适量的前提下,制取氯气时c中的液面不明显上升,估计可能的原因
是 。检查原因的简单方法是 ;怎样检验这一部分装置的气
密性 。
(3)用图示的Ⅱ或Ⅲ代替Ⅰ是否可行? 。简要说明理
由 。
(4)实验开始时,先点燃A处酒精灯,打开分液漏斗旋塞和Ⅰ处活塞,让氯气充满整个装置,再点燃G处酒精灯,回答下列问题:
a、怎样证明氯气已充满了整个装置
b、下列装置中的现象是B ;C ;D ;E ;F 。
(5)G装置的硬质玻璃管内盛有碳粉,发生氧化还原反应,其产物为二氧化碳、和氯化氢,写出G中
的反应的化学方程式 。装置F的作用
是 。
(6)在H处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是 。
(7)若将H处的烧杯中的溶液改为澄清的石灰水,反应过程中的现象为 (选填标号)
A、有白色沉淀 B、无现象 C、先生成白色沉淀而后消失
【答案】(1)MnO + 4HCl(浓) MnCl + H O + Cl ↑ 2NaCl + 2H SO (浓)+MnO
2 2 2 2 2 4 2
MnSO + Na SO + 2H O+ Cl ↑
4 2 4 2 2
6 HCl(浓)+ KClO KCl+ 3HO+ 3Cl ↑
3 2 2
(2)饱和食盐水 装置漏气 检查原因的简单方法:用湿润的碘化钾淀粉试纸靠近各接口处,漏气则试纸
变蓝。 检验这一部分装置的气密性:关闭分液漏斗旋塞和Ⅰ处活塞,从c中向容器内加饱和食盐水,当
c的下端浸入液面下且c中的液面高于b瓶内液面,并长时间不下降,则说明气密性好。
(3)Ⅱ可行,Ⅲ不行。Ⅱ与Ⅰ原理相同,而Ⅲ中因c瓶口密封,体积不能改变,增大压强会有危险。
(4)a、观察当整个装置内充满黄绿色气体时,说明氯气已充满整个装置。
b、B:有浅黄色沉淀生成。C:溶液由浅绿色变为深红棕色。D:溶液变蓝。
E:生成白色沉淀。F:溶液变为浅黄绿色。
(5)C + 2H O+ 2Cl == CO ↑+ 4HCl↑
2 2 2
向G中提供反应所需的水蒸气
(6)生成的HCI使紫色石蕊试液变红色,剩余的氯气又与水作用生成次氯酸,又起漂白作用,使红色褪
去。
(7)B