文档内容
2021 学年第二学期初三综合测试练习卷
(2022.06)
(完卷时间120分钟,满分135分)
考生注意:
1.试卷满分50分。
2.按要求在答题纸上规定的位置作答,在试卷、草稿纸上答题一律无效。
可能用到的相对原子质量:H-1 C-12 O-16 Ca-40 Cu-64 Zn-65
五、选择题(本大题共17题,共20分)
请将正确选项的代号用2B铅笔填涂在答题纸的相应位置上,更改答案时,用橡皮擦去,重新
填涂。21-34每题只有1个正确选项,每题1分,共14分。
1. 属于稀有气体的是
A. 氮气 B. 氦气 C. 氢气 D. 氧气
【答案】B
【解析】
【详解】由稀有气体包括氦气、氖气、氩气、氪气、氙气可知,B答案正确。故选B
2. Mg(OH) 属于
2
A. 氧化物 B. 酸 C. 碱 D. 盐
【答案】C
【解析】
【分析】氧化物是由两种元素组成,且其中一种元素为氧元素的化合物;酸为溶于水电离出的阳离子均为
氢离子的化合物;碱为电离出的阴离子均为氢氧根的化合物;盐是由金属阳离子或铵根离子和酸根阴离子
构成的化合物。
【详解】Mg(OH) 电离时产生的阴离子均为氢氧根,属于碱,故选C。
2
3. 灼烧氯化钠,火焰呈
A. 黄色 B. 紫色 C. 红色 D. 蓝色
【答案】A
【解析】
【分析】焰色反应,也称作焰色测试及焰色试验,是某些金属或它们的化合物在无色火焰中灼烧时使火焰
呈现特殊颜色的反应。
【详解】钠元素在焰色反应中使火焰呈黄色,钾元素在焰色反应中使火焰呈紫色,钙元素在焰色反应中使
火焰呈砖红色,铜元素在焰色反应中使火焰呈浅蓝色,故选A。4. 氯元素以游离态存在的物质是
A. Cl B. HCl C. KClO D. FeCl
2 3 2
【答案】A
【解析】
【详解】单质中的元素以游离态存在,故氯气中的氯元素以游离态存在,故选A。
5. 属于溶液的是
A. 牛奶 B. 豆浆 C. 冰水 D. 糖水
【答案】D
【解析】
【详解】A、牛奶属于混合物,但是不均一、不稳定,不属于溶液,选项错误;
B、豆浆属于混合物,但是不均一、不稳定,不属于溶液,选项错误;
C、冰水是纯净物,不属于混合物,故不是溶液,选项错误;
D、糖水是均一、稳定的混合物,属于溶液,选项正确。
故选D。
6. 次氯酸钠(NaClO)中,氯元素的化合价是
A. -1 B. +1 C. +5 D. +7
【答案】B
【解析】
【详解】次氯酸钠中钠元素显+1价,氧元素显-2价,设氯元素的化合价为x,根据化合物中,正、负化合
价的代数和为零,可得:(+1)+x+(-2)=0,x=+1。
故选B。
7. 和金刚石互为同素异形体的是
A. 碳-60 B. 木炭 C. 活性炭 D. 二氧化碳
【答案】A
【解析】
【分析】同素异形体是由相同元素组成的不同形态的单质。
【详解】A、碳-60和金刚石是由相同的碳元素组成的不同形态的单质。二者互为同素异形体。A正确。
B、木炭是无定形碳,含有杂质,是混合物,不是单质。B错。
C、活性炭是无定形碳,含有杂质,是混合物,不是单质。C错。
D、二氧化碳是化合物,不是单质。D错。
综上所述:选择A。
8. 属于氮肥的是
A. KCO B. NaSO C. Ca(HPO ) D. NH HCO
2 3 2 4 2 4 2 4 3【答案】D
【解析】
【分析】氮肥指的是一些含氮元素的化合物,如尿素、氨水、铵盐、硝酸盐等。
【详解】A、KCO 是钾肥。A错。
2 3
B、NaSO 不是化肥。B错。
2 4
C、Ca(HPO ) 是磷肥。C错。
2 4 2
D、NH HCO 是氮肥。D正确。
4 3
综上所述:选择D。
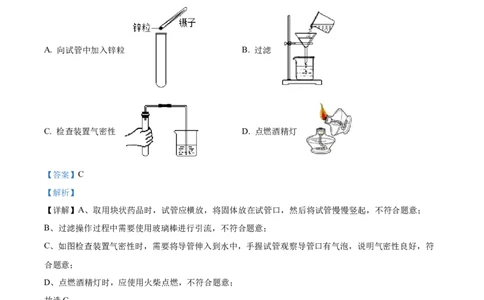
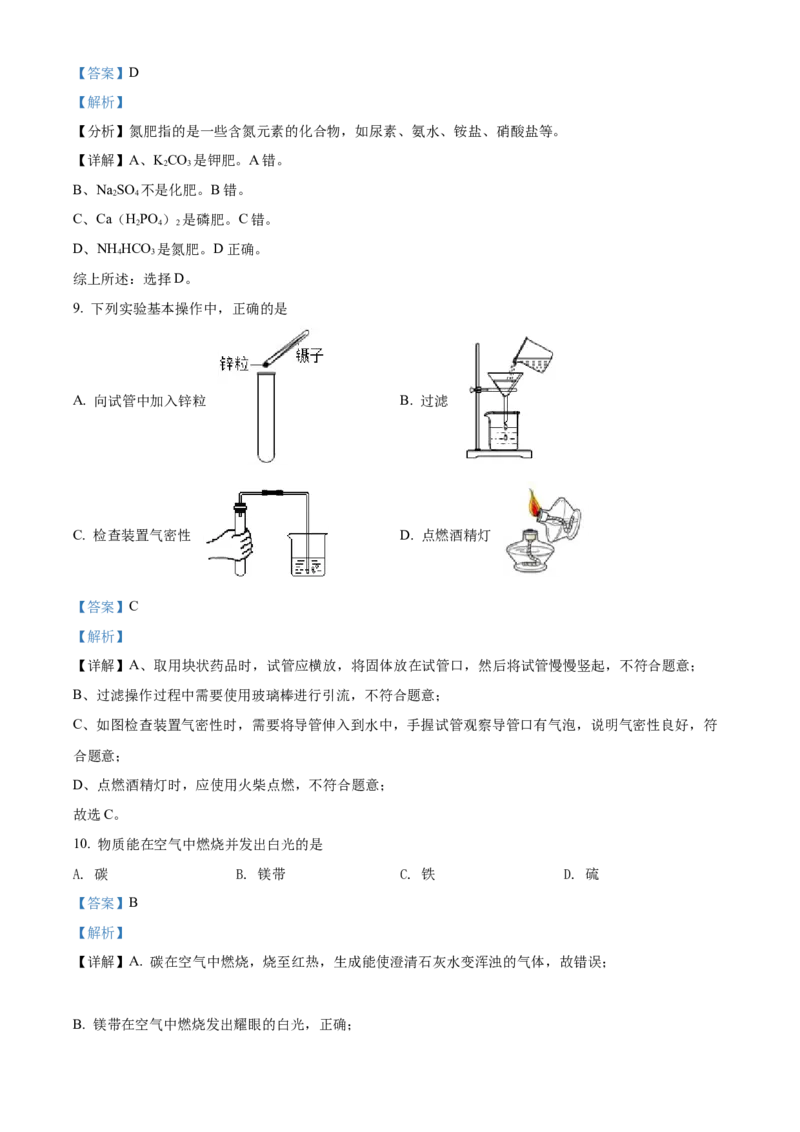
9. 下列实验基本操作中,正确的是
A. 向试管中加入锌粒 B. 过滤
C. 检查装置气密性 D. 点燃酒精灯
【答案】C
【解析】
【详解】A、取用块状药品时,试管应横放,将固体放在试管口,然后将试管慢慢竖起,不符合题意;
B、过滤操作过程中需要使用玻璃棒进行引流,不符合题意;
C、如图检查装置气密性时,需要将导管伸入到水中,手握试管观察导管口有气泡,说明气密性良好,符
合题意;
D、点燃酒精灯时,应使用火柴点燃,不符合题意;
故选C。
10. 物质能在空气中燃烧并发出白光的是
A. 碳 B. 镁带 C. 铁 D. 硫
【答案】B
【解析】
【详解】A. 碳在空气中燃烧,烧至红热,生成能使澄清石灰水变浑浊的气体,故错误;
B. 镁带在空气中燃烧发出耀眼的白光,正确;C. 铁在空气中不能燃烧,只能烧至红热,故错误;
D. 硫在在空气中燃烧出现微弱的淡蓝色火焰,故错误。
故选B。
11. 下列符号中的“2”与2CO中的“2”所表示的含义相似的是
A. 2C B. 2H C. CO D.
2 2
【答案】B
【解析】
【分析】化学符号前面的数字表示该符号所表示微粒的个数,2CO,表示2个一氧化碳分子。
【详解】A、化学符号前面的数字表示该符号所表示微粒的个数,2C,表示2个碳原子,不符合题意;
B、化学符号前面的数字表示该符号所表示微粒的个数,2H,表示2个氢气分子,符合题意;
2
C、化学符号右下角的数字表示该符号所表示微粒中的原子的个数。C中的“2”可以表示一个二氧化碳分
子中含有2个氧原子,不符合题意;
D、化学符号正上方的数字表示该元素或原子团的化合价。D中的“+2”表示碳元素的化合价为+2,不符合
题意;
故选B。
12. 用稀硫酸除铁锈的原理是
A. FeO+HSO ===FeSO+HO
2 4 4 2
B. Fe O+3HSO ===Fe (SO )+3H↑
2 3 2 4 2 4 3 2
C. Fe O+2HSO ===2FeSO+2HO
2 3 2 4 4 2
D. Fe O+3HSO ===Fe (SO )+3HO
2 3 2 4 2 4 3 2
【答案】D
【解析】
【详解】铁锈的主要成分是氧化铁,盐酸除铁锈的原理是 Fe O + 3H SO =Fe (SO ) + 3H O,故选D。
2 3 2 4 2 4 3 2
13. 为解决物质所含微粒数目大,不方便计量的问题,科学上引入的概念是
A. 相对原子质量 B. 物质的量 C. 相对分子质量 D. 摩尔质量
【答案】B
【解析】
【详解】科学上为解决物质所含微粒数目大,不方便计量的问题引入的概念是物质的量,故选B。
14. 将一定量锌和金属R的混合粉末加入一定量的氯化铜溶液中,溶液质量的变化情况如右图所示。反应
结束后过滤,下列说法正确的是A. 金属活动性:R>Zn>Cu
B. 滤液中一定有ZnCl 和金属R的盐,可能有CuCl
2 2
C. 滤渣中一定有Cu,可能有Zn和R
D. 若向滤渣中加入稀硫酸有气泡产生,则滤渣中一定有Zn
【答案】B
【解析】
【详解】A.由图像可知溶液质量先变大后减小之后不变,而锌和金属R混合粉末加入到一定量氯化铜溶液
中,锌的金属活动性比铜强,锌和氯化铜反应为 ,金属置换的质量关系为每65份
质量的锌置换出64份质量的铜,固体质量减小,溶质由氯化铜变为氯化锌,溶液质量变大,对应图像溶液
质量上升的斜线,则R和氯化铜反应应使溶液质量减少,对应图像溶液质量下降的斜线,反应完全后溶液
质量不变,对应图像中的水平横线。锌先和氯化铜反应,R之后再和氯化铜反应,所以锌的金属活动性比
R强,故三种金属活动性为Zn>R>Cu;故A错误,不符合题意;
的
B.根据三种金属 活动性Zn>R>Cu,结合图像,锌和氯化铜反应完全之后R再和氯化铜反应,锌被反
应完,但因为R的量和氯化铜的量不确定,因此氯化铜可能剩余,也可能被反应完。则滤液中一定含有氯
化锌、金属R的盐,可能含有氯化铜,故B正确,符合题意;
C.因为锌和R与氯化铜发生了反应,因此滤渣中一定有铜,但因为锌完全反应后,氯化铜才能和R反应,
因此锌没有剩余,因为R的量不确定,因此R可能剩余,故C错误,不符合题意;
D.因为锌完全反应后,氯化铜才能和R反应,因此锌已完全反应,滤渣中不可能含有锌,若向滤渣中加入
稀硫酸有气泡产生,说明滤渣中含有金属R,因为铜与稀硫酸不反应。故D错误,不符合题意。
故选B。
35-37每题有1-2个正确选项,每题2分,共6分。有2个正确选项的,选对1个得1分,多
选或错选得0分。
15. 物质的用途正确的是
A. 烧碱用于治疗胃酸过多
B. 食盐水用于清洗伤口
C. 无水硫酸铜用于检验水D. 明矾用于水的消毒
【答案】BC
【解析】
【分析】根据物质的性质判断。
【详解】A、烧碱是氢氧化钠的俗称,虽然氢氧化钠能中和过量的胃酸,但氢氧化钠具有强腐蚀性,如果
用氢氧化钠治疗胃酸过多,会严重腐蚀人的消化道,不符合题意;
B、食盐水具有一定的消毒杀菌作用,可用于清洗伤口,符合题意;
C、无水硫酸铜是白色粉末,遇水呈蓝色,因此可用于检验水,符合题意;
D、明矾净水是利用明矾溶于水后生成的胶状物吸附水中的固体杂质,使杂质沉降来达到净水目的,不能
用于水的消毒,不符合题意。
故选BC。
16. 有关化学反应的说法正确的是
A. 化学反应前后物质的总质量相等
B. 化学反应前后原子的物质的量总和相等
C. 化学反应前后物质种类相等
D. 化学反应前后分子的物质的量总和相等
【答案】AB
【解析】
【详解】A、根据质量守恒定律可知,化学反应前后物质的总质量相等,符合题意;
B、化学反应前后原子的种类和数目不变,故原子的物质的量总和相等,符合题意;
C、化学反应前后物质的种类一定发生改变,不符合题意;
的
D、化学反应前后分子 数目可能发生改变,故分子的物质的量总和不一定相等,不符合题意;
故选AB。
17. CO中混有少量的CO,用右图装置收集一瓶较纯净的CO,有关说法错误的是
2
A. 装置Ⅰ中可能是氢氧化钠溶液
B. 装置Ⅰ的作用是除去CO
2的
C. 装置Ⅱ 作用是收集CO
D. 若装置Ⅰ中导管始终保持液封,则不需要处理尾气
【答案】BC
【解析】
【详解】A、由于氢氧化钠能与二氧化碳反应而不与一氧化碳发生反应,故 I 中溶液可以是氢氧化钠溶液,
A 正确;
B、由装置的特点可知,气体通入后, I 中压强增大,液体会流向 Ⅱ , 反应结束后, CO 收集在 I 中,
故装置Ⅰ的作用是除去CO 并收集CO,B 错误;
2
C、由B可知, CO 收集在 I 中,C错误;
D、若 I 中导气管始终保持液封, CO 收集在 I 中,则不必处理尾气, D 正确。
故选BC。
六、简答题(本大题共4题,共30分)请根据要求在答题纸的相应位置作答。
18. 2022年北京成功举办冬奥会。
(1)冬奥火炬“飞扬”采用氢气作燃料。氢气燃烧的化学方程式为___________,该反应的基本类型是
___________,此处氢气作为燃料的主要优点是___________(写一条)。
(2)冬奥会速滑馆“冰丝带”,采用的是CO 跨临界直冷制冰技术,碳排放值趋近于零。水变成冰发生
2
了___________(选填“物理”或“化学”)变化,从微观角度分析变化的实质是___________。
(3)冬奥会场馆用低温消毒剂C H ClN 进行消毒,C H ClN 由___________种不同元素组成,属于
9 16 2 4 9 16 2 4
___________(选填“有机物”或“无机物”),1molC H ClN 中约含有___________个Cl原子(用科学
9 16 2 4
计数法表示)。
【答案】(1) ①. ②. 化合反应 ③. 环保
(2) ①. 物理 ②. HO分子间间隙变大
2
(3) ①. 4##四 ②. 有机物 ③. 1.204×1024
【解析】
【小问1详解】
氢气和氧气在点燃的条件下生成水,化学方程式为: ;该反应属于多变一的反应是
化合反应;氢气作为燃料,热值高,燃烧产物是水不污染环境;
【小问2详解】
水变成冰是物质的状态发生改变,发生的是物理变化;从微观角度来分析是水分子间的间隔变大;【小问3详解】
根据低温消毒剂的化学式可知,该物质是由碳、氢、氯、氮四种元素组成的,低温消毒剂C H C N 是含
9 16 l2 4
碳元素的化合物,属于有机物;1molC H ClN 中含有氯原子的个数约为
9 16 2 4
个。
19. 某小组同学对二氧化碳的制取和相关性质进行探究。
(1)用图一所示的装置制取二氧化碳。
Ⅰ.该装置能随时控制反应的发生和停止,请简述使反应停止的原理___________。
Ⅱ.若制得0.1摩尔二氧化碳,理论上需要消耗___________g碳酸钙(根据化学方程式列式计算)
(2)用实验证明碳酸型饮料中含有二氧化碳。
Ⅰ.用图二所示的装置进行实验:打开汽水瓶盖,立即塞上带导管的橡皮塞,将导管另一端伸入装有试剂的
试管中。
甲同学在试管中加入少量澄清石灰水,观察到试管内___________,由此得到结论:该汽水中含有二氧化
碳。乙同学在试管中加入少量紫色石蕊溶液,观察到试管内___________,乙同学认为也能得到甲同学的
结论。
Ⅱ.小组同学对甲、乙两位同学的实验方案进行评价。
认为甲同学的方案比较合理,其试管中发生反应的化学方程式为___________。质疑乙同学的方案不够严
密,认为也可能是该汽水中的柠檬酸随气体进入试管,而引起紫色石蕊溶液的变色。
Ⅲ.针对质疑,乙同学又进行了如下探究:
查阅资料:柠檬酸为无色晶体,易溶于水,常温稳定,分解温度约为175℃。
乙同学在自己实验的基础上,未添加试剂,只进行了一步实验操作,该操作是___________,观察到
___________,确认不是因为柠檬酸随气体进入试管而引起紫色石蕊溶液的变色。
【答案】(1) ①. 当用弹簧夹夹紧乳胶管时,继续产生的气体使试管内压强增大,液体被压回长颈漏
斗中,固液分离,反应停止 ②. 解:设至少需消耗xmolCaCO
3答:至少需消耗10gCaCO
3
(2) ①. 石灰水变浑浊 ②. 石蕊溶液变红色 ③. ④.
对试管稍微加热 ⑤. 溶液由红色变为紫色
【解析】
【小问1详解】
Ⅰ、图一装置能随时控制反应的发生和停止,该原理是当用弹簧夹夹紧乳胶管时,继续产生的气体使试管
内压强増大,液体被压回长颈漏斗中,固液分离,反应停止;
Ⅱ、见答案。
【小问2详解】
Ⅰ、二氧化碳与澄清石灰水反应生成碳酸钙沉淀和水,所以甲同学在试管中加入少量澄清石灰水,观察到
试管内澄清石灰水变浑浊;
二氧化碳溶于水并与水发生反应生成碳酸,所以乙同学在试管中加入少量紫色石蕊溶液,观察到试管内溶
液变红色;
Ⅱ、甲同学的方案比较合理,其试管中发生反应是二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,该反应
的化学方程式为 ;
Ⅲ、根据查阅资料:柠檬酸为无色晶体,易溶于水,常温稳定,分解温度约为175℃,而碳酸受热不稳定
易分解,所以乙同学在自己实验的基础上,未增加任何试剂,只需加热试管,可观察到溶液由红色变成紫
色。
的
20. 下表是KNO 在不同温度下 溶解度。
3
温度/℃ 0 20 40 60 80
溶解度(g/100gH O) 13.3 31.6 63.9 110 169
2(1)20℃时,KNO 的溶解度是___________。
3
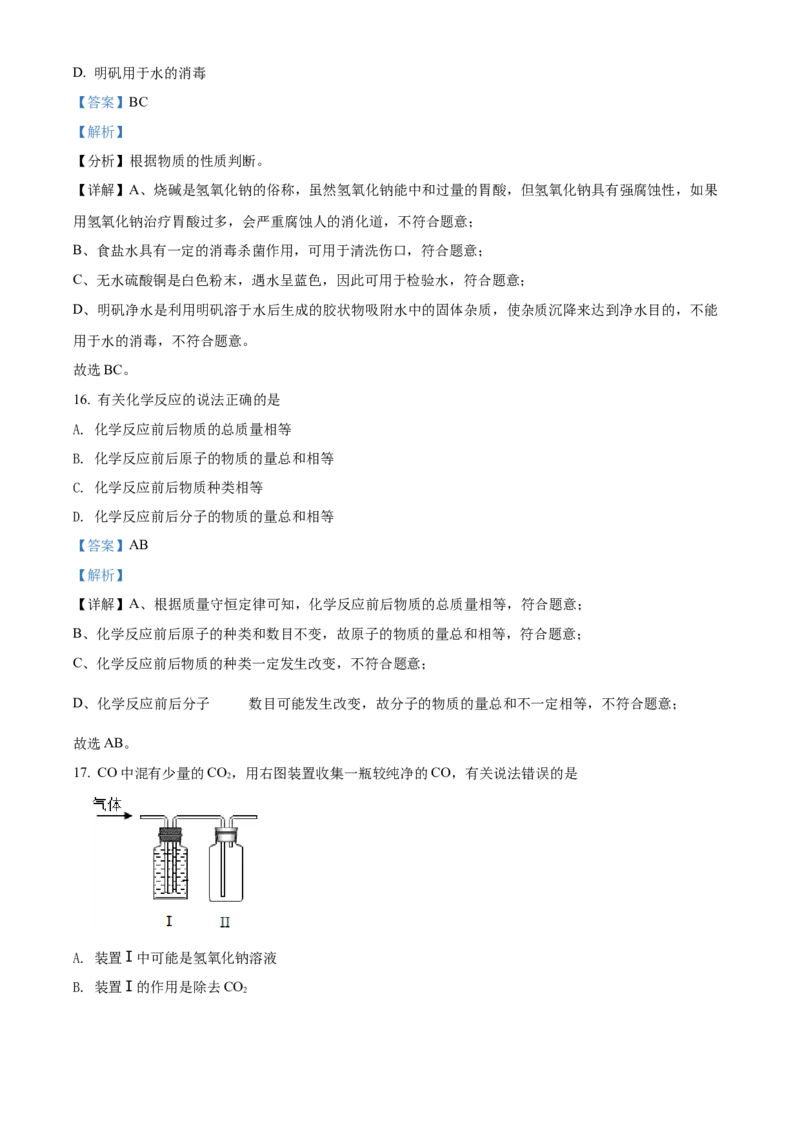
(2)将一定量的KNO 晶体加入盛有100g水的烧杯中,缓缓升温、充分溶解,不同温度下烧杯中溶液质
3
量如图所示。
Ⅰ.a、b、c、d四点对应的溶液中,属于饱和溶液的是___________(选填字母)。
Ⅱ.b点对应的溶液质量为___________g。
Ⅲ.d点对应的溶液,经过___________、___________、过滤、洗涤、干燥等操作,可以重新得到KNO 晶
3
体。
【答案】(1)31.6g/100gH O
2
(2) ①. a、b ②. 163.9 ③. 加热浓缩 ④. 降温结晶
【解析】
【小问1详解】
根据表格分析可知,20℃时,KNO 的溶解度是31.6g/100gH O;
3 2
【小问2详解】
Ⅰ、根据如图所示分析,60℃时,c点溶解的溶质质量为208g-100g=108g<110g(60℃时,KNO 的溶解
3
度),所以c、d对应的溶液不是饱和溶液,而a、b对应的溶液是饱和溶液;
Ⅱ、40℃时,b点对应的溶液质量为100g+63.9g=163.9g
Ⅲ、由于硝酸钾的溶解度受温度影响较大,故d点对应的不饱和溶液,经过加热浓缩、降温结晶、过滤、
洗涤、干燥等操作,可以重新得到KNO 晶体。
3
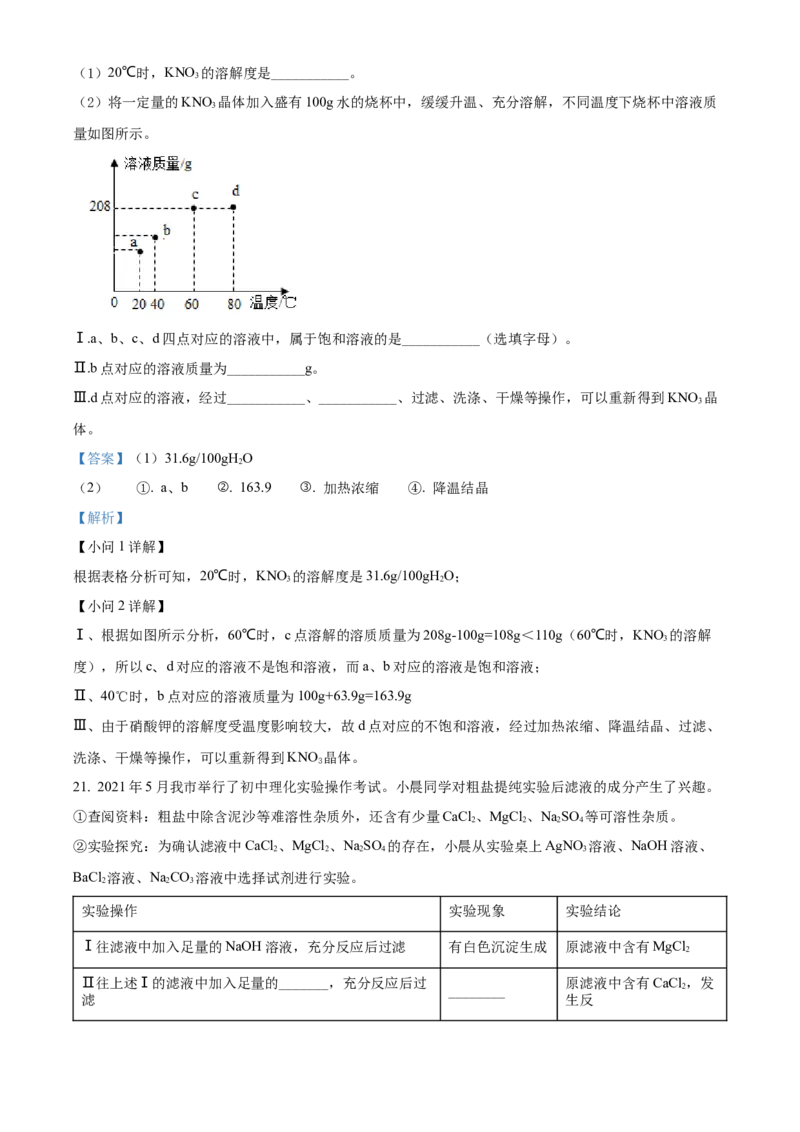
21. 2021年5月我市举行了初中理化实验操作考试。小晨同学对粗盐提纯实验后滤液的成分产生了兴趣。
①查阅资料:粗盐中除含泥沙等难溶性杂质外,还含有少量CaCl 、MgCl 、NaSO 等可溶性杂质。
2 2 2 4
②实验探究:为确认滤液中CaCl 、MgCl 、NaSO 的存在,小晨从实验桌上AgNO 溶液、NaOH溶液、
2 2 2 4 3
BaCl 溶液、NaCO 溶液中选择试剂进行实验。
2 2 3
实验操作 实验现象 实验结论
Ⅰ往滤液中加入足量的NaOH溶液,充分反应后过滤 有白色沉淀生成 原滤液中含有MgCl
2
Ⅱ往上述Ⅰ的滤液中加入足量的_______,充分反应后过 原滤液中含有CaCl ,发
________ 2
滤 生反应的化学方程式为
________
Ⅲ往上述Ⅱ的滤液中加入足量的___________,充分反应
有白色沉淀生成 原滤液中含有NaSO
后过滤 2 4
③实验反思:有同学认为实验Ⅲ不够严谨,理由是___________。老师另外提供试剂,建议小晨在实验
的
基础上继续验证NaSO 的存在,请写出实验方案___________。
2 4
【答案】 ①. NaCO 溶液 ②. 有白色沉淀生成 ③. ④.
2 3
BaCl 溶液 ⑤. 实验Ⅱ中碳酸钠若过量,也会和氯化钡反应产生白色沉淀,干扰NaSO 的检验 ⑥. 取
2 2 4
实验Ⅲ所得的沉淀,加入足量的稀盐酸(或稀硝酸),沉淀部分溶解(或沉淀不溶解),则原滤液中含有
NaSO
2 4
【解析】
【详解】②实验探究:
实验操作Ⅱ:因为氯化钙和碳酸钠反应生成碳酸钙和氯化钠,所以鉴定原滤液中含有CaCl ,可以往上述
2
Ⅰ的滤液中加入足量的NaCO 溶液,充分反应后过滤,有白色沉淀生成,证明原滤液中含有CaCl ,反应
2 3 2
的化学方程式为NaCO+CaCl =CaCO ↓+2NaCl;
2 3 2 3
实验操作Ⅲ:因为氯化钡与硫酸钠反应生成硫酸钡和氯化钠,所以鉴定原滤液中含有NaSO ,可以往上述
2 4
Ⅱ的滤液中加入足量的BaCl 溶液,充分反应后过滤,有白色沉淀生成,证明原滤液中含有NaSO ;
2 2 4
③实验反思:
因为实验Ⅱ中碳酸钠若过量,也会和氯化钡反应产生白色沉淀,干扰NaSO 的检验,所以认为实验Ⅲ不够
2 4
严谨;碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,为了排除碳酸钠对硫酸钡的干扰,可以通过以下实
验来进一步验证:取实验Ⅲ所得的沉淀,加入足量的稀盐酸(或稀硝酸),沉淀部分溶解(或沉淀不溶
解),则原滤液中含有NaSO 。
2 4