文档内容
2023 学年第二学期模拟检测 初三化学试卷
相对原子质量:H-1 C-12 O-16
一、选择题(共20分)
请将正确选项的代号用2B 铅笔填涂在答题纸的相应位置上,更改答案时,用橡皮擦去,重
新填涂。第1-14题,每题均只有1个正确选项。
1. 属于化学变化的是
A. 汽油挥发 B. 海水晒盐
C. 碳酸受热分解 D. 矿石粉碎
2. 空气中含量最多的气体是
A. O B. N C. He D. CO
2 2 2
3. 有关水的说法正确的是
A. 水是一种常见的溶质 B. 水可以用胆矾来检验
C. 水是由氢元素、氧元素组成 D. 水是由氢、氧原子构成的
4. 铁酸镍(NiFe O) 可作为催化剂将CO 转化为O,已知NiFe O 中 Fe 为+3 价, 则 Ni元素的化合
3 4 2 2 2 4
价为
A. +1 B. +2 C. +3 D. +4
5. 胃液中过多的盐酸可用止酸剂中的氢氧化镁缓解,发生的化学反应属于
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
6. 属于复合肥料的是
A. NH NO B. Ca(NO ) C. (NH )PO D. KSO
4 3 3 2 4 3 4 2 4
7. 取少量生石灰,加入适量的水形成的溶液,其pH 可能为
A. 4 B. 6 C. 7 D. 11
8. 俗名通常体现了物质的组成、性质或用途。下列对物质俗名的理解正确的是
A. 食盐:NaCl可用作食品调味剂 B. 水银: 汞(Hg) 是液态的银(Ag)
C. 火碱: NaOH 具有可燃性 D. 纯碱:纯净的碱
9. 下列化学方程式书写正确的是
A. CO+CuO═Cu+CO ↑ B. CaCO +2HCl=CaCl +H O+CO↑
2 3 2 2 2
C. Cu+2AgCl=CuCl +2Ag D. Fe O+3H SO =F (SO )+3H O
2 2 3 2 4 2 4 3 2
10. 下列物质的用途只利用其物理性质的是
A. CO 用于灭火 B. 稀有气体用作电光源
2
C. 熟石灰改良酸性土壤 D. 氢气冶炼金属
11. “赠人玫瑰,手留余香”,玫瑰中大马酮(化学式为C H O) 是其香味的来源。下列有关大马酮的
13 18说法,正确的是
A. 一个分子含有9个H B. 碳、氢元素的质量比为 13: 18
2
C. 该分子中氢元素的质量分数最大 D. 该物质的摩尔质量是 190g/mol
12. 据 Science杂志报道,科学家合成了一种环状碳分子——C ,这种分子具有广泛的应用前景。下列有
18
关说法正确的是
A. C 属于有机物 B. C 和金刚石是同素异形体
18 18
C. C 完全燃烧后的产物是CO D. C 和金刚石的化学性质完全不同
18 18
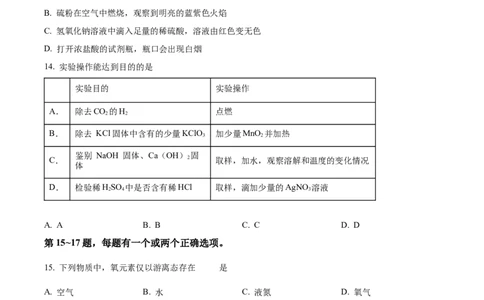
13. 实验现象描述正确的是
A. 木炭和氧化铜在高温的条件下反应,黑色固体变红色
B. 硫粉在空气中燃烧,观察到明亮的蓝紫色火焰
C. 氢氧化钠溶液中滴入足量的稀硫酸,溶液由红色变无色
D. 打开浓盐酸的试剂瓶,瓶口会出现白烟
14. 实验操作能达到目的的是
实验目的 实验操作
A. 除去CO 的H 点燃
2 2
B. 除去 KCl固体中含有的少量KClO 加少量MnO 并加热
3 2
鉴别 NaOH 固体、Ca(OH) 固
C. 2 取样,加水,观察溶解和温度的变化情况
体
D. 检验稀HSO 中是否含有稀HCl 取样,滴加少量的AgNO 溶液
2 4 3
A. A B. B C. C D. D
第15~17题,每题有一个或两个正确选项。
的
15. 下列物质中,氧元素仅以游离态存在 是
A. 空气 B. 水 C. 液氮 D. 氧气
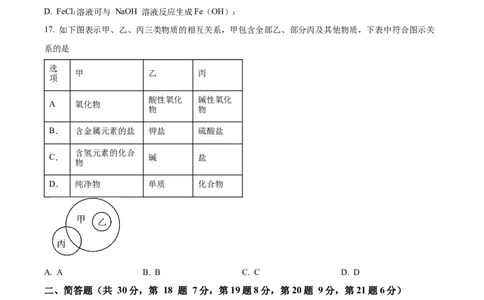
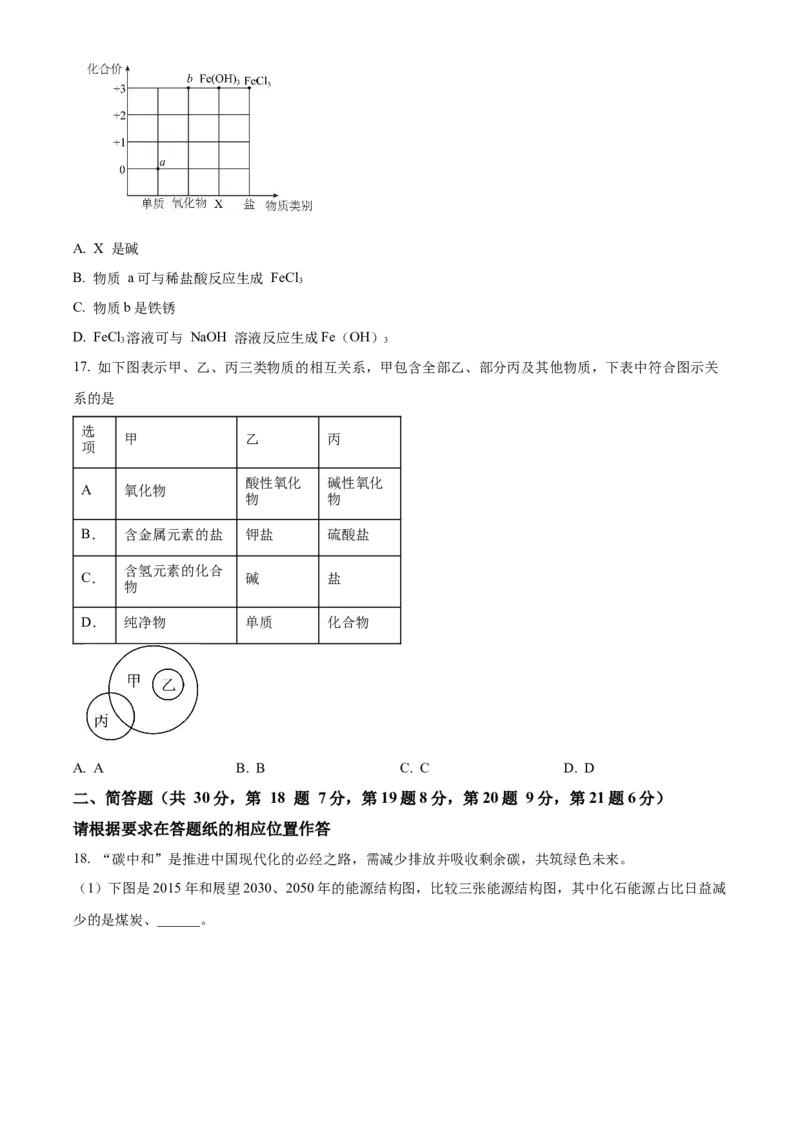
16. 以化合价为纵坐标,以物质类别为横坐标绘制的图像叫“价类图”。如图所示为铁元素的“价类二维
图”。下列说法正确的是A. X 是碱
B. 物质 a可与稀盐酸反应生成 FeCl
3
C. 物质b是铁锈
D. FeCl 溶液可与 NaOH 溶液反应生成Fe(OH)
3 3
17. 如下图表示甲、乙、丙三类物质的相互关系,甲包含全部乙、部分丙及其他物质,下表中符合图示关
系的是
选
甲 乙 丙
项
酸性氧化 碱性氧化
A 氧化物
物 物
B. 含金属元素的盐 钾盐 硫酸盐
含氢元素的化合
C. 碱 盐
物
D. 纯净物 单质 化合物
A. A B. B C. C D. D
二、简答题(共 30分,第 18 题 7分,第19题8分,第20题 9分,第21题6分)
请根据要求在答题纸的相应位置作答
18. “碳中和”是推进中国现代化的必经之路,需减少排放并吸收剩余碳,共筑绿色未来。
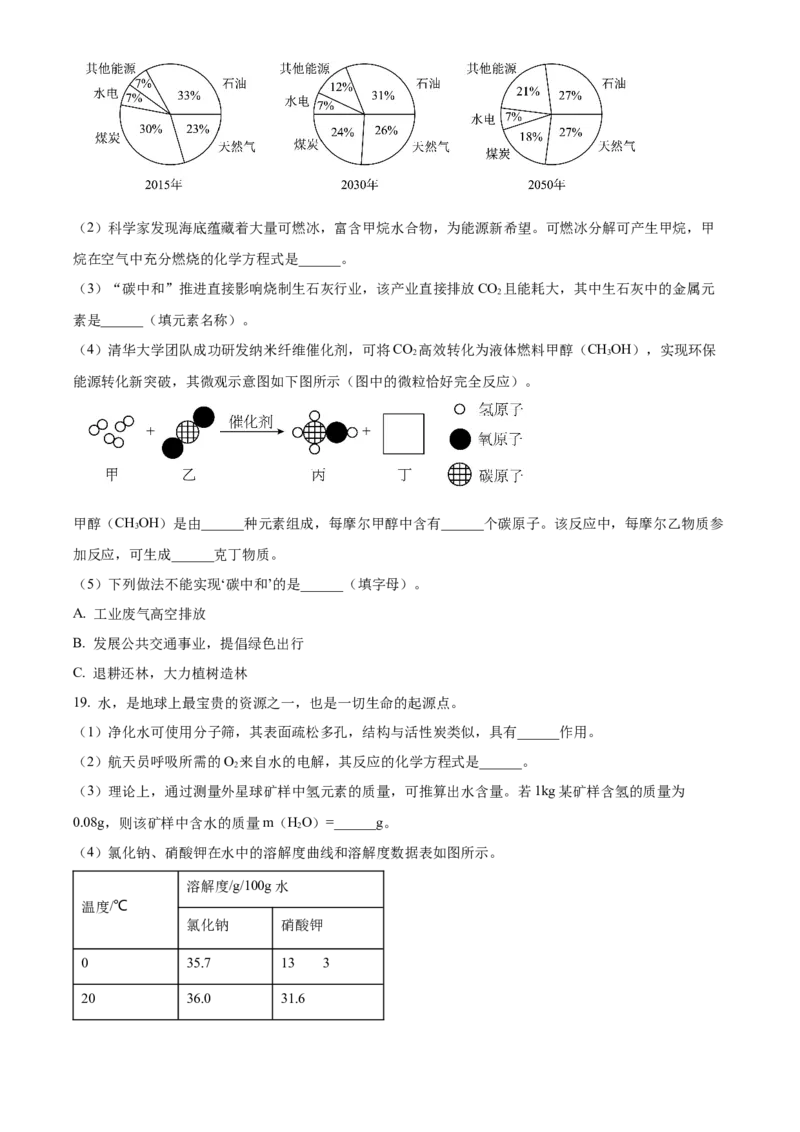
(1)下图是2015年和展望2030、2050年的能源结构图,比较三张能源结构图,其中化石能源占比日益减
少的是煤炭、______。(2)科学家发现海底蕴藏着大量可燃冰,富含甲烷水合物,为能源新希望。可燃冰分解可产生甲烷,甲
烷在空气中充分燃烧的化学方程式是______。
(3)“碳中和”推进直接影响烧制生石灰行业,该产业直接排放CO 且能耗大,其中生石灰中的金属元
2
素是______(填元素名称)。
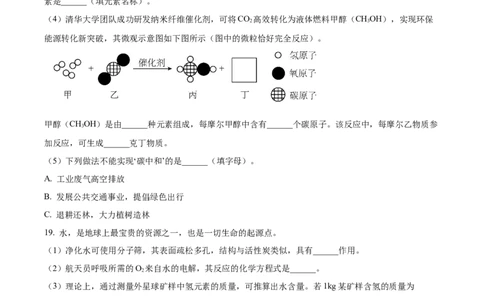
(4)清华大学团队成功研发纳米纤维催化剂,可将CO 高效转化为液体燃料甲醇(CHOH),实现环保
2 3
能源转化新突破,其微观示意图如下图所示(图中的微粒恰好完全反应)。
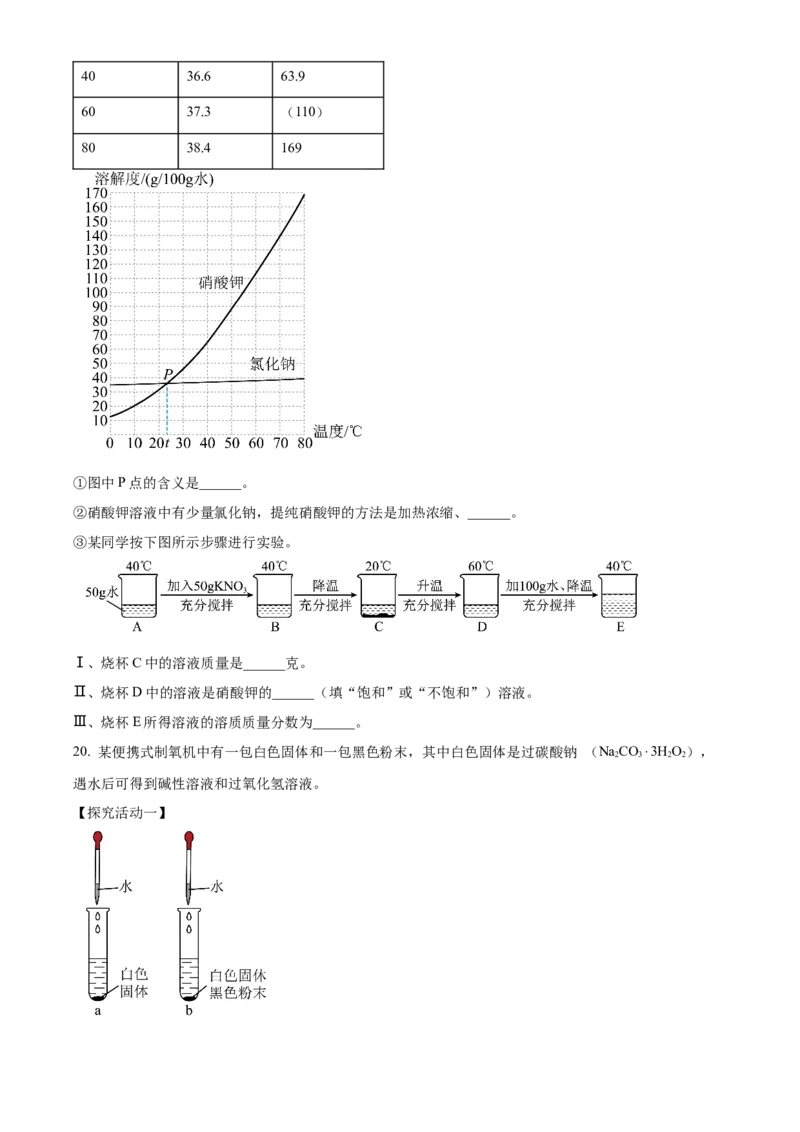
甲醇(CHOH)是由______种元素组成,每摩尔甲醇中含有______个碳原子。该反应中,每摩尔乙物质参
3
加反应,可生成______克丁物质。
(5)下列做法不能实现‘碳中和’的是______(填字母)。
A. 工业废气高空排放
B. 发展公共交通事业,提倡绿色出行
C. 退耕还林,大力植树造林
19. 水,是地球上最宝贵的资源之一,也是一切生命的起源点。
(1)净化水可使用分子筛,其表面疏松多孔,结构与活性炭类似,具有______作用。
(2)航天员呼吸所需的O 来自水的电解,其反应的化学方程式是______。
2
(3)理论上,通过测量外星球矿样中氢元素的质量,可推算出水含量。若1kg某矿样含氢的质量为
0.08g,则该矿样中含水的质量m(HO)=______g。
2
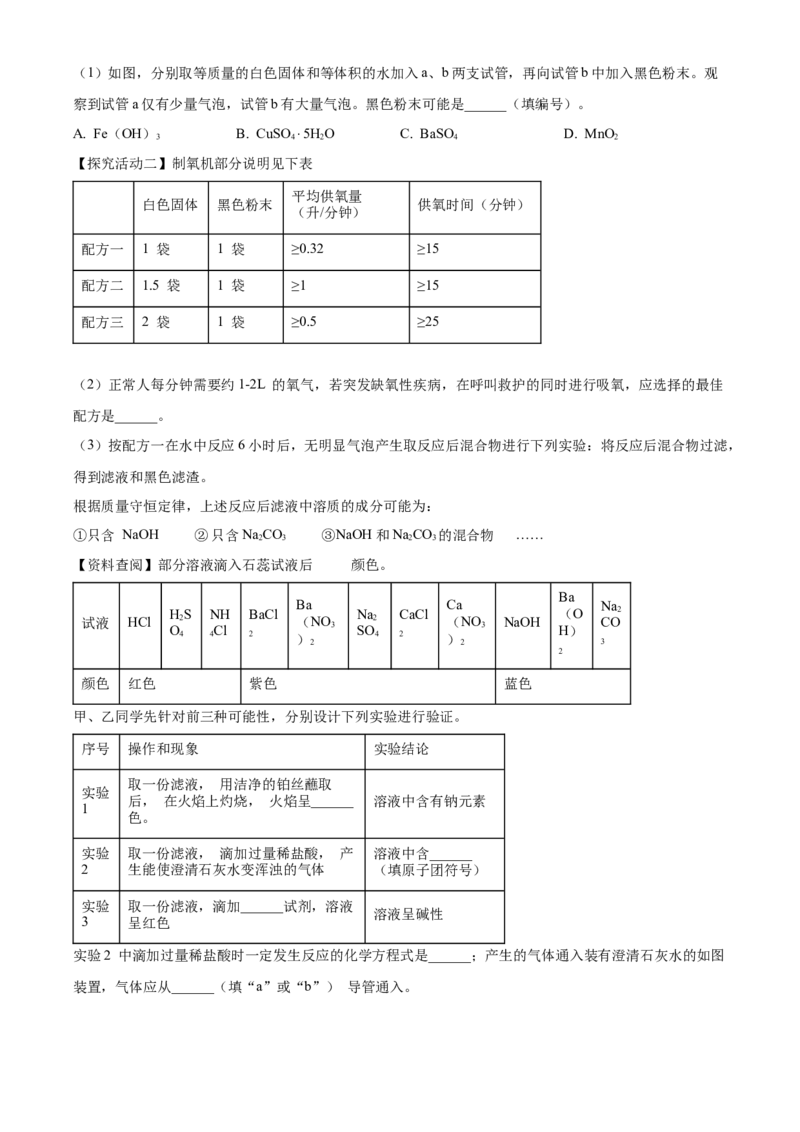
(4)氯化钠、硝酸钾在水中的溶解度曲线和溶解度数据表如图所示。
溶解度/g/100g水
温度/℃
氯化钠 硝酸钾
.
0 35.7 13 3
20 36.0 31.640 36.6 63.9
60 37.3 (110)
80 38.4 169
①图中P点的含义是______。
②硝酸钾溶液中有少量氯化钠,提纯硝酸钾的方法是加热浓缩、______。
③某同学按下图所示步骤进行实验。
Ⅰ、烧杯C中的溶液质量是______克。
Ⅱ、烧杯D中的溶液是硝酸钾的______(填“饱和”或“不饱和”)溶液。
Ⅲ、烧杯E所得溶液的溶质质量分数为______。
20. 某便携式制氧机中有一包白色固体和一包黑色粉末,其中白色固体是过碳酸钠 (NaCO⋅3HO),
2 3 2 2
遇水后可得到碱性溶液和过氧化氢溶液。
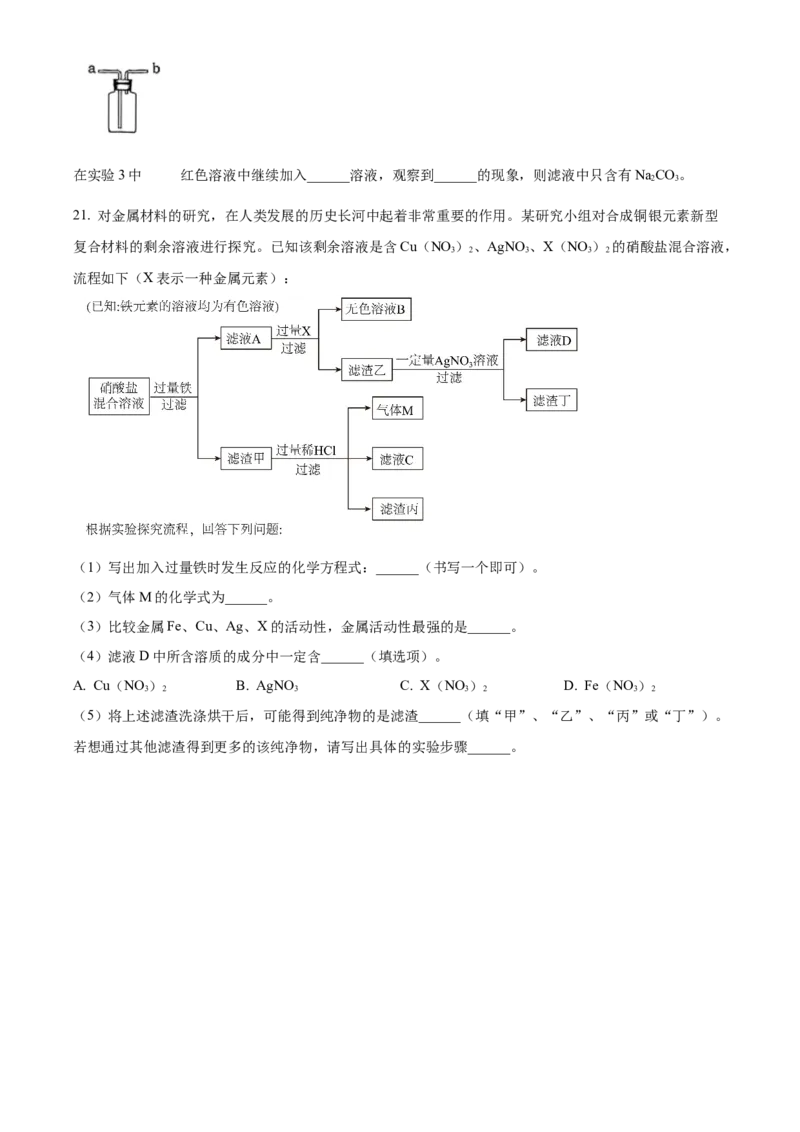
【探究活动一】(1)如图,分别取等质量的白色固体和等体积的水加入a、b两支试管,再向试管b中加入黑色粉末。观
察到试管a仅有少量气泡,试管b有大量气泡。黑色粉末可能是______(填编号)。
A. Fe(OH) B. CuSO ⋅5HO C. BaSO D. MnO
3 4 2 4 2
【探究活动二】制氧机部分说明见下表 。
平均供氧量
白色固体 黑色粉末 供氧时间(分钟)
(升/分钟)
配方一 1 袋 1 袋 ≥0.32 ≥15
配方二 1.5 袋 1 袋 ≥1 ≥15
配方三 2 袋 1 袋 ≥0.5 ≥25
(2)正常人每分钟需要约1-2L 的氧气,若突发缺氧性疾病,在呼叫救护的同时进行吸氧,应选择的最佳
配方是______。
(3)按配方一在水中反应6小时后,无明显气泡产生取反应后混合物进行下列实验:将反应后混合物过滤,
得到滤液和黑色滤渣。
根据质量守恒定律,上述反应后滤液中溶质的成分可能为:
①只含 NaOH ②只含NaCO ③NaOH和NaCO 的混合物 ……
2 3 2 3
【资料查阅】部分溶液滴入石蕊试液后 的颜色。
Ba
Ba Ca Na
HS NH BaCl Na CaCl (O 2
试液 HCl 2 (NO 2 (NO NaOH CO
O Cl 3 SO 3 H)
4 4 2 ) 4 2 )
2 2 3
2
颜色 红色 紫色 蓝色
甲、乙同学先针对前三种可能性,分别设计下列实验进行验证。
序号 操作和现象 实验结论
取一份滤液, 用洁净的铂丝蘸取
实验
后, 在火焰上灼烧, 火焰呈______ 溶液中含有钠元素
1
色。
实验 取一份滤液, 滴加过量稀盐酸, 产 溶液中含______
2 生能使澄清石灰水变浑浊的气体 (填原子团符号)
实验 取一份滤液,滴加______试剂,溶液
溶液呈碱性
3 呈红色
实验2 中滴加过量稀盐酸时一定发生反应的化学方程式是______;产生的气体通入装有澄清石灰水的如图
装置,气体应从______(填“a”或“b”) 导管通入。的
在实验3中 红色溶液中继续加入______溶液,观察到______的现象,则滤液中只含有NaCO。
2 3
21. 对金属材料的研究,在人类发展的历史长河中起着非常重要的作用。某研究小组对合成铜银元素新型
复合材料的剩余溶液进行探究。已知该剩余溶液是含Cu(NO )、AgNO、X(NO ) 的硝酸盐混合溶液,
3 2 3 3 2
流程如下(X表示一种金属元素):
(1)写出加入过量铁时发生反应的化学方程式:______(书写一个即可)。
(2)气体M的化学式为______。
(3)比较金属Fe、Cu、Ag、X的活动性,金属活动性最强的是______。
(4)滤液D中所含溶质的成分中一定含______(填选项)。
A. Cu(NO ) B. AgNO C. X(NO ) D. Fe(NO )
3 2 3 3 2 3 2
(5)将上述滤渣洗涤烘干后,可能得到纯净物的是滤渣______(填“甲”、“乙”、“丙”或“丁”)。
若想通过其他滤渣得到更多的该纯净物,请写出具体的实验步骤______。