文档内容
非金属及其化合物
1.(09年山东理综·10)下列关于氯的说法正确的是
A.Cl 具有很强的氧化性,在化学反应中只能作氧化剂
2
B.若35 Cl、37 若Cl为不同的核素,有不同的化学性质学科
17 17
C.实验室制备Cl,可用排放和食盐水集气法收集
2
D.1.12LCl 含有1.7N 个质子(N 表示阿伏伽德罗常数)
2 A A
答案:C
2(. 09年宁夏理综·7)将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相
同条件下测定),则该氮氧化合物的化学式为
A.NO B.NO C.NO D.NO
2 2 2 2 2 4
答案:A
3.(09年广东理基·22)下列关于硅单质及其化合物的说法正确的是
①硅是构成一些岩石和矿物的基本元素
②水泥、玻璃、水晶饰物都是硅酸盐制品
③高纯度的硅单质广泛用于制作光导纤维
④陶瓷是人类应用很早的硅酸盐材料
A.①② B.②③ C.①④ D.③④
答案:C
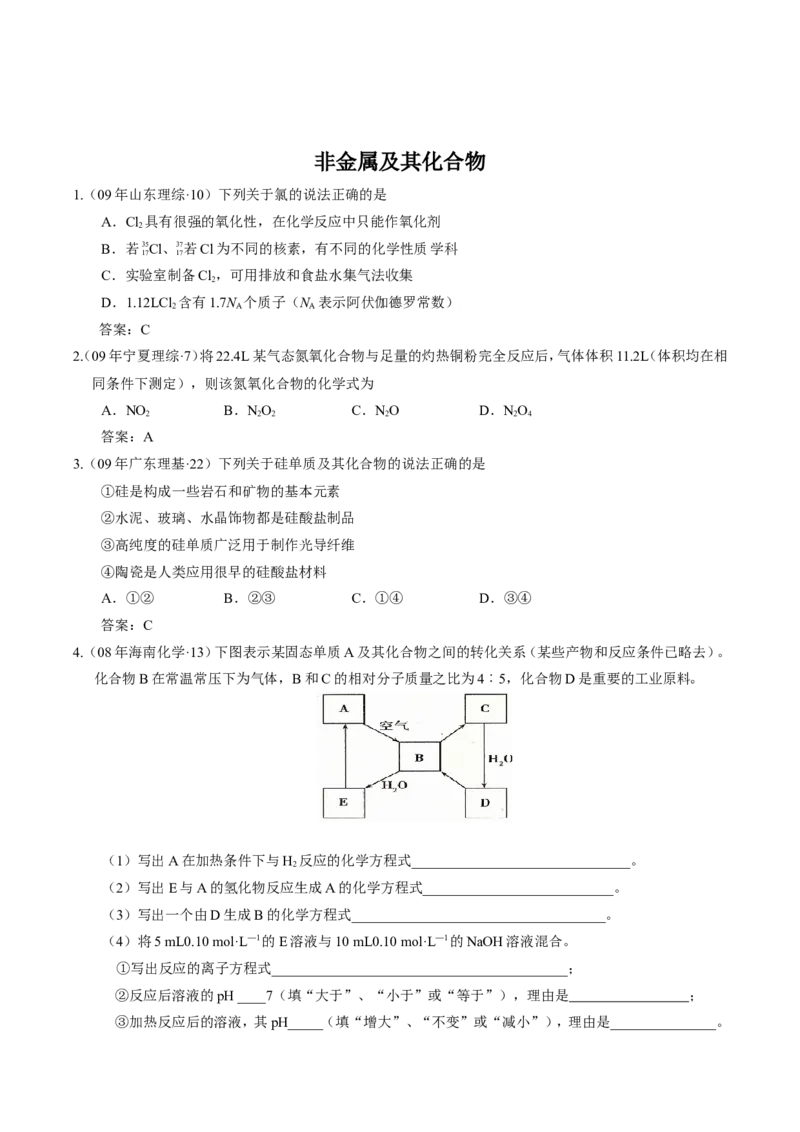
4. (08年海南化学·13)下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。
化合物B在常温常压下为气体,B和C的相对分子质量之比为4︰5,化合物D是重要的工业原料
(1)写出A在加热条件下与H 反应的化学方程式_______________________________。
2
(2)写出E与A的氢化物反应生成A的化学方程式___________________________。
(3)写出一个由D生成B的化学方程式____________________________________。
(4)将5 mL0.10 mol·L—1的E溶液与10 mL0.10 mol·L—1的NaOH溶液混合。
①写出反应的离子方程式__________________________________________;
②反应后溶液的pH ____7(填“大于”、“小于”或“等于”),理由是 ;
③加热反应后的溶液,其pH_____(填“增大”、“不变”或“减小”),理由是_______________。△
答案.(8分)(1)H+S HS(写成可逆反应也正确)
2 2
(2)HSO + 2H S=3S + 3H O
2 3 2 2
△ △
(3)C+2H SO(浓) CO ↑+2SO ↑+2H O(其他合理答案也给分如Cu+ 2HSO(浓) CuSO
2 4 2 2 2 2 4 4
+SO↑+ 2H O等)
2 2
(4)①HSO +2OH- = SO 2- + 2H O
2 3 3 2
②大于 NaSO 溶液中SO 2-发生水解使溶液显碱性
2 3 3
③增大 升高温度促进NaSO 溶液的水解
2 3
【知识动脉】
知识框架
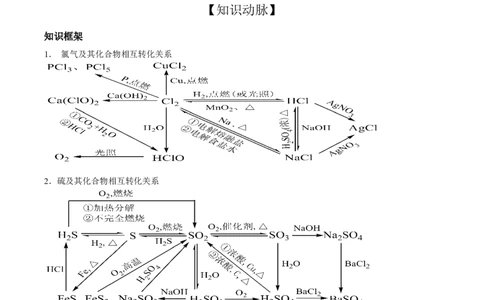
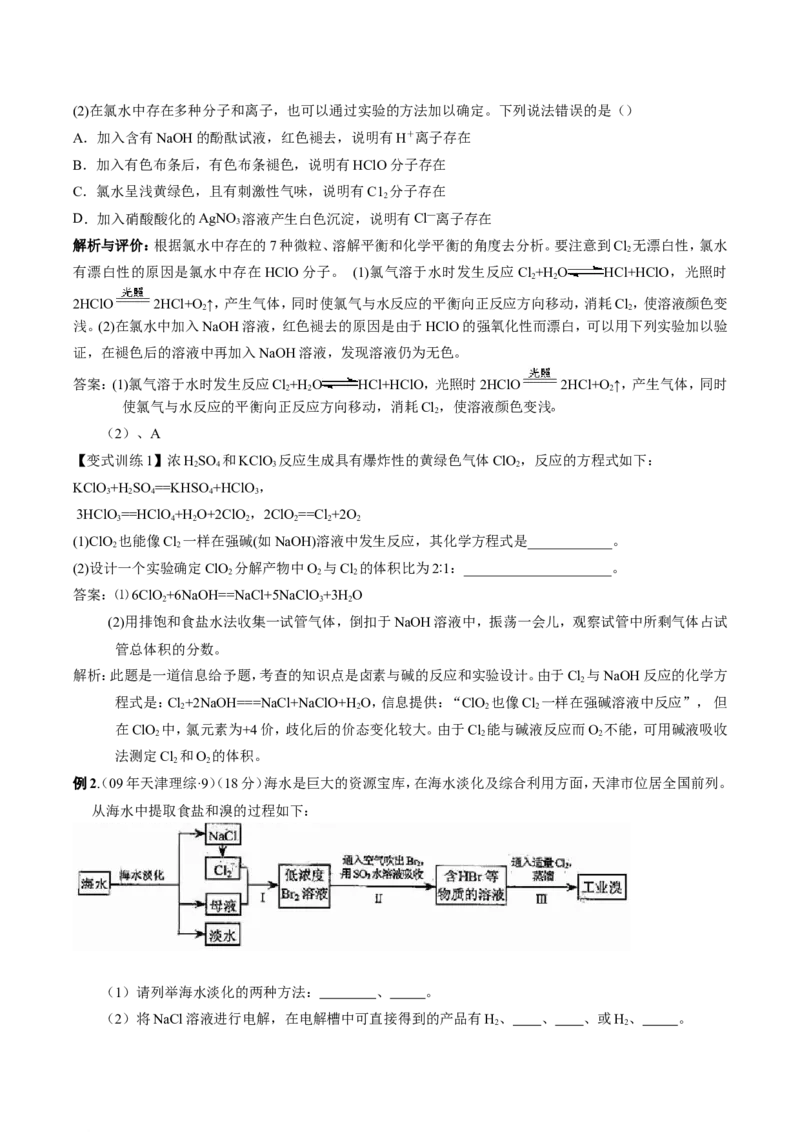
1. 氯气及其化合物相互转化关系
2.硫及其化合物相互转化关系
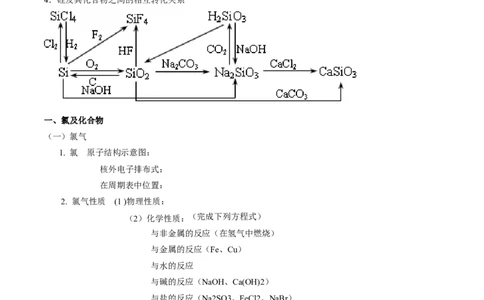
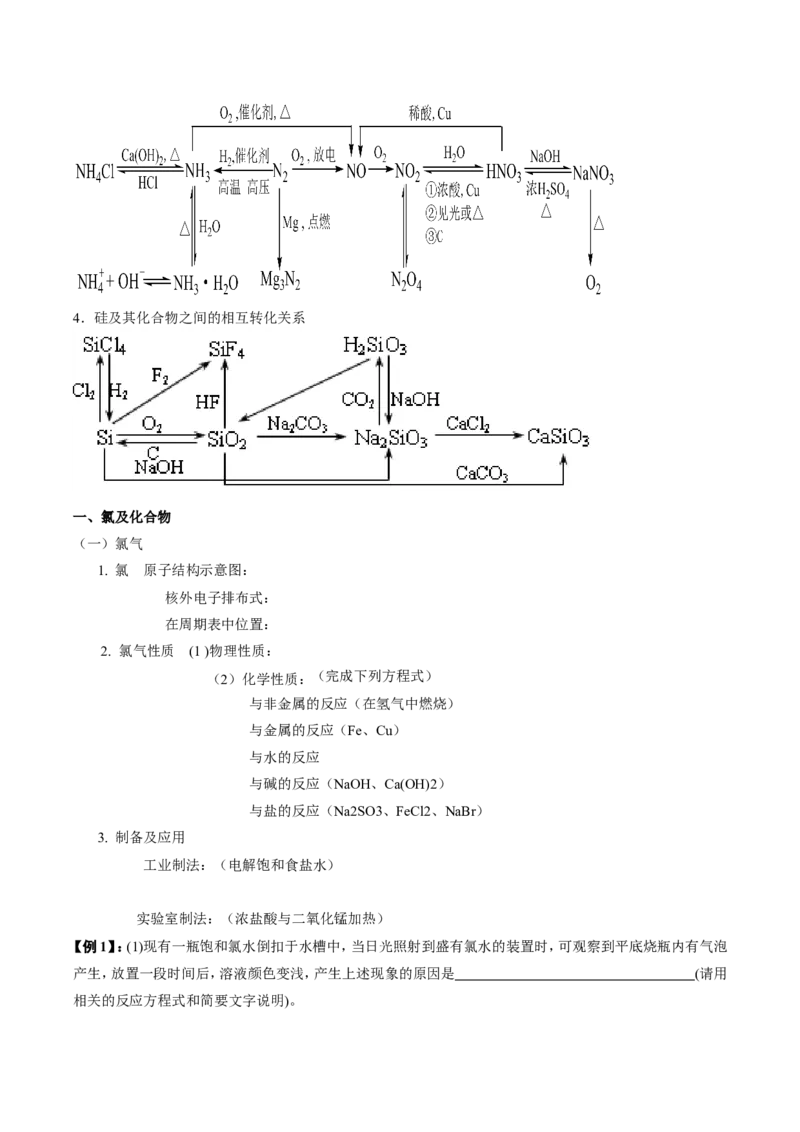
3.氮及其化合物相互转化关系4.硅及其化合物之间的相互转化关系
一、氯及化合物
(一)氯气
1. 氯 原子结构示意图:
核外电子排布式:
在周期表中位置:
2. 氯气性质 (1 )物理性质:
(2)化学性质:(完成下列方程式)
与非金属的反应(在氢气中燃烧)
与金属的反应(Fe、Cu)
与水的反应
与碱的反应(NaOH、Ca(OH)2)
与盐的反应(Na2SO3、FeCl2、NaBr)
3. 制备及应用
工业制法:(电解饱和食盐水)
实验室制法:(浓盐酸与二氧化锰加热)
【例1】:(1)现有一瓶饱和氯水倒扣于水槽中,当日光照射到盛有氯水的装置时,可观察到平底烧瓶内有气泡
产生,放置一段时间后,溶液颜色变浅,产生上述现象的原因是 (请用
相关的反应方程式和简要文字说明)。(2)在氯水中存在多种分子和离子,也可以通过实验的方法加以确定。下列说法错误的是()
A.加入含有NaOH的酚酞试液,红色褪去,说明有H+离子存在
B.加入有色布条后,有色布条褪色,说明有HClO分子存在
C.氯水呈浅黄绿色,且有刺激性气味,说明有C1 分子存在
2
D.加入硝酸酸化的AgNO 溶液产生白色沉淀,说明有Cl—离子存在
3
解析与评价:根据氯水中存在的7种微粒、溶解平衡和化学平衡的角度去分析。要注意到Cl 无漂白性,氯水
2
有漂白性的原因是氯水中存在HClO分子。 (1)氯气溶于水时发生反应Cl+H O HCl+HClO,光照时
2 2
2HClO 2HCl+O ↑,产生气体,同时使氯气与水反应的平衡向正反应方向移动,消耗Cl,使溶液颜色变
2 2
浅。(2)在氯水中加入NaOH溶液,红色褪去的原因是由于HClO的强氧化性而漂白,可以用下列实验加以验
证,在褪色后的溶液中再加入NaOH溶液,发现溶液仍为无色。
答案:(1)氯气溶于水时发生反应Cl+H O HCl+HClO,光照时2HClO 2HCl+O ↑,产生气体,同时
2 2 2
使氯气与水反应的平衡向正反应方向移动,消耗Cl,使溶液颜色变浅
2
(2)、A
【变式训练1】浓HSO 和KClO 反应生成具有爆炸性的黄绿色气体ClO ,反应的方程式如下:
2 4 3 2
KClO+H SO ==KHSO +HClO ,
3 2 4 4 3
3HClO ==HClO +H O+2ClO ,2ClO ==Cl +2O
3 4 2 2 2 2 2
(1)ClO 也能像Cl 一样在强碱(如NaOH)溶液中发生反应,其化学方程式是____________。
2 2
(2)设计一个实验确定ClO 分解产物中O 与Cl 的体积比为2∶1:_____________________。
2 2 2
答案:⑴6ClO +6NaOH==NaCl+5NaClO +3H O
2 3 2
(2)用排饱和食盐水法收集一试管气体,倒扣于NaOH溶液中,振荡一会儿,观察试管中所剩气体占试
管总体积的分数。
解析:此题是一道信息给予题,考查的知识点是卤素与碱的反应和实验设计。由于Cl 与NaOH反应的化学方
2
程式是:Cl+2NaOH===NaCl+NaClO+H O,信息提供:“ClO 也像Cl 一样在强碱溶液中反应”, 但
2 2 2 2
在ClO 中,氯元素为+4价,歧化后的价态变化较大。由于Cl 能与碱液反应而O 不能,可用碱液吸收
2 2 2
法测定Cl 和O 的体积。
2 2
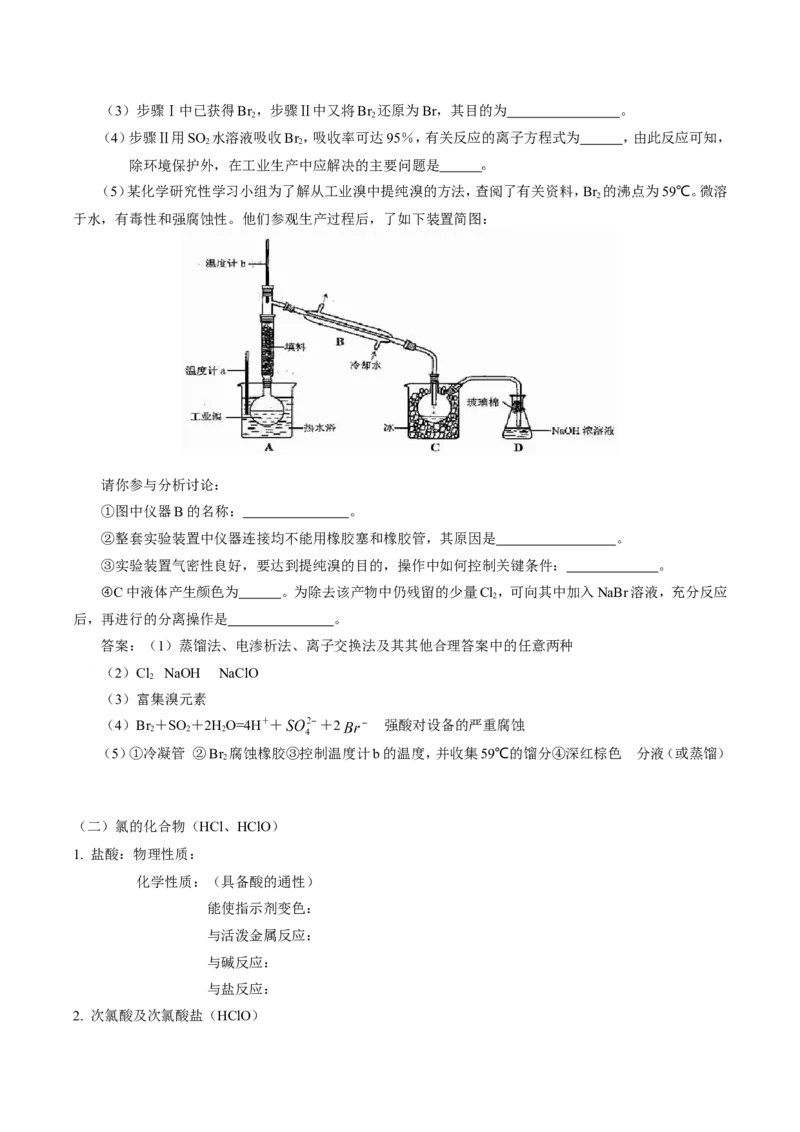
例2(. 09年天津理综·9)(18分)海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列。
从海水中提取食盐和溴的过程如下:
(1)请列举海水淡化的两种方法: 、 。
(2)将NaCl溶液进行电解,在电解槽中可直接得到的产品有H、 、 、或H、 。
2 2(3)步骤Ⅰ中已获得Br ,步骤Ⅱ中又将Br 还原为Br,其目的为 。
2 2
(4)步骤Ⅱ用SO 水溶液吸收Br ,吸收率可达95%,有关反应的离子方程式为 ,由此反应可知,
2 2
除环境保护外,在工业生产中应解决的主要问题是
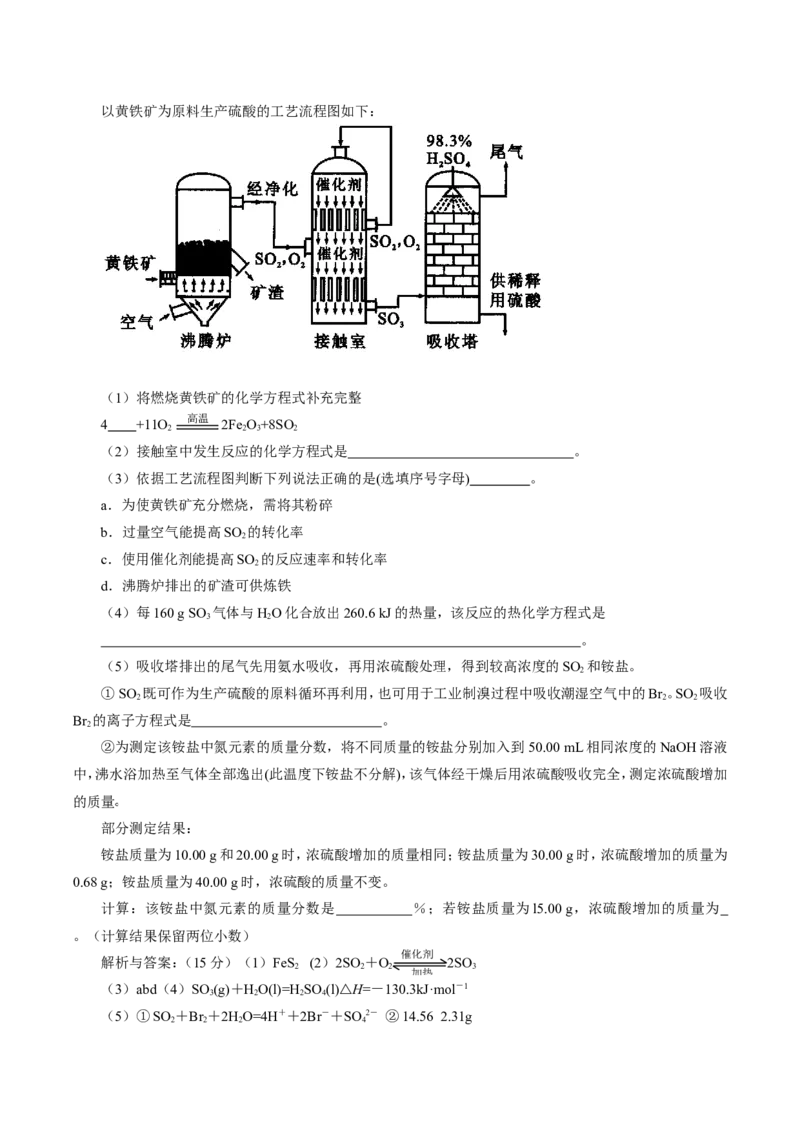
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br 的沸点为59℃。微溶
2
于水,有毒性和强腐蚀性。他们参观生产过程后,了如下装置简图:
请你参与分析讨论:
①图中仪器B的名称: 。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是 。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件: 。
④C中液体产生颜色为 。为除去该产物中仍残留的少量Cl,可向其中加入NaBr溶液,充分反应
2
后,再进行的分离操作是 。
答案:(1)蒸馏法、电渗析法、离子交换法及其其他合理答案中的任意两种
(2)Cl NaOH NaClO
2
(3)富集溴元素
(4)Br +SO +2HO=4H++ +2 强酸对设备的严重腐蚀
2 2 2
(5)①冷凝管 ②Br 腐蚀橡胶③控制温度计b的温度,并收集59℃的馏分④深红棕色 分液(或蒸馏)
2
(二)氯的化合物(HCl、HClO)
1. 盐酸:物理性质:
化学性质:(具备酸的通性)
能使指示剂变色:
与活泼金属反应:
与碱反应:
与盐反应:
2. 次氯酸及次氯酸盐(HClO)电子式:
性 质:弱酸性(用方程式解释):
不稳定性(用方程式解释):
强氧化性(漂白性):
例3(. 08年上海化学·13)已知在热的碱性溶液中,NaClO发生如下反应:3NaClO→2NaCl+NaClO 。在相同条
3
件下NaClO 也能发生类似的反应,其最终产物是( )
2
A.NaCl、NaClO B.NaCl、NaClO
3
C.NaClO、NaClO D.NaClO、NaClO
3 3 4
【变式训练2】氯胺(NH Cl)在中性或酸性条件下是一种有效的强力消毒剂,据此判断,氯胺在水溶液中因水解
2
产生的物质是 ( )
A.HClO和HCl B.NH C1和HCl C.NH Cl和HClO D.NH Cl和HClO
4 4 4 3
二、硫及化合物
(一)硫
1. 硫 原子结构示意图:
核外电子排布式:
在周期表中位置:
2. 硫性质 (1 )物理性质:
(2)化学性质:(完成下列方程式)
与非金属的反应(在氧气、氢气中燃烧)
与金属的反应(Fe、Cu)
与碱的反应(热NaOH、Ca(OH)2)
(二)硫的化合物
1、硫的氧化物(SO2、SO3)
SO2的性质:(1)物理性质:
(2)化学性质:
与氧气的反应
与水的反应
与HS的反应
2
与Cl 和HO的反应
2 2
与氢氧化钠的反应
漂白性(注意与Cl2漂白性的区别)
SO 的性质:(1)物理性质:
3
(2)化学性质:
与水的反应与氢氧化钠的反应
2、硫酸
浓硫酸的性质:(1)物理性质:
(2)化学性质:
吸水性(实验)
脱水性(实验)
强氧化性(实验)(与C的反应、与Cu的反应)
浓硫酸的制备:三设备:
三阶段:
三原理:
例4:不论以何种比例混合,将甲和乙两种混合气体同时通入过量的丙溶液中,一定能产生沉淀的组合是
序号 甲 乙 丙
① CO SO 石灰水
2 2
② HCl CO 石灰水
2
③ CO SO Ba(NO )
2 2 3 2
④ NO SO BaCl
2 2 2
⑤ CO NH CaCl
2 3 2
A.②③④ B.②③④⑤
C.①②④ D.①②③④
解析与评价:SO 是酸性氧化性,能和碱反应生成盐和水,SO 有较强的还原性,遇氧化性试剂易被氧化生成
2 2
。本题若忽略了在酸性条件下 离子的氧化性会漏选③,若未注意题干中“一定”两字会多选⑤。
对于①,由于石灰水过量,因此必有CaCO 和CaSO 沉淀,对于②,同样由于石灰水过量,因此必有CaCO 沉
3 3 3
淀生成,对于③,CO 气体与Ba(NO ) 不反应,SO 气体通入Ba(NO ) 溶液后,由于溶液酸性增强,SO 将被
2 3 2 2 3 2 2
离子氧化生成 ,因此有BaSO 沉淀生成,对于④,NO 和SO 混合后,SO 将被NO 氧化成SO ,通
4 2 2 2 2 3
入BaCl 溶液后有BaSO 沉淀生成,对于⑤,当NH 过量时溶液中有CaCO 沉淀生成,发生反应的化学方程
2 4 3 3
式为:2NH +CO +CaCl +H O=CaCO ↓+2NHCl,当NH 不足时,最终无沉淀生成,发生反应的化学方程式为:
3 2 2 2 3 4 3
2NH +2CO +CaCl +2H O=Ca(HCO )+2NHCl
3 2 2 2 3 2 4
答案:D
【变式训练3】在①HS ②SO ③CO ④Cl ⑤HI ⑥CO 六种气体中,属于酸酐的是_______;能使品红溶液褪
2 2 2 2
色的是_______;通入石蕊试液先变红后褪色的是_______,只变红不褪色的是_______;能使碘化钾淀粉试纸
变蓝的是_______;能与溴水反应的是_______。(填序号)
答案:②⑥ ②④ ④ ①②⑤⑥ ④ ①②⑤
解析:SO 、CO 分别是HSO 和HCO 的酸酐。SO 能使品红溶液褪色,而Cl 与水反应产生的HClO既能使
2 2 2 3 2 3 2 2
品红褪色,又能使石蕊试液先变红色后褪色,能使石蕊试液变红的气体还有HS、SO 、HI、CO 等酸性气体
2 2 2
与KI作用产生I 的气体是氯气,具有氧化性。能与溴水反应的气体是HS、SO 、HI等
2 2 2
例5.(09年北京理综·28)(15分)以黄铁矿为原料生产硫酸的工艺流程图如下:
(1)将燃烧黄铁矿的化学方程式补充完整
高温
4 +11O 2Fe O+8SO
2 2 3 2
(2)接触室中发生反应的化学方程式是 。
(3)依据工艺流程图判断下列说法正确的是(选填序号字母) 。
a.为使黄铁矿充分燃烧,需将其粉碎
b.过量空气能提高SO 的转化率
2
c.使用催化剂能提高SO 的反应速率和转化率
2
d.沸腾炉排出的矿渣可供炼铁
(4)每160 g SO 气体与HO化合放出260.6 kJ的热量,该反应的热化学方程式是
3 2
。
(5)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO 和铵盐。
2
① SO 既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br 。SO 吸收
2 2 2
Br 的离子方程式是 。
2
②为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00 mL相同浓度的NaOH溶液
中,沸水浴加热至气体全部逸出(此温度下铵盐不分解),该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加
的质量
部分测定结果:
铵盐质量为10.00 g和20.00 g时,浓硫酸增加的质量相同;铵盐质量为30.00 g时,浓硫酸增加的质量为
0.68 g;铵盐质量为40.00 g时,浓硫酸的质量不变。
计算:该铵盐中氮元素的质量分数是 %;若铵盐质量为l5.00 g,浓硫酸增加的质量为
。(计算结果保留两位小数)
催化剂
解析与答案:(15分)(1)FeS (2)2SO +O 2SO
2 2 2 3
加热
(3)abd(4)SO (g)+HO(l)=HSO (l)△H=-130.3kJ·mol-1
3 2 2 4
(5)①SO +Br +2HO=4H++2Br-+SO 2- ②14.56 2.31g
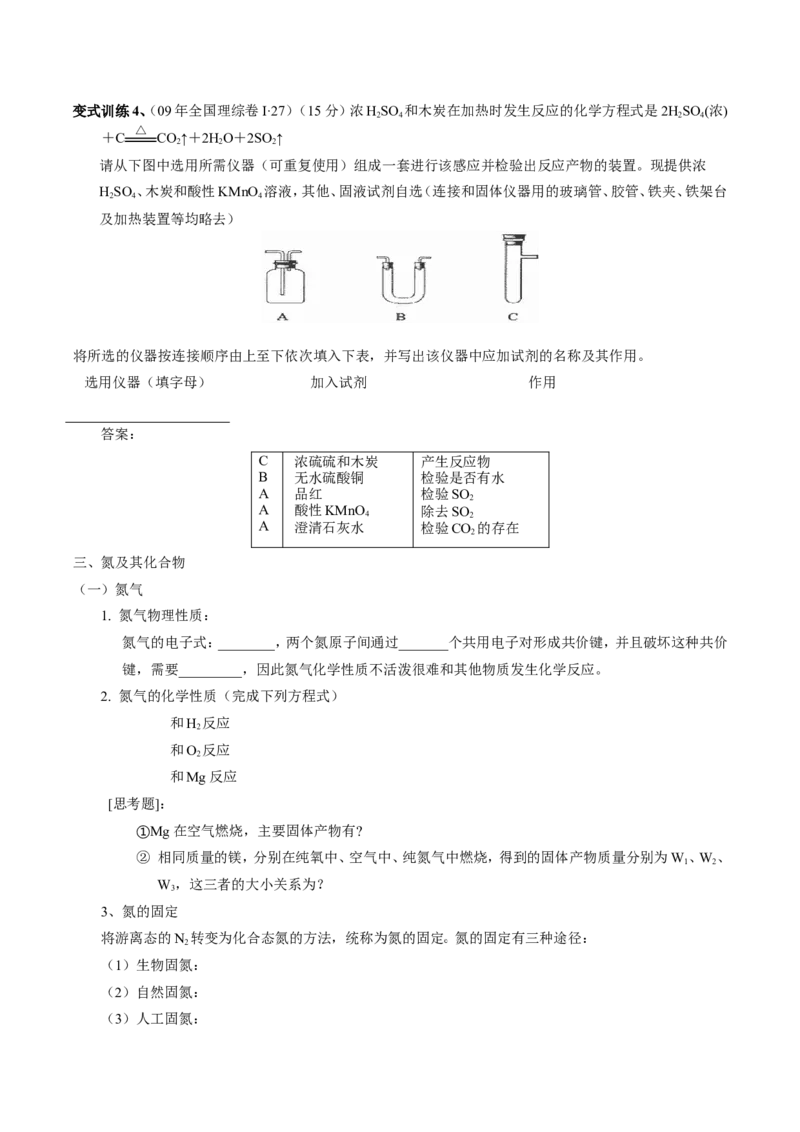
2 2 2 4变式训练4、(09年全国理综卷I·27)(15分)浓HSO 和木炭在加热时发生反应的化学方程式是2HSO (浓)
2 4 2 4
△
+C CO↑+2HO+2SO ↑
2 2 2
请从下图中选用所需仪器(可重复使用)组成一套进行该感应并检验出反应产物的装置。现提供浓
HSO 、木炭和酸性KMnO 溶液,其他、固液试剂自选(连接和固体仪器用的玻璃管、胶管、铁夹、铁架台
2 4 4
及加热装置等均略去)
将所选的仪器按连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用。
选用仪器(填字母) 加入试剂 作用
答案:
C 浓硫硫和木炭 产生反应物
B 无水硫酸铜 检验是否有水
A 品红 检验SO
2
A 酸性KMnO 除去SO
4 2
A 澄清石灰水 检验CO 的存在
2
三、氮及其化合物
(一)氮气
1. 氮气物理性质:
氮气的电子式:________,两个氮原子间通过_______个共用电子对形成共价键,并且破坏这种共价
键,需要_________,因此氮气化学性质不活泼很难和其他物质发生化学反应。
2. 氮气的化学性质(完成下列方程式)
和H 反应
2
和O 反应
2
和Mg反应
[思考题]:
①Mg在空气燃烧,主要固体产物有?
② 相同质量的镁,分别在纯氧中、空气中、纯氮气中燃烧,得到的固体产物质量分别为W、W、
1 2
W,这三者的大小关系为?
3
3、氮的固定
将游离态的N 转变为化合态氮的方法,统称为氮的固定 氮的固定有三种途径:
2
(1)生物固氮:
(2)自然固氮:
(3)人工固氮:(二)、氮的化合物
1、氨及铵盐
(1)氨气:分子结构: 电子式 结构式 分子极性
物理性质:
化学性质:
与水反应
与酸作用生成铵盐(硫酸、硝酸、盐酸的反应方程式):
与盐溶液 NH + H O + Fe3+ ——
3 2
NH + H O + Al3+ ——
3 2
Ag+ + NH + H O ——
3 2
NH + H O + CO + NaCl——
3 2 2
与非金属的反应(O、Cl)
2 2
实验室制NH
3
1.实验原理(实验室制法): (溶液还是固体?)
2.实验装置: ,与制取 完全相同。
3.收集: NH 应使用 法,要得到干燥的NH 可选用 __ _做干燥剂。
3 3
4.检验:
:
小结 ①氨水中存在哪些微粒:
②什么能在浓氨水中加入NaOH固体可制取NH ?
3
③氨水成分与液氨是否相同?给氨水加热,[ ]、电离度如何变化?若煮沸呢
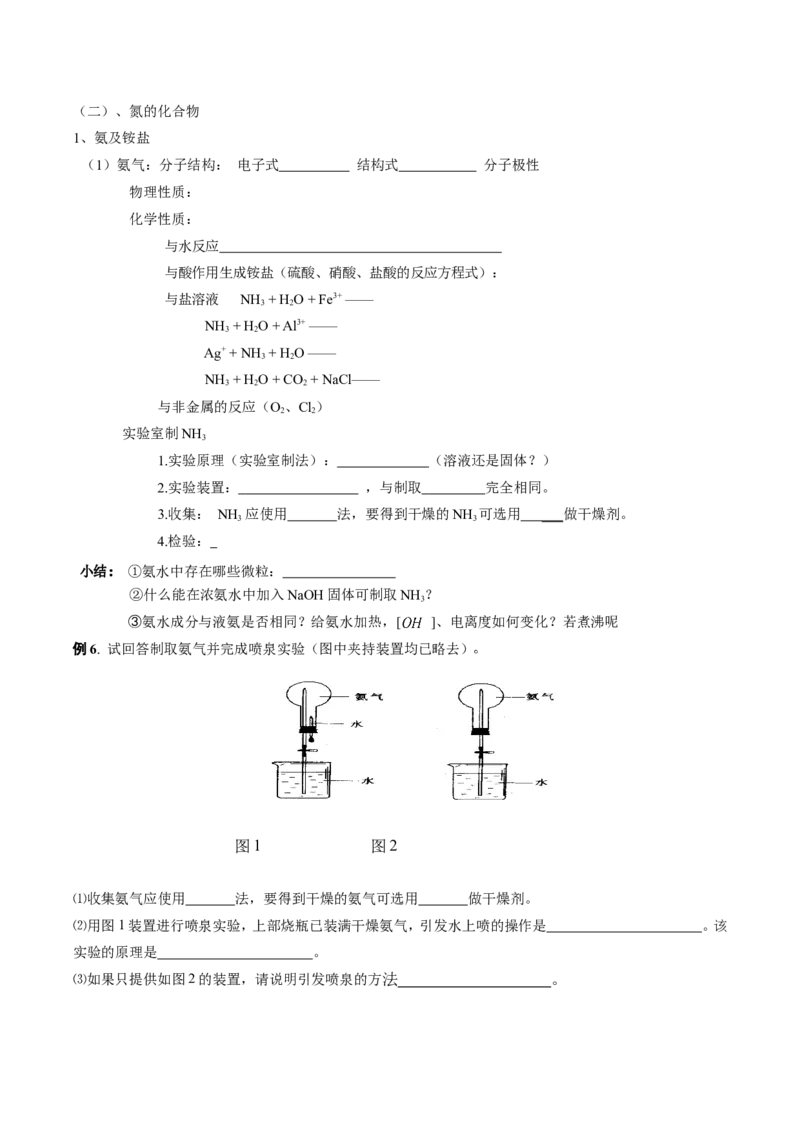
例6. 试回答制取氨气并完成喷泉实验(图中夹持装置均已略去)
图1 图2
⑴收集氨气应使用 法,要得到干燥的氨气可选用 做干燥剂。
⑵用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是 。该
实验的原理是 。
⑶如果只提供如图2的装置,请说明引发喷泉的方法 。解析与评价:本题以氨气的物理性质中极易溶于水为考察背景是常考容易题。(1)由于氨气极易溶于水,收
集时通常采用向下排气方法,干燥氨气宜选用碱石灰;(2)喷泉实验主要原理是容器的内外产生压强差,1中
是通过氨气溶于水使烧瓶内压强减小而出现喷泉;(3)中要想产生喷泉,可以将烧瓶内的氨气压入烧杯中,
先增大烧瓶内压强使氨气与水接触,进而使烧瓶内压强减少而出现喷泉。
答案:(1)向下排气方,碱石灰;
(2)将胶头滴管内的水挤入烧瓶内;
(3)用热毛巾覆于烧瓶顶部。
【变式训练5】下列气体与对应的液体不能进行喷泉实验的是 ( )
A.NH 和水 B.HCl和水 C.Cl 和水 D.CO 和NaOH溶液
3 2 2
【变式训练6】有关氨的说法不正确的是 ( )
A. NH 是4核10电子极性分子,三角锥型,具有还原性
3
B. NH 极易溶于水,可做喷泉实验,氨气易液化,液氨可用作制冷剂
3
C. 氨气是非电解质,氨水是电解质
D. 蘸有浓盐酸玻璃棒遇氨气可产生白烟
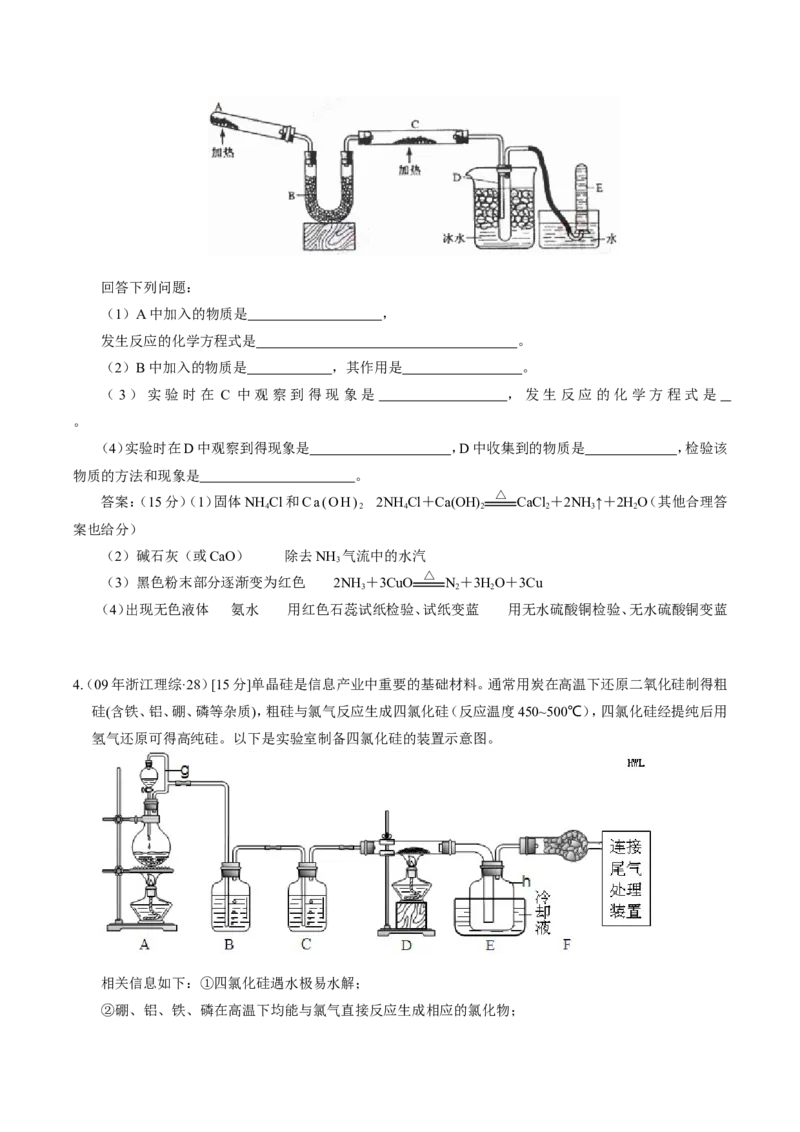
例7.(09年全国理综Ⅱ·28)(15分)
已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
回答下列问题:
(1)A中加入的物质是 ,
发生反应的化学方程式是 。
(2)B中加入的物质是 ,其作用是 。
(3)实验时在C中观察到得现象是 ,发生反应的化学方程式是 。
(4)实验时在D中观察到得现象是 ,D中收集到的物质是 ,检验该物质的方法和现象是
。
解析与评价:本题以氨气的制备,氨气的性质为考察要点,属于中档题。(1)、制备氨气的药品NH Cl和
4
Ca(OH) ,(2)干燥氨气用碱石灰(或CaO),(3)主要描述固体粉末的颜色变化,方程式见答案。(4)、描
2述D中的现象重点强调出现无色液体,氨气检验方法。
△
答 案:(1)固体NH Cl和Ca(OH) 2NHCl+Ca(OH) CaCl +2NH ↑+2HO
4 2 4 2 2 3 2
(2)碱石灰(或CaO) 除去NH 气流中的水汽
3
△
(3)黑色粉末部分逐渐变为红色 2NH +3CuO N+3HO+3Cu
3 2 2
(4)出现无色液体 氨水 用无水硫酸铜检验、无水硫酸铜变蓝
【变式训练7】(09年上海化学·4)用浓氯化铵溶液处理过的舞台幕布不易着火。其原因是
①幕布的着火点升高 ②幕布的质量增加
③氯化铵分解吸收热量,降低了温度 ④氯化铵分解产生的气体隔绝了空气
A.①② B.③④ C.③④ D.②④
答案:B
(2)铵盐
物理性质:
[思考]:写出电子式: NH Cl (NH )S
4 4 2
化学性质:(完成下列方程式)
水 解:请写出NH +在DO中水解的离子方程式
4 2
与碱反应:铵盐与碱反应离子反应
不稳 定性:热稳定性差,受热易分解:
△
NH Cl——
4
NH HC△O ——
4 3
铵根检验:
例8. 用加热方法可分离的一组物质是 ( )
A.氯化铵和消石灰 B.碳铵和过氧化钠
C.碘和食盐 D.硝酸铵和硫酸钠
【变式训练8】(05上海)对于某些离子的检验及结论一定正确的是 ( )
A.加入盐酸产生无色气体,将气体通入石灰水中,溶液变浑浊,一定有
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有
C.加入氢氧化钠并加热,产生气体能使湿润红色石蕊试纸变蓝,一定有
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
3. 氮的氧化物及其性质
①氮的氧化物的种类 、 、 、 、 、
其中HNO 的酸酐是 、HNO 的酸酐是
3 2
②NO、NO 的性质、制法
2
物理性质
NO通常为 、 的气体, ,微溶于水。NO 、 气味 气体。
2
化学性质
NO和氧气的反应:
NO 和水反应:
2
NO 和NO 的相互转化:
2 2 4
NO 和NaOH溶液反应:
2
NO 具有较强的氧化性,能______SO ;能使湿润的淀粉KI试纸______。
2 2
NO、NO 的制取
2
实验室制取NO的方程式为 ;用______法收集。
实验室制取NO 的方程式为 ;用______法收集。
2
氮的氧化物溶于水的计算
计算依据(用方程式表示)
例9(. 1)标况下,盛有NO 和N 以1:1混合气体的试管倒扣在水中,充分反应后余气体积占原体积的多少。
2 2
(2)将10mLNO和NO 混合气体缓慢通入倒立于水槽中的盛满水的试管中,充分反应后,有5mL剩
2
余气体,求原混合气体NO和NO 的体积比。
2
解析与评价:(1)、假设试管体积为V,V =0.5V,V =0.5V,由于3NO +HO=2HNO +NO,剩余气体总体积为:
NO2 N2 2 2 3
V =0.5V+1/6V=2/3V。
剩余
(2)、剩余气体应为 NO,设 10ml 气体中 NO 体积为 V1, NO 体积为 V2,则有
2
V+V =10,V +1/3V =5,求解得V=2.5,V2=7.5,V:V =1:3.
1 2 1 2 1 1 2
答 案:(1)2/3V,(2)、V:V =1:3.
1 2
【变式训练9】(1)一定条件下,16mlNO和O 混合充满试管倒扣水中余气为2ml求NO占原气体的多少
2
(2)将12mlNO 和O 的混合气体通入足量的水中,充分反应后余气2ml(气体均在相同状态下
2 2
测定)求原各气体的体积
答案:(1)分为两种情况讨论:当2ml为NO时,NO占原气体的5/8, 当2ml为O 时,NO占原气体的1/2.
2
(2)分为两种情况讨论:当2ml为NO时,V =10.8 V =1.2
NO2 O2
当2ml为O 时, V =8 V =4
2 NO2 O2
③氮的氧化物对空气的污染与防治
4. 硝酸的性质
(一)物理性质:
(二)化学性质:
●不稳定性:在常温下见光或受热就会分解,硝酸越浓就越 ,反应方程式:
[思考]久置的试剂颜色变化的较多。
①.如:NaO 、 、Fe2+ 化合物、AgX、AgNO 等。为什么?
2 2 3②下列呈现黄色的原因是
①久置的硝酸常呈黄色,如何去掉浓硝酸的黄色?
②碘化钾溶液和氢碘酸溶液久置均变黄
③工业盐酸呈现黄色
④纸张变黄
⑤硝酸沾在皮肤上,皮肤变黄
●强酸性(具有酸的通性)
思考、如何只用蓝色石蕊试纸鉴别三瓶失去标签的液体:浓HCl、浓HSO 、浓HNO?
2 4 3
①浓硝酸:现象: 原因
②浓硫酸:现象: 原因
③浓盐酸:现象: 原因
[讨论]只用铜丝鉴别三瓶失去标签的液体:浓HCl、浓HSO 、浓HNO。
2 4 3
●强氧化性(完成下列反应方程式)
①Cu+HNO(浓) ②Cu+HNO(稀)
3 3
③Mg+HNO(极稀)—Mg(NO ) + N O+ H O(配平,且标明电子转移方向和数目)
3 3 2 2 2
Mg+HNO(极稀)— Mg(NO ) + NHNO +HO(配平,且标明电子转移方向和数目)
3 3 2 4 3 2
④Fe+HNO(稀,过量) ⑤Fe(过量) +HNO(稀)
3 3
⑥C+HNO(浓) ⑦FeO+HNO(稀)
3 3
⑧NaSO +HNO(稀) ⑨SO +HNO(稀)
2 3 3 2 3
●与有机物的反应(完成下列反应方程式)
①与甲苯硝化反应
②与丙三醇酯化反应
③遇某些蛋白质显色反应
思考:现有稀HCl、稀HSO 、稀HNO、浓硝酸,请问如何除去附在试管壁上的银?
2 4 3
那么用浓硝酸好?还是稀硝酸好?(从污染和消耗酸的量来考虑)
(三)、硝酸的用途
是一种重要的化工原料: 制炸药、染料、塑料、硝酸盐等。
【规律总结】
①除Pt、Au等少数金属外,其余金属几乎都能与硝酸反应。
②常温下,浓硝酸对铁、铝等金属有钝化作用。故用 运输浓硝酸。
③硝酸与金属反应时,硝酸的还原产物与硝酸的浓度和金属的还原性有关,一般来说,浓硝酸还原为
,稀硝酸还原为 。
④硝酸与非金属反应时,非金属单质被氧化为相应的 。
⑤王水: 混合后所得溶液,可以溶解所有金属包括Pt、Au四、无机非金属材料----硅
(一)硅
1.存在:自然界中仅有 态存在,地壳里硅的含量居第 位。
2.晶体结构:晶体硅与金刚石结构相似:属于 晶体,该晶体中每个硅原子以 键与
个硅原子相连构成一个小正四面体,以此为单元向空间无限延伸构成空间网状结构。由于 ,
晶体硅的熔沸点或硬度均低于或小于金刚石。
3.物理性质:
【例10】下列物质:①HO+②晶体硅 ③金刚石 ④CH ⑤NH+ ⑥CHCl ⑦NH ,其中晶
3 4 4 3 3
体或分子的空间结构均不属于正四面体的是 ( )
A.①③⑤ B.②④⑥ C.①⑥⑦ D.①⑤⑦
4.化学性质:(完成下列方程式)
常温下(F、HF和强碱)
2
加热或高温下(O、Cl 反应)
2 2
5.工业制备:
思考与交流:硅和铝有哪些相同点、不同点?
(二)二氧化硅
1. 二氧化硅的晶体结构
在SiO 晶体中一个Si原子跟四个O原子形成 个共价键,即每1个Si原子周围结合 个
2
O原子,同时每个O原子跟 个Si原子相结合。二氧化硅晶体中Si原子与O原子以 的
比率组成立体网状结构的原子晶体。晶体中1个Si原子与周围的4个O原子形成 结构
2. 物理性质:
3. 化学性质:
a.弱氧化性:
b.具有酸性氧化物的通性:
c.与酸反应:SiO+HF---
2
4. 用途:_______________________________________________
例11. 下列说法正确的是( )
A.二氧化硅溶于水显酸性,所以二氧化硅属于酸性氧化物
B.二氧化硅是酸性氧化物,它不溶于任何酸
C.二氧化碳通入水玻璃可能得到原硅酸
D.因为高温时二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸的酸性比碳酸强
(三)硅酸、原硅酸
1. 硅酸(HSiO)、原硅酸(HSiO)的性质:
2 3 4 4
2. 硅酸(HSiO)的制备:
2 3(四)硅酸盐
1. 硅酸钠水溶液叫水玻璃。在空气中会变质,反应式为: 。
2. 硅酸盐氧化物表示法:金属氧化物·SiO·H O
2 2
硅酸钠(NaSiO)可表示为: ;正长石(KAlSi O)可表示为: 。
2 3 3 8
高岭石[Al (Si O)(OH) ]可表示为: ;
2 2 5 4
3. 硅酸盐的用途:
a.土壤保肥 b. 硅酸盐产品:
硅酸盐产品 主要原料 设备 反应原理 主要成分 特性
水泥
玻璃
陶瓷 不作要求 不作要求
例12. 不能用磨口玻璃瓶贮存的一组物质是 ( )
A.溴水 氯水 碘水 B.氢溴酸 盐酸 氢硫酸
C.浓硫酸 浓硝酸 浓盐酸 D.NaOH溶液 NaCO 溶液 水玻璃
2 3
【高考真题】
1.(09年江苏化学·3)下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
a b c
A Al AlCl Al(OH)
3 3
B HNO NO NO
3 2
C Si SiO H SiO
2 2 3
D CH =CH CH CH OH CH CHO
2 2 3 2 3
答案:B
2. (09年全国理综Ⅱ·6)物质的量之比为2︰5的锌与稀硝酸反应,若硝酸被还原的产物为NO,反应结束后
2
锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是
A.1︰4 B.1︰5 C.2︰3 D.2︰5
答案:A
3. (09年全国理综Ⅱ·28)(15分)
已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。回答下列问题:
(1)A中加入的物质是 ,
发生反应的化学方程式是 。
(2)B中加入的物质是 ,其作用是 。
(3)实验时在 C 中观察到得现象是 ,发生反应的化学方程式是
。
(4)实验时在D中观察到得现象是 ,D中收集到的物质是 ,检验该
物质的方法和现象是 。
△
答案:(15分)(1)固体NH Cl和Ca(OH) 2NHCl+Ca(OH) CaCl +2NH ↑+2HO(其他合理答
4 2 4 2 2 3 2
案也给分)
(2)碱石灰(或CaO) 除去NH 气流中的水汽
3
△
(3)黑色粉末部分逐渐变为红色 2NH +3CuO N+3HO+3Cu
3 2 2
(4)出现无色液体 氨水 用红色石蕊试纸检验、试纸变蓝 用无水硫酸铜检验、无水硫酸铜变蓝
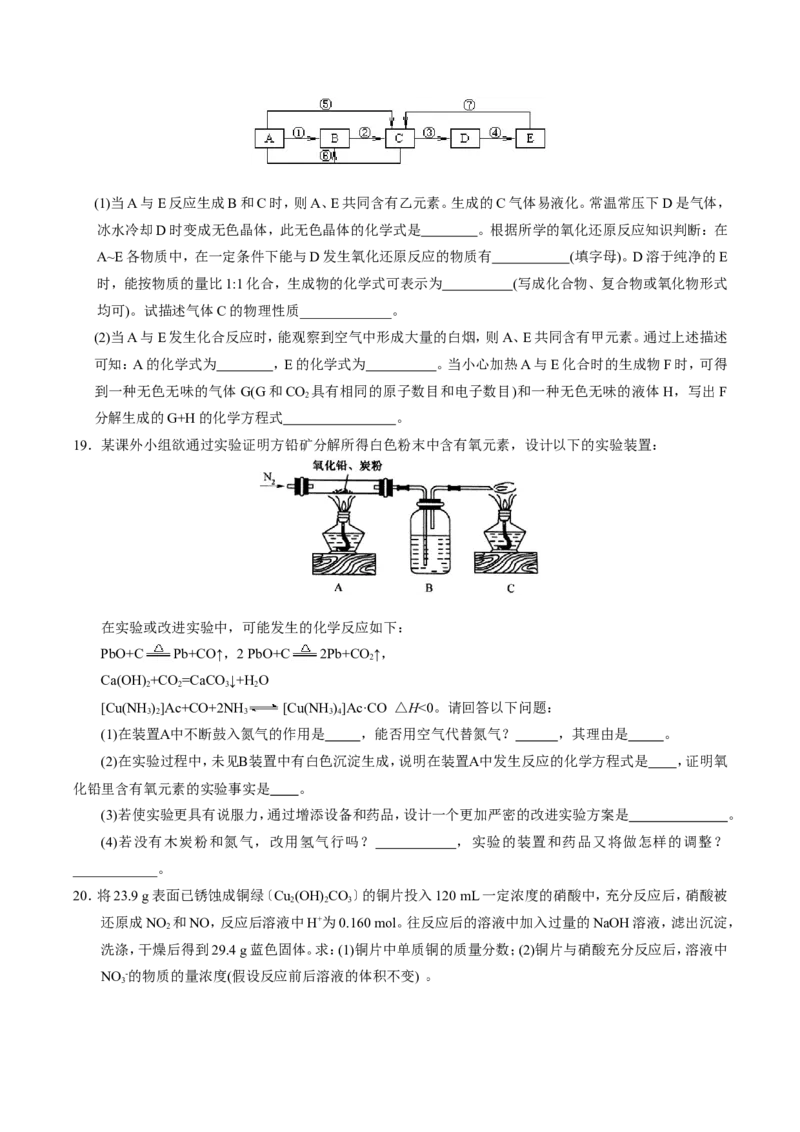
4.(09年浙江理综·28)[15分]单晶硅是信息产业中重要的基础材料。通常用炭在高温下还原二氧化硅制得粗
硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500℃),四氯化硅经提纯后用
氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
相关信息如下:①四氯化硅遇水极易水解;
②硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;③有关物质的物理常数见下表:
物质 SiCl BCl AlCl FeCl PCl
4 3 3 3 5
沸点/℃ 57.7 12.8 — 315 —
熔点/℃ -70.0 -107.2 — — —
升华温度/℃ — — 180 300 162
请回答下列问题:
(1)写出装置A中发生反应的离子方程式 。
(2)装置A中g管的作用是 ;装置C中的试剂是 ;
装置E中的h瓶需要冷却的理由是 。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除
铁元素外可能还含有的杂质元素是 (填写元素符号)。
(4)为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO 标准溶液在酸
4
性条件下进行氧化还原滴定,反应的离子方程式是:
5Fe2++MnO -+8H+ 5Fe3++Mn2++4HO
4 2
①滴定前是否要滴加指示剂? (填“是”或“否”),请说明理由 。
②某同学称取5.000g残留物后,经预处理后在容量瓶中配制成100 mL溶液,移取25.00 mL试样溶液,用
1.000×10-2 mol/L KMnO 标准溶液滴定。达到滴定终点时,消耗标准溶液20.00 mL,则残留物中铁元素的
4
质量分数是
答案:[15分]
(1)MnO +4H++2Cl― Mn2++Cl↑+2HO;
2 2 2
(2)平衡压强,使液体顺利流出并防止漏气;浓硫酸;产物SiCl 沸点低,需要冷凝收集;
4
(3)Al、P、Cl;
(4)①否;KMnO 溶液的紫红色可指示反应终点;②4.480%;
4
【感 悟】非金属相关考察题目广泛,有选择题,填空题(实验,推断,工业流程图题,元素化合物综合题,计算
题等),从09高考试题看多属于中等难度试题,在做题时必须兼顾知识与技能的统一,灵活使用所学知识,审
清题意。
【课后练习】
1.下图是年世界环境日主题宣传画《啊!地球出汗了》,这幅宣传画所揭示的全球主要环境问题是
A.酸雨 B.臭氧层空洞 C.温室效应 D.光化学烟雾2.为了探索月球上是否存在生命的痕迹,首先要分析月球岩中是否包藏有碳氢化合物。科学家用氘盐酸即
DCl的DO溶液处理岩石样品,收集放出的气体加以分析,结果只发现有一些气态碳氘化合物。试推断该
2
碳氘化合物是
A.岩石中的碳酸盐与氘盐酸反应的产物
B.岩石中的碳酸氢盐与氘盐酸反应的产物
C.岩石中的碳化物与氘盐酸反应的产物
D.岩石中的碳氢化合物与氘盐酸反应的产物
3.下面对氯气的叙述正确的是
A.氯气可使湿的红布条褪色,所以氯气具有漂白性
B.氯气没有漂白性,但通入品红溶液中,品红褪色
C.过量的铁在氯气中燃烧可生成氯化亚铁
D.闻其气味时要小心,将集气瓶放在鼻孔下直接闻
4.烧瓶中放入铜片和稀硝酸,用酒精灯加热来制取较纯净的一氧化氮,反应开始后发现烧瓶中充满棕红色气
体,这时的操作应是
A.立即接上收集容器,用向上排空气法收集
B.待烧瓶中红棕色消失后,用向上排空气法收集
C.立即用排水法收集
D.待烧瓶中红棕色气体消失后,用排水法收集
5.下列说法中不正确的是
A.普通玻璃呈淡绿色是由于含Fe2+
B.坩埚、蒸发皿都属于陶瓷制品
C.唐“三彩”是一种玻璃制品
D.高温下硅酸钙比碳酸钙稳定
6.含FeSA%的黄铁矿W吨,在用接触法硫酸的过程中,损失硫C%,可制得浓度为B%的硫酸为
2
A. 吨 B. 吨
C. 吨 D. 吨
7.下列对溴化钠的描述中,正确的是
A.是一种可溶于水的晶体,熔点较高
B.跟AgNO 溶液反应将生成白色沉淀
3
C.跟浓硫酸反应是制取溴化氢气体的常用方法
D.其工业制法之一是将金属钠跟单质溴反应
8.下列各组物质中,每一种物质都能使溴水褪色的是A.AgNO 溶液、CCl 、碘水
3 4
B.NaSO 溶液、FeCl 溶液、HS溶液
2 3 3 2
C.FeCl 溶液、KOH溶液、镁粉
2
D.NaOH溶液、CO气体、氯水
9.O2-由于离子半径较小,且带2个负电荷,在水中会强烈地吸引并结合水中的H+而生成OH-,下列反应中不
包含此步变化的是
A.NaO+HO=2NaOH
2 2
B.2NaO+2H O=4NaOH+O ↑
2 2 2 2
C.12Fe2++3O +6H O=8Fe3++4Fe(OH) ↓
2 2 3
D.Ag O+4NH ·H O=2[Ag(NH)]++2OH-+3H O
2 3 2 3 2 2
10.向NaBr、NaI、NaSO 混合液中,通入一定量氯气后,将溶液蒸干并充分灼烧,得到固体剩余物质的组成
2 3
可能是
A.NaCl Na SO B.NaCl NaBr Na SO
2 4 2 4
C.NaCl Na SO I D.NaCl NaI Na SO
2 4 2 2 4
11.次氯酸盐最大的用途是漂白和消毒。这类漂白剂氧化能力是以“有效氯”的含量来标志。“有效氯”的
含量定义为:从HI中氧化出相同量的I 所需Cl 的质量与指定化合物的质量之比,常以百分数表示。请问
2 2
纯LiClO的“有效氯”为
A.121% B.100% C.89% D.21%
12.用浓硫酸吸收SO 可以得到HSO •SO。用mg98%的HSO 充分吸收SO 后再进行稀释,可得到98%的硫
3 2 4 3 2 4 3
酸的质量为
A.2.42mg B.2.22mg C.2.02mg D.1.98mg
13.下列离子方程式不正确的是
A.银氨溶液中加入足量盐酸产生沉淀:
[Ag(NH)]++ +3H++ =AgCl↓+2 +HO
3 2 2
B.在亚硫酸钡沉淀中加入稀硝酸后,沉淀不溶解:
3BaSO+2H++2 =3BaSO↓+2NO↑+HO
3 4 2
C.碳酸钠溶液中通入少量SO :
2
2 +SO +H O=2 +
2 2
D.氧化铁可溶于氢碘酸:Fe O+6H+=2Fe3++3HO
2 3 2
14.NH 和O 混合气体100mL通过红热的铂丝,充分反应后的混合气体再通过足量水最终收集到10mL残留
3 2
气体,则原混合气体中O 体积不可能是(气体体积在相同条件下测定)
2
A.12.5mL B.21.5mL C.64.2mL D.70.0mL
15.(1)少量的Mn2+可以催化分解HO,其反应的机理可简单解释为:
2 2试写出上述2步反应的离子方程式_________________
(2)对于CO中毒、心肌梗塞、冠心病或小儿肺炎等危重患者都要采用吸氧治疗。普通医务室中没有氧气
瓶,但一般都有消毒用的30%的HO 溶液。同时还有可选用的试剂为:KMnO 、HCl、HSO 、MnO 、
2 2 4 2 4 2
Mg、CuSO 、NaCl、葡萄糖。请写出一种使 HO 中氧完全释放出来的理想反应方程式
4 2 2
______________________________。
16.氰(CN) 的结构式为N≡C—C≡N,其化学性质与卤素(X)很相似,化学上称之为拟卤素。(CN) 和水反应可
2 2 2
生成HCN和HCNO;(CN) 的氧化性比Br 弱,比I 强。
2 2 2
(1)下列有关反应的化学方程式不正确的是
(填选项标号) 。
A.(CN) 和NaOH溶液反应:(CN) +2NaOH==NaCN+NaCNO+H O
2 2 2
B.MnO 和HCN反应:MnO +4HCN Mn(CN) +(CN) ↑+2H O
2 2 2 2 2
C.向KCN溶液中加入碘水:I+2KCN==2KI+(CN)
2 2
D.在NaBr和KCN混合溶液中通入少量Cl:Cl+2NaBr==2NaCl+Br
2 2 2
(2)HCN 的电子式为 ,按电子云重叠方式分类分子内化学键类型为
_________________,碳原子的杂化类型为____________。
(3)处理含 (其中C为+2价)的工业废水常用 氧化,生成的 (其中C 为+4价)元素,反应的
离子方程式如下:
a +b +c =dCNO-+eN↑+f +b +cHO
2 2
上述化学方程式可能的配平系数有多组,请回答:
①方程式中e : f的值为 (填选项标号)。
A.1 B.1/2 C.2 D.不能确定
②若d=e=1, 则b= 。
17.试依据下列事实,作出有关的结论。
(1)硅的非金属性特征大于金属特征,而锗的金属特征大于非金属特征,_____。(2)金刚石是电的绝缘
体,石墨可以导电,而C 可作为制超导体材料,____________。
60
(3)在常温下硅的化学性质不活泼,但自然界中却没有单质硅存在,__ _。
(4)硅酸钠溶液中通入CO 气体时,可生成难溶于水的酸—硅酸,_ ___。
2
(3)碳单质的三种同素异形体:骨架型的金刚石、层型的石墨及球形的球碳分子,试确定那一种物质易
在火山喷发口附近发现,_________________________________。
18.已知A、B、C、D、E为中学化学常见物质,A、B、C、D、E中均含有同一种元素,A、C均为气体,E为液体,
下图中箭头上的反应物和反应条件均已略去(1)当A与E反应生成B和C时,则A、E共同含有乙元素。生成的C气体易液化。常温常压下D是气体,
冰水冷却D时变成无色晶体,此无色晶体的化学式是 。根据所学的氧化还原反应知识判断:在
A~E各物质中,在一定条件下能与D发生氧化还原反应的物质有 (填字母)。D溶于纯净的E
时,能按物质的量比1:1化合,生成物的化学式可表示为 (写成化合物、复合物或氧化物形式
均可)。试描述气体C的物理性质_____________。
(2)当A与E发生化合反应时,能观察到空气中形成大量的白烟,则A、E共同含有甲元素。通过上述描述
可知:A的化学式为 ,E的化学式为 。当小心加热A与E化合时的生成物F时,可得
到一种无色无味的气体G(G和CO 具有相同的原子数目和电子数目)和一种无色无味的液体H,写出F
2
分解生成的G+H的化学方程式 。
19.某课外小组欲通过实验证明方铅矿分解所得白色粉末中含有氧元素,设计以下的实验装置:
在实验或改进实验中,可能发生的化学反应如下:
PbO+C Pb+CO↑,2 PbO+C 2Pb+CO↑,
2
Ca(OH) +CO =CaCO ↓+H O
2 2 3 2
[Cu(NH )]Ac+CO+2NH [Cu(NH)]Ac·CO △H<0。请回答以下问题:
3 2 3 3 4
(1)在装置A中不断鼓入氮气的作用是 ,能否用空气代替氮气? ,其理由是 。
(2)在实验过程中,未见B装置中有白色沉淀生成,说明在装置A中发生反应的化学方程式是 ,证明氧
化铅里含有氧元素的实验事实是 。
(3)若使实验更具有说服力,通过增添设备和药品,设计一个更加严密的改进实验方案是 。
(4)若没有木炭粉和氮气,改用氢气行吗? ,实验的装置和药品又将做怎样的调整?
____________。
20.将23.9 g表面已锈蚀成铜绿〔Cu (OH) CO〕的铜片投入120 mL一定浓度的硝酸中,充分反应后,硝酸被
2 2 3
还原成NO 和NO,反应后溶液中H+为0.160 mol。往反应后的溶液中加入过量的NaOH溶液,滤出沉淀,
2
洗涤,干燥后得到29.4 g蓝色固体。求:(1)铜片中单质铜的质量分数;(2)铜片与硝酸充分反应后,溶液中
NO -的物质的量浓度(假设反应前后溶液的体积不变)
3【参考答案】
1.C 2.C 3.C 4.D 5.C 6.A 7.A 8.C
9.B 10.AB 11.A 12.B 13.D 14.B
15.(1)H O + Mn2+ = MnO + 2H+ HO +MnO + 2H+ = H O+ Mn2+ +O ↑
2 2 2 2 2 2 2 2
(2)5H O+2KMnO +3HSO =KSO +2MnSO +8HO+5O↑
2 2 4 2 4 2 4 4 2 2
16.(1)CD (2) sp 2个σ键和2个π键 (3)①B ②6
17.(1)表明同主族元素性质是递变的。(2)表明C 与石墨具有某种类似的结构。(3)说明在自然条件下,硅不如
60
其化合物稳定。(4)表明硅酸的酸性比碳酸弱。(5)三种物质中金刚石在火山口易被发现,因为该处温度高、
压力大,有利于破坏石墨中的化学键,有条件形成金刚石。
18.(1)SO A和B H SO 或HSO ·SO 或2SO ·H O SO 是无色有刺激性气味的气体,密度比空气大,易溶
3 2 2 7 2 4 3 3 2 2
于水,有毒 (2)NH HNO NHNO NO↑+2HO。
3 3 4 3 2 2
19.(1)N 可将实验装置内的空气排净,并作为动力源将PbO与C反应生成的气体,赶入B、C两个实验装置
2
处。不可用空气体代替N,空气中的O 可与灼热的炭反应,且空气中还含有CO、HO等含氧化合物,均
2 2 2 2
可导致实验失败。 (2) PbO+C Pb+CO↑,在装置C处可见一氧化碳燃烧产生的淡蓝色火焰。(3)可在
装置B后串联一个内盛[Cu(NH )]Ac溶液的洗气装置,吸收一氧化碳,反应完毕,取出吸收液加热解吸,
3 2
用排水取气法收集放出的气体,通过进一步实验证明该气体是一氧化碳。 (4)可用H 代替N 和木炭,
2 2
PbO+H Pb+HO,用无水CuSO 吸收生成的水,证明氧化铅中含有氧元素。装置 B应改用内盛
2 2 4
CuSO 白色粉末的干燥管。
4
20.(1)53.6% (2)6.33 mol·L-1