文档内容
绝密★考试启用前
2021年普通高等学校招生全国统一考试(甲卷)
理科综合能力测试·化学
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cu 64 Zr 91
一、选择题
1. 化学与人体健康及环境保护息息相关。下列叙述正确的是
A. 食品加工时不可添加任何防腐剂
B. 掩埋废旧电池不会造成环境污染
C. 天然气不完全燃烧会产生有毒气体
D. 使用含磷洗涤剂不会造成水体污染
2. N 为阿伏加德罗常数的值。下列叙述正确的是
A
A. 18g重水(D O)中含有的质子数为10N
2 A
B. 3mol的NO 与H O完全反应时转移的电子数为4N
2 2 A
C. 32g环状S ( )分子中含有的S-S键数为1N
8 A
D. 1L pH=4的0.1mol×L-1K Cr O 溶液中Cr O 2-离子数为0.1N
2 2 7 2 7 A
3. 实验室制备下列气体的方法可行的是
气体 方法
A 氨气 加热氯化铵固体
B 二氧化氮 将铝片加到冷浓硝酸中
C 硫化氢 向硫化钠固体滴加浓硫酸
D 氧气 加热氯酸钾和二氧化锰的混合物
A. A B. B C. C D. D
4. 下列叙述正确的是
第1页 | 共8页A. 甲醇既可发生取代反应也可发生加成反应
B. 用饱和碳酸氢纳溶液可以鉴别乙酸和乙醇
C. 烷烃的沸点高低仅取决于碳原子数的多少
D. 戊二烯与环戊烷互为同分异构体
5.
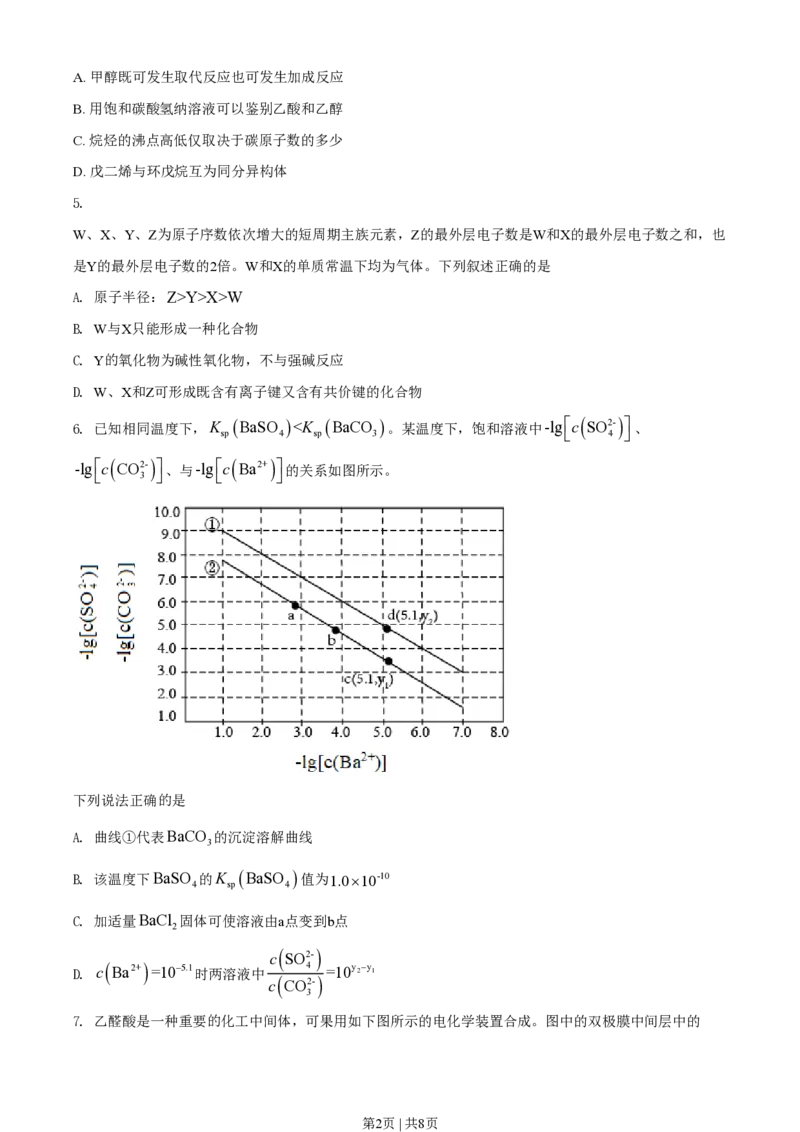
W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和X的最外层电子数之和,也
是Y的最外层电子数的2倍。W和X的单质常温下均为气体。下列叙述正确的是
A. 原子半径:Z>Y>X>W
B. W与X只能形成一种化合物
C. Y的氧化物为碱性氧化物,不与强碱反应
D. W、X和Z可形成既含有离子键又含有共价键的化合物
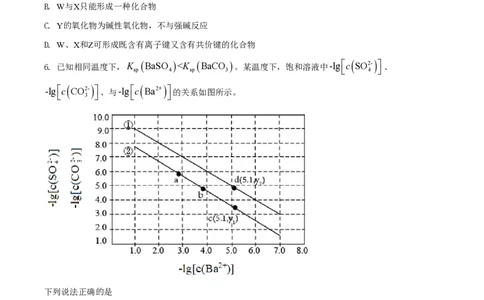
6. 已知相同温度下,K BaSO 1.5,单质碘的收率会降低,原因是
2 2 2 2
_______。
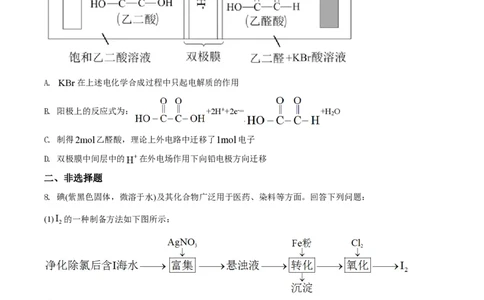
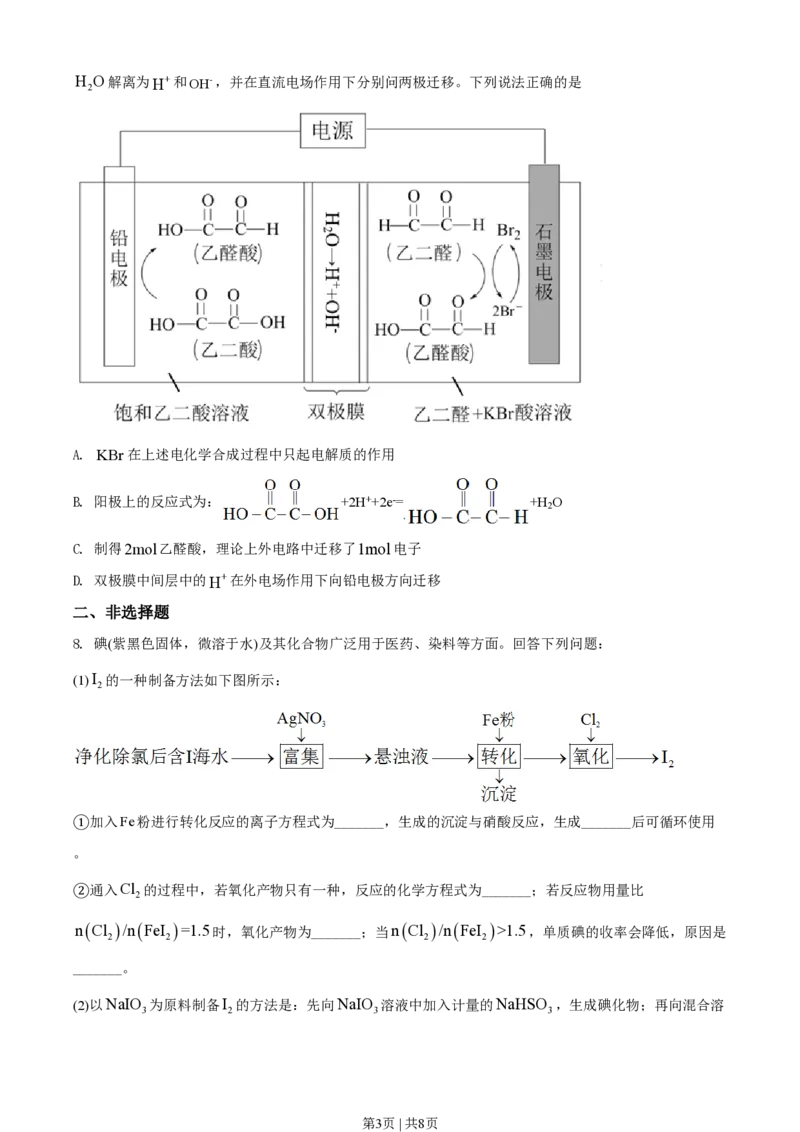
(2)以NaIO 为原料制备I 的方法是:先向NaIO 溶液中加入计量的NaHSO ,生成碘化物;再向混合溶
3 2 3 3
第3页 | 共8页液中加入NaIO 溶液,反应得到I ,上述制备I 的总反应的离子方程式为_______。
3 2 2
(3)KI溶液和CuSO 溶液混合可生成CuI沉淀和I ,若生成1mol I ,消耗的KI至少为_______mol。I
4 2 2 2
在KI溶液中可发生反应I +I- I-。实验室中使用过量的KI与CuSO 溶液反应后,过滤,滤液经水蒸
2 ƒ 3 4
气蒸馏可制得高纯碘。反应中加入过量KI的原因是_______。
9.
胆矾(CuSO ×5H O)易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的CuO(杂质为氧化铁及泥沙)
4 2
为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:
(1)制备胆矾时,用到的实验仪器除量筒、酒精灯、玻璃棒、漏斗外,还必须使用的仪器有_______(填标号)
。
A.烧杯 B.容量瓶 C.蒸发皿 D.移液管
(2)将CuO加入到适量的稀硫酸中,加热,其主要反应的化学方程式为_______,与直接用废铜和浓硫酸反
应相比,该方法的优点是_______。
(3)待CuO完全反应后停止加热,边搅拌边加入适量H
2
O
2
,冷却后用NH
3g
H
2
O调pH为3.5~4,再煮沸
10min,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、_______、乙醇洗涤、_______,得到
胆矾。其中,控制溶液pH为3.5~4的目的是_______,煮沸10min的作用是_______。
(4)结晶水测定:称量干燥坩埚的质量为m ,加入胆矾后总质量为m ,将坩埚加热至胆矾全部变为白色,
1 2
置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为m 。根据实验数据,胆矾分子中结晶
3
水的个数为_______(写表达式)。
(5)下列操作中,会导致结晶水数目测定值偏高的是_______(填标号)。
①胆矾未充分干燥 ②坩埚未置于干燥器中冷却 ③加热时有少胆矾迸溅出来
10. 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为:
CO (g)+3H (g)= CH OH(g)+H O(g)
2 2 3 2
该反应一般认为通过如下步骤来实现:
①CO (g)+H (g)=CO(g)+H O(g) ΔH =+41kJ mol-1
2 2 2 1 g
②CO(g)+2H (g)=CH OH(g) ΔH =-90kJ mol-1
2 3 2 g
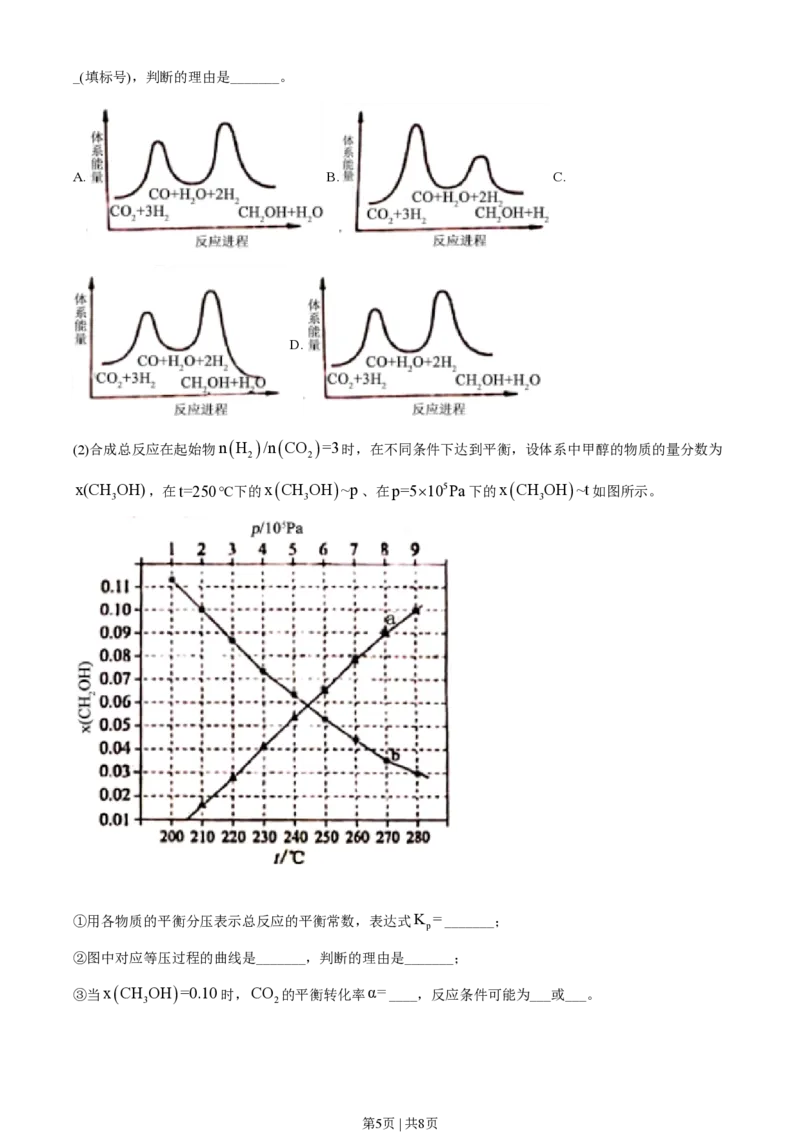
总反应的ΔH=_______kJ×mol-1;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是______
第4页 | 共8页_(填标号),判断的理由是_______。
A. B. C.
D.
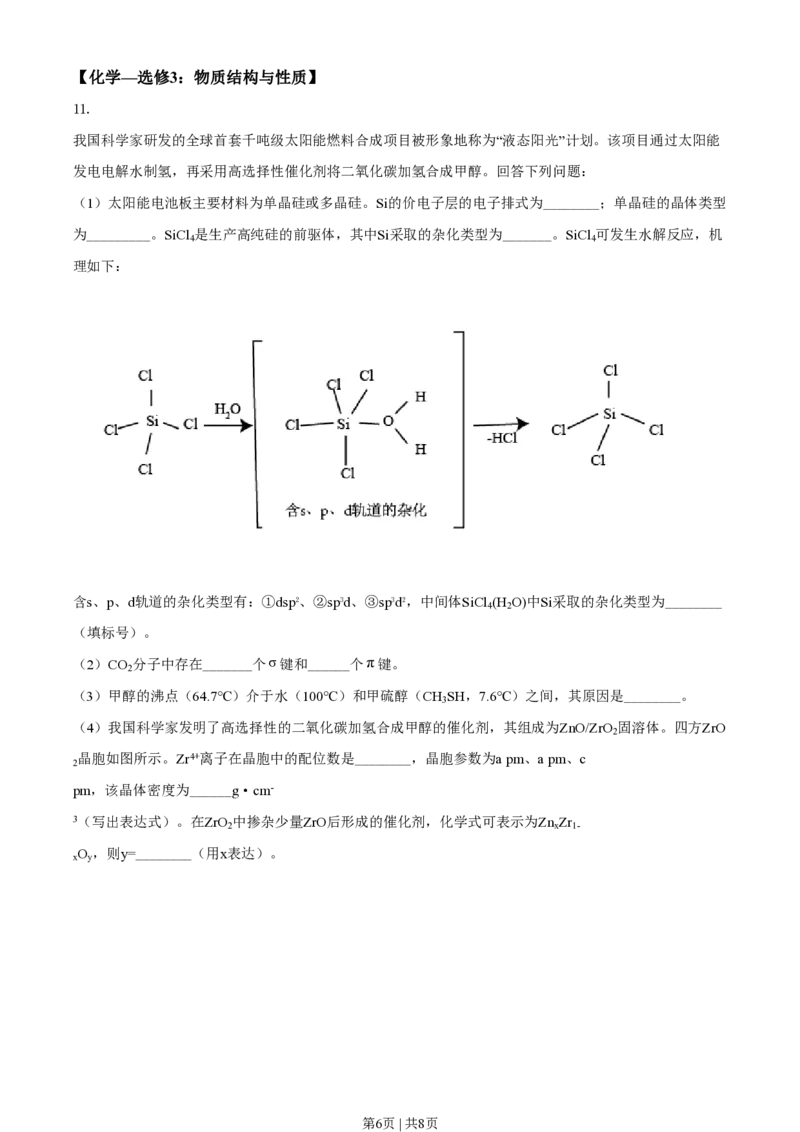
(2)合成总反应在起始物nH /nCO =3时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
2 2
x(CH OH),在t=250℃下的xCH OH~p、在p=5´105Pa下的xCH OH~t如图所示。
3 3 3
①用各物质的平衡分压表示总反应的平衡常数,表达式K =_______;
p
②图中对应等压过程的曲线是_______,判断的理由是_______;
③当xCH OH=0.10时,CO 的平衡转化率α=____,反应条件可能为___或___。
3 2
第5页 | 共8页【化学—选修3:物质结构与性质】
11.
我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象地称为“液态阳光”计划。该项目通过太阳能
发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。回答下列问题:
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排式为________;单晶硅的晶体类型
为_________。SiCl 是生产高纯硅的前驱体,其中Si采取的杂化类型为_______。SiCl 可发生水解反应,机
4 4
理如下:
含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl (H O)中Si采取的杂化类型为________
4 2
(填标号)。
(2)CO 分子中存在_______个σ键和______个π键。
2
(3)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH SH,7.6℃)之间,其原因是________。
3
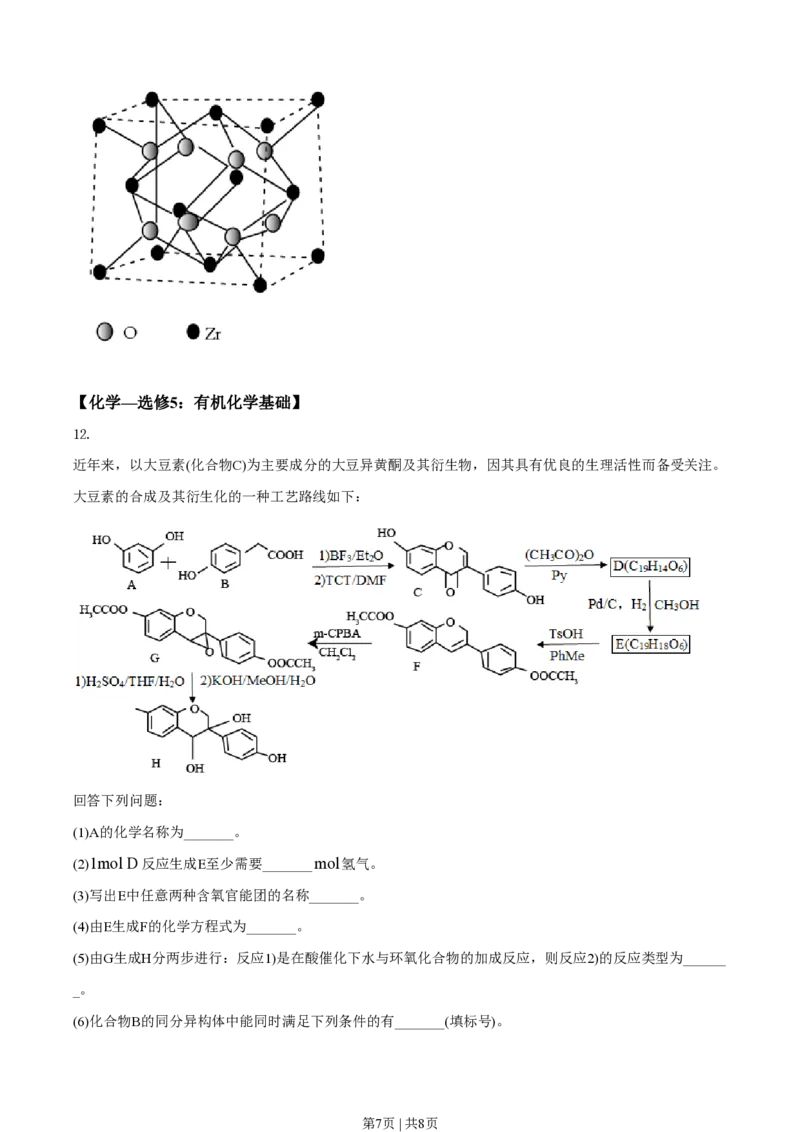
(4)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO 固溶体。四方ZrO
2
晶胞如图所示。Zr4+离子在晶胞中的配位数是________,晶胞参数为a pm、a pm、c
2
pm,该晶体密度为______g·cm-
3(写出表达式)。在ZrO 中掺杂少量ZrO后形成的催化剂,化学式可表示为Zn Zr
2 x 1-
O ,则y=________(用x表达)。
x y
第6页 | 共8页【化学—选修5:有机化学基础】
12.
近年来,以大豆素(化合物C)为主要成分的大豆异黄酮及其衍生物,因其具有优良的生理活性而备受关注。
大豆素的合成及其衍生化的一种工艺路线如下:
回答下列问题:
(1)A的化学名称为_______。
(2)1mol D反应生成E至少需要_______mol氢气。
(3)写出E中任意两种含氧官能团的名称_______。
(4)由E生成F的化学方程式为_______。
(5)由G生成H分两步进行:反应1)是在酸催化下水与环氧化合物的加成反应,则反应2)的反应类型为______
_。
(6)化合物B的同分异构体中能同时满足下列条件的有_______(填标号)。
第7页 | 共8页a.含苯环的醛、酮
b.不含过氧键(-O-O-)
c.核磁共振氢谱显示四组峰,且峰面积比为3∶2∶2∶1
A.2个 B.3个 C.4个 D.5个
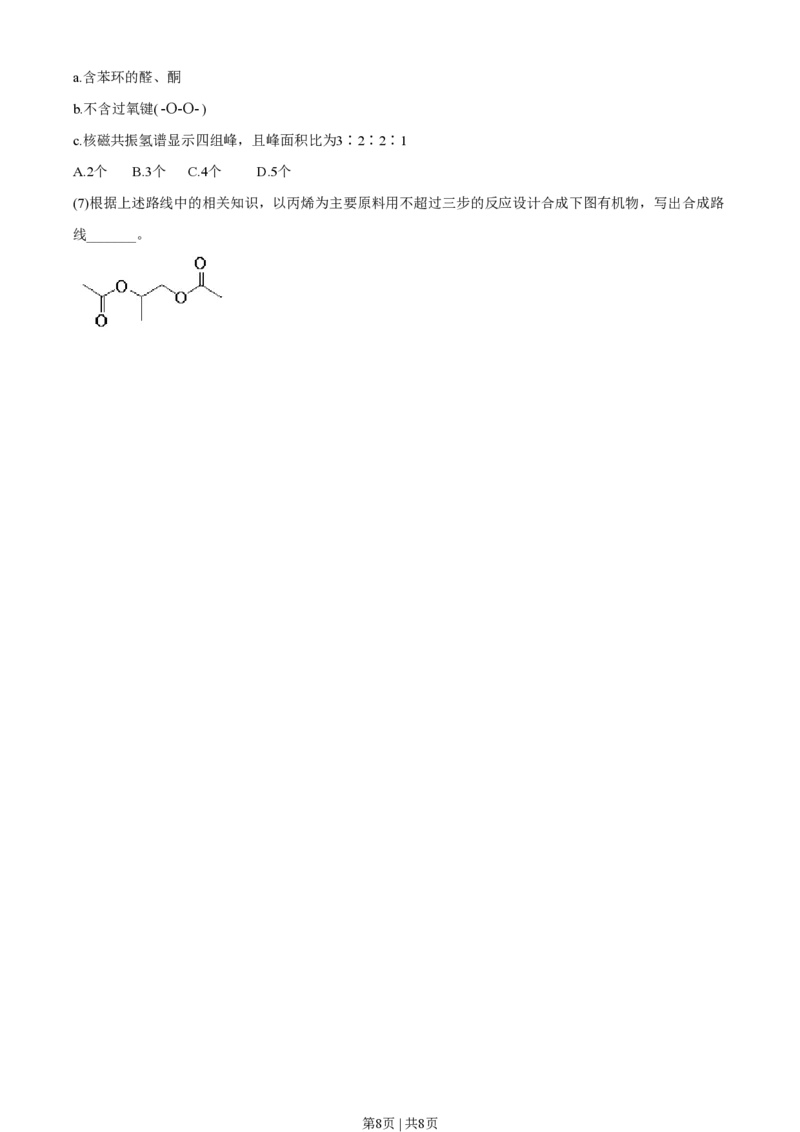
(7)根据上述路线中的相关知识,以丙烯为主要原料用不超过三步的反应设计合成下图有机物,写出合成路
线_______。
第8页 | 共8页