文档内容
2021 年湖北省普通高中学业水平选择性考试
化学
可能用到的相对原子质量:H-1 C-12 N-14 O-16 F-19 S-32 Cl-35.5 K-39
Ga-70 In-115 Sb-122
一、选择题:本题共 15小题,每小题 3分,共 45 分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. “碳中和”有利于全球气候改善。下列有关CO 的说法错误的是
2
A. CO 是Ⅴ形的极性分子 B. CO 可催化还原为甲酸
2 2
C. CO 晶体可用于人工增雨 D. CO 是侯氏制碱法的原料之一
2 2
2. “乌铜走银”是我国非物质文化遗产之一。该工艺将部分氧化的银丝镶嵌于铜器表面,艺人用手边捂边揉搓
铜器,铜表面逐渐变黑,银丝变得银光闪闪。下列叙述错误的是
A. 铜的金属活动性大于银
B. 通过揉搓可提供电解质溶液
C. 银丝可长时间保持光亮
D. 用铝丝代替银丝铜也会变黑
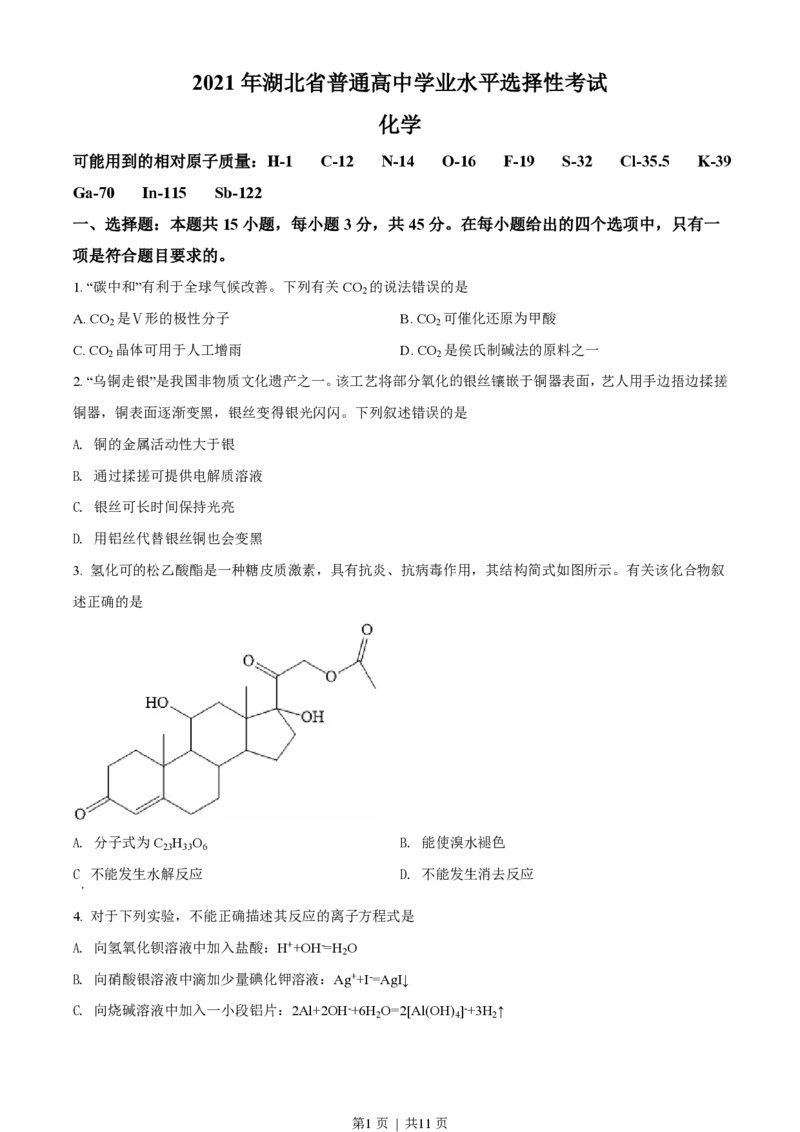
3. 氢化可的松乙酸酯是一种糖皮质激素,具有抗炎、抗病毒作用,其结构简式如图所示。有关该化合物叙
述正确的是
A. 分子式为C H O B. 能使溴水褪色
23 33 6
C 不能发生水解反应 D. 不能发生消去反应
.
4. 对于下列实验,不能正确描述其反应的离子方程式是
A. 向氢氧化钡溶液中加入盐酸:H++OH-=H O
2
B. 向硝酸银溶液中滴加少量碘化钾溶液:Ag++I-=AgI↓
C. 向烧碱溶液中加入一小段铝片:2Al+2OH-+6H O=2[Al(OH) ]-+3H ↑
2 4 2
第1页 | 共11页D. 向次氯酸钙溶液中通入少量二氧化碳气体:ClO-+CO +H O=HClO+HCO-
2 2 3
5. 下列实验现象与实验操作不相匹配的是
实验操作 实验现象
将盛有Fe(OH) 胶体的烧杯置于暗处,用红色激光笔照射烧杯 在与光束垂直的方向看到一条光
3
A.
中的液体 亮的“通路”
向盛有少量Mg(OH) 沉淀的试管中加入适量饱和NH Cl溶液,
2 4
B. 白色沉淀溶解
振荡
C. 向盛有3.0mL无水乙醇的试管中加人一小块金属钠 有气泡产生
向盛有2.0mL甲苯的试管中加人3滴酸性KMnO ,溶液,用
4
D. 紫色不变
力振荡
A. A B. B C. C D. D
6. N 为阿伏加德罗常数的值。下列说法错误的是
A
A. 23gCH CH OH中sp3杂化的原子数为N
3 2 A
B. 0.5molXeF 中氙的价层电子对数为3N
4 A
C. 1mol[Cu(H O) ]2+中配位键的个数为4N
2 4 A
D. 标准状况下,11.2LCO和H 的混合气体中分子数为0.5N
2 A
7. 某兴趣小组为制备1—氯—2—甲基丙烷(沸点69℃),将2—甲基—1—丙醇和POCl 溶于CH Cl 中,加
3 2 2
热回流(伴有HCl气体产生)。反应完全后倒入冰水中分解残余的POCl ,分液收集CH Cl 层,无水MgSO
3 2 2 4
干燥,过滤、蒸馏后得到目标产物。上述过程中涉及的装置或操作错误的是(夹持及加热装置略)
A. B. C. D.
A. A B. B C. C D. D
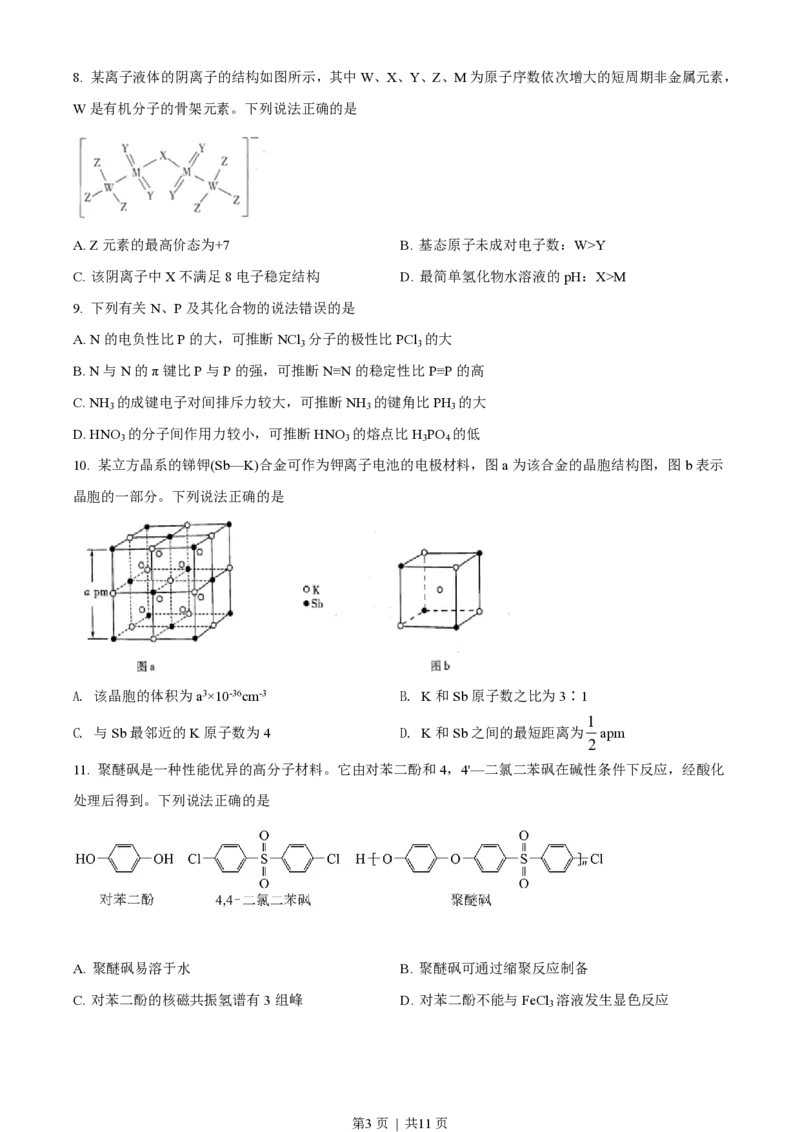
第2页 | 共11页8. 某离子液体的阴离子的结构如图所示,其中W、X、Y、Z、M为原子序数依次增大的短周期非金属元素,
W是有机分子的骨架元素。下列说法正确的是
A. Z元素的最高价态为+7 B. 基态原子未成对电子数:W>Y
C. 该阴离子中X不满足8电子稳定结构 D. 最简单氢化物水溶液的pH:X>M
9. 下列有关N、P及其化合物的说法错误的是
A. N的电负性比P的大,可推断NCl 分子的极性比PCl 的大
3 3
B. N与N的π键比P与P的强,可推断N≡N的稳定性比P≡P的高
C. NH 的成键电子对间排斥力较大,可推断NH 的键角比PH 的大
3 3 3
D. HNO 的分子间作用力较小,可推断HNO 的熔点比H PO 的低
3 3 3 4
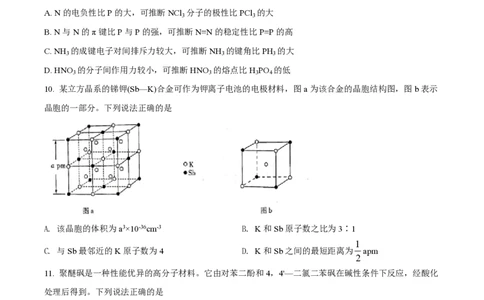
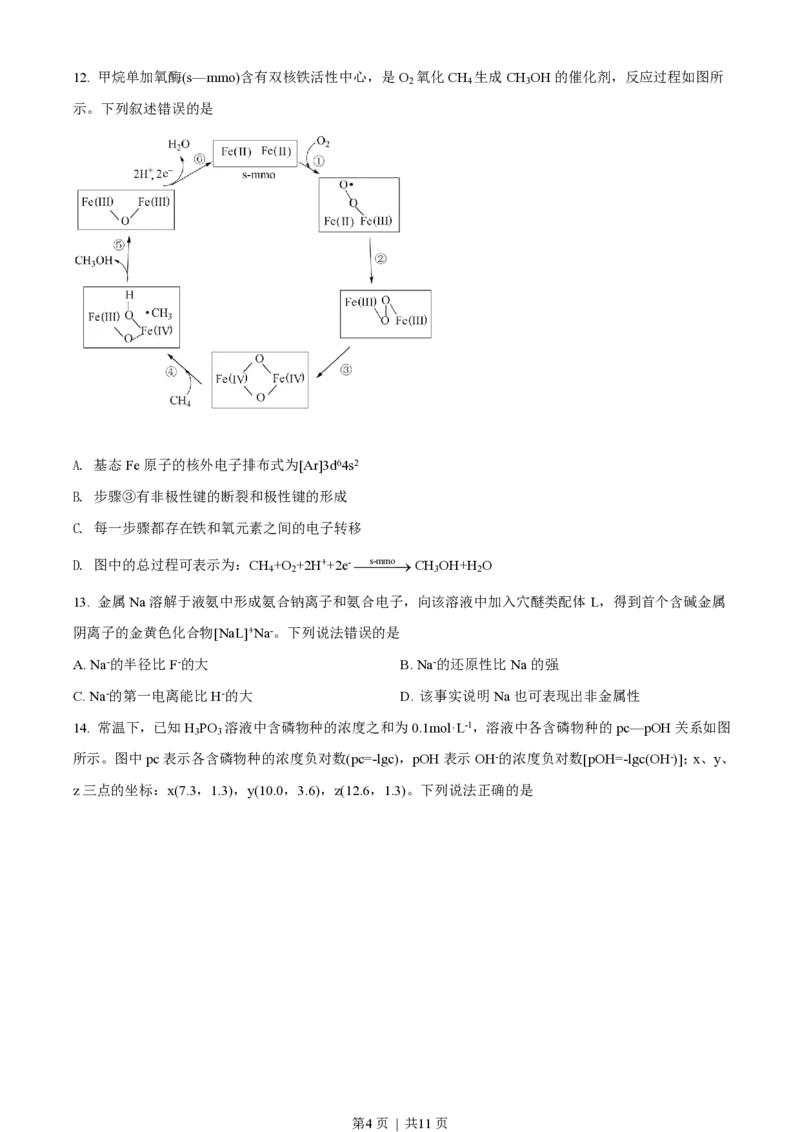
10. 某立方晶系的锑钾(Sb—K)合金可作为钾离子电池的电极材料,图a为该合金的晶胞结构图,图b表示
晶胞的一部分。下列说法正确的是
A. 该晶胞的体积为a3×10-36cm-3 B. K和Sb原子数之比为3∶1
1
C. 与Sb最邻近的K原子数为4 D. K和Sb之间的最短距离为 apm
2
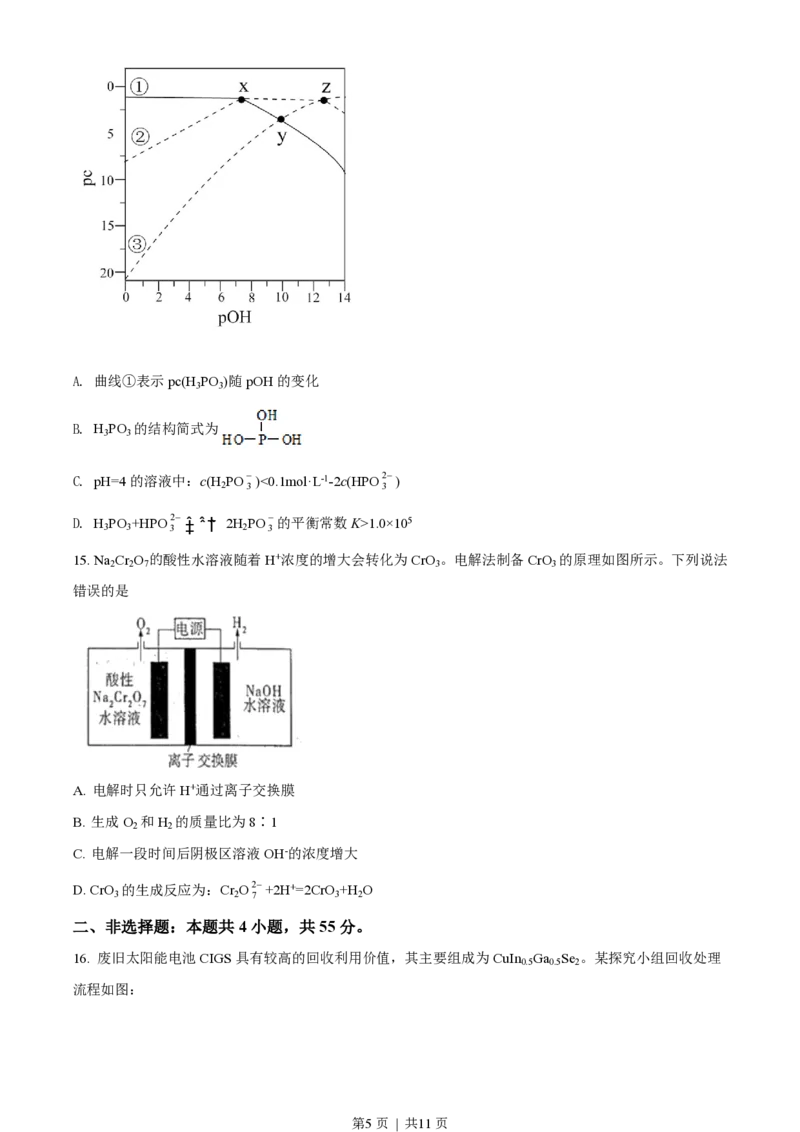
11. 聚醚砜是一种性能优异的高分子材料。它由对苯二酚和4,4'—二氯二苯砜在碱性条件下反应,经酸化
处理后得到。下列说法正确的是
A. 聚醚砜易溶于水 B. 聚醚砜可通过缩聚反应制备
C. 对苯二酚的核磁共振氢谱有3组峰 D. 对苯二酚不能与FeCl 溶液发生显色反应
3
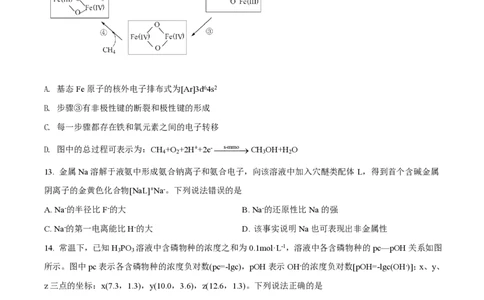
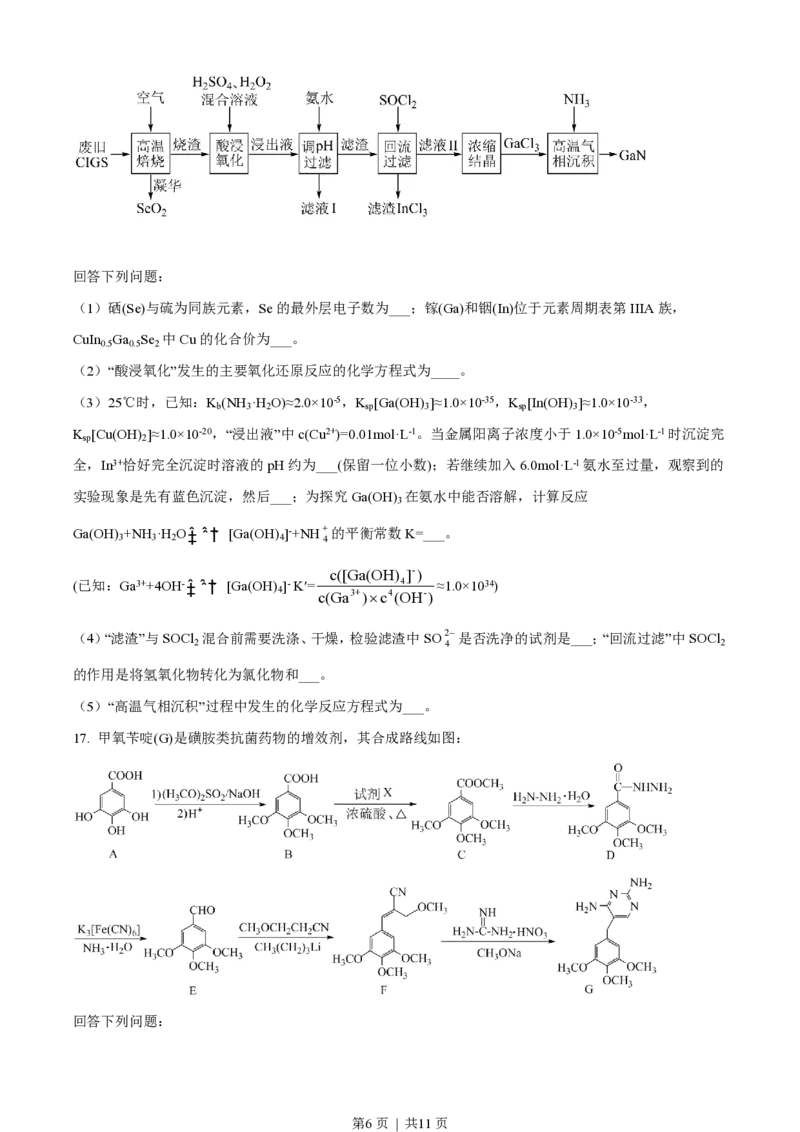
第3页 | 共11页12. 甲烷单加氧酶(s—mmo)含有双核铁活性中心,是O 氧化CH 生成CH OH的催化剂,反应过程如图所
2 4 3
示。下列叙述错误的是
A. 基态Fe原子的核外电子排布式为[Ar]3d64s2
B. 步骤③有非极性键的断裂和极性键的形成
C. 每一步骤都存在铁和氧元素之间的电子转移
D. 图中的总过程可表示为:CH +O +2H++2e-¾s¾-mm¾o®CH OH+H O
4 2 3 2
13. 金属Na溶解于液氨中形成氨合钠离子和氨合电子,向该溶液中加入穴醚类配体L,得到首个含碱金属
阴离子的金黄色化合物[NaL]+Na-。下列说法错误的是
A. Na-的半径比F-的大 B. Na-的还原性比Na的强
C. Na-的第一电离能比H-的大 D. 该事实说明Na也可表现出非金属性
14. 常温下,已知H PO 溶液中含磷物种的浓度之和为0.1mol·L-1,溶液中各含磷物种的pc—pOH关系如图
3 3
所示。图中pc表示各含磷物种的浓度负对数(pc=-lgc),pOH表示OH-的浓度负对数[pOH=-lgc(OH-)];x、y、
z三点的坐标:x(7.3,1.3),y(10.0,3.6),z(12.6,1.3)。下列说法正确的是
第4页 | 共11页A. 曲线①表示pc(H PO )随pOH的变化
3 3
B. H PO 的结构简式为
3 3
C. pH=4的溶液中:c(H PO-)<0.1mol·L-1-2c(HPO2-)
2 3 3
D. H
3
PO
3
+HPO
3
2- ‡ˆ ˆˆ†ˆ 2H
2
PO
3
-的平衡常数K>1.0×105
15. Na Cr O 的酸性水溶液随着H+浓度的增大会转化为CrO 。电解法制备CrO 的原理如图所示。下列说法
2 2 7 3 3
错误的是
A. 电解时只允许H+通过离子交换膜
B. 生成O 和H 的质量比为8∶1
2 2
C. 电解一段时间后阴极区溶液OH-的浓度增大
D. CrO 的生成反应为:Cr O2-+2H+=2CrO +H O
3 2 7 3 2
二、非选择题:本题共 4小题,共 55分。
16. 废旧太阳能电池CIGS具有较高的回收利用价值,其主要组成为CuIn Ga Se 。某探究小组回收处理
0.5 0.5 2
流程如图:
第5页 | 共11页回答下列问题:
(1)硒(Se)与硫为同族元素,Se的最外层电子数为___;镓(Ga)和铟(In)位于元素周期表第IIIA族,
CuIn Ga Se 中Cu的化合价为___。
0.5 0.5 2
(2)“酸浸氧化”发生的主要氧化还原反应的化学方程式为____。
(3)25℃时,已知:K (NH ·H O)≈2.0×10-5,K [Ga(OH) ]≈1.0×10-35,K [In(OH) ]≈1.0×10-33,
b 3 2 sp 3 sp 3
K [Cu(OH) ]≈1.0×10-20,“浸出液”中c(Cu2+)=0.01mol·L-1。当金属阳离子浓度小于1.0×10-5mol·L-1时沉淀完
sp 2
全,In3+恰好完全沉淀时溶液的pH约为___(保留一位小数);若继续加入6.0mol·L-1氨水至过量,观察到的
实验现象是先有蓝色沉淀,然后___;为探究Ga(OH) 在氨水中能否溶解,计算反应
3
Ga(OH)
3
+NH
3
·H
2
O‡ˆ ˆˆ†ˆ [Ga(OH)
4
]-+NH
4
+的平衡常数K=___。
c([Ga(OH) ]-)
(已知:Ga3++4OH-‡ˆ ˆˆ†ˆ [Ga(OH)
4
]- K′=
c(Ga3+)´c4(O
4
H-)
≈1.0×1034)
(4)“滤渣”与SOCl 混合前需要洗涤、干燥,检验滤渣中SO2-是否洗净的试剂是___;“回流过滤”中SOCl
2 4 2
的作用是将氢氧化物转化为氯化物和___。
(5)“高温气相沉积”过程中发生的化学反应方程式为___。
17. 甲氧苄啶(G)是磺胺类抗菌药物的增效剂,其合成路线如图:
回答下列问题:
第6页 | 共11页(1)E中的官能团名称是___、___。
(2)B→C的反应类型为___;试剂X的结构简式为___。
(3)若每分子F的碳碳双键加上了一分子Br ,产物中手性碳个数为___。
2
(4)B的同分异构体中能同时满足以下三个条件的有___种(不考虑立体异构)。
①属于A的同系物;②苯环上有4个取代基;③苯环上一氯代物只有一种。
(5)以异烟醛( )和乙醇为原料,制备抗结核杆菌药异烟肼的合成路线如图:
¾¾¾O 2¾¾®Y¾¾¾CH 3 C¾H 2 O¾H ¾® ¾H¾2 N-¾NH 2¾gH 2¾O®异烟肼
催化剂 浓HSO,Δ
4
写出生成Y的化学反应方程式___;异烟肼的结构简式为___。
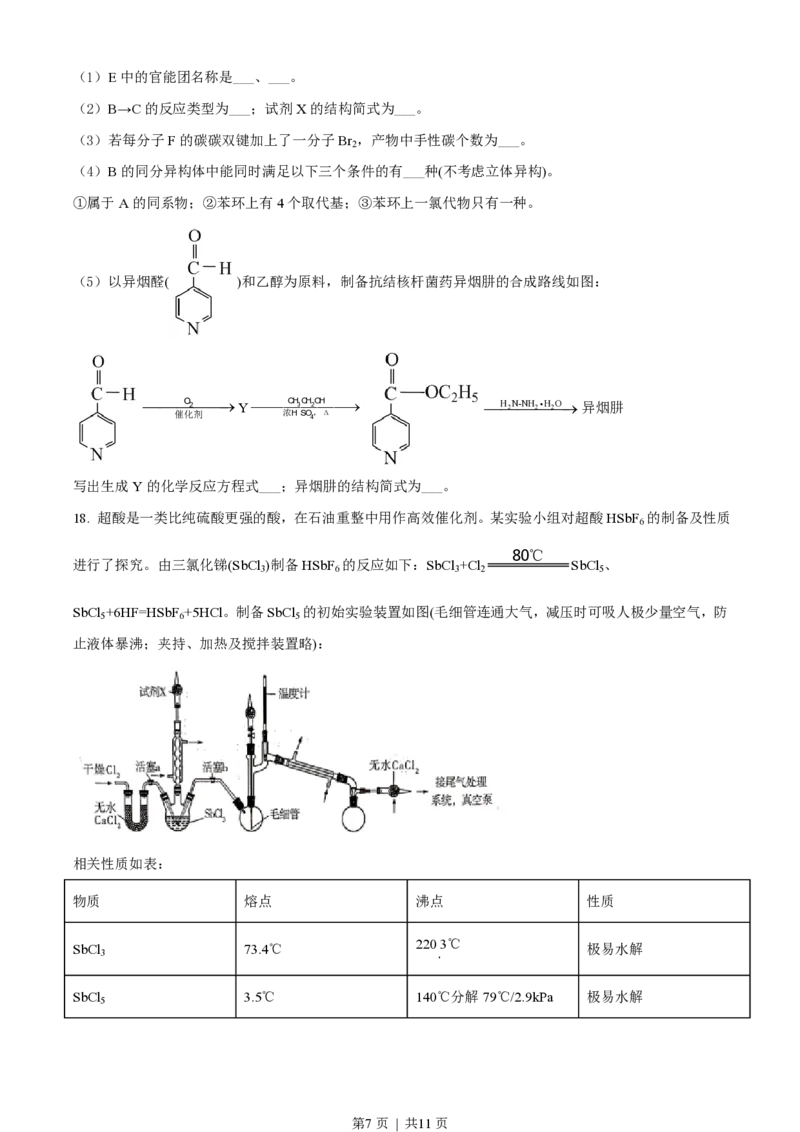
18. 超酸是一类比纯硫酸更强的酸,在石油重整中用作高效催化剂。某实验小组对超酸HSbF 的制备及性质
6
80℃
进行了探究。由三氯化锑(SbCl )制备HSbF 的反应如下:SbCl +Cl SbCl 、
3 6 3 2 5
SbCl +6HF=HSbF +5HCl。制备SbCl 的初始实验装置如图(毛细管连通大气,减压时可吸人极少量空气,防
5 6 5
止液体暴沸;夹持、加热及搅拌装置略):
相关性质如表:
物质 熔点 沸点 性质
2203℃
SbCl 73.4℃ . 极易水解
3
SbCl 3.5℃ 140℃分解79℃/2.9kPa 极易水解
5
第7页 | 共11页回答下列问题:
(1)实验装置中两个冷凝管___(填“能”或“不能”)交换使用。
(2)试剂X的作用为___、___。
(3)反应完成后,关闭活塞a、打开活塞b,减压转移___(填仪器名称)中生成的SbCl 至双口烧瓶中。用真
5
空泵抽气减压蒸馏前,必须关闭的活塞是___(填“a”或“b”);用减压蒸馏而不用常压蒸馏的主要原因是___。
(4)实验小组在由SbCl 制备HSbF 时,没有选择玻璃仪器,其原因为___。(写化学反应方程式)
5 6
(5)为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,
如冰醋酸与纯硫酸之间的化学反应方程式为CH COOH+H SO =[CH C(OH) ]+[HSO ]-。以此类推,H SO 与
3 2 4 3 2 4 2 4
HSbF 之间的化学反应方程式为___。
6
(6)实验小组在探究实验中发现蜡烛可以溶解于HSbF 中,同时放出氢气。已知烷烃分子中碳氢键的活性
6
大小顺序为:甲基(—CH )<亚甲基(—CH —)<次甲基( )。写出2—甲基丙烷与HSbF 反应的离子方
3 2 6
程式___。
19. 丙烯是一种重要的化工原料,可以在催化剂作用下,由丙烷直接脱氢或氧化脱氢制备。
反应Ⅰ(直接脱氢):C H (g)=C H (g)+H (g)△H =+125kJ·mol-1
3 8 3 6 2 1
1
反应Ⅱ(氧化脱氢):C H (g)+ O (g)=C H (g)+H O(g)△H =-118kJ·mol-1
3 8 2 3 6 2 2
2
(1)已知键能:E(C—H)=416kJ·mol-1,E(H—H)=436kJ·mol-1,由此计算生成1mol碳碳π键放出的能量为
___kJ。
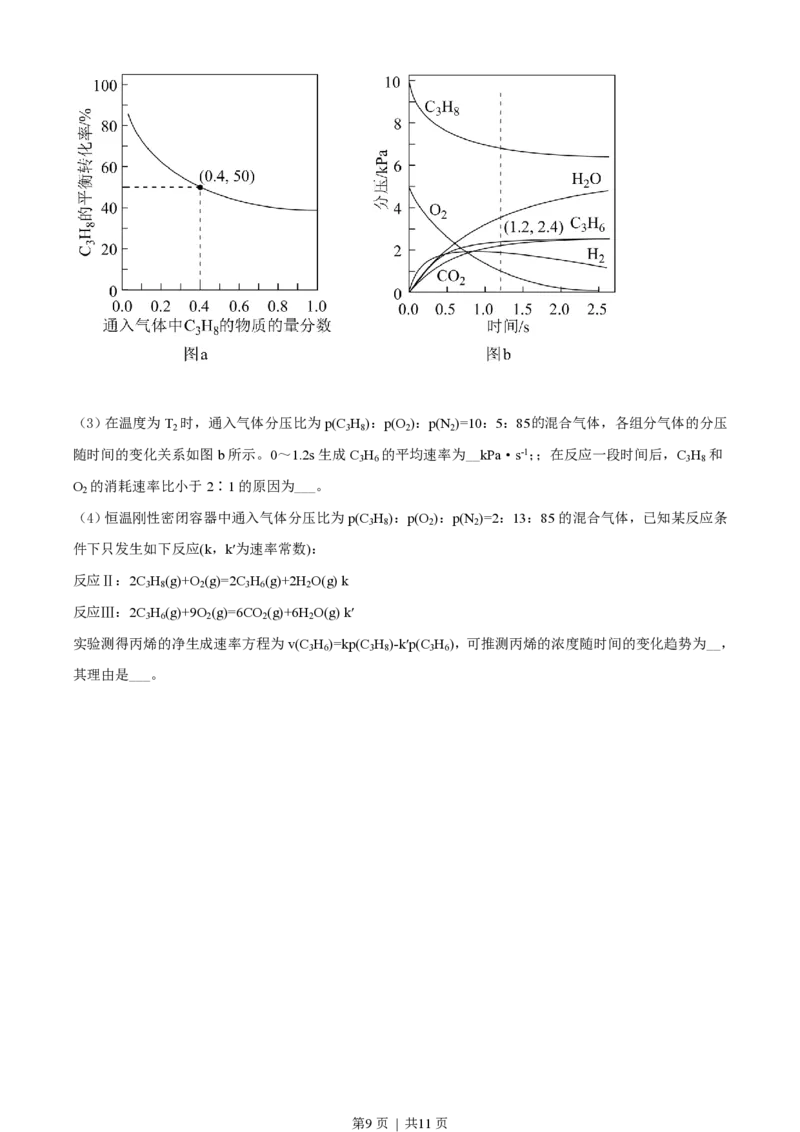
(2)对于反应Ⅰ,总压恒定为100kPa,在密闭容器中通入C H 和N 的混合气体(N 不参与反应),从平衡
3 8 2 2
移动的角度判断,达到平衡后“通入N ”的作用是___。在温度为T 时,C H 的平衡转化率与通入气体中C H
2 1 3 8 3 8
的物质的量分数的关系如图a所示,计算T 时反应Ⅰ的平衡常数K =__kPa(以分压表示,分压=总压×物质
1 p
的量分数,保留一位小数)。
第8页 | 共11页(3)在温度为T 时,通入气体分压比为p(C H ):p(O ):p(N )=10:5:85的混合气体,各组分气体的分压
2 3 8 2 2
随时间的变化关系如图b所示。0~1.2s生成C H 的平均速率为__kPa·s-1;;在反应一段时间后,C H 和
3 6 3 8
O 的消耗速率比小于2∶1的原因为___。
2
(4)恒温刚性密闭容器中通入气体分压比为p(C H ):p(O ):p(N )=2:13:85的混合气体,已知某反应条
3 8 2 2
件下只发生如下反应(k,k′为速率常数):
反应Ⅱ:2C H (g)+O (g)=2C H (g)+2H O(g) k
3 8 2 3 6 2
反应Ⅲ:2C H (g)+9O (g)=6CO (g)+6H O(g) k′
3 6 2 2 2
实验测得丙烯的净生成速率方程为v(C H )=kp(C H )-k′p(C H ),可推测丙烯的浓度随时间的变化趋势为__,
3 6 3 8 3 6
其理由是___。
第9页 | 共11页第10页 | 共11页第11页 | 共11页