文档内容
山东省 2022 年普通高中学业水平等级考试
化学
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在
本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 S 32 Cl 35.5 Ti 48 Co 59
一、选择题:本题共 10小题,每小题 2分,共 20 分。每小题只有一个选项符合题目要求。
1. 古医典富载化学知识,下述之物见其氧化性者为
A. 金(Au):“虽被火亦未熟"
B. 石灰(CaO):“以水沃之,即热蒸而解”
C. 石硫黄(S):“能化……银、铜、铁,奇物”
D 石钟乳(CaCO ):“色黄,以苦酒(醋)洗刷则白”
. 3
2. 下列试剂实验室保存方法错误的是
A. 浓硝酸保存在棕色细口瓶中 B. 氢氧化钠固体保存在广口塑料瓶中
C. 四氯化碳保存在广口塑料瓶中 D. 高锰酸钾固体保存在棕色广口瓶中
3. 13O、15O的半衰期很短,自然界中不能稳定存在。人工合成反应如下:16O+3He®13 O+aX;
8 8 8 2 8 b
16O+3He®15 O+mY。下列说法正确的是
8 2 8 n
A. X的中子数为2
B. X、Y互为同位素
C. 13O、15O可用作示踪原子研究化学反应历程
8 8
D. 自然界不存在13O 、15O 分子是因其化学键不稳定
8 2 8 2
4. 下列高分子材料制备方法正确的是
A. 聚乳酸( )由乳酸经加聚反应制备
B. 聚四氟乙烯( )由四氟乙烯经加聚反应制备
第1页 | 共13页C. 尼龙-66( )由己胺和己酸经缩聚反应制备
D. 聚乙烯醇( )由聚乙酸乙烯酯( )经消去反应制备
5. AlN、GaN属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在N-Al键、N-Ga
键。下列说法错误的是
A. GaN的熔点高于AlN B. 晶体中所有化学键均为极性键
C. 晶体中所有原子均采取sp3杂化 D. 晶体中所有原子的配位数均相同
6. 实验室用基准Na CO 配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐酸滴定Na CO
2 3 2 3
标准溶液。下列说法错误的是
A. 可用量筒量取25.00mL Na CO 标准溶液置于锥形瓶中
2 3
B. 应选用配带塑料塞的容量瓶配制Na CO 标准溶液
2 3
C. 应选用烧杯而非称量纸称量Na CO 固体
2 3
D. 达到滴定终点时溶液显橙色
7. γ-崖柏素具天然活性,有酚的通性,结构如图。关于γ-崖柏素的说法错误的是
A. 可与溴水发生取代反应
B. 可与NaHCO 溶液反应
3
C. 分子中的碳原子不可能全部共平面
D. 与足量H 加成后,产物分子中含手性碳原子
2
8. 实验室制备KMnO 过程为:①高温下在熔融强碱性介质中用KClO 氧化MnO 制备K MnO ;②水
4 3 2 2 4
溶后冷却,调溶液pH至弱碱性,K MnO 歧化生成KMnO 和MnO ;③减压过滤,将滤液蒸发浓
2 4 4 2
缩、冷却结晶,再减压过滤得KMnO 。下列说法正确的是
4
第2页 | 共13页A. ①中用瓷坩埚作反应器
B. ①中用NaOH作强碱性介质
C ②中K MnO 只体现氧化性
. 2 4
D. MnO 转化为KMnO 的理论转化率约为66.7%
2 4
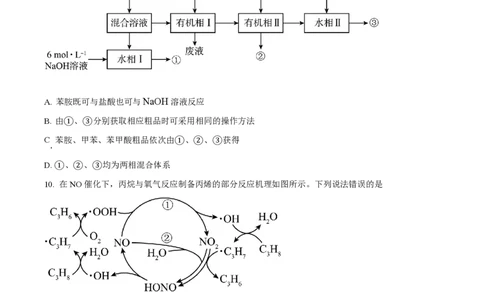
9. 已知苯胺(液体)、苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。实验室初步分离甲苯、苯胺、苯甲酸
混合溶液的流程如下。下列说法正确的是
A. 苯胺既可与盐酸也可与NaOH溶液反应
B. 由①、③分别获取相应粗品时可采用相同的操作方法
C 苯胺、甲苯、苯甲酸粗品依次由①、②、③获得
.
D. ①、②、③均为两相混合体系
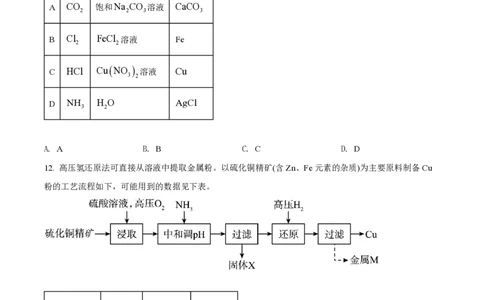
10. 在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的是
A. 含N分子参与的反应一定有电子转移
B. 由NO生成HONO的反应历程有2种
C. 增大NO的量,C H 的平衡转化率不变
3 8
D. 当主要发生包含②的历程时,最终生成的水减少
二、选择题:本题共 5小题,每小题 4分,共 20 分。每小题有一个或两个选项符合题目要
求,全部选对得 4分,选对但不全的得 2分,有选错的得 0分。
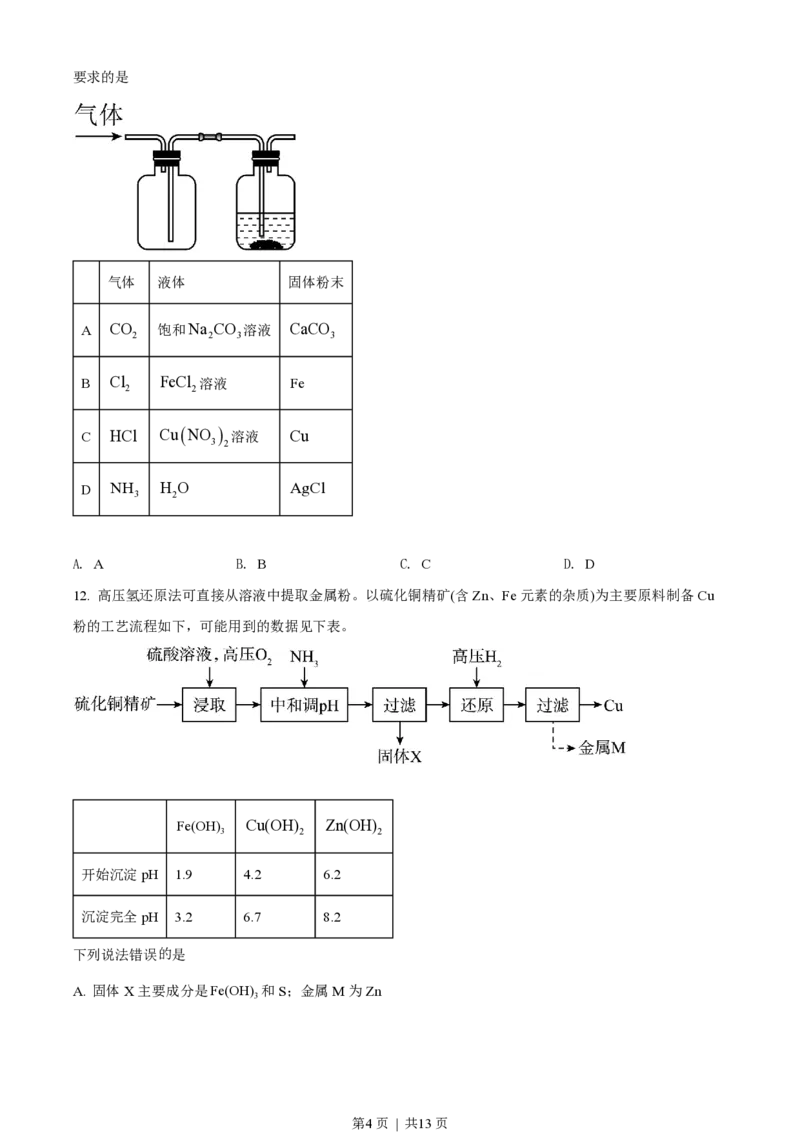
11. 某同学按图示装置进行实验,欲使瓶中少量固体粉末最终消失并得到澄清溶液。下列物质组合不符合
第3页 | 共13页要求的是
气体 液体 固体粉末
A CO 饱和Na CO 溶液 CaCO
2 2 3 3
B Cl FeCl 溶液 Fe
2 2
C HCl
CuNO
溶液 Cu
3 2
D NH H O AgCl
3 2
A. A B. B C. C D. D
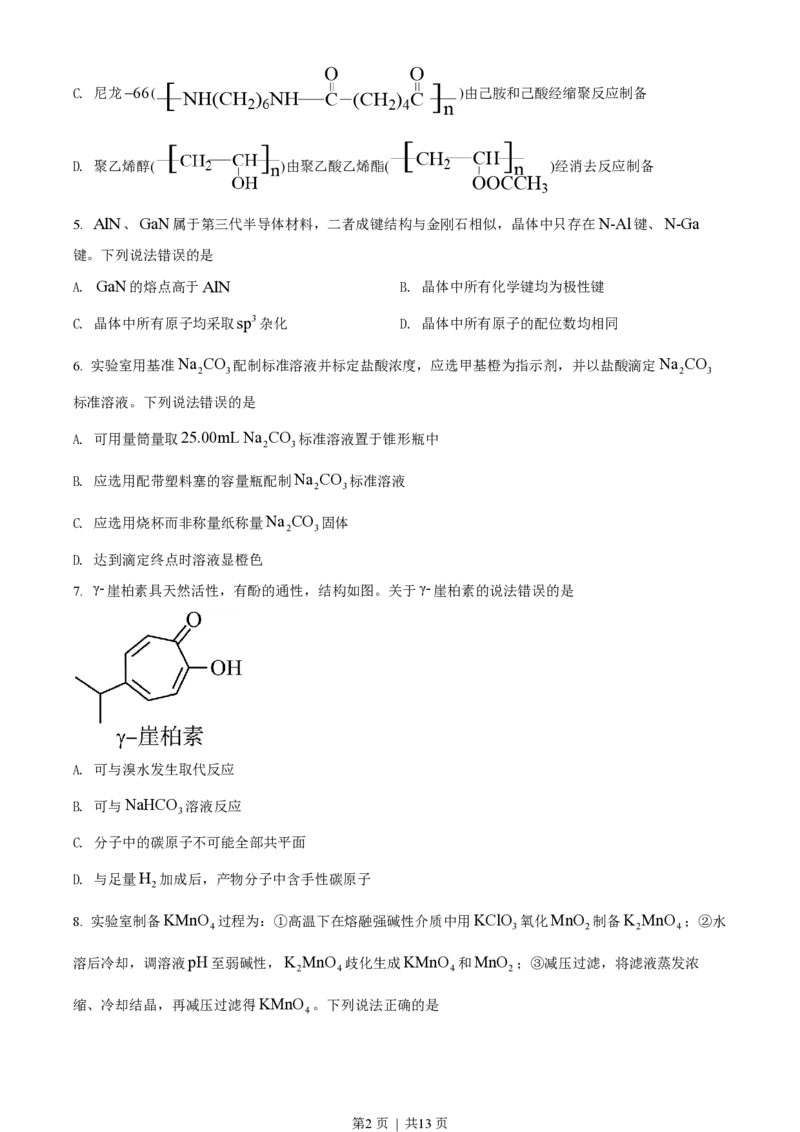
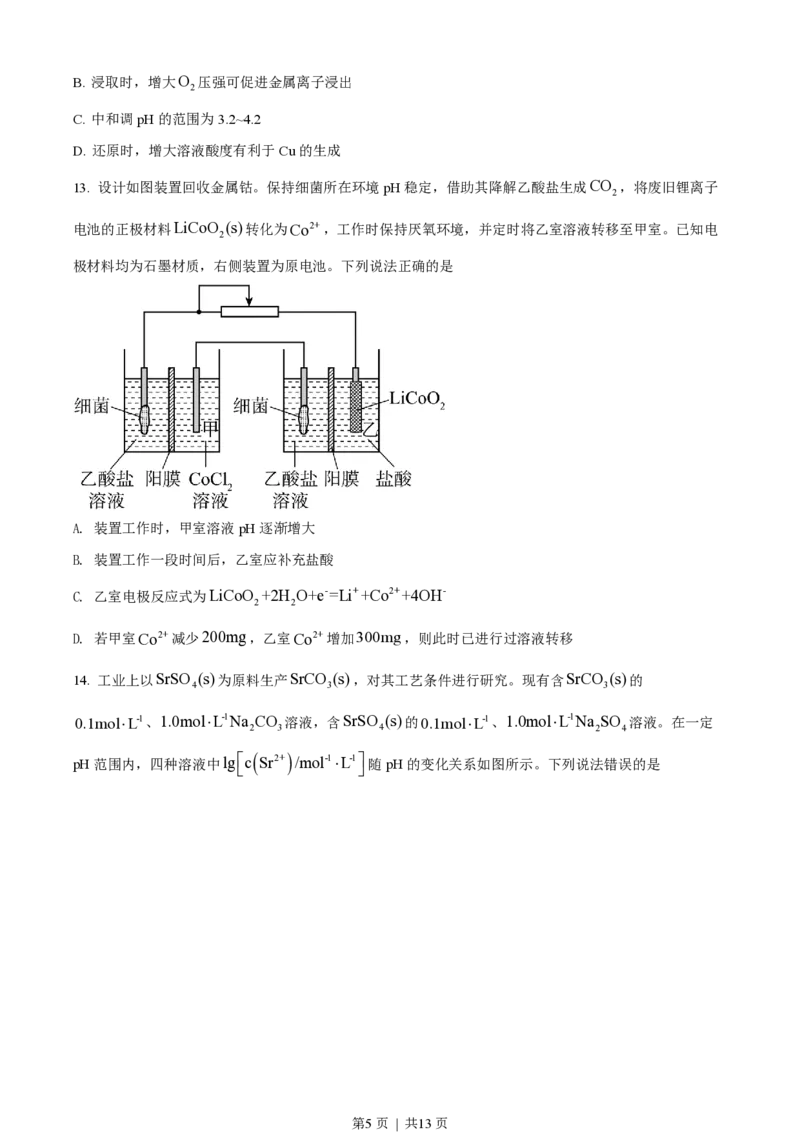
12. 高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元素的杂质)为主要原料制备Cu
粉的工艺流程如下,可能用到的数据见下表。
Fe(OH) Cu(OH) Zn(OH)
3 2 2
开始沉淀pH 1.9 4.2 6.2
沉淀完全pH 3.2 6.7 8.2
下列说法错误的是
A. 固体X主要成分是Fe(OH) 和S;金属M为Zn
3
第4页 | 共13页B. 浸取时,增大O 压强可促进金属离子浸出
2
C. 中和调pH的范围为3.2~4.2
D. 还原时,增大溶液酸度有利于Cu的生成
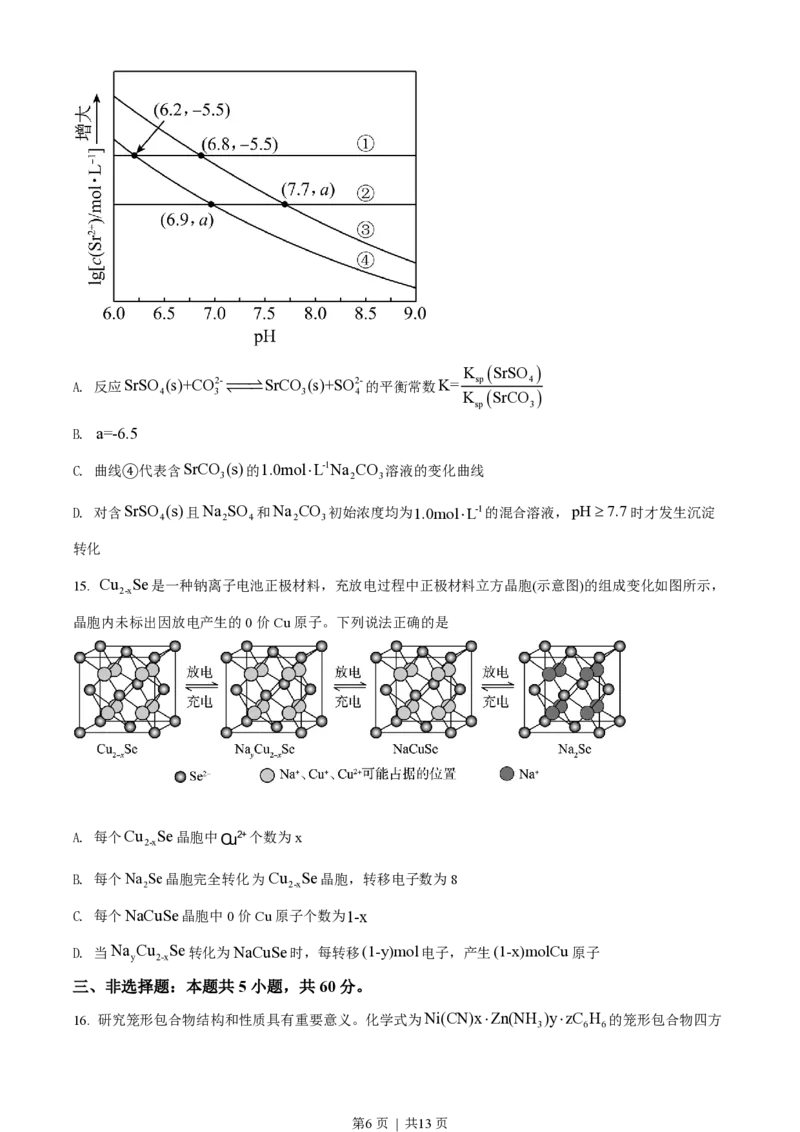
13. 设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成CO ,将废旧锂离子
2
电池的正极材料LiCoO (s)转化为Co2+,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电
2
极材料均为石墨材质,右侧装置为原电池。下列说法正确的是
A. 装置工作时,甲室溶液pH逐渐增大
B. 装置工作一段时间后,乙室应补充盐酸
C. 乙室电极反应式为LiCoO +2H O+e-=Li++Co2++4OH-
2 2
D. 若甲室Co2+减少200mg,乙室Co2+增加300mg,则此时已进行过溶液转移
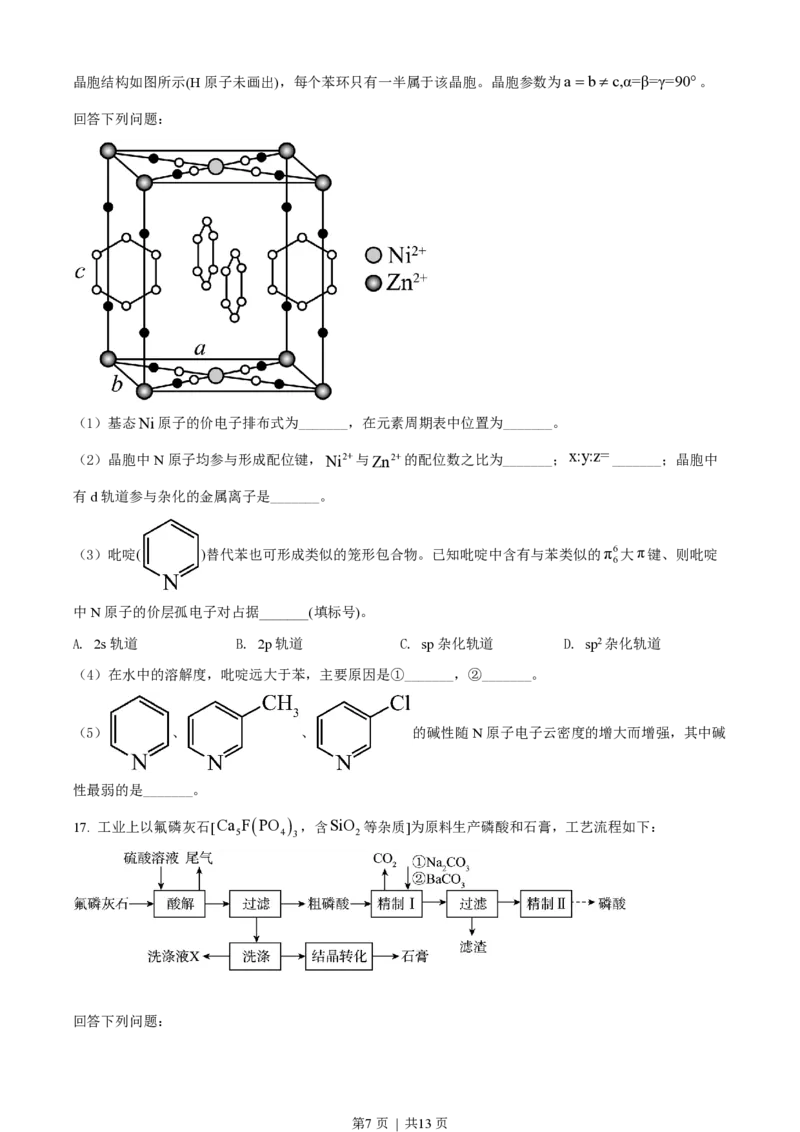
14. 工业上以SrSO (s)为原料生产SrCO (s),对其工艺条件进行研究。现有含SrCO (s)的
4 3 3
0.1mol×L-1、1.0mol×L-1Na CO 溶液,含SrSO (s)的0.1mol×L-1、1.0mol×L-1Na SO 溶液。在一定
2 3 4 2 4
pH范围内,四种溶液中lgéc Sr2+ /mol-1×L-1ù随pH的变化关系如图所示。下列说法错误的是
ë û
第5页 | 共13页K SrSO
A. 反应SrSO (s)+CO2- ˆˆ†SrCO (s)+SO2-的平衡常数K= sp 4
4 3 ‡ˆˆ 3 4 K SrCO
sp 3
B. a=-6.5
C. 曲线④代表含SrCO (s)的1.0mol×L-1Na CO 溶液的变化曲线
3 2 3
D. 对含SrSO (s)且Na SO 和Na CO 初始浓度均为1.0mol×L-1的混合溶液,pH³7.7时才发生沉淀
4 2 4 2 3
转化
15. Cu Se是一种钠离子电池正极材料,充放电过程中正极材料立方晶胞(示意图)的组成变化如图所示,
2-x
晶胞内未标出因放电产生的0价Cu原子。下列说法正确的是
A. 每个Cu Se晶胞中Cu2+个数为x
2-x
B. 每个Na Se晶胞完全转化为Cu Se晶胞,转移电子数为8
2 2-x
C. 每个NaCuSe晶胞中0价Cu原子个数为1-x
D. 当Na Cu Se转化为NaCuSe时,每转移(1-y)mol电子,产生(1-x)molCu原子
y 2-x
三、非选择题:本题共 5小题,共 60分。
16. 研究笼形包合物结构和性质具有重要意义。化学式为Ni(CN)x×Zn(NH )y×zC H 的笼形包合物四方
3 6 6
第6页 | 共13页晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数为a =b¹c,α=β=γ=90°。
回答下列问题:
(1)基态Ni原子的价电子排布式为_______,在元素周期表中位置为_______。
(2)晶胞中N原子均参与形成配位键,Ni2+与Zn2+的配位数之比为_______;x:y:z=_______;晶胞中
有d轨道参与杂化的金属离子是_______。
(3)吡啶( )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的π6大π键、则吡啶
6
中N原子的价层孤电子对占据_______(填标号)。
A. 2s轨道 B. 2p轨道 C. sp杂化轨道 D. sp2杂化轨道
(4)在水中的溶解度,吡啶远大于苯,主要原因是①_______,②_______。
(5) 、 、 的碱性随N原子电子云密度的增大而增强,其中碱
性最弱的是_______。
17. 工业上以氟磷灰石[Ca FPO ,含SiO 等杂质]为原料生产磷酸和石膏,工艺流程如下:
5 4 3 2
回答下列问题:
第7页 | 共13页(1)酸解时有HF产生。氢氟酸与SiO 反应生成二元强酸H SiF ,离子方程式为_______。
2 2 6
(2)部分盐的溶度积常数见下表。精制Ⅰ中,按物质的量之比nNa CO :n SiF2- =1:1加入Na CO 脱
2 3 6 2 3
氟,充分反应后,c
Na+
=_______mol×L-1;再分批加入一定量的BaCO ,首先转化为沉淀的离子是
3
_______。
BaSiF Na SiF CaSO BaSO
6 2 6 4 4
K 1.0´10-6 4.0´10-6 9.0´10-4 1.0´10-10
sp
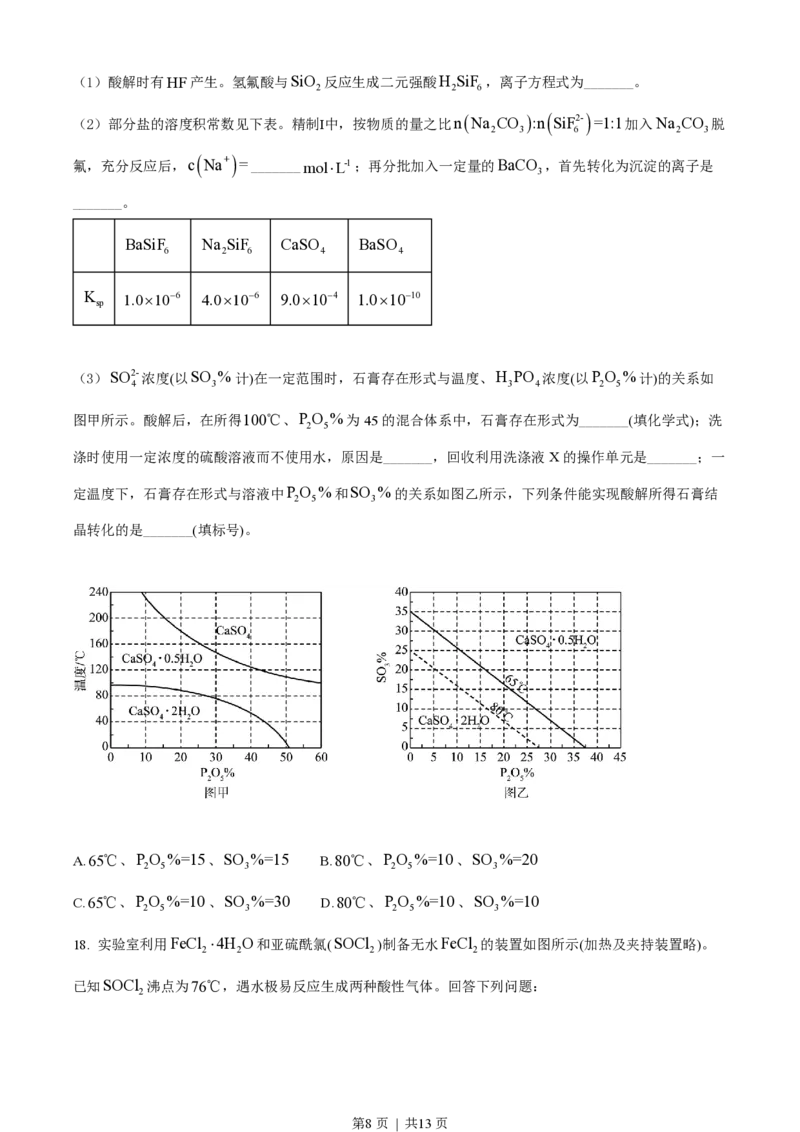
(3)SO2-浓度(以SO %计)在一定范围时,石膏存在形式与温度、H PO 浓度(以PO %计)的关系如
4 3 3 4 2 5
图甲所示。酸解后,在所得100℃、PO %为45的混合体系中,石膏存在形式为_______(填化学式);洗
2 5
涤时使用一定浓度的硫酸溶液而不使用水,原因是_______,回收利用洗涤液X的操作单元是_______;一
定温度下,石膏存在形式与溶液中PO %和SO %的关系如图乙所示,下列条件能实现酸解所得石膏结
2 5 3
晶转化的是_______(填标号)。
A.65℃、PO %=15、SO %=15 B.80℃、PO %=10、SO %=20
2 5 3 2 5 3
C.65℃、PO %=10、SO %=30 D.80℃、PO %=10、SO %=10
2 5 3 2 5 3
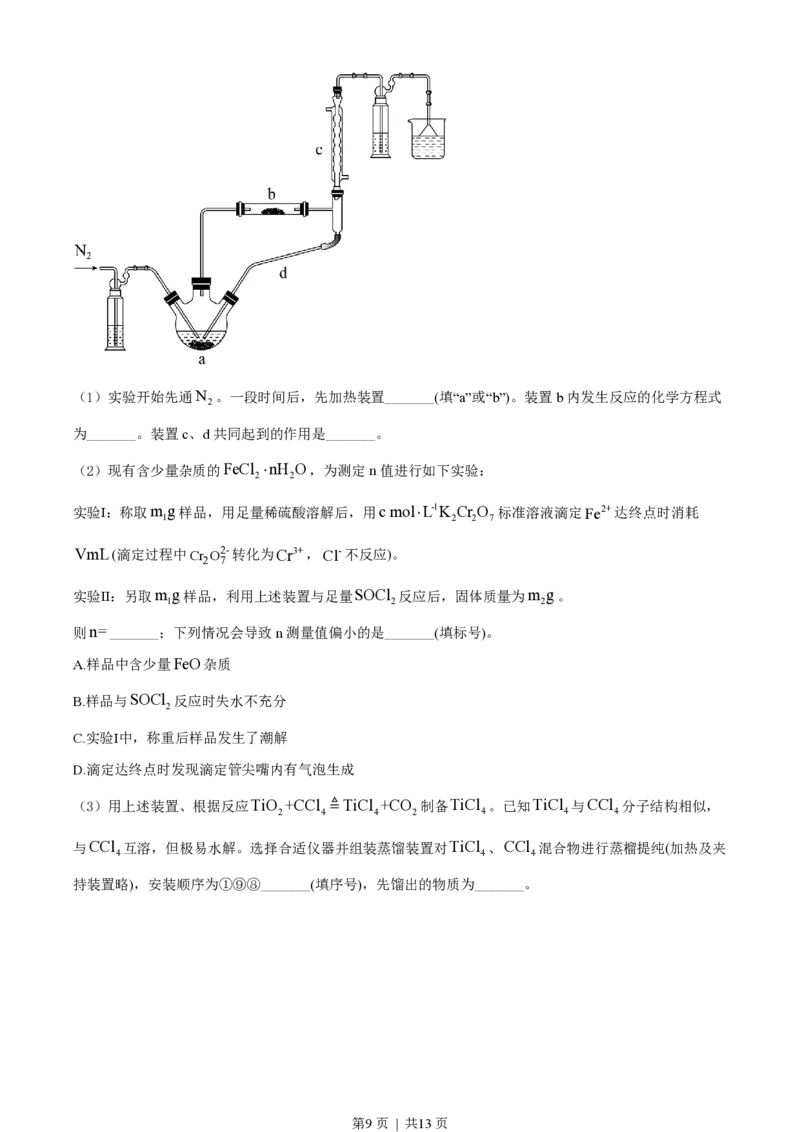
18. 实验室利用FeCl ×4H O和亚硫酰氯(SOCl )制备无水FeCl 的装置如图所示(加热及夹持装置略)。
2 2 2 2
已知SOCl 沸点为76℃,遇水极易反应生成两种酸性气体。回答下列问题:
2
第8页 | 共13页(1)实验开始先通N 。一段时间后,先加热装置_______(填“a”或“b”)。装置b内发生反应的化学方程式
2
为_______。装置c、d共同起到的作用是_______。
(2)现有含少量杂质的FeCl ×nH O,为测定n值进行如下实验:
2 2
实验Ⅰ:称取m g样品,用足量稀硫酸溶解后,用c mol×L-1K Cr O 标准溶液滴定Fe2+达终点时消耗
1 2 2 7
VmL(滴定过程中Cr O 2-转化为Cr3+,Cl-不反应)。
2 7
实验Ⅱ:另取m g样品,利用上述装置与足量SOCl 反应后,固体质量为m g。
1 2 2
则n=_______;下列情况会导致n测量值偏小的是_______(填标号)。
A.样品中含少量FeO杂质
B.样品与SOCl 反应时失水不充分
2
C.实验Ⅰ中,称重后样品发生了潮解
D.滴定达终点时发现滴定管尖嘴内有气泡生成
(3)用上述装置、根据反应TiO +CCl TiCl +CO 制备TiCl 。已知TiCl 与CCl 分子结构相似,
2 4 @ 4 2 4 4 4
与CCl 互溶,但极易水解。选择合适仪器并组装蒸馏装置对TiCl 、CCl 混合物进行蒸榴提纯(加热及夹
4 4 4
持装置略),安装顺序为①⑨⑧_______(填序号),先馏出的物质为_______。
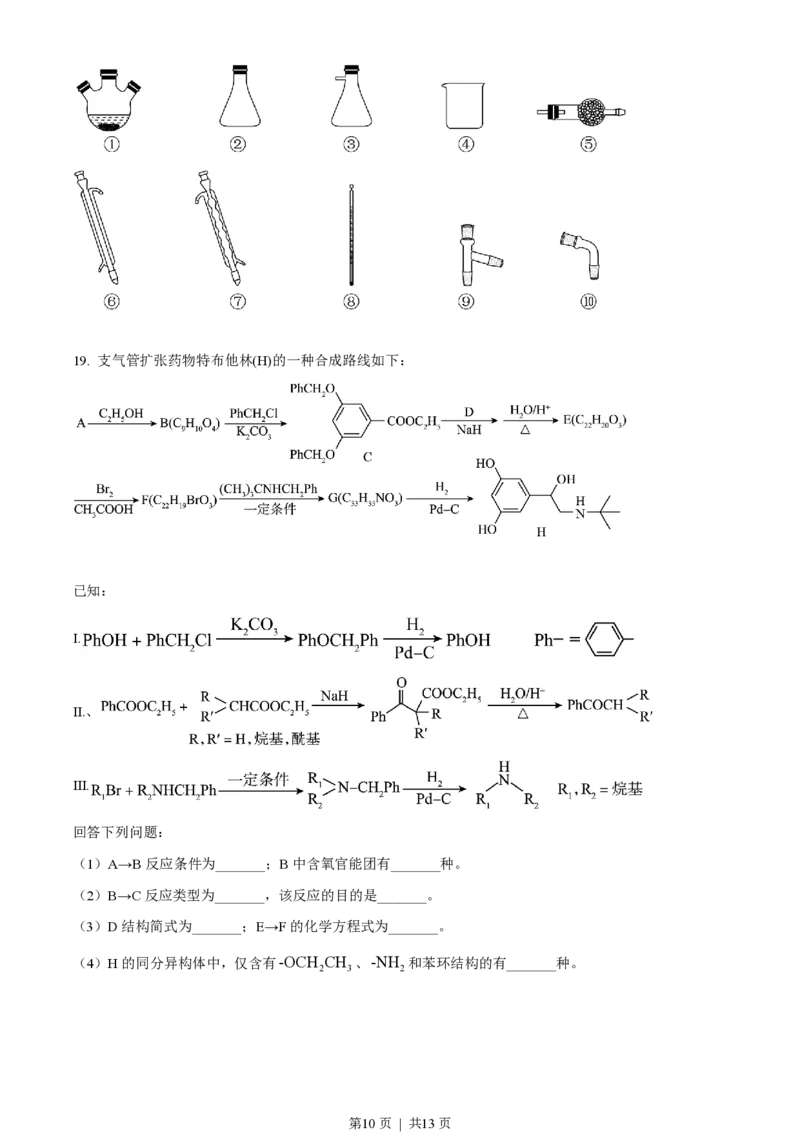
第9页 | 共13页19. 支气管扩张药物特布他林(H)的一种合成路线如下:
已知:
Ⅰ.
Ⅱ.、
Ⅲ.
回答下列问题:
(1)A→B反应条件为_______;B中含氧官能团有_______种。
(2)B→C反应类型为_______,该反应的目的是_______。
(3)D结构简式为_______;E→F的化学方程式为_______。
(4)H的同分异构体中,仅含有-OCH CH 、-NH 和苯环结构的有_______种。
2 3 2
第10页 | 共13页(5)根据上述信息,写出以4-羟基邻苯二甲酸二乙酯为主要原料制备合成 的
路线_______。
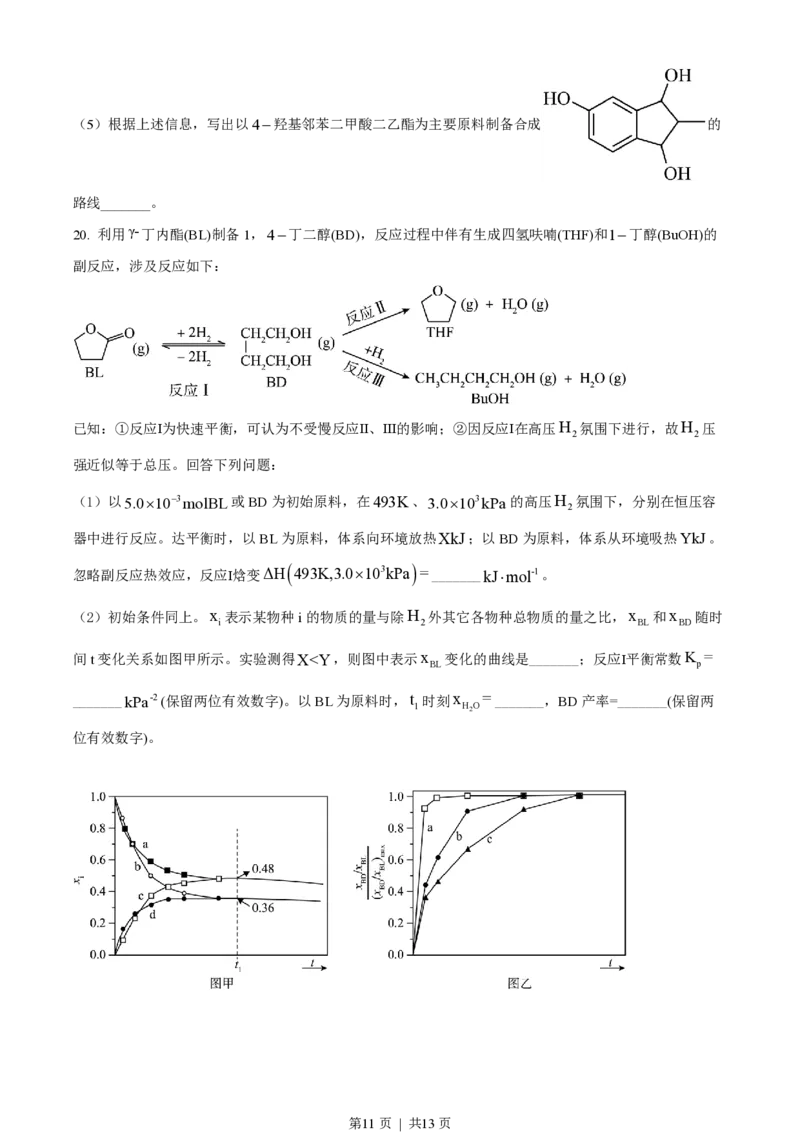
20. 利用γ-丁内酯(BL)制备1,4-丁二醇(BD),反应过程中伴有生成四氢呋喃(THF)和1-丁醇(BuOH)的
副反应,涉及反应如下:
已知:①反应Ⅰ为快速平衡,可认为不受慢反应Ⅱ、Ⅲ的影响;②因反应Ⅰ在高压H 氛围下进行,故H 压
2 2
强近似等于总压。回答下列问题:
(1)以5.0´10-3molBL或BD为初始原料,在493K、3.0´103kPa的高压H 氛围下,分别在恒压容
2
器中进行反应。达平衡时,以BL为原料,体系向环境放热XkJ;以BD为原料,体系从环境吸热YkJ。
忽略副反应热效应,反应Ⅰ焓变ΔH 493K,3.0´103kPa =_______kJ×mol-1。
(2)初始条件同上。x 表示某物种i的物质的量与除H 外其它各物种总物质的量之比,x 和x 随时
i 2 BL BD
间t变化关系如图甲所示。实验测得X